24 березня, 2020
Ведення хворих на ЦД 2 типу із супутньою серцево-судинною патологією
 Попри великі досягнення в дослідженні патогенезу цукрового діабету (ЦД) 2 типу, діагностиці та лікуванні цього захворювання, а також появу нових класів цукрознижувальних препаратів, які дозволили оновити терапевтичний алгоритм, чисельність хворих на ЦД неухильно зростає. Нині на ЦД хворіє кожен 11-й індивід, а до 2040 року хворітиме кожен 10-й. У розвинених країнах ЦД мають 8-10% населення.
Попри великі досягнення в дослідженні патогенезу цукрового діабету (ЦД) 2 типу, діагностиці та лікуванні цього захворювання, а також появу нових класів цукрознижувальних препаратів, які дозволили оновити терапевтичний алгоритм, чисельність хворих на ЦД неухильно зростає. Нині на ЦД хворіє кожен 11-й індивід, а до 2040 року хворітиме кожен 10-й. У розвинених країнах ЦД мають 8-10% населення.
У пацієнтів із ЦД підвищений ризик розвитку низки серцево-судинних захворювань (ССЗ), таких як захворювання периферичних артерій, ішемічний інсульт, стенокардія, інфаркт міокарда (ІМ) і серцева недостатність (СН). Окрім того, діабет визнається фактором ризику смерті від ССЗ. Своєю чергою, ССЗ сьогодні є основною причиною передчасної смерті пацієнтів із ЦД і призводять до значного збільшення витрат на допомогу хворим.
Визначення поняття та класифікація ЦД
Починається ЦД як порушення вуглеводного обміну, а завершується як серцево-судинна хвороба. Провідною причиною смерті пацієнтів із ЦД є гострі ССЗ, саме від них помирають 8 із 10 хворих. Високу смертність пацієнтів із ЦД від гострих ССЗ визначає комбінування як факторів ризику, властивих для загальної популяції, а саме зловживання алкоголем, гіперкоагуляція, артеріальна гіпертензія (АГ), малорухливий спосіб життя, ожиріння, дисліпідемія, куріння, так і притаманних ЦД внутрішніх чинників ризику, як-от інсулінорезистентність, гіперглікемія, гіперінсулінемія, протеїнурія й мікроальбумінурія за наявності діабетичної нефропатії.
 При цьому необхідно зауважити, що захворюваність і смертність від ішемічної хвороби серця в пацієнтів із ЦД перевищує прогнозований ступінь при звичайному підсумовуванні ризиків, що свідчить про прямий вплив гіперглікемії на атеросклеротичний процес. Діабет і серцево-судинні порушення – це дві сторони однієї медалі, тож невипадково Американська діабетична асоціація (ADA) визначає ці хвороби як рівні між собою.
При цьому необхідно зауважити, що захворюваність і смертність від ішемічної хвороби серця в пацієнтів із ЦД перевищує прогнозований ступінь при звичайному підсумовуванні ризиків, що свідчить про прямий вплив гіперглікемії на атеросклеротичний процес. Діабет і серцево-судинні порушення – це дві сторони однієї медалі, тож невипадково Американська діабетична асоціація (ADA) визначає ці хвороби як рівні між собою.
Слід зауважити, що діагностичні критерії ЦД за останні 20 років істотних змін не зазнали (табл. 1). Лікарі загальної практики, терапевти, кардіологи повинні їх знати і грамотно аналізувати у своїй повсякденній практиці.
Глікозильований гемоглобін як діагностичний критерій ЦД
Глікозильований гемоглобін (HbA1c) є показником стану вуглеводного обміну протягом 3 міс і відображає середній уміст глюкози в крові за цей період. У 2011 р. Всесвітня організація охорони здоров’я (ВООЗ) схвалила можливість використання HbA1c для діагностики ЦД. Дослідження має виконуватися з використанням методу визначення HbA1c, сертифікованого відповідно до National Glycohemoglobin Standardization Program (NGSP Complications Trial) або International Federation of Clinical Chemists (IFCC) і стандартизованого відповідно до референтних значень, визначених у Diabetes Control and Complicaitions Trial (DCCT). Нормальним вважається рівень HbA1c до 6,0% (42 ммоль/моль). Згідно з рекомендаціями ВООЗ, показник HbA1c 6,0-6,4% сам по собі не дозволяє встановити будь-який діагноз, але не виключає можливості діагностики ЦД за рівнем глюкози крові. Як діагностичний критерій ЦД 2 типу обраний рівень HbA1c ≥6,5% (48 ммоль/моль).
Визначення рівня HbA1c – зручний і надійний метод діагностики ЦД, який не потребує спеціальної підготовки (стану натще), не залежить від часу доби, фізичних навантажень, емоційних, стресових факторів напередодні дослідження, тому знайшов широке застосування в клінічній практиці. Утім, є певні ситуації, в яких дослідження на визначення HbA1c може дати неправильні результати. До них належать серпоподібноклітинна анемія, II і III триместри вагітності, проведення гемодіалізу, недавня крововтрата чи переливання крові, лікування еритропоетином. Для діагностики ЦД у цієї категорії пацієнтів слід визначати рівень глюкози в плазмі крові.
У разі відсутності симптомів гострої метаболічної декомпенсації діагноз ЦД має бути встановлений на підставі двох цифр, які перебувають у діабетичному діапазоні, наприклад двічі визначений рівень HbA1c або одноразове визначення HbA1c у поєднанні з одноразовим визначенням рівня глюкози крові.
Методи контролю рівня глюкози крові
Для самоконтролю рівня глюкози крові рекомендується застосовувати глюкометри, призначені для індивідуального використання. Самоконтроль глюкози за допомогою глюкометрів наразі є основним у світовій практиці й надалі залишатиметься таким. За допомогою результатів самоконтролю можна оцінити конкретну ситуацію – поточний стан хворого на ЦД залежно від рівня глюкози в крові до та після їди, на тлі впливу різних харчових продуктів, фізичного навантаження, прийому цукрознижувальних препаратів.
Рекомендована частота обстежень при ЦД залежить від факту встановлення діагнозу, наявності ускладнень, варіантів цукрознижувальної терапії, віку пацієнта, типу ЦД. Так, у дебюті ЦД 2 типу самоконтроль глікемії в дорослого пацієнта має проводитися щонайменше 4 рази на добу. Кількість досліджень може підвищуватися при підборі дози інсуліну в пацієнтів із декомпенсацією ЦД, при стресах, інтеркурентних захворюваннях і фізичних навантаженнях.
Загальні принципи лікування ЦД у поєднанні із ССЗ в амбулаторних умовах
Переконливі дані рандомізованих контрольованих досліджень показали, що суворий контроль глікемії може зменшити мікросудинні ускладнення ЦД. Ефект жорсткого глікемічного контролю на макросудинні порушення менш очевидний. Тоді як гіперглікемія пов’язана з підвищеним ризиком ССЗ, нещодавні рандомізовані контрольовані дослідження не змогли продемонструвати явне зменшення серцево-судинного ризику при поліпшенні глікемії. Невеликий, але сприятливий вплив на ССЗ може спостерігатися через багато років. Наявність множинних супутніх захворювань при тривалому ЦД і фенотип комплексного ризику, що розвивається в контексті інсулінорезистентності, ймовірно, пояснює, чому контроль HbA1c не вирішує проблему ризику ССЗ достатньою мірою.
Чинники, що зумовлюють збільшення ризику розвитку ССЗ при ЦД, включають гіперінсулінемію, інсулінорезистентність, гіперглікемію, гіпертензію, ліпідемію та тромбоз. Запалення й мікробіом теж можуть бути додані в список залучених факторів. Отже, терапія ЦД в ідеалі має бути націлена на всі чи принаймні більшість цих процесів.
Лікування ЦД охоплює такі напрями: зміна способу життя (дієта, фізичні навантаження); цукрознижувальна терапія; контроль факторів ризику (АГ, дисліпідемія, хронічна хвороба нирок); навчання пацієнта та самоконтроль. Основними цілями лікування ЦД є нормалізація вуглеводного обміну, зниження артеріального тиску (АТ) і нормалізація рівня ліпідів у крові.
Вибір індивідуальних цілей лікування залежить від віку пацієнта, очікуваної тривалості життя, наявності тяжких ускладнень і ризику тяжкої гіпоглікемії.
Нефармакологічний контроль гіперглікемії
ADA та Європейська асоціація з вивчення діабету (EASD) спільно опублікували клінічні рекомендації, в яких підкреслено провідну роль модифікації способу життя як першочергового заходу профілактики та/або лікування ЦД. Здоровий спосіб життя має першорядне значення для запобігання переходу від порушення толерантності до глюкози (ПТГ) до розвитку діабету та включає в себе здорове харчування, фізичну активність, підтримання здорової ваги та припинення куріння.
Дієта
У цілому визнається, що можуть бути прийнятними кілька типів харчування, при цьому дієта повинна бути фізіологічно грамотною: кількість енергії в спожитих продуктах має відповідати енергетичним потребам хворого; кількість білків, жирів, вуглеводів повинна бути збалансованою; прийом їжі протягом дня – 5-6 разів.
Хворим на діабет із надмірною вагою, щоб посилити відчуття насичення, потрібно включати в дієту такі овочі, як свіжа та квашена капуста, салат, шпинат, зелений горошок, огірки, помідори. Для поліпшення функції печінки, котра страждає при діабеті, потрібно вводити в дієту продукти, що містять ліпотропні фактори (сир, соя, вівсяна каша та ін.), а також обмежувати вживання м’ясних, рибних бульйонів і смажених страв. Споживання солі теж слід обмежити.
Є кілька варіантів дієти в разі ЦД, але практично в домашніх умовах можна користуватись однією, котру легко пристосувати до лікування будь-якого хворого, виключаючи або додаючи окремі страви чи продукти.
Фізична активність
Фізична активність важлива для запобігання розвитку ЦД у пацієнтів із ПТГ, а також для контролю глікемії та пов’язаних із нею ускладнень ССЗ. Аеробні тренування та тренування з обтяженнями покращують дію інсуліну й рівень глюкози в плазмі, а також позитивно впливають на АТ, ліпідний профіль й інші фактори ризику ССЗ. При цьому необхідні регулярні фізичні вправи. Комбінація аеробних і силових тренувань забезпечує краще поліпшення глікемічного контролю, ніж будь-який інший тип тренування. У проспективних когортних дослідженнях було також показано, що фізичні вправи пов’язані з поліпшенням результатів лікування ССЗ і зниженням загальної смертності в пацієнтів із ЦД та осіб із ПТГ.
Куріння
Оскільки куріння підвищує ризик розвитку ЦД, ССЗ і передчасної смерті, його слід уникати. Відмова від куріння знижує ризик ССЗ. Людям із ЦД, які курять, має бути запропонована структурована програма відмови від куріння, включно з фармакологічною підтримкою.
Зниження ваги
Більшість європейців із ЦД страждають на ожиріння, тому контроль ваги вважається центральним компонентом модифікації способу життя. Без втручань щодо контролю маси тіла складно домогтися значного поліпшення перебігу ЦД і ССЗ. Дослідження Look AHEAD оцінило вплив довгострокової втрати ваги на глікемію та профілактику ССЗ у разі ЦД. Через рік пацієнти, в яких проводилась інтенсивна корекція способу життя, показали в середньому втрату ваги на 8,6%, значно нижчий рівень HbA1c і зменшення кількох факторів ризику ССЗ. Ці переваги зберігалися через 4 роки. Проте жодної різниці щодо ССЗ не було помічено між групою інтенсивного втручання й контрольною групою, тому дослідження було припинено. У пацієнтів з ожирінням баріатрична хірургія може забезпечити тривалу втрату ваги; було показано, що цей метод знижує частоту виникнення ЦД і смерті.
Слід зазначити, що, як продемонструвало кластерне рандомізоване клінічне дослідження з вивчення ремісії при діабеті (DiRECT), у пацієнтів із ЦД тривалістю до 6 років можна досягти значного покращення перебігу захворювання шляхом зниження маси тіла, котре досягається за допомогою заснованої на фактичних даних програми структурованого контролю ваги (проводиться на рівні первинної медичної допомоги). Втручання являло собою початкову фазу загальної дієти з використанням низькоенергетичної дієтичної формули (близько 830 ккал/добу, 59% вуглеводів, 13% жирів, 26% білків, 2% клітковини) з подальшою структурною зміною їжі та щомісячними візитами для довгострокової підтримки досягнутого результату. Майже в половини (46%) учасників у групі втручання спостерігалася ремісія діабету через 12 міс порівняно з 4% у контрольній групі.
Терапія протидіабетичними препаратами
Стратифікація цукрознижувальної терапії проводиться залежно від вихідного рівня HbA1c при встановленні діагнозу ЦД. Залежно від того, наскільки вихідний рівень перевищує індивідуальний цільовий показник HbA1c конкретного пацієнта, на старті лікування можуть бути обрані або монотерапія, або комбіноване лікування. Якщо вихідний показник HbA1c перевищує індивідуальний цільовий рівень пацієнта не більш ніж на 1%, показана монотерапія; при перевищенні цільових цифр на 1,0-2,5% рекомендована подвійна терапія відразу зі старту; якщо йдеться про різницю в понад 2,5%, можна розпочати лікування з потрійної терапії або інсулінотерапії.
Залежно від домінуючої клінічної ситуації, наявності ускладнень, супутньої патології проводиться персоналізація вибору цукрознижувальних препаратів.
За наявності ризику ССЗ як додатковий цукрознижувальний засіб слід призначити один із препаратів із наявною доказовою базою щодо зниження ризику серйозних серцево-судинних подій та/або кардіоваскулярної смерті.
Нині перевагу слід віддавати комбінації метформіну з агоністами рецепторів глюкагоноподібного пептиду‑1 (арГПП‑1) – екзенатиду та ліраглутиду, а також із селективними інгібіторами натрій-глюкозного котранспортера 2 типу (ІНГКТ‑2) / гліфлозинами (емпагліфлозін і канагліфлозін), які мають доведені серцево-судинні переваги в пацієнтів з атеросклеротичним ССЗ.
Рекомендації ґрунтуються на результатах дослідження LEADER, у якому на великому клінічному матеріалі (9340 пацієнтів із ЦД 2 типу та високим серцево-судинним ризиком) переконливо продемонстровано зниження ризику первинної комбінованої кінцевої точки (серцево-судинна смерть, нефатальний ІМ, нефатальний мозковий інсульт), зниження ризику серцево-судинної смерті, зниження композитної кінцевої точки (коронарна реваскуляризація, нестабільна стенокардія, госпіталізація з приводу СН) у групі пацієнтів, які отримували ліраглутид (арГПП‑1) порівняно з плацебо.
Результати інших багатоцентрових клінічних досліджень, зокрема EMPA-REG OUTCOME, показали, що ІНГКТ‑2 емпагліфлозин асоційований зі зниженням ризику 4-компонентної кінцевої точки (серцево-судинної смерті, нефатального ІМ, нефатального мозкового інсульту, госпіталізації з приводу нестабільної стенокардії) та 3-компонентної кінцевої точки (серцево-судинної смерті, нефатального ІМ, нефатального мозкового інсульту) в групі пацієнтів із ЦД, у тому числі у хворих із низьким/помірним або високим серцево-судинним ризиком.
У разі недосягнення цільових рівнів HbA1c або за наявності небажаних ефектів у застосовуваних препаратів слід призначити цукрознижувальні засоби з інших груп із доведеною серцево-судинною безпекою: інгібітори дипептидилпептидази‑4 (ІДПП‑4), тіазолідиндіони (ТЗД), препарати сульфонілсечовини (ПСС) останнього покоління в невеликих дозах, базальний інсулін.
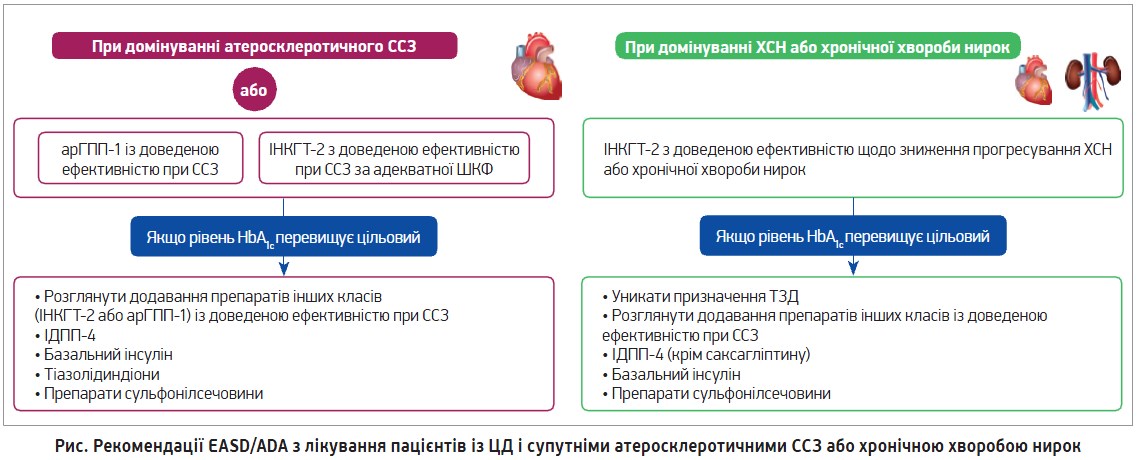
При встановленні діагнозу хронічної СН (ХСН) показане призначення препаратів із доведеними перевагами щодо ХСН. Обирати слід ІНГКТ‑2 із доведеними перевагами щодо ХСН при адекватній швидкості клубочкової фільтрації (ШКФ). Якщо цільових рівнів HbA1c досягти не вдається, необхідно інтенсифікувати терапію, додавши препарати інших груп із доведеною серцево-судинною безпекою (арГПП‑1 або представники інших класів: ІДПП‑4, крім саксагліптину, базальний інсулін, ПСС останнього покоління). При ХСН рекомендується уникати призначення ТЗД.
Отже, слід дотримуватися певних правил ведення хворих на ЦД 2 типу із серцево-судинними ускладненнями (рис.).
У пацієнтів із ССЗ у складі цукрознижувальної терапії рекомендується використовувати ІНГКТ‑2 або арГПП‑1, які мають доведені серцево-судинні переваги. В осіб із ХСН або високим ризиком її розвитку рекомендується використовувати в складі терапії ІНГКТ‑2. За наявності множинних факторів ризику перевагу має призначення ІНГКТ‑2 або арГПП‑1. При застосуванні комбінацій слід зважати на раціональність поєднання цукрознижувальних препаратів.
Контроль порушень ліпідного обміну
У хворих на ЦД часто спостерігається поєднане підвищення рівнів холестерину та тригліцеридів. Лікування гіперхолестеринемії – один із головних механізмів зниження серцево-судинного ризику в пацієнтів як з ЦД 2 типу, так і з ЦД 1 типу.
Усі пацієнти з ЦД віком понад 40 років незалежно від наявності факторів ризику й молодші пацієнти з хронічною хворобою нирок або множинними факторами ризику повинні отримувати терапію статинами з метою зниження рівня ліпопротеїнів низької щільності (ЛПНЩ).
У хворих на ЦД дуже високого ризику необхідно добиватися зниження рівня ЛПНЩ <1,4 ммоль/л або принаймні на 50% від вихідного. У пацієнтів із ЦД високого ризику цей показник становить <1,8 ммоль/л або слід прагнути зниження рівня ЛПНЩ принаймні на 50% від вихідного. У хворих на ЦД із недостатнім зниженням рівня ЛПНЩ на тлі статинотерапії рекомендується розглянути можливість призначення езетимібу чи блокатора пропротеїнової конвертази субтилізин/кексинового типу 9 (PCSK9).
Терапія фібратами у хворих на ЦД не сприяє зниженню серцево-судинних ускладнень.
Контроль артеріального тиску
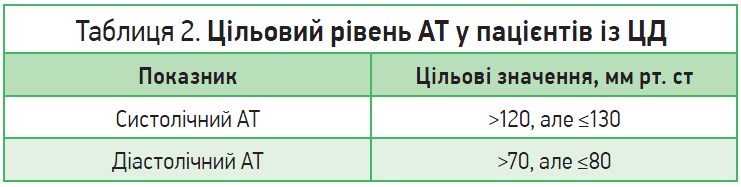
Параметри цільового АТ для пацієнтів із діабетом є такими: систолічний АТ – до 130 мм рт. ст., але не нижче 120 мм рт. ст.; діастолічний АТ – до 80 мм рт. ст., але не нижче 70 мм рт. ст., оскільки інакше тиск буде надмірно низьким, особливо в літніх людей (табл. 2).
Основні вимоги для медикаментозної терапії АГ при ЦД:
- перевага віддається інгібітору ангіотензинперетворювального ферменту (ІАПФ) або антагоністу рецепторів ангіотензину ІІ (АРА) в осіб із непереносимістю ІАПФ;
- часто потрібна комбінована медикаментозна терапія, тобто блокатор ренін-ангіотензин-альдостеронової системи (ІАПФ чи АРА) та блокатор кальцієвих каналів або сечогінний засіб; як перша лінія рекомендується комбінована терапія;
- комбінована терапія ІАПФ та АРА не рекомендується.
Прогноз
При ефективній терапії ЦД прогноз для життя хворих зазвичай відносно сприятливий. При неадекватному контролі глікемії, АТ і ліпідів у крові різко зростає ризик мікро- й макросудинних ускладнень ЦД. Понад 55% хворих на ЦД помирають від ІМ. У проспективному епідеміологічному дослідженні UKPDS показано, що зниження рівня середнього HbA1c на кожен 1% у пацієнтів з уперше виявленим ЦД забезпечує зменшення загальної частоти смерті й ускладнень ЦД у середньому на 21%. При цьому смертність від ЦД знижується на 21%, частота ІМ – на 14%, мікросудинних ускладнень – на 37%.
Висновки
Згідно зі світовим досвідом, лікування ЦД має розпочинатися якомога раніше. Якщо людина тривалий час (роками) житиме з високим рівнем глюкози в крові, не контролювати процес, то можуть запуститися реакції метаболічної пам’яті, змінити які згодом дуже складно, а то й узагалі неможливо. Тому призначення медикаментозної терапії – не найголовніше з того, що має можливість зробити сімейний лікар для хворого. Досить значимою видається освітня діяльність.
У сучасних посібниках медикаментозне втручання регламентується виходячи зі скринінгових даних рівня глікозильованого гемоглобіну. Проте чим раніше відновити контроль над глікемією й метаболізмом жиру, тим більші надії можемо покладати на те, що лікування пацієнта буде більш ефективним і безпечним. Під контролем хвороби розуміють не тільки кваліфіковану діяльність лікаря, а й фізичні, розумові та вольові зусилля з боку хворого, оскільки дієва терапія ЦД 2 типу неможлива без інтенсивного залучення пацієнта, без його найвищої мотивованості.