26 березня, 2020
Імунобіологічні препарати крові в акушерстві: міждисциплінарний діалог
19-20 вересня в Києві за підтримки компанії «Біофарма Плазма» відбулась науково-практична конференція з міжнародною участю «Актуальні питання промислового виробництва препаратів крові». Захід був присвячений питанням патології вагітності, резус-конфлікту та сучасним методам профілактики й лікування цих станів за допомогою препаратів крові та збалансованих електролітних розчинів, що виготовляються в Україні.
 Про погляд на проблему резус-конфлікту у розрізі міжнародних рекомендацій доповіла заступник головного лікаря з акушерсько-гінекологічної допомоги Вінницької обласної клінічної лікарні ім. М.І. Пирогова, керівник обласного перинатального центру, кандидат медичних наук Інна Леонідівна Кукуруза.
Про погляд на проблему резус-конфлікту у розрізі міжнародних рекомендацій доповіла заступник головного лікаря з акушерсько-гінекологічної допомоги Вінницької обласної клінічної лікарні ім. М.І. Пирогова, керівник обласного перинатального центру, кандидат медичних наук Інна Леонідівна Кукуруза.
Вона зазначила, що профілактика ізоімунізації за часом її проведення поділяється на декілька категорій.
Антенатальна специфічна профілактика, що виконується за наступних умов:
- загроза викидня після 12 тиж гестації;
- повний або частковий самовільний викидень на терміні ≥12 тиж гестації;
- планове хірургічне переривання вагітності незалежно від терміну гестації;
- планове медикаментозне переривання вагітності незалежно від терміну гестації;
- після проведення інвазивної пренатальної діагностики (амніоцентез, біопсія хоріона, кордоцентез);
- накладення швів на шийку матки (при істміко-цервікальній недостатності);
- трофобластична хвороба;
- трансфузія резус-позитивних тромбоцитів;
- внутрішньоматкові процедури;
- допологова кровотеча незалежно від терміну вагітності;
- зовнішній поворот плода на голівку (включаючи спробу);
- редукція одного ембріона у програмах допоміжної репродукції;
- будь-які абдомінальні травми (пряма, непряма, гостра, тупа, відкрита, закрита);
- позаматкова вагітність;
- антенатальна загибель плода.
До 12 тиж гестації вводять 75 мкг або 100 мкг, 120 мкг, 125 мкг (375 МО, 500 МО, 600 МО, 625 МО) антирезусного імуноглобуліну внутрішньом’язово (IА).
Після 12 тиж гестації слід призначати стандартну разову дозу 300 мкг (1500 МО) (IIB).
АнтиRh0(D)імуноглобулін 300 мкг (1500 МО) має бути призначений резус-негативним несенсибілізованим жінкам у термін 28 тиж гестації, коли тип крові плода є невідомим або позитивним (А).
Постнатальна профілактика:
- анти-Rh0(D)-імуноглобулін у дозі 300 мкг (1500 МО) внутрішньом’язово призначається протягом 72 год після пологів у несенсибілізованої резус-негативної жінки, що народила резус-позитивну дитину (IA);
- додаткова доза вводиться у випадку очікуваної фето-материнської кровотечі (ФМК) об’ємом >30 мл (15 мл еритроцитів плода) (IA).
Якщо жінка не отримала профілактику протягом 72 год, слід призначити її, щойно така потреба буде виявлена (протягом 28 днів) (IIIB);
- якщо резус-негативна мати не отримала післяпологову профілактику після народження резус-позитивної дитини, частота сенсибілізації при подальших вагітностях становить 12-16% порівняно з 0,8-1,9% у матерів, які отримали профілактику;
- існує недостатньо доказів для рутинного проведення тестування на ФМК після пологів (тест Клейхауера та протокова цитометрія).
Однак за наявності таких факторів, як травма живота, відшарування плаценти, передлежання із кровотечою, зовнішній оберт плода, дане дослідження рекомендоване (додатково анти-Rh0(D)-імуноглобулін 10 мкг на 0,5 мл еритроцитів плода) (IIIC).
Профілактика за відсутності імунізації під час вагітності проводиться шляхом внутрішньом’язового введення 1 дози (300 мкг) анти-Rh0(D)-імуноглобуліну:
- планово – у термін гестації 28-32 тиж;
- у разі появи вищезазначених станів вагітності – до 28 тиж;
- у термін гестації <13 тиж доза анти-Rh0(D)-імуноглобуліну становить 75 мкг, у термін >13 тиж – 300 мкг.
Дані рекомендації затверджені наказом МОЗ від 31.12.2004 р. № 676 як клінічний протокол з акушерської та гінекологічної допомоги «Ведення вагітності у жінок з імунними конфліктами».
Що стосується закордонних настанов, то рекомендації Товариства акушерів та гінекологів Канади (SOGC) стверджують, що резус-негативній несенсибілізованій жінці слід вводити анти-Rh0(D)-імуноглобулін у дозі 300 мкг у випадку:
- викидня, загрози переривання, ектопічної вагітності, амніоцентезу, біопсії хоріону після 12 тиж гестації;
- після викидня або загрози переривання вагітності, або індукованого аборту протягом перших 12 тиж гестації слід призначати мінімум 120 мкг анти-Rh0(D)-імуноглобуліну;
- рутинна профілактика на 28-му тиж гестації;
- у перші 72 год після пологів при народженні резус-позитивної дитини.
У рекомендаціях Американського коледжу акушерів та гінекологів (ACOG) «Запобігання Rh(D)-алоімунізації» зазначається, що за будь-яких обставин, коли еритроцити плода можуть потрапити в організм матері, слід вводити профілактичну дозу анти-D-імуноглобуліну 300 мкг. Така доза забезпечує захист проти сенсибілізації для 30 мл крові плода або 15 мл фетальних еритроцитів. Рутинну ж профілактику слід проводити на 28-му тижні гестації. Постнатальна профілактика анти-Rh0(D)-імуноглобуліном у дозі 300 мкг є стандартом у перші 72 год після пологів для резус-негативних жінок, що народили резус-позитивних дітей.
Експерти Британського комітету зі стандартизації в гематології (BCSH, 2014) вважають, що однократний режим введення анти-D-імуноглобуліну 1500 МО у період між 28-м і 30-м тижнями вагітності є більш доцільним у плані ефективності та фармакоекономічності. Усі несенсибілізовані Rh-негативні вагітні жінки мають підлягати профілактиці в дозі 300 мкг анти-Rh0(D)-імуноглобуліну.
Акушери-гінекологи та трансфузіологи Італії проводять антенатальну профілактику всім неімунізованим Rh-негативним жінкам на терміні гестації 28 тиж анти-Rh0(D)-імуноглобуліном у дозі 1500 МО (300 мкг) (1В); на терміні <12 тиж – у дозі 250-600 МО (50-120 мкг).
На вітчизняному фармацевтичному ринку препарат, який застосовують для профілактики резус-конфлікту, представлений Імуноглобуліном антирезус Rh0(D) людини (ТОВ «Біофарма Плазма»), що має стандартне дозування 1500 МО (300 мкг).
? Чи є препарати плазми безпечними в застосуванні, адже це препарати крові?
Препарати ТОВ «Біофарма Плазма» є цілком безпечними, оскільки виготовляються з дотриманням суворих стандартів:
• плазма для сировини препарату тричі перевіряється на відсутність ВІЛ та вірусів гепатиту В і С (на етапах збору плазми, при потраплянні на завод і у процесі виробництва);
• виготовлення препарату відбувається за суворого дотримання температурного режиму;
• у процесі виробництва плазма не лише тестується на відсутність вірусів методом імуноферментного аналізу, а й перевіряється на відсутність вірусної ДНК методом ПЛР;
• проводиться обов’язкова обробка плазми з метою вірусної інактивації.
У результаті виходить якісна й безпечна продукція, що підтверджується лабораторіями МОЗ України та провідними лабораторіями ЄС.
 Серію доповідей стосовно актуальності профілактики резус-конфліктної вагітності в Україні розпочав своїм виступом заступник директора ДУ «Інститут педіатрії, акушерства і гінекології ім. акад. О.М. Лук’янової НАМН України» (м. Київ), керівник відділення проблем здоров’я жінки фертильного віку, доктор медичних наук, професор Василь Васильович Подольський.
Серію доповідей стосовно актуальності профілактики резус-конфліктної вагітності в Україні розпочав своїм виступом заступник директора ДУ «Інститут педіатрії, акушерства і гінекології ім. акад. О.М. Лук’янової НАМН України» (м. Київ), керівник відділення проблем здоров’я жінки фертильного віку, доктор медичних наук, професор Василь Васильович Подольський.
Відомо, що у патогенезі розвитку ізосенсибілізації при резус-конфліктній вагітності є резус-позитивний плід та резус-негативна мати.
Ланцюжок патогенетичних змін при виникненні ізосенсибілізації має такий вигляд:
- проникнення еритроцитів плода у кровотік матері;
- синтез антитіл до еритроцитів плода класу IgM (не проникають через плаценту);
- утворення антитіл до еритроцитів плода класу IgG (легко проникають через плаценту, синтезуються через 3 міс);
- зв’язування антитіл з еритроцитами плода;
- пошкодження мембрани та руйнування еритроцитів з утворенням непрямого білірубіну;
- розвиток гепато- і спленомегалії (печінка й селезінка беруть участь в утилізації зруйнованих еритроцитів);
- розвиток анемії плода, внутрішньоутробної гіпоксії та, власне, гемолітичної хвороби плода та новонародженого (ГХПН).
Згідно з даними статистики, за 2018 р. в Україні зареєстровано 2691 випадок ГХПН, що становить 1 випадок на 117 пологів. Кожна 7-ма вагітна знаходиться в зоні ризику.
? Яким чином відбувається материнська алоімунізація?
Імунізація жінки може настати під час вагітності й пологів. Для вироблення анти-Rh0(D)-антитіл необхідно потрапляння у кровотік матері від 0,1 до 250 мл D-позитивних еритроцитів плода. Частота допологової первинної ізоімунізації протягом першої резус-несумісної вагітності становить <1%.
Під час вагітності еритроцити плода проникають через плаценту:
- у 5% вагітних протягом I триместру;
- у 47% вагітних протягом III триместру;
- при проникненні крові плода в систему кровообігу матері під час пологів.
До факторів ризику ізоімунізації відносяться:
- позаматкова вагітність – 1%;
- вагітність доношеного терміну до розродження – 2%;
- амніоцентез – 3%;
- самовільний викидень – 4%;
- медичний аборт – 5%;
- пологи (за сумісності по АВО-системі) – 16%.
Діагностувати гемолітичну хворобу плода на антенатальному етапі дозволяють неінвазивні та інвазивні методи:
- неінвазивні – УЗД плода (набрякова форма); допплерографія (визначення пікової систолічної швидкості кровотоку фетальної середньої мозкової артерії);
- інвазивні (лише за наявності показань) – забір фетальної крові та гематологічне обстеження.
? Чи можливо уникнути резус-конфлікту за наявності факторів, що йому сприяють?
ГХПН практично подолали в економічно розвинутих країнах завдяки досягненню 100% рівня профілактики. Натомість в Україні за останні три роки спостерігається зростання захворюваності на ГХПН. Єдиним способом профілактики розвитку ізоімунізації є анте- й постнатальне введення анти-D-імуноглобуліну. Для вирішення цього питання необхідно 75 тис. доз антирезусного імуноглобуліну (300 мкг) (згідно з рекомендаціями ВООЗ – найвищий рівень доказовості).
Антенатальна профілактика проводиться шляхом внутрішньом’язового введення 1 дози (300 мкг) анти-Rh0(D)-імуноглобуліну планово – у терміні 28-32 тиж, у разі появи симптомів загрози переривання вагітності – до 28 тиж. Постнатальна профілактика здійснюється при народженні Rh-позитивної дитини: протягом перших 72 год внутрішньом’язово вводиться 1 доза (300 мкг) анти-Rh0(D)-імуноглобуліну.
Протипоказання до ізоімунізації:
- резус-позитивні породіллі, а також резус-негативні породіллі, що сенсибілізовані до антигену Rh0(D), у сироватці крові яких виявлено резус-антитіла;
- резус-негативні жінки, сенсибілізовані до антигену Rh0(D), у плазмі яких виявлені резус-антитіла;
- особи, які мають в анамнезі тяжкі алергічні реакції на введення білкових препаратів крові людини;
- при селективному дефіциті IgА за умови наявності антитіл проти IgА;
- у випадку тяжкої тромбоцитопенії та інших порушень гемостазу.
За відсутності вищеописаних протипоказань та наявності факторів ризику ізоімунізації препарат Біовен моно 5% має бути введений у рекомендованих дозах, що затверджено міжнародними стандартами. Це дає можливість уникнути резус-конфлікту й сприяє збереженню імунного гомеостазу матері та плода.
 У продовження теми резус-конфлікту виступила директор Центру науково-доказової медицини, професор кафедри акушерства, гінекології та репродуктології Українського державного інституту репродуктології Національної медичної академії післядипломної освіти ім. П.Л. Шупика (м. Київ), доктор медичних наук Олена Миколаївна Борис.
У продовження теми резус-конфлікту виступила директор Центру науково-доказової медицини, професор кафедри акушерства, гінекології та репродуктології Українського державного інституту репродуктології Національної медичної академії післядипломної освіти ім. П.Л. Шупика (м. Київ), доктор медичних наук Олена Миколаївна Борис.
Вона зазначила, що, згідно з даними статистики, резус-позитивними є близько 85% людей європеоїдної раси, резус-негативними, відповідно, – 15%. Ризик резус-конфлікту під час вагітності виникає у пар із резус-негативною матір’ю та резус-позитивний батьком. Мінімальний об’єм крові, який здатний викликати ізоімунізацію, становить 0,1 мл.
В Україні профілактика резус-конфлікту проводиться згідно з наказом МОЗ № 676 і включає наступні заходи.
Профілактика Rh-сенсибілізації у допологовому періоді:
- за відсутності імунізації вагітної вводиться 1 доза (300 мкг) анти-Rh0(D)-імуноглобуліну внутрішньом’язово, застосування якого показано під час вагітності, на терміні 28-32 тиж;
- у випадку появи симптомів загрози переривання вагітності – у термін до 28 тиж;
- після амніоцентезу, біопсії хоріону, видалення пухирного заносу, при втраті вагітності після застосування допоміжних репродуктивних технологій.
Профілактика Rh-сенсибілізації у післяпологовому періоді:
- лише при народженні Rh-позитивної дитини;
- протягом перших 72 год після пологів вводиться 1 доза анти-Rh0(D)-імуноглобуліну (300 мкг) внутрішньом’язово.
Ведення неімунізованих вагітних:
- визначення титру антитіл при взятті на облік з вагітності й у термін 28 тиж;
- при виявленні на будь-якому терміні вагітності анти-Rh0(D)-антитіл пацієнтку слід вести як таку, що має резус-імунізацію;
- за відсутності ізоімунізації вагітній вводять анти-Rh0(D)-імуноглобулін на 28-му тижні гестації;
- якщо у термін 28 тиж проводилась профілактика анти-Rh0(D)-імуноглобуліном, то визначення антитіл у крові вагітної не має клінічного значення.
Ведення Rh-імунізованих (сенсибілізованих) вагітних:
- неінвазивні методи оцінки тяжкості стану плода;
- ультразвукова діагностика (набрякова форма гемолітичної хвороби новонароджених);
- за відсутності водянки немає достовірних критеріїв, які могли б вказувати на ознаки тяжкої анемії у плода.
? Який препарат для ізоімунізації доступний в Україні?
На українському фармацевтичному ринку такий препарат представлений Імуноглобуліном антирезус Rh0(D) людини (ТОВ «Біофарма Плазма»):
- діюча речовина – специфічні антитіла до анти-Rh0(D) 300 мкг; титр антитіл до анти-Rh0(D) 1:2000;
- допоміжні речовини – гліцин (глікокол, кислота амінооцтова), натрію хлорид;
- форма випуску: розчин для ін’єкцій;
- несумісність: не допускається змішування препарату в одному шприці з будь-якими іншими лікарськими засобами;
- умови зберігання: в сухому, захищеному від світла місці при температурі від 2 до 8 °C;
- упаковка: по 1 та 2 мл (300 мкг імуноглобуліну при титрі антитіл 1:2000) в ампулі, по 1, 3, 5 ампул в упаковці;
- препарат заборонено вводити новонародженим.
? Коли потрібно призначати імуноглобулін?
- вагітним на 28-му тижні гестації;
- обов’язкове введення ще однієї дози (300 мкг) протягом 72 год після пологів, якщо новонароджений має резус-позитивний статус;
- для проведення профілактики у післяпологовому періоді протягом 72 год після розродження;
- при штучному перериванні вагітності у термін >13 тиж доцільне введення однієї дози; якщо ж вагітність була перервана у період <13 тиж, можливе одноразове введення мінімальної дози імуноглобуліну (50 мкг);
- при викидні та загрозі викидня – на будь-якому терміні гестації;
- при проведенні амніоцентезу або при травмах органів черевної порожнини у ІІ і/або І триместрі вагітності – введення однієї дози препарату безпосередньо після закінчення операції;
- при проведенні амніоцентезу або при травмах органів черевної порожнини необхідне введення препарату в період 13-18 тиж гестації й додатково 300 мкг (1 ампула) – у період 26-28 тиж.
Особливості застосування препарату Імуноглобулін антирезус Rh0(D) людини:
- вводиться по 300 мкг (1 ампула) внутрішньом’язово одноразово;
- заборонено вводити препарат внутрішньовенно;
- пацієнтки після отримання препарату мають перебувати під наглядом медпрацівника протягом 30 хв;
- перед застосуванням препарат має бути витриманий близько 2 год при кімнатній температурі (20-22 °C);
- не допускається зберігання препарату у відкритій ампулі;
- імунізацію жінки живими вакцинами слід проводити не раніше ніж через 3 міс після введення Імуноглобуліну антирезус Rh0(D) людини.
Препарат Імуноглобулін антирезус Rh0(D) людини виробництва ТОВ «Біофарма Плазма» відповідає всім міжнародним стандартам і за якістю стоїть в одному ряду з іноземними препаратами цієї групи, такими як Імуноро Кедріон (Італія), КамРОУ (Ізраїль) та Grifols Therapeutics (США).
 Головний спеціаліст із питань акушерської реанімації департаменту охорони здоров’я м. Києва, завідувач курсу тематичного удосконалення з акушерської анестезіології та реанімації, заслужений лікар України, професор кафедри акушерства, гінекології та репродуктології Національної медичної академії післядипломної освіти ім. П.Л. Шупика, доктор медичних наук Руслан Опанасович Ткаченко зупинився на особливостях інфузійної терапії тяжкої прееклампсії.
Головний спеціаліст із питань акушерської реанімації департаменту охорони здоров’я м. Києва, завідувач курсу тематичного удосконалення з акушерської анестезіології та реанімації, заслужений лікар України, професор кафедри акушерства, гінекології та репродуктології Національної медичної академії післядипломної освіти ім. П.Л. Шупика, доктор медичних наук Руслан Опанасович Ткаченко зупинився на особливостях інфузійної терапії тяжкої прееклампсії.
Прееклампсія – це розвиток артеріальної гіпертензії після 20-го тижня вагітності у жінки, артеріальний тиск якої до цього часу був у нормі, або посилення артеріальної гіпертензії, яка існувала до 20-го тижня вагітності, із супутньою протеїнурією і/або ознаками ураження інших органів та систем.
Епідеміологія прееклампсії на сьогодні виглядає наступним чином:
- прееклампсія відзначається у 2-8% усіх вагітностей, що становить у світовій популяції 10 млн випадків щорічно;
- 76 тис. жінок помирають від прееклампсії щорічно (210 осіб щодня);
- 500 тис. дітей, народжених від матерів із прееклампсією, помирають щорічно (1380 щодня);
- перинатальна захворюваність варіює від 463 до 780‰.
До фатальних ускладнень тяжкої прееклампсії відносять: крововилив у мозок, наднирники, набряк мозку та легень, відшарування плаценти, розшаровуючу аневризму аорти, субкапсулярний крововилив у печінку, синдром дисемінованого внутрішньосудинного згортання крові, HELLP-синдром (гемоліз, підвищення активності печінкових ферментів і тромбоцитопенія).
Останнім часом стало приділятися більше уваги питанню ураження ендотелію судин та водно-електролітного дисбалансу як причинам розвитку прееклампсії. Патогенетичний ланцюг цих порушень можна відобразити наступним чином:
- тотальне ураження ендотелію судин, результатом якого є збільшення його проникності, у тому числі й для великих молекул альбуміну;
- вихід альбуміну із судинного русла в інтерстиціальний простір і його проникнення через нирковий фільтр, що супроводжується альбумінурією (протеїнурія – один із основних симптомів прееклампсії);
- втрати білка плазми крові призводять до зниження онкотичного тиску крові, при цьому вода активно виходить з судинного русла слідом за альбуміном, накопичуючись в інтерстиціальному просторі, що клінічно проявляється набряками, у тому числі генералізованими.
Таким чином, у пацієнток із прееклампсією спостерігається асоційоване порушення водно-електролітного балансу, за якого одночасно із внутрішньосудинною дегідратацією відбувається позасудинна гіпергідратація.
Для корекції порушення водно-електролітного балансу існують два шляхи:
- підвищення онкотичного тиску плазми крові за рахунок інфузії альбуміну 20-25% (показанням до його введення є рівень альбуміну в плазмі крові <25 г/л);
- призначення осмотично-активних препаратів (наприклад, реосорбілакту), що дозволяє підвищити осмолярність плазми крові й запобігає втратам води із судинного русла, а також сприяє поверненню її в судинне русло.
Препарат Альбумін-Біофарма підвищує онкотичний тиск плазми крові, запобігає утворенню онкотичних набряків та втраті рідини із судинного русла. На фоні його застосування має місце зниження смертності у пацієнтів з опіками, перитонітом, септичним шоком, після парацентезу при цирозі та напруженому асциті, що значно підвищує виживаність хворих і покращує їхній прогноз.
Згідно із клінічною настановою з акушерської допомоги «Гіпертензивні розлади під час вагітності, пологів та в післяпологовому періоді» (2019), доцільно дотримуватися принципу малооб’ємної інфузійної терапії, що впливає на перерозподіл рідини інтерстиціального простору без введення значних об’ємів інфузійного розчину. З цією метою слід використовувати 6% розчин сорбітолу в електролітному розчині (реосорбілакт).
Механізм дії розчину реосорбілакту робить його призначення у пацієнток із прееклампсією абсолютно виправданим. Це зумовлено наступними особливостями препарату:
викликає дилатацію пре- і посткапілярних сфінктерів, що знижує гідростатичний тиск;
має невелику осмолярність (900 мосм/л) і поліпшує реологію крові;
ефективний у невисоких дозах – рекомендовано 3-6 мл/кг/добу (200-400 мл/добу) упродовж 7 днів.
 Питанню імунокорекції у вагітних з антифосфоліпідним синдромом присвятив свою доповідь головний лікар Київського міського пологового будинку № 5, кандидат медичних наук Дмитро Олександрович Говсєєв.
Питанню імунокорекції у вагітних з антифосфоліпідним синдромом присвятив свою доповідь головний лікар Київського міського пологового будинку № 5, кандидат медичних наук Дмитро Олександрович Говсєєв.
Антифосфоліпідний синдром (АФС) – хронічний вазооклюзивний процес, що виникає внаслідок рецидивуючого тромбоутворення у дрібних судинах на фоні циркуляції в крові антифосфоліпідних антитіл (АФА). Питома вага АФС в етіології передчасних пологів, звичного невиношування, порушення імплантації становить 10-35%. Доповідач зауважив, що вагітні з АФС піддаються підвищеному ризику розвитку прееклампсії (особливо ранньої, тяжкої форми), внутрішньоутробної затримки росту та передчасних пологів. Рутинне лікування вагітних із АФС спрямоване на профілактику тромбозу та є частково успішним. Останні дані стосовно етіопатогенезу АФС свідчать, що виникненню ускладнень сприяє не лише тромбоз дрібних судин, а й активація прозапальних факторів, зумовлена розвитком запального процесу у стінці судини.
На підставі цього автор та його команда провели клінічне дослідження, мета якого полягала в оцінці показників ефективності традиційного лікування АФС у відповідності до чинного протоколу та його комбінації із введенням внутрішньовенних імуноглобулінів у пацієнток зі звичним невиношуванням в анамнезі. Крім того, аналізувався перебіг періоду адаптації передчасно народжених дітей у цих досліджуваних. До І групи увійшло 28 жінок, які отримували стандартну терапію АФС (відповідно до наказу МОЗ України від 08.10.2007 № 626); до ІІ групи – 25 осіб, яким разом зі стандартним лікуванням застосовано Біовен моно 5%. Контрольна група включала 26 жінок зі звичним невиношуванням без АФС. У ході дослідження усім пацієнткам проводився контроль рівня АФА класу IgG до β‑2-глікопротеїну 1, параметрів імунного статусу (IgG, IgМ, IgА), цитокінів, імунорегуляторного індексу (CD4/CD8), глюкози, лактату, буферних основ, прокальцитоніну.
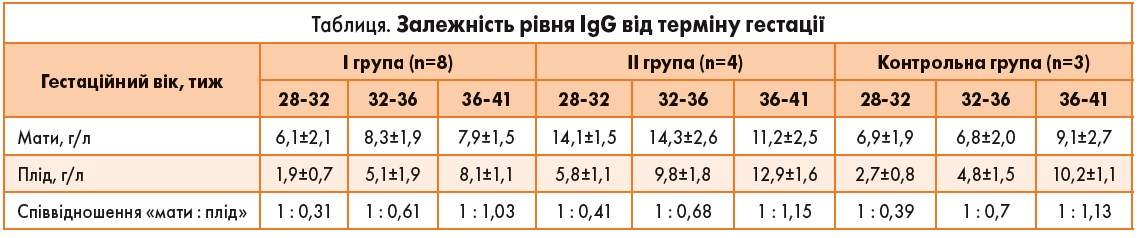
Дослідження показало, що штучне підвищення рівня IgG у матері шляхом використання Біовен моно 5% (ТОВ «Біофарма Плазма») дозволяє досягти цільового рівня IgG у плода залежно від терміну гестації (таблиця).
Поєднана терапія АФС із використанням Біовен моно 5% збільшує «потік» IgG від матері до плода, сприяючи зменшенню клінічних та лабораторних ознак АФС. Досягнення у плода рівня IgG >4 г/л є прогностично сприятливим критерієм для кращого періоду адаптації новонародженого.
Перевагою застосування Біовен моно 5% для новонароджених є наступні його властивості:
- забезпечення імунного гомеостазу;
- запобігання розвитку автоімунної продукції антитіл завдяки послабленню запальної автореактивності (інактивація автореактивних IgG при автоімунних захворюваннях);
- захист від багатьох вірусних, бактеріальних, грибкових та паразитарних інфекцій;
- полегшення зв’язування з патогенами, а також посилення нейтралізації та аглютинації інфекційних збудників.
Резюмуючи результати конференції, слід зазначити, що сучасні препарати крові широко використовуються в акушерстві, а отже, мають відповідати найвищим стандартам якості та безпеки. Препарати ТОВ «Біофарма Плазма» цілком задовольняють даним вимогам і можуть бути застосовані за наявності показань для їх використання.
Підготувала Іванна Садівська
Тематичний номер «Акушерство, Гінекологія, Репродуктологія» № 4 (36), грудень 2019 р.