30 червня, 2016
Лечение и профилактика фибрилляции предсердий: возможности терапии «против течения»
По материалам VI Научно-практической конференции Ассоциации аритмологов Украины (19-20 мая 2016 года, г. Киев)
Upstream-терапия (от англ. upstream – против течения) – это профилактика развития и рецидивирования фибрилляции предсердий (ФП) путем назначения препаратов, действие которых направлено на предупреждение или замедление ремоделирования миокарда вследствие артериальной гипертензии (АГ), сердечной недостаточности (СН), процессов воспаления и фиброза. Иными словами, это терапия против течения заболеваний, вызывающих морфологические и электрофизиологические изменения, которые становятся субстратом развития и прогрессирования ФП. Возможности upstream-терапии активно обсуждались ведущими украинскими специалистами в формате лекций и мастер-классов.
 Основные принципы upstream-терапии озвучил в своем докладе сопредседатель Ассоциации аритмологов Украины, руководитель отдела нарушений ритма сердца ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Олег Сергеевич Сычев.
Основные принципы upstream-терапии озвучил в своем докладе сопредседатель Ассоциации аритмологов Украины, руководитель отдела нарушений ритма сердца ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Олег Сергеевич Сычев.
Патогенетически обоснованная терапия и профилактика ФП включает назначение ингибиторов ангиотензинпревращающего фермента (ИАПФ), блокаторов рецепторов ангиотензина (БРА), антагонистов альдостерона, статинов и омега-3 полиненасыщенных жирных кислот (ПНЖК) – препаратов, которые не являются антиаритмическими по своему действию, но влияют на различные механизмы развития и поддержания аритмии при структурных заболеваниях сердца (рис. 1).
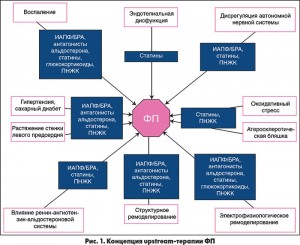
В европейских рекомендациях 2010 года по лечению и профилактике ФП upstream-терапия представлена в контексте первичной и вторичной профилактики. Для предотвращения новых случаев ФП у пациентов с АГ и гипертрофией левого желудочка (ЛЖ) или СН со сниженной фракцией выброса ЛЖ (ФВ ЛЖ) рекомендуются ИАПФ и БРА. Также доказан профилактический эффект статинов у больных, перенесших операцию коронарного шунтирования или ее комбинацию с вмешательствами на клапанах сердца.
В качестве вторичной профилактики ИАПФ и БРА рекомендуется назначать пациентам с пароксизмальной и рецидивирующей ФП, которые получают антиаритмическую терапию, если для их применения есть другие показания, например, АГ.
ИАПФ никогда не рассматривались как антиаритмические препараты, но на фоне их приема отмечается значительное снижение риска развития новых случаев ФП у пациентов с сердечно-сосудистой патологией – АГ, ишемической болезнью сердца (ИБС), СН. Также доказано, что ИАПФ, назначенные пациентам с ФП после кардиоверсии, оказывают эффект вторичной профилактики – достоверно сокращают частоту рецидивов аритмии на 45%, по данным метаанализа (M.P. Schneider et al., 2010). Кроме того, ИАПФ снижают риск внезапной аритмической смерти по причине желудочковых нарушений ритма, что положительно отражается на выживаемости больных. Этот эффект считается классовым, он обнаружен у различных ИАПФ. Одним из наиболее изученных является периндоприл, который обеспечивал эффективный контроль АГ в исследовании ASCOT, улучшал прогноз у пациентов с ИБС в исследовании EUROPA, снижал частоту инсультов в исследовании PROGRESS, оказывал влияние на ремоделирование миокарда и течение СН. В исследовании PREMIER терапия периндоприлом (2-8 мг/сут) и индапамидом (0,625-2,5 мг/сут) достоверно эффективнее уменьшала альбуминурию по сравнению с эналаприлом. А известно, что протеинурия и нарушение функции почек ассоциируются с худшим прогнозом у пациентов с АГ, повышают риск развития инсульта и тромбоэмболий. Высокая антигипертензивная эффективность препарата периндоприл (Периндоприл Сандоз) подтверждена нами в 12-недельном исследовании: достигнуто снижение офисного систолического артериального давления (САД) в среднем на 32 мм рт. ст. от исходного, диастолического АД (ДАД) – на 26 мм рт. ст.
Электрофизиологическое ремоделирование миокарда при ФП связано с изменением формы потенциала действия: он теряет плато и приобретает треугольную форму, в результате чего повышается возбудимость кардиомиоцитов. Препараты, задерживающие калий в клетке, восстанавливают плато потенциала действия и нормальную возбудимость миокарда (рис. 2).
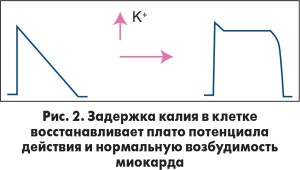
Такими средствами являются калийсберегающие диуретики или антагонисты альдостерона. Спиронолактон* – конкурентный антагонист альдостерона. Удобство этого препарата заключается в том, что таблетку 50 мг можно делить пополам, и это позволяет титровать дозу, начиная с 25 мг.
Еще один хорошо знакомый класс препаратов, в отношении которых доказано опосредованное влияние на механизмы аритмогенеза, – это статины. В исследовании AVID у пациентов с ИБС, которые принимали статины, достоверно реже регистрировали эпизоды желудочковой тахикардии и фибрилляции желудочков по сравнению с группой контроля (22 и 57% соответственно; р=0,003), причем этот результат не зависел от эффекта снижения уровня холестерина.
Существует теория относительно влияния статинов на ионные каналы клеточной мембраны кардиомиоцитов через модуляцию обмена жирных кислот. За счет этого достигается гиперполяризация мембраны и подавление патологической возбудимости и проводимости желудочков. Одним из самых мощных препаратов данного класса на сегодняшний день является розувастатин**.
Применение перечисленных препаратов для upstream-терапии ФП идеально вписывается в концепцию снижения общего сердечно-сосудистого риска, связанного с гиперактивацией ренин-ангиотензиновой системы (РАС), эндотелиальной дисфункцией и атеросклерозом.
 Старший научный сотрудник отдела нарушений ритма сердца и проводимости ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, кандидат медицинских наук Таисия Вячеславовна Гетьман прокомментировала порядок назначения upstream-терапии пациенту с ФП на клиническом примере.
Старший научный сотрудник отдела нарушений ритма сердца и проводимости ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, кандидат медицинских наук Таисия Вячеславовна Гетьман прокомментировала порядок назначения upstream-терапии пациенту с ФП на клиническом примере.
Мужчина, 81 год. Пароксизм ФП длительностью около 6 нед. Пациент не ощущает аритмию, она была выявлена случайно при очередном осмотре. СН с ФВ ЛЖ 42%. АД – 150/90 мм рт. ст.
Клиренс креатинина – 60,3 мл/мин. Частота сердечных сокращений (ЧСС) – 75-88 уд/мин.
В истории болезни пациента – АГ, стабильная стенокардия напряжения, перенесенный инфаркт миокарда. В настоящее время принимает ацетилсалициловую кислоту (АСК) 75 мг/сут и эналаприл по 5 мг 2 раза в сутки. При выборе дальнейшей тактики ведения пациента возникают следующие вопросы:
– восстанавливать или не восстанавливать синусовый ритм?
– нужна ли коррекция АД?
– нужно ли назначить оральный антикоагулянт, и какой при этом риск кровотечений?
Ответы заложены в европейских руководствах по ведению пациентов с ФП (2010), АГ (2013) и других рекомендательных документах. Поскольку симптомы ФП в нашем случае отсутствуют, пациент соответствует классу I по классификации Европейской ассоциации ритма сердца (EHRA). Контроль ЧСС должен быть начальным подходом к ведению больных пожилого возраста с ФП и невыраженной симптоматикой (1 балл по EHRA). Контроль ритма рекомендован при наличии симптоматики ФП (≥2 баллов по EHRA), несмотря на адекватный контроль ЧСС. Следовательно, для нашего пациента выбираем стратегию контроля ЧСС. Следующий вопрос – что с этой целью назначить?
Для снижения ЧСС у пациентов с СН и низкой ФВ ЛЖ, что имеет место в нашем случае, в качестве первой линии терапии рекомендованы β-блокаторы. Если монотерапия не обеспечивает достаточного контроля ЧСС, необходимо добавить к β-блокатору дигоксин.
Под контролем ЧСС следует понимать снижение ЧСС до <110 уд/мин в состоянии покоя (гибкий контроль) или до <80 уд/мин в состоянии покоя и <110 уд/мин при умеренных физических нагрузках (жесткий контроль). Оба подхода в рекомендациях Европейского общества кардиологов имеют одинаковый уровень доказательств. Дискуссии по этому вопросу продолжаются.
В пользу жесткого контроля свидетельствуют данные исследований о повышении общей смертности среди мужчин с АГ пропорционально величине ЧСС.
Следующий вопрос – как поступить в отношении уровня АД? Для лечения АГ у пациентов со стабильной стенокардией препаратами первой линии являются β-блокаторы и антагонисты кальция длительного действия. Также рекомендовано присоединять ИАПФ к β-блокатору у большинства пациентов с установленным диагнозом ИБС. Приоритетными ИАПФ для пациентов с ИБС являются периндоприл и рамиприл.
β-Блокаторы не только оказывают антиишемическое действие, но и обладают антиаритмическим потенциалом за счет угнетения проводимости и автоматизма. Кроме того, в контексте upstream-терапии β-блокаторы выступают в качестве мощных ингибиторов РАС, блокируя β1-рецепторы в юкстагломерулярном аппарате почек. Это вызывает гипотензивный эффект и угнетение образования ангиотензина II, который играет важную роль в прогрессировании сердечно-сосудистой патологии.
До каких цифр необходимо снижать АД? Ответ находим в европейских рекомендациях по лечению АГ (2013). У лиц старше 80 лет с исходным САД ≥160 мм рт. ст. рекомендуется снижать этот показатель до 150-140 мм рт. ст. при условии, что они находятся в хорошем физическом и психическом состоянии. Целевое ДАД <90 мм рт. ст. рекомендуется всегда, кроме пациентов с сахарным диабетом, которым рекомендован показатель <85 мм рт. ст. Однако значение 80-85 мм рт. ст. должно быть рассмотрено, если такой уровень безопасен и хорошо переносится.
Подбирая лечение нашему пациенту, нельзя игнорировать его преклонный возраст. Стратегии лечения АГ пациентов старшей возрастной группы изучались в исследовании HYVET (средний возраст участников – 83 года). В этом исследовании терапия комбинацией периндоприл + индапамид в течение 4 лет снижала общую смертность на 30%, частоту фатальных и нефатальных инсультов – на 21%, инсультов, которые привели к смерти, – на 39%, частоту случаев развития СН – на 64%.
Следующий вопрос – какую антикоагулянтную терапию назначить нашему пациенту для профилактики инсульта и системной тромбоэмболии? Прежде всего, оцениваем риск развития инсульта по шкале CHA2DS2-VASc. У пациента имеет место АГ, ИБС, перенесенный инфаркт миокарда, возраст старше 75 лет. Суммарно это 5 баллов по шкале CHA2DS2-VASc, что означает высокий риск развития инсульта. Риск кровотечений по шкале HAS-BLED составляет 2 балла, он обусловлен наличием АГ и преклонным возрастом. Это относительно низкий риск, однако следует помнить о том, что именно у пациентов старше 80 лет в ходе исследований отмечался повышенный риск кровотечений в первый год приема варфарина (E.M. Hylek et al., 2007). Более безопасной альтернативой может быть назначение новых оральных антикоагулянтов, но не всегда наши пациенты могут позволить себе такую терапию.Если пациент по каким-либо причинам (кроме высокого риска кровотечений) не может или отказывается принимать антикоагулянты, следует назначить антиагрегантную терапию АСК 75-100 мг/сут + клопидогрель 75 мг/сут (при невысоком риске кровотечений) или, что менее эффективно, – только АСК в дозе 75-325 мг/сут.
Таким образом, тщательная оценка индивидуальных факторов риска с учетом экспертных рекомендаций позволяет подобрать терапию основного заболевания, которая одновременно защищает пациента от прогрессирования ФП и связанных с аритмией осложнений.
 Старший научный сотрудник отдела нарушений ритма сердца и проводимости ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, кандидат медицинских наук Елена Николаевна Романова представила еще один пример подбора оптимальной терапии основного заболевания для пациента с ФП и перенесенным инсультом в анамнезе. Клинический случай хорошо демонстрирует, что пациента высокого риска может ничего не беспокоить. Мужчина 46 лет, рост 170 см, вес 102 кг, окружность талии 109 см. Курит. Жалоб не предъявляет. При прохождении профосмотра АД 150/100 мм рт. ст. Семейный анамнез: отец умер в 53 года от инсульта, мать умерла в 69 лет от инфаркта.
Старший научный сотрудник отдела нарушений ритма сердца и проводимости ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, кандидат медицинских наук Елена Николаевна Романова представила еще один пример подбора оптимальной терапии основного заболевания для пациента с ФП и перенесенным инсультом в анамнезе. Клинический случай хорошо демонстрирует, что пациента высокого риска может ничего не беспокоить. Мужчина 46 лет, рост 170 см, вес 102 кг, окружность талии 109 см. Курит. Жалоб не предъявляет. При прохождении профосмотра АД 150/100 мм рт. ст. Семейный анамнез: отец умер в 53 года от инсульта, мать умерла в 69 лет от инфаркта.
Уровень общего холестерина – 6,2 ммоль/л, холестерина липопротеидов низкой плотности – 4,2 ммоль/л, холестерина липопротеидов высокой плотности – 0,8 ммоль/л, триглицеридов – 2,1 ммоль/л. Глюкоза натощак – 5,1 ммоль/л, после нагрузочной пробы – 8,9 ммоль/л. Клиренс креатинина – 43 мл/мин.
По данным эхокардиографии: левое предсердие – 4,4 см, конечно-диастолический размер ЛЖ – 5,3 см, толщина межжелудочковой перегородки – 1,3 см, ФВ ЛЖ – 65%.
При более подробном опросе пациент сообщает о редких приступах сердцебиения (1-2 за 3-5 мес), которые раньше проходили спонтанно, но в последнее время участились и стали более длительными. Один из приступов стал причиной вызова бригады скорой помощи. На ЭКГ была зафиксирована ФП. После успешной медикаментозной кардиоверсии пропафеноном пациент самостоятельно принимал пропафенон для купирования повторных приступов (стратегия «таблетка в кармане»). Через год приступы участились до 2-3 раз в месяц, длительностью до 2 суток. Пациент перенес ишемический инсульт после восстановления ритма.
Наличие неконтролируемой АГ (в истории болезни с 38 лет) с признаками поражения органов мишеней (гипертензивное сердце) диктует необходимость лечения основного заболевания для профилактики ремоделирования сердца, которое является причиной прогрессирования аритмии. С этой целью целесообразно назначить ИАПФ и бета-блокатор. ИАПФ не являются антиаритмическими средствами по своему основному эффекту, но оказывают мощное влияние на субстрат развития ФП посредством изменения внутрисердечной гемодинамики, обмена электролитов, снижая уровень симпатического влияния и повышенную эктопическую активность в миокарде.
Важно, что у пациента снижен клиренс креатинина. Нарушение функции почек и ФП – опасный дуэт: снижение клиренса креатинина на 10 мл/мин повышает риск развития инсульта на 12%. В связи с этим еще в 2012 г. было предложено добавлять 2 балла к оценке по шкале CHADS2, если у пациента клиренс креатинина <60 мл/мин (J. Piccini et al., 2012). Для пациентов с нарушенной функцией почек предпочтительным ИАПФ является периндоприл в связи с доказанным эффектом уменьшения альбуминурии (исследование PREMIER).
Оценка риска развития инсульта по шкале CHA2DS2-VASc у нашего пациента составляет 3 балла (перенесенный инсульт в анамнезе – 2 балла, АГ– 1 балл). Оценка риска кровотечений по шкале HAS-BLED – 2 балла (нарушение функции почек – 1 балл, перенесенный инсульт в анамнезе – 1 балл). Если по шкале CHA2DS2-VASc балл начисляется при наличии диагноза АГ, то по шкале HAS-BLED гипертензию можно уже не учитывать, поскольку уровень САД на фоне адекватно подобранной гипотензивной терапии не достигает 160 мм рт. ст. В этом заключается реальная возможность снизить риски путем подбора оптимальной терапии основного заболевания.
Выбор бета-блокатора основывается на профиле связывания с рецепторами и гидрофильности. В данном случае относительно молодому пациенту для сохранения эректильной функции целесообразно назначить небиволол или бисопролол. Небиволол – препарат с двумя механизмами вазодилатации (эндотелийзависимой и эндотелийнезависимой). Бисопролол – высокоселективный блокатор β-1 подтипа рецепторов.
Нарушенная толерантность к глюкозе, которая имеется у нашего пациента, связана с риском развития в будущем сахарного диабета 2 типа и диктует выбор бета-блокатора с максимальной метаболической нейтральностью. Оптимальным выбором является бисопролол – кардиоселективный препарат с амфифильными свойствами молекулы (растворяется как в воде, так и в липидах), который не метаболизируется при первом прохождении через печень и отличается двойным путем выведения.
После перенесенного ишемического инсульта у данного пациента следует возобновить антикоагулянтную терапию для профилактики повторных кардиоэмболических событий.
Подготовил Дмитрий Молчанов
1-80-КРД-РЕЦ-0616
*в Украине зарегистрирован генерический препарат Спиронолактон Сандоз.
**в Украине зарегистрирован генерический препарат Розувастатин Сандоз.


