1 червня, 2016
Гиполипидемическая терапия у пациентов с ишемической болезнью сердца: фокус на аторвастатин
Ишемическая болезнь сердца (ИБС) остается самым распространенным кардиоваскулярным заболеванием и ведущей причиной смерти во всем мире. Развитию ИБС способствуют различные факторы риска, такие как артериальная гипертензия, курение, диабет, малоактивный образ жизни, депрессия и др., однако ключевым патогенетическим механизмом выступают атерогенная дислипидемия и ассоциированный атеросклероз коронарных артерий. Соответственно, коррекция дислипидемии является неотъемлемой составляющей ведения пациентов с ИБС или высоким риском развития этого заболевания. Вместе с тем цель лечения состоит не в устранении дислипидемии как таковой, а в снижении риска сосудистых событий и в улучшении прогноза.
При атерогенной дислипидемии (повышенных уровнях холестерина липопротеинов низкой плотности – ХС ЛПНП – и триглицеридов (ТГ) на фоне сниженных уровней холестерина липопротеинов высокой плотности – ХС ЛПВП) наиболее эффективными лекарственными средствами являются ингибиторы ГМГ-КоА-редуктазы, или статины. Препарат этой группы, как и ацетилсалициловая кислота, при отсутствии абсолютных противопоказаний должен назначаться каждому пациенту с установленным диагнозом ИБС независимо от исходных уровней ХС ЛПНП. При выборе статина следует учитывать, что наибольшую доказательную базу в отношении лечения пациентов с ИБС имеет аторвастатин. Кроме того, этот статин обладает самым широким спектром нелипидных эффектов. Существует аргументированное мнение, что именно нелипидные эффекты отвечают за основной результат лечения – улучшение выживаемости у больных высокого риска.
Аторвастатин – гиполипидемический препарат, при применении которого впервые зарегистрировано прекращение прогрессирования атеросклеротических изменений сосудов. Это было установлено в исследовании REVERSAL (REVERSing Atherosclerosis with Aggressive Lipid Lowering), в котором сравнивалось влияние интенсивного и умеренного режимов терапии (соответственно 80 мг/сут аторвастатина и 40 мг/сут правастатина) на выраженность коронарного атеросклероза. В исследование были включены 657 пациентов с клиническими проявлениями ИБС, ангиографическими признаками стеноза коронарных артерий >20% и уровнем ХС ЛПНП от 3,2 до 5,4 ммоль/л (125-210 мг/дл). Основным критерием оценки различных режимов статинотерапии являлось процентное изменение общего объема атером. Дополнительным критерием было процентное и номинальное изменение объема атеромы, оцениваемое в 10 последовательных поперечных сечениях коронарных артерий с наибольшим и наименьшим объемом атеромы. Исследование проводилось с помощью внутрисосудистого ультразвукового датчика, выполнялось в начале наблюдения и через 18 мес. Результаты исследования продемонстрировали статистически значимое замедление прогрессирования атеросклероза коронарных артерий в группе аторвастатина. За время наблюдения средний исходный уровень ХС ЛПНП, составлявший в обеих группах 3,89 ммоль/л (150,2 мг/дл), статистически значимо снизился до 2,85 ммоль/л (110 мг/дл) в группе правастатина и до 2,05 ммоль/л (79 мг/дл) в группе аторвастатина.
В исследовании TNT (Treating to New Targets) проверялась гипотеза о том, что снижение уровня ХС ЛПНП с помощью статина <2,6 ммоль/л позволит получить лучший клинический результат при стабильной ИБС. Различие в уровнях ХС ЛПНП между двумя крупными группами больных в этом исследовании обеспечивалось использованием двух доз аторвастатина – 10 и 80 мг/сут, также планировалось оценить клиническую эффективность достижения более низких уровней ХС ЛПНП у пациентов со стабильными формами ИБС.
Согласно результатам исследования, в сравнении с менее интенсивным лечением (аторвастатин 10 мг/сут) режим интенсивной гиполипидемической терапии (аторвастатин 80 мг/сут) у пациентов со стабильной стенокардией и исходным уровнем липидов крови, близким к целевому, позволяет на 22% снизить риск кардиоваскулярных катастроф при ИБС, обеспечивая существенное клиническое преимущество.
Фибрилляция предсердий (ФП) является одним из частых осложнений ИБС наряду с другими нарушениями сердечного ритма. ARMYDA‑3 (Atorvastatin for Reduction Myocardial Dysrhytmia After cardiac surgery) было первым рандомизированным контролированным исследованием (РКИ) статинов перед плановым аортокоронарным шунтированием (АКШ). В этом исследовании изучалось, предотвращает ли аторвастатин в дозе 40 мг/сут, прием которого начинался за 1 нед до операции, возникновение ФП после вмешательства. Популяция исследования была представлена 200 пациентами, из них 99 получали плацебо и 101 – аторвастатин в дозе 40 мг/сут. Лечение начиналось за 7 дней до планового АКШ. Первичной конечной точкой была частота возникновения ФП после операции в госпитальном периоде в 2 группах исследования. Оценивались эпизоды ФП продолжительностью более 5 мин, зарегистрированные системой мониторинга или электрокардиографически, а также любой эпизод ФП, требовавший вмешательства по поводу стенокардии либо гемодинамической нестабильности.
ФП после операции возникла у 35 (35%) из 101 пациента в группе аторвастатина по сравнению с 56 (57%) из 99 пациентов группы плацебо (p=0,003). Средняя частота сокращений желудочков составляла 115±12 уд./мин в группе аторвастатина и 118±15 уд./мин в группе плацебо (р=0,12). ФП возникала в среднем через 51±15 ч после операции в группе аторвастатина и 50±17 ч после операции в группе плацебо (р=0,59), а общая продолжительность эпизодов ФП была практически одинаковой (24±4 vs 24±5 ч; p=0,88). Средние сроки пребывания в стационаре после операции оказались существенно короче в группе аторвастатина (6,3±1,2 vs 6,9±1,4 дня в группе плацебо; p=0,001). Многофакторный анализ показал, что лечение аторвастатином ассоциировалось со снижением риска ФП после операции на сердце на 61% (p=0,017).
Стенокардия, возникающая вследствие ишемии миокарда, наблюдается у половины пациентов с ИБС. В последние годы появляется все больше доказательств, что за счет нелипидных свойств статины, прежде всего аторвастатин, могут обеспечивать антиангинальное и антиишемическое действие, сопоставимое с таковым стандартных антиангинальных препаратов и хирургических вмешательств. Так, в исследовании Vascular Basis for the Treatment of Myocardial Ischemia Study у пациентов со стабильной ИБС после 1 года приема аторвастатина наблюдалось значительное снижение частоты и продолжительности ишемии при улучшении толерантности к физическим нагрузкам. В исследовании SAGE аторвастатин в дозе 80 мг/сут уже через 3 мес лечения обеспечил значительное снижение общей длительности ишемии на 37% (помимо снижения общей смертности на 77%).
Результаты ряда исследований свидетельствуют о том, что у пациентов с ИБС и сердечной недостаточностью (СН) терапия статинами может снижать риск кардиоваскулярных осложнений и улучшать выживаемость. Однако в этом отношении наблюдаются значительные клинические различия между гидрофильными (розувастатин) и липофильными (аторвастатин) статинами при их использовании у больных с СН. Например, в метаанализе 17 РКИ, включивших в общей сложности 1473 пациента с СН, было продемонстрировано, что аторвастатин значительно улучшает фракцию выброса левого желудочка (ФВ ЛЖ) и снижает уровни мозгового натрийуретического пептида (BNP) и его N-терминального фрагмента (NT-proBNP), тогда как розувастатин подобными эффектами не обладает. Такое различие в динамике показателей, вероятно, связано с тем, что липофильный аторвастатин может проникать в кардиомиоциты и вызывать изменения непосредственно в этих клетках, в то время как гидрофильный розувастатин подобной возможности лишен. Поскольку уровень NT-proBNP является предиктором больших кардиоваскулярных событий, а более высокие значения ФВ ЛЖ достоверно ассоциируются со снижением смертности у пациентов с СН, существенное улучшение этих показателей на фоне применения аторвастатина может обеспечивать более выраженное снижение кардиоваскулярного риска по сравнению с розувастатином.
На сегодня доказано, что дислипидемия вызывает прогрессирующее снижение почечной функции и повышает риск развития хронической болезни почек. В то же время некоторые статины посредством целого ряда механизмов могут оказывать заметное защитное влияние на функциональные способности почек. В частности, значительная способность аторвастатина к нефропротекции подтверждается результатами многочисленных исследований, таких как GREACE, ALLIANCE, TNT, PLANET I, PLANET II.
Сравнение нефропротекторных эффектов аторвастатина и розувастатина проводилось в двух РКИ – PLANET I и PLANET II, включавших пациентов с исходной умеренной протеинурией и гиперхолестеринемией с сахарным диабетом (СД) (PLANET I, n=325) и нормальным обменом глюкозы (PLANET II, n=220). После вводного периода длительностью 8 нед пациенты в каждом исследовании были рандомизированы в группы лечения аторвастатином (целевая доза 80 мг/сут) и розувастатином (целевая доза 40 мг/сут); продолжительность наблюдения составила 52 нед. Результаты исследования показали, что изучаемые препараты по-разному влияют на функцию почек: аторвастатин в обоих исследованиях достоверно снижал тяжесть протеинурии (в среднем на 15% в PLANET I и более чем на 20% в PLANET II), тогда как розувастатин не влиял на этот показатель (PLANET I) или же его влияние не было статистически значимым (в PLANET II). В дополнение к этим эффектам в PLANET I при применении розувастатина было отмечено увеличение частоты осложнений со стороны почек на фоне хорошей общей переносимости терапии (4-кратное повышение риска развития острой почечной недостаточности (р<0,05) и 5-кратное – удвоения уровней креатинина сыворотки крови (р<0,01) по сравнению с соответствующими показателями при приеме 80 мг/сут аторвастатина). Таким образом, РКИ PLANET I и PLANET II показали, что высокие дозы аторвастатина значительно уменьшают выраженность протеинурии (снижение на 20%) без нежелательного влияния на функцию почек, в то время как терапия розувастатином приводит к значительному снижению почечной функции без уменьшения выраженности протеинурии.
Следует отметить, что розувастатин в любых дозах противопоказан пациентам с тяжелым нарушением функции почек (клиренс креатинина <30 мл/мин), а больным с умеренным снижением почечной функции (клиренс креатинина <60 мл/мин) противопоказана доза розувастатина 40 мг. Аторвастатин подобных ограничений не имеет и может безопасно применяться у пациентов с заболеваниями почек.
Большой практический интерес при гиполипидемической терапии представляет соотношение эффективность/стоимость. В масштабном исследовании CURVES было показано, что высокая эффективность аторвастатина по влиянию на уровень ХС ЛПНП предопределяет лучшие фармакоэкономические показатели данного препарата по сравнению с таковыми других статинов.
Среди причин, ограничивающих применение статинов, на первом месте стоит высокая стоимость лекарственных препаратов этой группы. Решением проблемы может стать использование препаратов-генериков. При этом следует назначать только генерики с фармакокинетической и терапевтической эквивалентностью оригинальному аторвастатину.
Необходимо подчеркнуть, что пациенты с ИБС должны получать статины непрерывно и длительно (как правило, пожизненно) – только так можно добиться максимального эффекта от их применения. При использовании аторвастатина через 2 нед терапии появляются достоверные признаки восстановления функции эндотелия; через 3 мес выявляется эффект в отношении липидов, через 6 мес улучшается течение ИБС. При терапии длительностью более года наблюдается стабилизация каротидного, более 2 лет – коронарного атеросклероза, более 5 лет – снижение смертности.
Клинический случай
Терапия ИБС на фоне гипотиреоза
Больная П., 59 лет, поступила с жалобами на боли за грудиной сжимающего характера, возникающие при подъеме на 2-й этаж, одышку при физической нагрузке, слабость.
Анамнез. Пять лет назад на фоне менопаузального периода впервые были отмечены подъемы АД до 180/95 мм рт. ст. Тогда же эндокринологом на основании лабораторных данных (ТТГ=5,0 мЕд/л; свободный Т4=11,0 пмоль/л) был установлен диагноз: «Аутоиммунный тиреоидит, субклинический гипотиреоз». Назначена заместительная тиреоидная терапия (ЗТТ), которую пациентка не принимала.
Через 2 года состояние ухудшилось: впервые стали беспокоить ангинозные боли (при ходьбе до 50 м), отмечались перебои в работе сердца, выраженная слабость, сухость кожи, прибавка в весе (15 кг за год). Пациентка была направлена на стационарное лечение. По лабораторным данным присутствовали признаки манифестного гипотиреоза (ТТГ=13,2 мЕд/л, свободный Т4=9,2 пмоль/л). В связи с частыми приступами стенокардии для выбора дальнейшей тактики лечения выполнена коронаровентрикулография (КВГ): выявлены стеноз передней межжелудочковой ветви (ПМЖВ) левой коронарной артерии в средней трети 90%, стеноз правой коронарной артерии (ПКА) в дистальной части 99%. Проведено стентирование ПМЖВ с полным восстановлением кровотока.
После выписки из стационара назначенную терапию – симвастатин, клопидогрель, ингибиторы ангиотензинпревращающего фермента, β-блокаторы, а также ЗТТ (тироксин 25 мг/сут) – стала принимать регулярно. Однако через 9 мес больная обратилась в клинику в связи с учащением (почти ежедневно) и повышением интенсивности ангинозных болей, снижением толерантности к физической нагрузке (ходьба до 20 м) и выраженной одышкой. При повторном проведении КВГ обнаружены стеноз ПМЖВ в проксимальном отделе 70%, снижение проходимости в зоне стентирования до 50%.
На следующий день проведено АКШ с установкой 2 шунтов. В связи с отсутствием достижения целевых уровней показателей липидограммы на фоне приема симвастатина пациентке был назначен аторвастатин (Торвакард, Zentiva, Чехия) в суточной дозе 40 мг, а также увеличена доза ЗТТ до 50 мг/сут, поскольку имелись умеренные проявления тиреоидной недостаточности. В остальном терапия не изменилась. Через 5 мес после АКШ была проведена плановая госпитализация больной для контрольного обследования. По данным лабораторных анализов отмечался эутиреоз (ТТГ=2,3 мЕд/л; свободный Т4=17,3 пмоль/л).
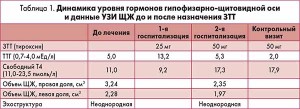
Динамика уровней гормонов щитовидной железы (ЩЖ) и показателей липидного профиля представлена в таблицах 1, 2.
Установлен диагноз: «ИБС. Стабильная стенокардия напряжения ІІІ ФК. Стенозирующий атеросклероз ПМЖВ и ПКА (на основании КВГ). Стентирование ПМЖВ. АКШ (2 шунта). Комбинированная дислипидемия. Гипертоническая болезнь IIІ ст. 2 ст. Гипертоническая ангиопатия сосудов сетчатки. СН ІIA ст. с сохраненной систолической функцией ЛЖ. Аутоиммунный тиреоидит. Гипотиреоз в стадии компенсации. Ожирение I cт.».
Назначено лечение: диета с ограничением содержания жиров животного происхождения.
Медикаментозная терапия: аспирин 100 мг/сут; клопидогрель 75 мг/сут; аторвастатин (Торвакард) 40 мг/сут; лозартан/гидрохлортиазид (Лозап плюс) 1 таблетка в сутки; бисопролол 5 мг/сут; ЗТТ (тироксин 50 мг).
Выводы
У больной прослеживалась четкая связь между наступлением менопаузального периода и появлением субклинического гипотиреоза. В данном клиническом случае были наглядно продемонстрированы проатерогенные свойства гипотиреоза и его способность обусловливать возникновение ИБС и влиять на ее течение. В отсутствие ЗТТ наблюдался переход субклинического гипотиреоза в манифестную форму, что ассоциировалось с прогрессированием ИБС. Таким образом на вопрос, лечить или не лечить доклиническую гипофункцию ЩЖ, однозначно должен быть дан положительный ответ. При этом чем раньше начато лечение, тем лучше прогноз у пациентов. Кроме того, лечение дислипидемий у гипотиреоидных больных ИБС эффективно лишь при назначении адекватной комбинированной терапии: статина (аторвастатин в индивидуально подобранной дозе) и ЗТТ.