24 квітня, 2020
Метаболический синдром: взгляд терапевта
 Метаболический синдром (МС) – это комплекс взаимосвязанных патологических состояний, главными из которых являются инсулинорезистентность (ИР), ожирение, дислипопротеинемия, артериальная гипертензия (АГ). Понятие «метаболический синдром» – это проявление современной тенденции развития патологии человека, предполагающей сочетание болезней и синдромов, которым присущи полиэтиологичность, полипатогенетичность, полиморфность клинических проявлений.
Метаболический синдром (МС) – это комплекс взаимосвязанных патологических состояний, главными из которых являются инсулинорезистентность (ИР), ожирение, дислипопротеинемия, артериальная гипертензия (АГ). Понятие «метаболический синдром» – это проявление современной тенденции развития патологии человека, предполагающей сочетание болезней и синдромов, которым присущи полиэтиологичность, полипатогенетичность, полиморфность клинических проявлений.
МС является основой поражения практически всех органов и систем, предиктором развития сердечно-сосудистых болезней и сахарного диабета (СД) 2 типа. Вместе с тем МС – это плата человека за нерациональный образ жизни, гиподинамию, переедание, курение, злоупотребление алкоголем, варварское использование достижений цивилизации.
История вопроса
Изучение данной патологии началось в 1966 г., когда J. Cammus предложил термин «метаболический трисиндром» для обозначения сочетания у одного больного гипертриглицеридемии, инсулиннезависимого СД и подагры. Год спустя P. Avodaro и соавт. выдвинули гипотезу о существовании особого синдрома, отметив частое сочетание и взаимосвязь СД с гиперлипидемией и умеренным ожирением. H. Mehnert в 1968 г. назвал сочетание СД, АГ и дислипопротеинемии синдромом изобилия. M. Hanefeld и W. Leonhardt в 1980 г. предложили термин «метаболический синдром». В начале 80-х годов многие авторы отмечали взаимосвязь между АГ, гиперлипидемией, гиперинсулинемией и ожирением.
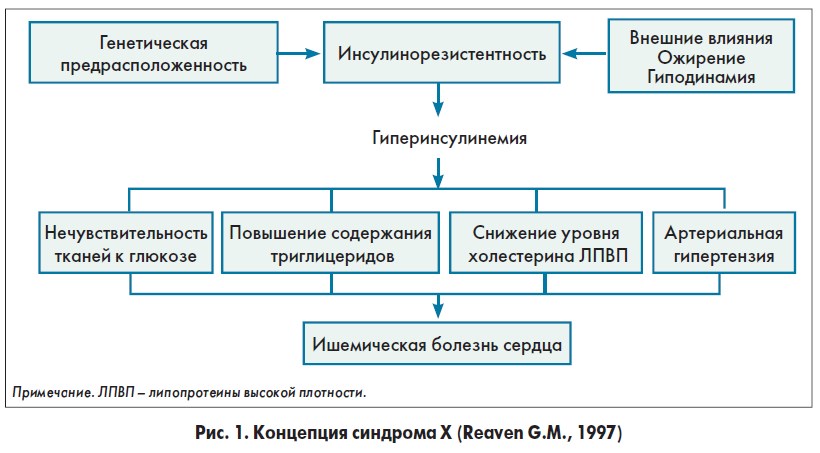
Однако, несмотря на все эти публикации и уже почти 20-летнюю историю проблемы, основоположником концепции новой патологии – МС – считается профессор Стэнфордского университета Джеральд Ривен (G.M. Reaven). Он опубликовал статью «Роль инсулинорезистентности в болезнях человека» и предложил термин «синдром Х» [1]. Дж. Ривен считал ИР объединяющим патогенетическим механизмом АГ, СД и атеросклероза, а абдоминальное ожирение (АО) – обязательным компонентом этой патологии. В результате многолетнего изучения Дж. Ривен разработал собственную концепцию развития МС (рис. 1).
За время существования этой концепции для обозначения МС было предложено множество названий: полиметаболический синдром, метаболический трисиндром, синдром изобилия, синдром хорошей жизни, частичная липодистрофия, метаболический синдром, синдром Х, смертельный квартет, гормонально-метаболический синдром, генерализованная сердечно-сосудистая метаболическая болезнь, метаболическая петля, синдром инсулинорезистентности.
Диагностические критерии МС
В 1998 г. консультативной группой Всемирной организации здравоохранения (ВОЗ) по определению, классификации и диагностике СД были опубликованы первые диагностические критерии МС (табл. 1) [2]. Экспертами ВОЗ инсулинорезистентность признана обязательным критерием для определения этой патологии.
В 2001 г. были предложены критерии National Cholesterol Education Program Adult Treatment Panel III (АТР ІІІ) [3], в соответствии с которыми нет одного обязательного признака, а для постановки диагноза необходимо наличие каких-либо двух из пяти следующих признаков:
- АО (ОТ >102 см у мужчин и >88 см у женщин);
- триглицериды ≥1,7 ммоль/л;
- холестерин ЛПВП <1,0 ммоль/л у мужчин и <1,3 ммоль/л у женщин;
- артериальное давление (АД) ≥130/85 мм рт. ст.;
- гликемия натощак ≥6,1 ммоль/л.
В 2005 г. экспертами Международной диабетической федерации (International Diabetes Federation, IDF) [4] были разработаны новые диагностические критерии, согласно которым АО является обязательным признаком МС (для европейцев ОТ >94 см у мужчин и >80 см у женщин, что приблизительно соответствует ИМТ >25 кг/м2 у мужчин). Остальные критерии аналогичны предложенным АТР ІІІ.
В том же году еще один вариант критериев был рекомендован Американской кардиологической ассоциацией (American Heart Association, АНА) и Национальным институтом сердца, легких и крови США (National Heart, Lung and Blood Institute, NHLBI) [5]. Они отличаются от рекомендаций IDF отсутствием обязательного признака и величиной показателей, определяющих АО (ОТ >102 см у мужчин и >88 см у женщин, что соответствует ИМТ >30 кг/м2 у мужчин). Остальные критерии идентичны АТР ІІІ.
Дискуссия о необходимости обязательного критерия и о количественных показателях АО продолжалась между экспертами IDF и АНА/NHLBI до 2009 года, и наконец был найден компромисс. На сегодня диагностические критерии МС включают [6]:
- увеличение ОТ (определяется специфически для данной страны или популяции);
- триглицериды ≥1,7 ммоль/л или применение препаратов, снижающих уровень триглицеридов;
- холестерин ЛПВП <1,0 ммоль/л у мужчин и <1,3 у женщин или применение препаратов, нормализирующих холестерин;
- АД ≥130/85 мм рт. ст. или применение антигипертензивных средств;
- гликемия натощак ≥6,1 ммоль/л или прием сахароснижающих препаратов.
Диагноз МС устанавливают на основании наличия трех из пяти перечисленных признаков, при этом отсутствует какой-либо один обязательный критерий.
Этиопатогенез МС
Среди причин развития МС основное значение имеет генетическая предрасположенность. Роль наследственных факторов подтверждена во многих экспериментальных исследованиях, были даже выведены животные с фенотипом МС. Кроме того, часто наблюдаются семейные случаи заболевания. В настоящее время доказана полигенность синдрома и обнаружены маркеры этой патологии, расположенные на хромосоме 1d21.
Кроме генетической предрасположенности на развитие МС, безусловно, влияют эпигенетические факторы: экология (загрязнение окружающей среды); условия жизни (урбанизация, высокий экономический уровень страны); особенности образа жизни пациентов (гиподинамия, курение, употребление алкоголя и др.).
Инсулинорезистентность
Основу патогенеза МС составляет ИР, которая представляет собой генетически обусловленную недостаточность биологического ответа тканей на инсулин. Механизм ИР заключается в пострецепторной блокаде инсулинзависимого транспортера глюкозы с последующим снижением ее усвоения тканями (прежде всего скелетными мышцами). По данным разных авторов, распространенность ИР в популяции составляет от 2 до 25%.
Наиболее простой метод оценки ИР – определение индекса HOMA (Hоmeostasis Model Assessment). Первоначально для расчета этого показателя была предложена следующая формула
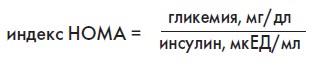
Значение рассчитанного по этой формуле индекса НОМА <6,0 натощак имело равенство специфичности для МС 84%.
Сегодня для определения индекса НОМА используют другую формулу

Норма индекса по этой формуле составляет <3,0; значения говорит о наличии ИР.
В пользу основной роли ИР в развитии МС свидетельствуют результаты популяционного исследования, проведенного в Италии (2002) с участием 888 пациентов в возрасте 40-79 лет [7]. Только 10% участников этого испытания, у которых была ИР, не имели метаболических нарушений. ИР выявлена у 58% пациентов с АГ (АД >160/95 мм рт. ст.); у 63% – с гиперурикемией; у 66% – с нарушением толерантности к глюкозе; у 84% – с СД 2 типа; у 84% – с гипертриглицеридемией (>2,85 ммоль/л); у 88% больных с низким уровнем холестерина ЛПВП.
Вследствие ИР активируется липолиз висцерального жира брюшины, что приводит к повышению концентрации свободных жирных кислот (СЖК). Последние с током крови поступают в печень, где происходит синтез триглицеридов. Выходя в кровь, эти вещества обусловливают гипертриглицеридемию, что клинически проявляется в виде гиперлипопротеинемии IV типа. СЖК становятся основой для синтеза липопротеинов очень низкой плотности (ЛПОНП), которые под действием печеночной липазы превращаются в липопротеины низкой плотности (ЛПНП), обусловливающие гиперлипопротеинемию ІІа или ІІб типа.
Связь ИР и гипергликемии осуществляется по типу замкнутого круга. Первым этапом является активация липолиза в жире брюшины с образованием СЖК. Поступившие в печень СЖК включаются в процесс глюконеогенеза, что приводит к гипергликемии. Повышение глюкозы в крови вызывает гиперинсулинемию, усугубляющую явления ИР.
Ожирение
Ожирение – это избыточное содержание в организме жировой ткани. Ошибочно рассматривать ожирение как избыток общей массы тела по отношению к норме, рассчитанной статистически, поскольку увеличенная масса может образоваться не только за счет жира. Тем не менее в клинической практике обычно оценивают именно ИМТ и по нему судят о наличии и степени ожирения.
Норма содержания жира у мужчин составляет 15-20%, у женщин – 20-25%.
Для оценки типа и степени ожирения изучают ряд антропометрических показателей: ОТ, ОБ, индексы ОТ/ОБ, ОТ/рост (см), сагиттальный диаметр бедра (СДБ). Используют следующие формулы:
- общий объем жировой ткани (ОЖТ, л) = масса тела (кг) – рост (см) – 42,0;
- объем висцеральной жировой ткани (л) = 0,731 × СДБ (см) – 11,5;
- общая масса жировой ткани (МЖТ, кг) = ОЖТ (л) × 0,923.
Ожирение – это состояние, при котором масса жира на 15% превышает идеальную или на 10% – максимально допустимую.
Значительно чаще на практике используют определение ИМТ:
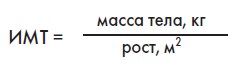
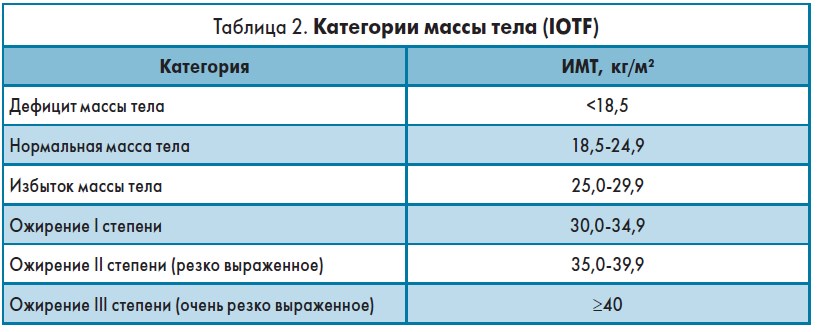
Специалистами общества по изучению ожирения (International Obesity Task Force, IOТF) предложены категории массы тела в зависимости от величины ИМТ (табл. 2).
Важное значение имеет не только степень, но и тип ожирения. В зависисмости от места преимущественного отложения жира выделяют такие типы ожирения:
- андроидный (центральный, абдоминальный): ОТ/ОБ >0,9 для мужчин и >0,8 для женщин;
- гиноидный (периферический, глютеофеморальный): ОТ/ОБ <0,9 для мужчин и <0,8 для женщин.
Андроидный, или мужской, тип ожирения является более неблагоприятным и ассоциируется с развитием многих болезней, в частности и МС.
Сегодня ожирение приобрело характер мировой пандемии, оно наблюдается у 40-60% лиц после 40 лет, уменьшая продолжительность жизни на 10-12 лет. Доказано, что ожирение является фактором риска сердечно-сосудистых заболеваний, СД 2 типа, патологии опорно-двигательного аппарата и гепатобилиарной системы, онкологических заболеваний.
Развитие ожирения зависит от возраста, пола, расы, уровня образования и доходов, семейного положения, количества родов, характера питания, курения, употребления алкоголя, физической активности.
В патогенезе ожирения прослеживается два механизма:
- увеличение размеров адипоцитов вследствие накопления в них липидов;
- возрастание числа адипоцитов вследствие усиленного их образования из клеток-предшественников – проадипоцитов.
Адипоциты выполняют две функции: депонирование энергетических субстратов (триглицеридов) и секрецию биологически активных веществ – гормонов (лептин, адипсин), простагландинов, интерлейкинов и др.
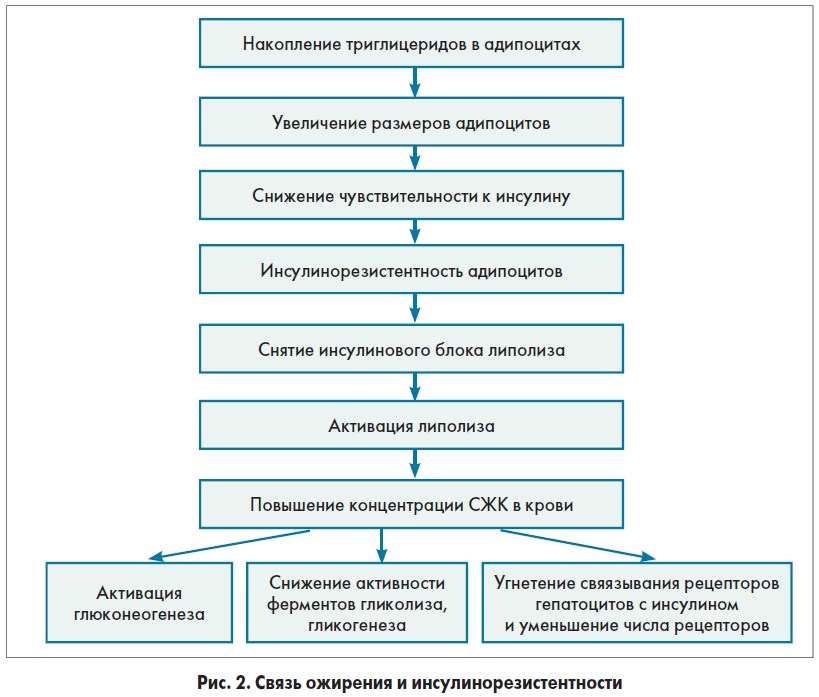
Связь ожирения и ИР показана на рисунке 2. Эта взаимосвязь представляет собой замкнутый круг: ИР обусловливает гиперинсулинемию, которая способствует развитию ожирения, в свою очередь усугубляющего ИР.
В отсутствие пищи происходит процесс липолиза, в ходе которого в адипоцитах продуцируется адипсин, стимулирующий центр голода в гипоталамусе. При поступлении пищи активируется липогенез и вырабатывается лептин, оказывающий стимулирующее действие на центр насыщения и ингибирующее – на центр голода. Ожирение обусловливает блокирование этой цепочки, из-за чего стимуляции центра насыщения не происходит, соответственно, человек «переедает».
Артериальная гипертензия
Распространенность АГ среди взрослой популяции составляет 30-35%, у лиц старше 60 лет – 40-50%. В 70-е годы прошлого века был описан феномен «половина-к половине-к половине». Расшифровывается эта формула таким образом: только половина живущих на Земле гипертоников знает о наличии у них АГ, только половина знающих о заболевании принимают лекарственные средства, и только у половины из них терапия эффективна, т.е. АД находится под медикаментозным контролем. Этот феномен отражает истинное положение и сегодня.
В течение жизни у человека наблюдаются физиологические изменения уровня АД. Так, у новорожденных АД составляет 70/50 мм рт. ст., в 1-3 года – 95/50 мм рт. ст. От 3 до 18 лет систолическое АД (САД) ежегодно повышается примерно на 2 мм рт. ст., а диастолическое АД (ДАД) – на 0,5-1 мм рт. ст., при этом темп повышения более значительный у мальчиков. После 18 лет уровень АД продолжает постепенно повышаться, причем несколько быстрее у женщин, к 60 годам АД у представителей обоих полов сравнивается. После 60 лет чаще растет САД – при сохранении нормального или даже сниженного уровня ДАД.
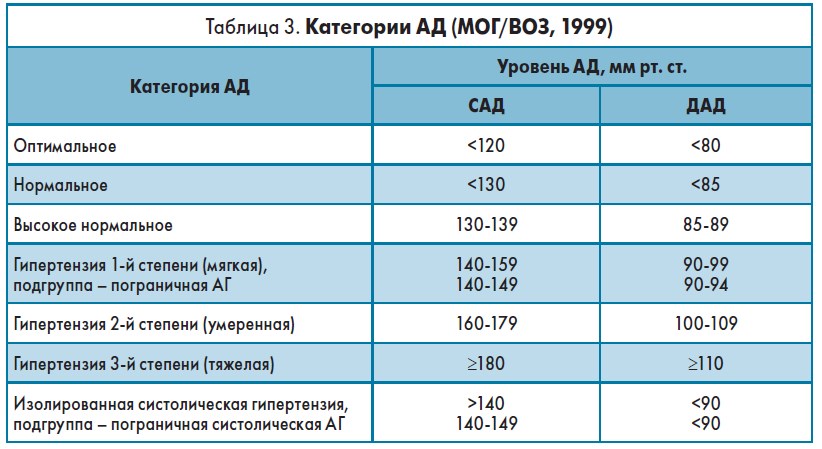
В 1999 г. Международное общество гипертензии (МОГ) и ВОЗ определили несколько категорий АД (табл. 3) [8].
АД имеет огромное клиническое значение. В метаанализе Lewington и соавт. (2002) показано, что начиная с уровня 115/75 мм рт. ст. рост АД на каждые 20/10 мм рт. ст. обусловливает повышение риска сердечно-сосудистых осложнений в 2 раза [9]. Такие факторы, как СД, хроническая болезнь почек, инфаркт миокарда в анамнезе, ожирение, курение дополнительно повышают риск сердечно-сосудистых заболеваний.
В 2007 г. Европейское общество кардиологов (ESС) совместно с Европейским обществом гипертензии (ESH) приняли концепцию изменчивого граничного уровня АД. Этот уровень определяется индивидуально, исходя из общего сердечно-сосудистого риска пациента. Для лиц, не имеющих отягощающих факторов, уровень нормального АД составляет <140/90 мм рт. ст., при превышении этого значения следует начинать антигипертензивное лечение. Целевой уровень АД для пациентов высокого риска составляет <130/80 мм рт. ст. [10].
ИР и АГ объединяет общая генетическая детерминированность. ИР способствует развитию АГ через гиперинсулинемию, которая усиливает выработку ангиотензина ІІ, приводит к гипертрофии мышечного слоя и интимы артерий, вызывает задержку натрия и воды, повышение сердечного выброса, периферическую вазоконстрикцию.
Метаболический синдром и беременность
Основные факторы, влияющие на перинатальный и материнский исходы беременности при МС, таковы:
- ожирение;
- АГ;
- ИР, обусловливающая развитие гестационного диабета;
- связанные с ИР гиперкоагуляция, тромботические осложнения.
А.Д. Макацария и соавт. (2015) провели исследование с участием 77 женщин в возрасте 25-42 года, соответствующих критериям МС. В акушерском анамнезе пациенток частота синдрома потери плода составила 84,4%, плацентарной дисфункции – 71,4%, преэклампсии средней тяжести и тяжелой – 75,3% [11].
Были выделены две подгруппы участниц, которых целенаправленно наблюдали и лечили. При позднем начале лечения МС потеря плода произошла в пяти случаях, преждевременные роды – у 22,1% женщин, преэклампсия средней тяжести – у 53,3%, тяжелой степени – у 22,2%, необходимость в проведении кесарева сечения возникла у 77,9% беременных. В случае начала наблюдения и лечения пациенток с І триместра исходы были существенно лучше.
В процессе исследования А.Д. Макацария и соавт. показали ключевую роль дефицита прогестерона в развитии осложнений беременности у женщин с МС. У пациенток с висцеральным ожирением дефицит прогестерона обнаружен в 100% случаев. Его последствиями были нарушение имплантации и инвазии трофобласта, выкидыши, потеря плода, преждевременные роды. В комплекс терапии беременным с ожирением и МС авторы включали утрожестан, учитывая его биоидентичность эндогенному прогестерону, метаболическую нейтральность, возможность применения до наступления беременности и на различных ее сроках, оптимальность вагинального пути введения.
Терапия МС
Целью терапии МС является предотвращение развития сердечно-сосудистых заболеваний, в частности ишемической болезни сердца, и СД. Такое лечение предполагает:
- снижение массы тела (диета, физическая активность);
- нормализацию АД (модификация образа жизни, антигипертензивная терапия);
- снижение степени ИР и улучшение утилизации глюкозы (метформин);
- достижение нормогликемии;
- нормализацию липидного спектра крови.
В 2010 г. эксперты ВОЗ опубликовали специальный отчет по МС и стратегии здравоохранения по преодолению этой патологии [12]. В соответствии с их заключением МС представляет собой понятие, в котором внимание акцентировано на комплексных многофакторных проблемах здоровья. МС признан преморбидным состоянием, ввиду чего данная патология не может быть выявлена у лиц с уже установленным СД или известными кардиоваскулярными заболеваниями. Понятие и термин «метаболический синдром» не рекомендовано использовать в качестве диагноза.
Список литературы находится в редакции.
Медичні аспекти здоров’я жінки, Спецвипуск № 2, 2017 р.