4 жовтня, 2016
Эффективность препарата Актовегин в лечении постинсультных когнитивных нарушений

В этом году в Буковеле состоялась научно-практическая конференция с международным участием «Современные аспекты клинической неврологии», организаторами которой выступили ГВУЗ «Ивано-Франковский национальный медицинский университет», департамент здравоохранения Ивано-Франковской областной государственной администрации. В рамках мероприятия рассматривались новые подходы к лечению таких распространенных в наше время неврологических заболеваний, как деменция, болезнь Альцгеймера, рассеянный склероз, болезнь Паркинсона, инсульт, а также обсуждались нюансы постинсультной реабилитации.
Особое внимание участников привлек сателлитный симпозиум «Постинсультные когнитивные нарушения (ПИКН): проблемы и новые стратегии», организованный компанией «Такеда». Ранее, в №№ 13-14, были опубликованы статьи, подготовленные на основе прозвучавших на нем докладов – «Нерешенные проблемы в терапии постинсультных когнитивных нарушений» профессора клинической неврологии, руководителя отделения неврологии Университетской клиники Барселоны доктора Джерзи Крупински (Dr. Jerzy Krupinski, Universitar Mutua Terrassa) и «Перспективы и возможности постинсультной реабилитации в Украине» заведующего кафедрой неврологии, нейрохирургии и психиатрии Ужгородского национального университета, профессора Михаила Михайловича Ороса. Выступающие сошлись во мнении относительно целесообразности использования препарата Актовегин в качестве средства выбора для терапии ПИКН, а также с целью профилактики последующих неврологических событий, основываясь на данных, полученных в недавно завершившемся исследовании ARTEMIDA, а также в более ранних исследованиях.
 Директор Центра по исследованию проблем старения и здоровья Университета Гетеборга (Швеция), профессор Ингмар Скуг (Ingmar Skoog) остановился на аспектах доказательной медицины – он представил результаты исследования ARTEMIDA, в котором изучалась эффективность препарата Актовегин в терапии пациентов с ПИКН.
Директор Центра по исследованию проблем старения и здоровья Университета Гетеборга (Швеция), профессор Ингмар Скуг (Ingmar Skoog) остановился на аспектах доказательной медицины – он представил результаты исследования ARTEMIDA, в котором изучалась эффективность препарата Актовегин в терапии пациентов с ПИКН.
ARTEMIDA – это мультицентровое рандомизированное двойное слепое плацебо-контролированное международное исследование, которое длилось 12 мес (6 мес – период терапии и 6 мес – период наблюдения). Впервые его результаты были представлены в Берлине в 2015 г. на Первом конгрессе Европейской академии неврологии (EAN).
Основной целью исследования стала оценка эффективности и профиля безопасности препарата Актовегин в лечении ПИКН. Также оценивались:
- потенциал Актовегина относительно модификации течения заболевания (на основании сохранения эффектов после прекращения лечения в конце 6-месячного периода наблюдения);
- эффективность терапии в предупреждении деменции у больных, недавно перенесших ишемический инсульт (ИИ);
- влияние препарата Актовегин на другие исходы инсульта (помимо ПИКН).
Профессор И. Скуг отметил, что исследование ARTEMIDA выполняли в 36 центрах трех стран (Россия, Беларусь, Казахстан) с участием 503 пациентов. В течение первых 6 мес пациенты в дополнение к стандартной терапии получали терапию Актовегином или плацебо, а в последующие 6 мес осуществлялось наблюдение за каждой из групп участников с целью определения сохранения полученного эффекта. В исследование включались пациенты в первые 7 дней после ИИ. Терапия Актовегином или плацебо продолжалась на протяжении 6 мес (2000 мг/сут в/в до 20 сут, затем 1200 мг/сут перорально).
Критерии включения в исследование:
- возраст ≥60 лет;
- перенесенный супратенториальный ИИ, подтвержденный компьютерной или магнитно-резонансной томографией;
- оценка по Шкале тяжести инсульта национальных институтов здоровья США (National Institutes of Health Stroke Scale, NIHSS) – 3-18 баллов (включительно);
- наличие признаков когнитивной недостаточности;
- возможность выполнить тестирование с помощью Монреальской шкалы оценки когнитивных функций МоСА (Montreal Cognitive Assessment Scale)В исследование включались пациенты с оценкой по шкале МоСА ≤25 баллов.
Напротив, были исключены из исследования пациенты:
- с деменцией, депрессией или психическими нарушениями в анамнезе;
- перенесшие кардиоэмболический инсульт (несмотря на адекватную антикоагулянтную терапию);
- с подозрением на церебральный васкулит;
- с инсультом вследствие осложнения церебральной ангиографии, реваскуляризации или травмы;
- с подтвержденным инсультом другого типа (кроме ишемического);
- с проведенным тромболизисом либо нейрохирургическим вмешательством для лечения текущего инсульта;
- с показаниями для ангиографии сонных артерий;
- с установленной аллергией или идиосинкразией к Актовегину.
В качестве первичной конечной точки оценивалось изменение по когнитивной подшкале Шкалы оценки тяжести болезни Альцгеймера (Alzheimer’s Disease Assessment Scale-cognitive subscale, ADAS-Cog+) по сравнению с исходным значением спустя 6 мес в сравнении с плацебо. Шкала ADAS-Cog+ включает 11 субтестов для оценки различных когнитивных функций (память, речь, зрительно-пространственные функции и т. д.), которая была дополнена субтестами на регуляторные функции и внимание, что позволило увеличить чувствительность шкалы даже к умеренным когнитивным расстройствам дизрегуляторного профиля.
В качестве вторичных конечных точек исследования оценивались:
- изменения по шкале ADAS-Cog+ от исходного значения через 3 и 12 мес;
- количество пациентов, ответивших на терапию (оценка по ADAS-Cog+) через 3, 6 и 12 мес;
- изменения по шкале MoCA по сравнению с исходным значением через 3, 6 и 12 мес;
- количество пациентов с признаками деменции по Международной классификации болезней 10-го пересмотра (МКБ-10 )через 6 и 12 мес;
- показатель изменения по шкале NIHSS от исходного значения через 3, 6 и 12 мес;
- индекс Бартела (Barthel Index; индекс активности повседневной жизнедеятельности) через 6 мес;
- показатель качества жизни по опроснику EuroQol EQ-5D через 6 и 12 мес;
- наличие депрессии (согласно BDI-II – Beck Depression Inventory v2) через 3, 6 и 12 мес.
Профессор также рассказал, что при оценке профиля безопасности учитывались только побочные эффекты (ПЭ), возникшие не позже 10 дней после окончания терапевтического периода. Кроме того, должны были быть представлены все ПЭ, оцененные как связанные с исследуемым препаратом, а также все серьезные ПЭ, о которых стало известно.
При оценке профиля безопасности учитывалось, в том числе, следующее:
- витальные функции (систолическое/диастолическое артериальное давление и частота сердечных сокращений);
- психический статус;
- электрокардиограмма;
- лабораторные показатели (включая гематологические и биохимические);
- сопутствующая медикаментозная терапия.
Говоря о популяционной составляющей исследования ARTEMIDA, доктор Скуг сообщил, что из 503 участников 255 принимали в качестве терапии плацебо, а 248 – Актовегин.
Профессор отметил, что средний возраст участников составлял примерно 70 лет (65,2% – пациенты ≥65 лет, 34,2% – ≤65 лет).
19,3% пациентов имели среди сопутствующих патологий сахарный диабет. Ишемический инсульт в анамнезе присутствовал у 15,5% пациентов.
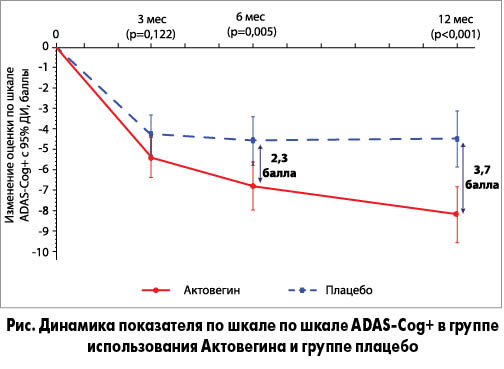
Сообщая о результатах исследования, профессор указал, что по первичной конечной точке (изменение по ADAS-Cog+ через 6 мес терапии) Актовегин показал положительный результат. Разница между группами Актовегина и плацебо по шкале ADAS-Cog+ через 6 мес составила >2 баллов, а через 12 мес – 3,7 балла. Оба показателя достигли статистической значимости (рис.).
Таким образом, исследователи пришли к выводу, что со временем положительный эффект Актовегина становится более выраженным. Докладчик наглядно продемонстрировал на графике, что если среднее значение изменений в группе плацебо незначительно повышается через 3 и 6 мес после наблюдений, а затем остается примерно на прежнем уровне, то у Актовегина этот показатель постоянно растет.
Наблюдая за пациентами, ответившими на терапию (ответом на лечение считалось улучшение на ≥4 балла от исходного), доктор Скуг отметил, что по этому параметру разница между Актовегином и плацебо в конце периода терапии составляла 10% в пользу Актовегина и сохранялась в течение всего периода наблюдения, что, по словам докладчика, является очень хорошим показателем для этой группы препаратов.
При сравнении изменений по шкале MoCA с исходными показателями было обнаружено статистически значимое преимущество препарата над плацебо во всех временных точках, что согласуется с первичной конечной точкой.
Кроме того, исследование показало, что доля пациентов с диагностированной деменцией по МКБ-10 через 12 мес была значительно ниже (на 30%) в группе Актовегина в сравнении с группой плацебо.
Говоря о результатах исследования профиля безопасности Актовегина, докладчик подчеркнул, что в целом общее количество ПЭ в группах плацебо и Актовегина было сопоставимым (37,9 и 35,6% соответственно), причем количество серьезных нежелательных явлений в группах активного препарата и плацебо также оказалось аналогичным.
Докладчик озвучил следующие выводы, сделанные на основании исследования ARTEMIDA:
- У пациентов с ПИКН Актовегин более выраженно, по сравнению с плацебо, улучшал когнитивные функции через 6 мес терапии, что подтверждено статистически значимой разницей (p=0,005) в первичной конечной точке по шкале ADAS-Cog+.
- Вторичные конечные точки согласуются с первичной конечной точкой в отношении когнитивных нарушений (изменения по шкале ADAS-Cog+ в сравнении с исходным через 3 и 12 мес; доля ответивших на лечение по ADAS-Cog+ через 3, 6 и 12 мес; изменения по шкале МоСА в сравнении с исходным через 3, 6 и 12 мес).
- В ходе исследования подтвержден хороший профиль безопасности и хорошая переносимость Актовегина пациентами.
Подводя итоги исследования ARTEMIDA, профессор И. Скуг отметил, что назначание Актовегина может быть использовано как один из основных методов лечения ПИКН и деменции у пациентов, перенесших инсульт.
Подготовил Роман Долинский
UA/AVG/0916/0089
При содействии ООО «Такеда Украина»
Медична газета «Здоров’я України» № 17 (390), вересень 2016 p.