23 липня, 2015
Особливості тиреоїдної та глюкокортикоїдної активності при неспецифічних захворюваннях органів дихання та туберкульозі легень у пацієнтів старшого віку

Негативна динаміка демографічних показників, що є характерною і для України (п’яту частину всього населення складають люди пенсійного віку), супроводжується зростанням питомої ваги захворювань органів дихання у загальній структурі хвороб [2]. Серед пенсіонерів Західного регіону (до якого належить Чернівецька область) вона становить 13,3%. Нині все актуальнішим стає питання високого рівня поширеності хронічних неспецифічних захворювань легень (ХНЗЛ) серед осіб старшого віку, діагностика та лікування яких у таких пацієнтів спричинює значні труднощі внаслідок нетиповості перебігу основного захворювання [12], а однією з найскладніших проблем є поліморбідність, у тому числі і поєднання з туберкульозом (ТБ) легень [8].
Зростання частоти розвитку швидко прогресуючих форм медикаментозно-стійкого ТБ з тяжким клінічним перебігом, значною поширеністю патологічного процесу, деструкціями і бактеріовиділенням, що підтримує епідемічний процес у цілому, є проблемним питанням сучасної фтизіатрії. Кожного року в Україні від ТБ помирає близько 870 наших співвітчизників [5]. Прогресуюче збільшення кількості випадків зараження антибіотико-рефрактерними штамами мікобактерій, стійких до двох, трьох і більше протитуберкульозних препаратів, є негативною тенденцією останніх років [2]. Враховуючи вищенаведені дані, очікування швидкої ліквідації епідемії ТБ є сумнівним.
Аналіз літературних джерел свідчить, що з віком зростає не тільки частота ХНЗЛ та супутніх захворювань [8], а й кількість можливих факторів ризику, вплив яких на розвиток та прогресування бронхообструктивного синдрому (БОС) і хронічної запальної реакції з погіршенням респіраторної функції є ще не до кінця вивченим, і, зокрема, це різні варіанти гормонального дисбалансу [14].
Численні дослідження засвідчують, що тривала гіпоксія при запальних захворюваннях бронхолегеневої системи призводить до активації анаеробного гліколізу, перерозподілу кровообігу з переважним кровопостачанням життєво важливих органів (головний мозок, серце, надниркові залози) та, відповідно, зниженням оксигенації інших органів та систем, у тому числі й щитоподібної залози (ЩЗ), спостерігається підсилення тканинного метаболічного ацидозу, що сприяє формуванню тиреоїдної гіпофункції [15].
Отримано нові дані, що недостатня функція ЩЗ та надниркових залоз може бути предиктором тяжчого перебігу ТБ легень [13]. Хоча висловлюється й така думка, що провідна роль у порушенні функціонального стану гіпофіза й надниркових залоз належить хронічній гіпоксії внаслідок поширеного ТБ легень [27]. Гіпоксія тяжкого ступеня може супроводжуватися функціональною недостатністю ЩЗ і спричинювати зрив механізмів компенсації з виснаженням симпато-адреналової системи (САС) як негайного механізму стресорної адаптації [17].
Дослідження механізму виникнення тиреопатій та наслідків впливу порушення функціональної активності ЩЗ і гіпофізу на перебіг захворювань органів дихання специфічного й неспецифічного ґенезу викликає значний інтерес, адже такий аналіз може об’єктивізувати значення тиреоїдної дисфункції як фактора прогресування запальних захворювань дихальної системи та формування ускладнень, оскільки більшість метаболічних процесів у організмі людини перебувають під контролем регуляторної системи, яку утворюють тиреоїдні та глюкокортикоїдні гормони (ГК), а адекватний рівень синтезу, секреції та рецепції йодотиронінів (ЙТ) є необхідною умовою для підтримання гомеостазу і нормального перебігу фізіологічних процесів у організмі [20].
Виходячи з вищевказаних позицій, метою нашого огляду стало визначення особливостей функціонування ЩЗ та ГК-функції надниркових залоз при захворюваннях органів дихання специфічного й неспецифічного ґенезу з формулюванням концепції визначальних чинників прогресування та формування системних проявів обтяжливого впливу гормонально-метаболічно-цитокінової дисфункції при хронічному запаленні.
Аналіз доступних нам джерел літератури та результати власних досліджень щодо тиреоїдного гомеостазу при хронічних захворюваннях органів дихання неспецифічного ґенезу вказує на те, що загострення і тривалий перебіг захворювання є чинником, який спричинює структурну й функціональну нестабільність ЩЗ і гіпофіза, зумовлює формування тиреоїдного та ГК-дисбалансу.
Центральним механізмом регуляції біологічної дії тиреоїдних гормонів на клітини організму, скринінговим тестом для оцінки функції ЩЗ є синтез і секреція гіпофізом тиреотропного гормону (ТТГ) [7]. За результатами цілої низки досліджень установлено пригнічення тиреотропної функції гіпофіза в пацієнтів із хронічними захворюваннями бронхолегеневої тканини, що супроводжується не тільки зниженням умісту ТТГ у плазмі крові (у 91,9% пацієнтів), а і його структурно-морфологічними змінами [12].
За результатами проведеного нами ретроспективного патоморфологічного дослідження тканини гіпофіза у померлих від ХНЗЛ пацієнтів старшого віку, спостерігається вірогідне збільшення кількості базофільних ендокриноцитів за рахунок тиреотропних та кортикотропних типів, що є адаптаційною реакцією напруження регуляторної функції ендокринних залоз при ХНЗЛ в умовах системної дії хронічного запалення на тлі вентиляційно-перфузійної, циркуляторної та тканинної гіпоксії, що супроводжується у частині випадків (8,1%) компенсаторним збільшенням рівня ТТГ. Збільшення кількості хромофобних клітин гіпофіза зумовлено зменшенням числа ацидофільних тропоцитів внаслідок швидкого «аварійного» викиду тропних гормонів при загостренні ХНЗЛ, одночасно вони є джерелом диференціації хромофільних ендокриноцитів (див. рисунок) [9].
Установлено, що на тлі гіпотиреотропонінемії при ХНЗЛ у хворих старших вікових груп має місце гіпотироксинемія (у 75,3% випадків) і зменшення вмісту вільного тироксину (вТ4) не лише нижче середнього значення (СЗ) та у практично здорових осіб, а й відносно нижньої межі фізіологічних коливань (у 42,7%), що можна розглядати як результат посилення периферійного дейодування в Т4 у вільний трийодтиронін (в Т3) – біологічно активніший гормон, який опосередковує метаболічні ефекти вільних тиреоїдних гормонів (ВТГ) на периферії в умовах системного запалення при ХНЗЛ, що свідчить про посилену дисфункційну регуляцію та обмін адаптативних гормонів, які впливають на бронхолегеневу паренхіму.
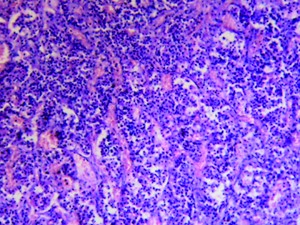 Аденогіпофіз при ХНЗЛ в осіб старшого віку.
Аденогіпофіз при ХНЗЛ в осіб старшого віку.Гістологічний мікропрепарат. Помірна декомплексація, нерівномірне кровонаповнення синусоїдних капілярів, еритростази. Співвідношення базофільних, еозинофільних та хромофобних аденотропоцитів – 1:4:4. Гематоксилін-еозин. Об. х20; ок. х10
Зменшення концентрації ЙТ у старшому віці при тяжкому перебігу ХНЗЛ може бути зумовлено і зниженням синтезу тиронінзв’язувального білка печінкою, у тому числі внаслідок зменшення стимулювальної дії кортизолу. Оскільки зв’язані і вільні форми гормонів перебувають у динамічній рівновазі [7], а здатність проникати у клітини мають лише вільні форми, це означає, що будь-яке зниження концентрації вільного гормону у крові автоматично зменшує зв’язування, і навпаки. Отже, зрозуміло, що не тільки сама ЩЗ, але й білки плазми служать джерелом доступних для клітини вільних ЙТ, тобто відіграють достатньо важливу роль у визначенні «тиреоїдного статусу» організму.
Слід зазначити, що прискорений розпад гормонів ЩЗ за рахунок підвищення їх метаболізму в тканинах при ХНЗЛ супроводжується зниженням з віком тироксинзв’язувальних властивостей сироватки крові [10]. У свою чергу, в осіб старшого віку зменшення концентрації йоду в плазмі крові при підсиленому поглинанні його залозою або виділенні з сечею призводить до відносної субклінічної довготривалої тиреоїдної недостатності [11]. Це узгоджується з даними літератури про підвищення кругообігу ТГ в умовах стресу [27]. Слід мати на увазі, що вся кількість вТ4 секретується ЩЗ, тоді як лише 1/3 визначеного в сироватці Т3 безпосередньо походить з ЩЗ, решта 2/3 – з дейодованого у периферійних тканинах вТ4 [18].
Оптимізація тиреоїдного балансу при змінах фізіологічного стану організму внаслідок загострення ХНЗЛ відбувається за рахунок компенсаторного посилення синтезу вТ3, тобто метаболічні адаптації обумовлені синтезом менш йодованого і більш активного гормону, про що свідчить отримана за результатами нашого дослідження стійка динаміка гіпертрийодотиронінемії у 89,9% пацієнтів на тлі збереження базального рівня тироксину (при цьому не встановлено надмірного зростання рівня ТТГ), що сприяє пристосуванню організму до нових умов існування при прогресуванні захворювання і спрямоване на стимуляцію окиснювальних та метаболічних процесів, які знижені за рахунок різних варіантів гіпоксії (як наслідок інтоксикаційного та бронхолегеневого синдромів). Зокрема, під регуляторним контролем ВТГ знаходиться синтез мітохондріального і загальноклітинного білка, синтез РНК в ядрі й цитоплазмі [18]. Враховуючи схожість хімічної структури ВТГ та катехоламінів, не можна виключати і їх безпосередній вплив на бронхи.
У зв’язку з вищезазначеним можна висунути гіпотезу, що гіпотиреоїдна реакція зі зниженням рівня тироксину в пацієнтів із ХНЗЛ є своєрідною біохімічною адаптацією, яка базується на максимальному використанні йоду з крові і його економному метаболізмі, особливо в умовах екологічного регіонального йододефіциту [14]. На нашу думку, системний дефіцит ВТГ через Т4-залежне зниження функціональної активності ЩЗ, що має місце в пацієнтів із ХНЗЛ та ТБ, зумовлює зниження тиреоїдного дисбалансу на клітинному (тканинному) рівні також і за рахунок потенціювання кортизол-залежного поглинання тироксину клітинами, що підтверджується отриманими нами результатами підвищеного вмісту кортизолу в плазмі крові в 41,6% пацієнтів із ХНЗЛ та практично у всіх обстежуваних хворих на ТБ, а встановлена гіперкортизолемія, у частини пацієнтів, сприяє зростанню активності дейодинази-ІІ (Д-ІІ), яка збільшує локальну концентрацію Т3 у клітинах [11].
Визначені зміни, очевидно, вказують і на те, що зниження синтезу тироксину в обстежених хворих може бути наслідком підвищення утилізації ЙТ тканинами, що підтверджується одержаними значеннями прискорення периферійної конверсії ВТГ у всіх досліджуваних хворих. Тканинні рецептори ВТГ мають набагато більшу спорідненість до Т3, ніж до Т4 [14], і порушення периферійного дейодування Т4 може зумовлювати зміни тиреоїдного статусу організму при ХНЗЛ та ТБ. При цьому зміни рівня вТ3 у пацієнтів із ХНЗЛ, на наш погляд, мають значно більше патогенетичне значення, ніж зміни рівня вТ4.
Так, існує наукова концепція [12], згідно з якою зниження рівня тироксину (мова йде про патологічні стани з інтактною ЩЗ) може бути розцінено як адаптивний механізм, спрямований на збереження енергії й запобігання або сповільнення катаболізму білка в організмі, а зміни утворення вТ3 (можливо, через зниження надходження в клітину Т4) – з позиції патогенезу (зниження активності окиснювальних процесів в тканинах, збереження енергії в організмі при ХНЗЛ та ТБ, особливо в старшому віці). Саме периферійний тканинний дефіцит ВТГ, на нашу думку, впливає на розвиток синдрому «нетиреоїдних захворювань» і відіграє провідну роль у виникненні клінічних проявів гіпотиреозу. Слід подумати про нетиреоїдне захворювання і при зниженому рівні вТ4, що супроводжується нормальним рівнем ТТГ. Однак установлена нами у 75,3% пацієнтів із ХНЗЛ гіпотироксинемія є не тільки загрозою формування синдрому «нетиреоїдної» патології, а й біохімічною ознакою тиреоїдної гіпофункції.
Отже, однією зі значимих причин формування функціональної недостатності ЩЗ при ХНЗЛ та ТБ є найменш вивчені на сьогодні периферійні порушення дії гормонів. Вони охоплюють патологію зв’язування тиреоїдних рецепторів, їх резистентність, пострецепторні порушення, у тому числі й перетворення вТ4 на вТ3 [27].
Загальновідомо, що вільні ЙТ відносно легко проникають крізь мембрану клітини, а внутрішньоклітинні ефекти ВТГ тісно пов’язані з процесами їх метаболізму (у першу чергу з механізмами дейодування) [11]. Найважливішим із таких перетворень є конверсія Т4 у більш активний Т3 шляхом монодейодування зовнішнього тирозильного кільця тироксину в периферійних тканинах. Установлено, що ВТГ модулюють активність Д-ІІ шляхом регуляції швидкості деградації або інактивації ферменту (Т4 і реверсивний Т3 (рТ3) переважно гальмують її активність), тим самим виключаючи можливість участі в цьому процесі ядерних рецепторів вТ3 [7].
При гіпоксії, коли необхідно зберегти енергетичний потенціал, переважає конверсія Т4 у практично позбавлений активності рТ3, в якому атом йоду у внутрішньому кільці відсутній. Цей важливий механізм, завдяки якому самі клітини регулюють кількість активного гормону в мікрооточенні, пояснює, чому в пацієнтів старшого віку з ХНЗЛ коефіцієнт трансформації вТ3/вТ4 не завжди відповідає ступеню тиреоїдної дисфункції. Виявлену нами у частини пацієнтів із ХНЗЛ та ТБ видозміну фону ЙТ (24,7% осіб з гіпертироксинемією і 10,1% – з гіпотрийодтиронінемією) зі змінами трансформації вТ4 у метаболічно активний вТ3 також можна пояснити з позиції утворення рТ3. Регулятори переключення конверсії з біологічно-активного Т3 на неактивний, реверсивний допоки невідомі, але основного значення набуває, очевидно, забезпеченість організму енергією та киснем, особливо в умовах порушення функції зовнішнього дихання (ФЗД) внаслідок ХНЗЛ чи поширеного ТБ легень. Цей процес може залежати також від особливостей циркадного ритму та «пульсуючої» секреторної функції гіпофіза, яка порушується внаслідок підвищення тонусу бронхів у нічний час при ХНЗЛ через порушення його вагусної регуляції, особливо в старшому віці. При цьому може виникати відносний транзиторний гіпотиреоз.
Отже, порушення метаболізму ВТГ у периферійних тканинах може призвести до симптомів гіпотиреозу і, як правило, не відображається на структурі ЩЗ [27]. Однак для пацієнтів із ХНЗЛ та ТБ старшого віку характерною може бути адаптивна функціональна гіперплазія ЩЗ через зниження активності гіпоталамо-гіпофізарної системи. Оскільки ЙТ, за принципом зворотного зв’язку, пригнічують рівень ТТГ, який є одним із факторів, що стимулює гіпертрофію й гіперплазію тиреоцитів, а отже, мають антипроліферативний ефект, то зниження їх вмісту при запальних процесах бронхолегеневої паренхіми різної етіології не забезпечує цього. Відсутність адекватної гіпофізарної реакції на зменшення вмісту ВТГ, можливо, пов’язана і з підвищеним рівнем дофаміну в структурах головного мозку при гіпоксії, який є інгібітором секреції ТТГ [7], та вірогідно високим рівнем кортизолу за отриманими нами результатами досліджень у хворих на ТБ та ХНЗЛ [3, 16, 21].
Ймовірно, що зростання вмісту кортизолу сприяє зменшенню синтезу ТТГ навіть в умовах установленої нами гіпотироксинемії, що може зменшувати прояви субклінічного гіпотиреозу, однак його гіперреактивність сприяє персистенції запалення та системним ефектам при ХНЗЛ, оскільки встановлено, що ГК збільшують тривалість життя нейтрофілів та імунокомпетентних клітин за рахунок гальмування їх апоптозу [24— 26]. Гіперкортизолемія також є одним з регуляторів переключення конверсії Т4 у Т3 за рахунок збільшення синтезу рТ3.
На нашу думку, біологічна активність гормонів у осіб старшого віку може знижуватися внаслідок того, що з віком зменшується геномний ефект дії ГК та ВТГ зі зниженням ацетилювання гістонів і доступності до ДНК, що супроводжується зменшенням транскрипційної активності. Зокрема, ГК зумовлюють геномний ефект (трансактивацію) шляхом ацетилювання гістонів, навколо яких закручується спіраль ДНК, що відкриває доступ до структури хроматину, запускаючи процес транскрипції генів, які беруть участь у синтезі протизапальних білків (ліпокортину, антагоніста рецепторів інтерлейкіну-1 (ІЛ-1), інгібітора ядерного фактора-κВ (NF-κB), ІЛ-10, нейтральної ендопептидази, β2-рецепторів тощо) [12, 23].
Суттєву роль у пригніченні запальної реакції при ХНЗЛ відіграє і позагеномний ефект ГК (трансрепресія), одним з молекулярних механізмів якого є гальмування, під дією кортизолу, запальних генів через активацію деацетилази, що призводить до ущільнення структури хроматину й обмеження доступу до ДНК факторів транскрипції з подальшим пригніченням синтезу низки прозапальних медіаторів (ІЛ-1, -2, -3, -4, -6, -8; фактора некрозу пухлин- α (ФНП-α); гранулоцитарно-макрофагального колонієстимулювального фактора (ГМКСФ); матричної металопротеїнази-9) [26]. Окремі повідомлення свідчать про зниження під впливом паління й вільних радикалів при ХНЗЛ та ТБ активності деацитилази гістонів, яка і є мішенню для дії ГК [1], що також може зменшувати їх гальмівний вплив на транскрипцію генів і послаблювати протизапальну та системну дію.
Направленість впливу кортизолу на функціональну активність ЩЗ при ХНЗЛ залежить від загального метаболізму, а з віком формується прогресуюче виснаження ГК-функції кіркової речовини надниркових залоз, що може супроводжуватися зниженням його рівня в плазмі крові. Аналіз вмісту кортизолу у пацієнтів із ХНЗЛ показав, що СЗ показника у досліджуваній вибірці є нижчим за норму. Індивідуальний розподіл продемонстрував, що у 58% випадків він є нижчим за вікову норму (нижче нижньої межі індивідуальної чутливості у 11,24% хворих і в межах референтних коливань – у 48%). Нормалізація гіпокортизолемії у таких пацієнтів із ХНЗЛ може мати ефект активації метаболізму та впливати на загальні обмінні процеси в організмі, у тому числі й клінічні прояви перебігу та прогресування захворювання.
У 41,6% хворих на ХНЗЛ вміст кортизолу вірогідно перевищував вікову норму і СЗ, що забезпечило адаптацію до стану хронічного гіпоксично-метаболічного стресу при ХНЗЛ на тлі гіпофункції ЩЗ шляхом активації стійких ендокринних механізмів, які спрямовані на реакції автоагресії в організмі та зниження рівня ТТГ, що підтверджується результатами патоморфологічного дослідження (вірогідно збільшується середній об’єм каріона клубочкової, пучкової та сітчастої зон надниркових залоз). Це є компенсаторним механізмом системної реакції на загострення захворювання, який, однак, у старшому віці є недосконалим, оскільки морфометрія кіркової речовини надниркових залоз засвідчила невірогідне збільшення її клубочкової та пучкової зон. Про компенсаторне напруження негайного механізму стресорної адаптації з тривалою активацією САС в умовах хронічного запалення при ХОЗЛ свідчить збільшення мозкового шару надниркових залоз (у 2 рази), що підтверджується отриманими нами показниками зростання катехоламіндепонувальної функції еритроцитів у загальній вибірці хворих. У старшому віці цей механізм не супроводжується збільшенням об’єму каріона, що свідчить про зниження адаптаційних можливостей САС.
Виявлене нами напруження функціональних резервів гіпоталамо-гіпофізарно-тиреоїдної системи за результатами кореляційного аналізу, аж до повного виснаження її резервних можливостей, може призводити до підвищеної стимуляції продукції ТТГ гіпофізом, що з плином часу сприяє маніфестації прихованої тиреоїдної недостатності та призводить до запуску механізмів формування морфологічних патологічних змін ЩЗ при ХНЗЛ в осіб старшого віку. Згідно з існуючою теорією тиреотропної залежності збільшення поглинання екзогенного і повторного використання ендогенного йоду для синтезу ВТГ, вважають, що під впливом ТТГ може наставати гіпертрофія й гіперплазія фолікулярних клітин ЩЗ [19, 22].
Так, за результатами патоморфологічних проспективних досліджень установлено, що зміни функціонального стану ЩЗ при ХНЗЛ у старшому віці впливали на ступінь вираженості морфологічних змін її паренхіми, що характеризувалися дистрофічними й атрофічними процесами і залежали від варіанту тиреопатії. Вірогідне збільшення площі й діаметру фолікула та накопичення колоїду при морфометричному дослідженні супроводжується зростанням функціональної активності ЩЗ (гіпертироксинемія у 51,7% випадків, гіпертрийодтиронінемія – у 34,8%).
Функціональні ознаки гіпофункції ЩЗ узгоджуються з морфологічними змінами будови її паренхіми (переважання великих фолікулів, сплощення тиреоїдного епітелію та зменшення площі фолікулярного епітелію, середньої площі та висоти тироцита, зниження фолікулярно-колоїдного індексу та збільшення індексу накопичення колоїду). Проліферація та гіперплазія екстрафолікулярного епітелію, фокальне потовщення стінок окремих фолікулів, поява фестончастих фолікулів у паренхімі ЩЗ, переважно при ХНЗЛ та ТБ в осіб жіночої статі, свідчать про гіперплазію епітеліального компоненту залози і нагадують зобоподібні зміни.
Зниження рівня ТТГ при ХНЗЛ (у 91,9%) зумовлює зменшення поглинання йоду тироцитами, а низька інтратиреоїдна концентрація йоду спричинює швидке збільшення розмірів вузлових утворень і об’єму ЩЗ [11]. У результаті цих процесів залоза, для забезпечення організму достатньою кількістю гормонів, збільшується в розмірах, і формується дифузний чи вузловий зоб. Однак проліферативні й трофічні ефекти ТТГ у пацієнтів старшого віку при ХНЗЛ не є провідними та можуть бути опосередковані, на наш погляд, іншими факторами.
Так, йод, потрапляючи в тироцит, утворює з ліпідами сполуки (йодолактони), які є потужними блокаторами продукування інсуліноподібного росткового фактора-1 (ІРФ-1) та інших росткових факторів, а зниження його вмісту в тканині ЩЗ спричинює посилене продукування місцевих факторів росту (ІРФ 1-β типу, епідермальний ростовий фактор, основний фактор росту фібробластів, трансформуючий фактор росту-β) [4, 6]. Отже, за відсутності чи нестачі йоду послаблюється блокада факторів росту, які стимулюють проліферативні процеси, закономірним результатом чого є гіперплазія тироцитів. Крім того, йодовані ліпіди пригнічують в тироциті цАМФ-залежні процеси, активність інозитолтрифосфату і цим самим запобігають проліферувальному та гормонсинтезувальному ефектам ТТГ в умовах достатньої кількості йоду в тироцитах [12].
Пріоритетним дослідженням щодо встановлення автоімунної патології ЩЗ є виявлення позитивних антитіл до тиреопероксидази (АТ-ТПО). Показано, що в пацієнтів літнього та старечого віку із ХНЗЛ частота виявлення АТ-ТПО становить 18,7%, і частіше спостерігається в осіб з підвищеним рівнем ТТГ, не залежить від стадії перебігу захворювання, переважає в осіб жіночої статі. На думку багатьох дослідників [14], рівень АТ-ТПО є більш специфічним маркером тиреоїдної автоагресії, у той час як вміст антитіл до тиреоглобуліну хоч і є маркером автоімунної реакції проти антигену ЩЗ, але може бути підвищеним при багатьох інших станах [27]. У зв’язку з цим, саме АТ-ТПО посідають пріоритетне місце в оцінці специфічної тиреоїдної автоагресії ЩЗ в умовах коморбідності при ХНЗЛ та ТБ, яка зумовлює у подальшому формування тиреопатій у пацієнтів старших вікових груп.
За результатами наших досліджень, у частини хворих на ХНЗЛ формуються дисфункціональні зміни в тиреоїдній системі з переважанням явищ гіпертиреозу. Про зростання гормонсинтетичної активності ЩЗ при ХНЗЛ свідчить вірогідне збільшення рівня вТ3 (34,8%) на тлі гіпертироксинемії (24,7%) і зниження рівня ТТГ (8,1%). Збільшення співвідношення вТ3/вТ4 також вказує на переважання утворення вТ3 власне в ЩЗ. Це може бути зумовлено тим, що при гіпоксії у ЩЗ збільшується внутрішньотиреоїдне дейодування Т4 у Т3. Ймовірно, в осіб старшого віку гіпертиреоз може характеризуватися значним підвищенням чутливості периферійних тканин до ТГ при порівняно невисокій їх концентрації у крові (верхня межа норми), що узгоджується з результатами цілої низки досліджень, які стосуються власне патології ЩЗ [12]. При гіпертиреозі порушується метаболізм ГК, що підтверджується отриманими нами результатами зменшення рівня кортизолу у цій вибірці обстежуваних, знижується чутливість гладенької мускулатури бронхів до β-адреностимуляторів, спотворюється обмін простагландинів і гістаміну [20], що в сукупності сприяє розвитку БОС.
Таким чином, у хворих на ХНЗЛ та ТБ старшого віку мають місце істотні порушення тиреоїдного гомеостазу, які носять різноспрямований характер і свідчать про приховані порушення функції ЩЗ. Біохімічним вираженням тиреоїдної дисрегуляції є економізація гормонального метаболізму, яка заснована на зміні співвідношення ВТГ за рахунок зсуву протеідизації в бік вТ3, що є проявом однієї з компенсаторних реакцій підтримання тиреоїдного гомеостазу і підтверджується встановленим дуже сильним вірогідним прямим кореляційним зв’язком між вільними формами ЙТ (r=0,99, р<0,001). Оптимізація тиреоїдного статусу при змінах фізіологічного стану організму внаслідок ХНЗЛ, що відбувається за рахунок трийодотиронінемії, сприяє метаболічній адаптації організму до нових умов існування, що відбувається за гіпотиреоїдним адаптативним типом.
Дезадаптаційний тиреоїдний синдром проявляється зниженням рівня тироксину, ТТГ, гіпертрийодтиронінемією, помірним зростанням периферійної конверсії ВТГ. На нашу думку, порушення периферійного метаболізму ТГ та зниження функціональної активності ЩЗ в осіб старшого віку відіграють провідну роль у виникненні біохімічних ознак та клінічних проявів гіпотиреоїдизму в пацієнтів із ХНЗЛ та ТБ легень і формують синдром «нетиреоїдних захворювань», можуть відігравати важливу роль у розходженні між клінічною картиною гіпотиреозу і нормальними лабораторними тестами, рівнем ТТГ.
Характерною рисою перебігу ХНЗЛ та ТБ у пацієнтів старшого віку, у більшості випадків, особливо при інфекційному характері запального процесу в дихальних шляхах, є відносна субклінічна довготривала тиреоїдна недостатність, що не компенсується зростанням периферійної конверсії ВТГ. Функціональні порушення в тиреоїдній системі та ГК-дисбаланс у осіб старшого віку є одними з чинників частих рецидивів ТБ та загострення ХНЗЛ і одними з проявів системної запальної реакції, що потребує медикаментозної корекції для сповільнення темпів прогресування хвороби та формування ремоделювання незворотних змін бронхолегеневої паренхіми.
Зміни механізму гормональної взаємодії ендокринних залоз при ХНЗЛ у старшому віці проявляються на рівні вертикальної регуляції гіпофіз-ЩЗ-периферійна конверсія, про що свідчать виявлені сильні корелятивні зв’язки між ТТГ та вТ4 і вТ3, та між Т3 і Т4. Зростання кількості кореляційних зв’язків між окремими показниками тиреоїдної системи в пацієнтів із ХНЗЛ є ознакою її функціонального напруження. Наявність пермісивної ендокринної взаємодії при ХНЗЛ підтверджується встановленими тісними прямими кореляційними зв’язками між рівнями кортизолу та ВТГ і ТТГ. Отримані результати дають змогу деталізувати існуючі на сьогодні відомості про схильність у осіб старшого віку до формування синдрому полігландулярної недостатності через порушення пермісивної гормональної взаємодії внаслідок зниження активності метаболічних процесів при ХНЗЛ та ТБ у хворих старших вікових груп та порушення інтратиреоїдального метаболізму йоду і синтезу кортизолу.
Аналіз отриманих результатів вказує на те, що різноспрямована компенсаторна реакція гіпофізарно-тиреоїдної та ГК-систем при ХНЗЛ у осіб старшого віку залежить від ступеня морфологічних змін бронхолегеневої паренхіми, що відповідає стадії перебігу захворювання і включає в себе більшу частину компоненту незворотної обструкції. За результатами проведеного патоморфологічного дослідження встановлено, що характерною морфологічною картиною слизової оболонки бронхів при ХНЗЛ у хворих старшого віку є ознаки хронічного запалення: деструкція тканини з пошкодженням епітелію; підвищена судинна проникність, яка поєднується з набряком і міграцією ефекторних клітин (нейтрофіли, макрофаги); розростання сполучної тканини підслизового шару; гіперплазія та гіпертрофія бронхіальних залоз з гіперсекрецією слизу, що супроводжується компенсаторною гіперплазією внутрішньої еластичної мембрани легеневих артерій, яка має пристосувальний характер.
Метаболічні стимулювальні чинники, що утворюються при ХНЗЛ, визначають адаптацію тиреоїдних механізмів і обумовлюють підвищені вимоги до ЩЗ, яка відповідає на них посиленням синтезу ВТГ (рівень яких, однак, не виходить за межі еутиреозу). Компенсаторною реакцією тиреоїдного дисбалансу є збільшення внутрішньотиреоїдного дейодування вТ4 у вТ3 з утворенням надлишку активного трийодтироніну (збільшується співвідношення вТ3/вТ4), тобто відбувається оптимізація тиреоїдного статусу. Підвищений рівень ТТГ і вТ4 при ХНЗЛ та ТБ можна пояснити транзиторною адаптаційною активацією гіпоталамо-гіпофізарно-тиреоїдної та ГК-вісі. Зростання рівня вТ3 при ХНЗЛ нетяжкого перебігу, ймовірно, пов’язане з компенсаторною активацією САС та більш частим прийомом адреноміметиків цією категорією осіб, що забезпечує підвищену дейодизацію вТ4 на периферії.
Література
1. Абдулаев Р. Сдвиги в системе гемостаза – компонент системного воспалительного ответа при туберкулезе легких / Р. Абдулаев, Г. Каминская, О. Комиссарова // Врач. – 2012. – № 2. – С. 7–11.
2. Александріна Т.А. Особливості епідемії туберкульозу в Україні / Т.А. Александріна // Туберкульоз, легеневі хвороби, ВІЛ-інфекція. – 2012. – № 2. – С. 7–13.
3. Карачунский М.А. Молекулярная эпидемиология туберкулеза / М.А. Карачунский // Проблемы туберкулеза и болезней легких. – 2007. – № 4. – С. 3–7.
4. Лядова И.В. Реакция Т-клеточного иммунитета при туберкулезе: экспериментальные и клинические исследования / И.В. Лядова, В.А. Гергерт [и др.] // Туберкулез и болезни легких. – 2009. – № 11. – С. 9–18.
5. Москаленко В.Ф. Досягнення та перспективи розвитку фтизіатрії / В.Ф. Москаленко, В.І. Петренко, Г.В. Радиш // Туберкульоз, легеневі хвороби, ВІЛ-інфекція. – 2013. – № 1. – С. 5–13.
6. Продукція деяких цитокінів та її залежність від стану імунної системи у хворих на туберкульоз легенів / К.Ф.Чернушенко [та ін.] // Імунологія та алергологія. – 2007. – № 4. – С. 109–110.
7. Самсонова Л.Н., Касаткина Э.П. Нормативы уровня тиреотропного гормона в крови: современное состояние проблемы // Проблемы эндокринологии. – 2007. – Т. 53, № 6. – С. 40–43.
8. Синдром системного воспалительного ответа при туберкулезе легких / Г.О. Каминская, Р.Ю. Абдулаев, Е.В. Мартынова [и др.] // Туберкулез и болезни легких. – 2009. – № 11. – С. 40–48.
9. Тодоріко Л.Д. Структурно-морфологічні та функціональні зміни гіпофізу, щитоподібної залози, наднирників при ХОЗЛ у пацієнтів літнього та старечого віку / Л.Д. Тодоріко // Здобутки клін. та експ. мед. – 2008. – № 2. – С. 87–93.
10. Тодоріко Л.Д. Розповсюдженість та характер тиреопатій у пацієнтів старшого віку при ХОЗЛ / Л.Д. Тодоріко, О.В. Бесединська, С.А. Андрєєв // Бук. мед. вісник. – 2008. – № 3. – С. 45–48.
11. Тодоріко Л. Д. Функціональні зміни щитоподібної залози, тиреотропна функція гіпофізу та дія кортизолу при хронічних обструктивних захворюваннях легень у хворих старшого віку / Л.Д. Тодоріко // Укр. пульмон. ж. – 2008. – № 4 – С. 50–54.
12. Тодоріко Л.Д. Хронічні обструктивні захворювання легень: особливості патогенезу системних проявів та удосконалення лікування хворих старших вікових груп / Л.Д. Тодоріко, І.О. Сем’янів // Чернівці, Буковинський державний медичний університет, 2011. – 249 с.
13. Тодоріко Л.Д. Функціональний стан ЩЗ при ТБ легень – сучасний стан проблеми / Л.Д. Тодоріко, А.О. Герман, А.В.Бойко // Бук. мед. вісник. – 2012. – № 3. – С. 132–135.
14. Тронько М.Д., Замотаєва Г.А. Імуноендокринологія: основні досягнення, проблеми і перспективи // Внутрішня медицина. – 2007. – № 3. – С. 7–14.
15. Филинюк О.В. Факторы риска, ассоциированные с множественно лекарственно-устойчивым туберкулезом: автореф. дис. на соискание научн. степени доктора мед. наук: спец. 14.01.16 «Фтизиатрия» / О.В. Филинюк. – Новосибирск, 2011. – 36 с.
16. Chemokine/cytokine production bymononuclear cells from human lymphoid tissuesandt heirmodulationby Mycobacterium tuberculosisantigens / N.V. Serbina, V. Lazorevic, J.L. Flynn [et al.] // J. Immunol. – 2001. – Vol. 167. – P. 6991–7000.
17. Correlates of non-thyroidal illness syndrome in chronic obstructive pulmonary disease / F.Karadag, H. Ozcan, A.B. Karul [et al.] // Respir. Med. – 2007. – № 7. – P. 1439–1446.
18. Davidson A. Autoimmune thyroid diaseases //А. Davidson, В. Diamond // Curr. Opin. Rheumatol. – 2007. – Vol. 19, № 1. – P. 44–48.
19. Functional characteristics of neutrophil sand mononuclear cells from tuberculosis patientsti mulated in vitro with heatkilled M. tuberculosis / G. Fiorenza, M.A. Farroni, C. Bogu [et al.] // Arch. Med. Res. – 2007. – Vol. 38, № 5. – Р. 526–533.
20. Gallegos A. Central tolerance: good but imperfect / А. Gallegos, M.J. Bevan // Immunol Rev. – 2006. – Vol. 209. – P. 290–297.
21. Innate Immune Recognition of Mycobacterium tuberculosis / J. Kleinnijenhuis, M. Oosting, L.A.B. Joosten [et al.] // Cpn Dev Immunol. 2011: [Электронный pecypc]. – Режим доступа к документу: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3095423.
22. Khader S.A. IL-23 and IL-17 in tuberculosis / S.A. Khader, A.M. Cooper // Cytokine. – 2008. – Vol. 41, № 2. – P. 79–83.
23. Kruuner A. Evaluation of MGIT 960-based antimicrobial testing and determination of critical concentrations of first- and second-pne antimicrobial drugs with drug-resistant cpnical strains of Mycobacterium tuberculosis/ A. Kruuner, M.D. Yates, F.A. Drobniewski // J. Cpn. Microbiol. – 2006. – № 44. – P. 811–818.
24. Lalvani A. T Cells and Tuberculosis: Beyond Interferon-gamma / A. Lalvani. K.A. Milpngton // J. Infect. Dis. 2008. – Vol. 197. – P. 941–943.
25. Lymphocyte subpopulations in pulmonary tuberculosis patients / F. Defeci, H.H. Akbulut, I. Cepk [et al.] // Mediators Inflamm. – 2006. – P. 1 –6 ID89070.
26. Making sense of a missense nutation: characterization of MutT2, a Nudix hydrolase from Mycobacterium tuberculosis, and the G58R mutant encoded in W-Beijing strains of M.Tuberculosis / N.J. Moreland, C. Charper, A.J. Dingley [et al.] // Biochemistry. – 2009. – Vol. 8.– P. 699–708.
27. Visser J. The elemental importance of sufficient iodine intake: a trace is not enough / J. Visser // Endocrinology. – 2006. – Vol. 147 (5). – P. 2095–2097.


