27 листопада, 2016
Клиническая эффективность и безопасность высокодозовой терапии дорипенемом у пациентов с пневмонией
По данным ВОЗ, пневмония занимает третье место среди ведущих причин смерти в Японии.
В развивающихся странах смертность от пневмонии в 3-5 раз выше по сравнению с развитыми странами.
В ближайшее десятилетие ожидается рост заболеваемости пневмонией, прежде всего за счет старения населения.
В лечении тяжелых бактериальных инфекций, в частности пневмонии, важнейшую роль играют антибактериальные препараты класса карбапенемов. В соответствии с Протоколом по оказанию медицинской помощи пациентам с пневмонией (приказ МЗ № 128 от 19 марта 2007 г.) карбапенемы показаны пациентам с внебольничной пневмонией III группы (с нетяжелым заболеванием, требующим госпитализации в терапевтическое отделение по медицинским показаниям) на втором этапе антибактериальной терапии, а также больным ранней нозокомиальной пневмонией с факторами риска наличия полирезистентных штаммов возбудителей и пациентам с поздней нозокомиальной пневмонией. Согласно зарубежным руководствам карбапенемы рекомендуются для лечения пациентов с умеренно тяжелой, тяжелой и очень тяжелой пневмонией при наличии факторов риска мультирезистентных патогенов, больных умеренно тяжелой и тяжелой нозокомиальной пневмонией (hospital-acquired pneumonia – HAP), включая вентилятор-ассоциированную пневмонию (ventilator-associated pneumonia – VAP).
Дорипенем (Дорибакс®) – современный карбапенем для парентерального введения, впервые появившийся на фармацевтическом рынке Японии в 2005 г.
Дорипенем характеризуется широким спектром антимикробной активности, включающим грамположительные и грамотрицательные, аэробные и анаэробные микроорганизмы, в том числе неферментирующие бактерии (P. aeruginosa, Acinetobacter spp.). Дорипенем активен в отношении метициллинчувствительных стафило-, стрептококков (в том числе пенициллинрезистентных), микроорганизмов семейства Enterobacteriaceae, Haemophilus influenzae, Bacteroides spp., Prevotella spp., Clostridium spp. и других грамположительных анаэробов. Особое значение имеет высокая активность дорипенема в отношении патогенов, обладающих множественной устойчивостью к различным антибиотикам, в частности в отношении грамотрицательных бактерий, продуцирующих бета-лактамазы: Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis. Среди всех карбапенемов дорипенем является наиболее активным в отношении пенициллинрезистентных стрептококков, а также проявляет более высокую in vitro активность, чем имипенем и меропенем, в отношении грамотрицательных микроорганизмов, продуцирующих ряд бета-лактамаз расширенного спектра (extended-spectrum beta-lactamases, ESBL) и бета-лактамаз класса С (AmpC) (X. -Y. Qu et al., 2015).
Терапевтическая эффективность дорипенема в лечении взрослых пациентов с нозокомиальной пневмонией была продемонстрирована в рандомизированных контролированных исследованиях. Метаанализ эффективности и безопасности дорипенема в лечении бактериальных инфекций, включая пневмонию, подтвердил высокую эффективность и благоприятный профиль безопасности препарата (X. -Y. Qu et al., 2015).
Недавно было опубликовано новое исследование, проведенное в Японии, в котором оценивали эффективность и безопасность высокодозовой терапии дорипенемом (3 г/сут; 1-часовая внутривенная инфузия 1 г дорипенема 3 раза в сутки) у пациентов с пневмонией, в том числе нозокомиальной. (Yatera K. et al. Clinical efficacy and safety of high-dose doripenem in Japanese patients with pneumonia. J Infect Chemother. 2016; 22: 137-142).
Материалы и методы
Проспективное многоцентровое исследование проводилось с декабря 2013 по апрель 2015 года, было одобрено локальными этическими комитетами в каждом клиническом центре в Японии и включило 59 пациентов. Трое из них были позже исключены из-за легочного микоза (n=1) и неинфекционных причин (n=2), а характеристики оставшихся 56 представлены в табл. 1. Все больные предоставили письменное информированное согласие на участие.
Пневмонию диагностировали при наличии трех критериев: по крайней мере 1 симптом (лихорадка, кашель, гнойная мокрота, влажные хрипы, плевральная боль, одышка, тахипноэ); новые легочные инфильтраты по данным рентгенографии грудной клетки; по крайней мере 1 признак воспаления (лейкоцитоз >10×109/л или <4,5×109/л, повышенный уровень С-реактивного белка (СРБ) в сыворотке, температура тела ≥37 °С).
Критерии исключения: противопоказания к назначению дорипенема; почечная недостаточность с >5-кратным повышением уровней аланинаминотрансферазы (АЛТ) и/или аспартатаминотрансферазы (АСТ) выше верхней границы нормы; почечная недостаточность с >2-кратным повышением азота мочевины в сыворотке и/или креатинина в сыворотке; фебрилитет неинфекционной этиологии; судорожные заболевания; терапия вальпроевой кислотой.
Дорипенем (1 г) назначали внутривенно в течение 1 ч с интервалом 8 ч, лечение продолжалось от 3 до 14 дней. Помимо стартовой высокодозовой терапии дорипенемом (3 г/сут), дорипенем 3 г/сут назначали пациентам, которые изначально получали дорипенем 1,5 г/сут или другие антибиотики (кроме карбепенемов) и в течение 3 дней не ответили на эти препараты согласно критериям клинической эффективности при лечении респираторных инфекций. Сопутствующее применение кортикостероидов и других противомикробных средств, в том числе макролидов, на протяжении исследования не разрешалось.
Первичной конечной точкой была клиническая эффективность (КЭ) в конце лечения, определяемая по изменениям клинических симптомов, лабораторных и радиографических данных. КЭ констатировалась при удовлетворении ≥3 критериев из следующих: уменьшение или полное разрешение клинических симптомов; нормализация температуры тела; улучшение радиографической картины – размеры легочных инфильтратов ≤70% от исходных; лейкоцитоз <9,0×109/л; снижение уровня СРБ до ≤30% от исходного. При несоответствии критериям эффективности лечение считали неэффективным.
Побочные реакции регистрировали с начала терапии до 3 дней после отмены дорипенема в соответствии с Общими терминологическими критериями неблагоприятных событий (Common Terminology Criteria for Adverse Events, CTCAE, версия 4.0).
До начала терапии дорипенемом были взяты образцы крови, мокроты и жидкости, полученной с помощью бронхоальвеолярного лаважа, для последующей окраски по Граму и, по возможности, культурального исследования.
Результаты
Клиническая эффективность
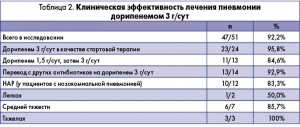
На протяжении исследования 5 пациентов были исключены из общего числа из-за значительного повышения печеночных ферментов (n=2) или ухудшения рака легких (n=3). Клиническая эффективность лечения, оцененная у 51 больного, представлена в таблице 2. Лечение дорипенемом 3 г/сут было эффективным у 92,2% (47/51) пациентов, в том числе у 95,8% (23/24) больных, изначально получавших дорипенем 3 г/сут, у 92,9% (13/14) участников, переведенных на дорипенем с других антибиотиков, и у 84,6% (11/13) пациентов, у которых доза дорипенема была увеличена с 1,5 до 3 г/сут (табл. 2). Статистически значимые различия по эффективности между этими тремя группами отсутствовали.
Частота ответа у пациентов НАР составила 83,3% (10/12) (табл. 2), средняя продолжительность терапии дорипенемом 3 г/сут – 7,9±3,2 дня.
Безопасность лечения
Отмеченные побочные реакции представлены в таблице 3. Повышения креатинина сыворотки не отмечено ни в одном случае. Печеночная дисфункция 3 степени наблюдалась у 1 пациента; остальные побочные реакции соответствовали 1 степени. Во всех случаях лабораторные отклонения нормализовались в ближайшем периоде после отмены дорипенема.
Обсуждение
У пациентов с пневмонией высокодозовая терапия дорипенемом (3 г/сут) продемонстрировала высокую эффективность (в среднем 92,2%) и благоприятный профиль безопасности. При назначении дорипенема 3 г/сут в качестве стартовой антибиотикотерапии эффективность была несколько выше (95,8%), чем при переводе на дорипенем 3 г/сут с других антибиотиков (92,9%) или дорипенема 1,5 г/сут (84,6%), хотя разница была статистически незначимой.
Дорипенем ингибирует биосинтез бактериальной стенки путем инактивации пенициллинсвязывающих протеинов и является резистентным к большинству β-лактамаз, включая пенициллиназы и карбапенемазы, что обеспечивает широкий спектр активности против грамотрицательных бактерий. In vitro дорипенем демонстрировал такой же спектр активности в отношении грамотрицательных и грамположительных микроорганизмов, как и меропенем и имипенем соответственно. Кроме того, по сравнению с имипенемом и меропенемом дорипенем обладает такой же или более высокой активностью против таких продуцентов ESBL, как Enterobacteriaceae (Escherichia coli and Klebsiella spp.) и Enterobacter spp. Активность дорипенема против P. aeruginosa и Acinetobacter spp. соответствует таковой меропенема, при этом дорипенем обладает более высокой активностью в отношении большого количества анаэробов. Вышеуказанные характеристики дорипенема позволяют рассматривать его в качестве стартового антибиотика выбора в лечении нозокомиальной пневмонии, включая пневмонию, связанную с искусственной вентиляцией легких.
Повышение дозы дорипенема с 1,5 до 3 г/сут сопровождалось высокой частотой ответа (84,6%). Нарушенный клиренс дыхательных путей и низкий кровоток в пораженных легочных очагах могут приводить к низкому распределению антимикробных препаратов у таких больных; это объясняет недостаточный ответ на дорипенем 1,5 мг/сут и хорошую эффективность дозы 3 г/сут. Ранее в фармакокинетическом исследовании у пациентов с нозокомиальной пневмонией геометрическая средняя максимальной концентрации в плазме после 1-часовой инфузии дорипенема 0,5 г составила 22,4 мкг/мл через 1 ч, период полувыведения – 1,89 ч, в результате чего у 40% пациентов был превышен показатель ТАМ (time above MIC/24h – процент времени, на протяжении которого концентрация препарата в плазме превышает минимальную подавляющую концентрацию – МПК – при оценке за 24 ч) при МПК 2 мкг/мл. Повышенная доза дорипенема может обеспечивать более высокий ТАМ; в свою очередь, достижение более высоких концентраций препарата в легочной ткани реализуется в лучшей клинической эффективности. Таким образом, в группе пациентов с нарушенным клиренсом и/или кровотоком в дыхательных путях (хроническая обструктивная болезнь легких, легочный абсцесс, инфицированная булла, обструктивная пневмония), более целесообразно использование дорипенема 3 г/сут.
Побочные реакции наблюдались у 19,7% пациентов; подавляющее большинство таких реакций имели легкий или умеренный характер (≤2 степень по классификации CTCAE) и представляли собой незначительное повышение АЛТ и/или АСТ, которое нормализовалось после отмены препарата. Согласно ранее опубликованным данным при оценке высокодозовой терапии меропенемом (3 г/сут) и биапенемом (1,2 г/сут) у пациентов с респираторными инфекциями дорипенем продемонстрировал более низкую частоту побочных реакций (16,1%) в отличие от меропенема (35,4%) и биапенема (33,0%). Результаты настоящего исследования согласуются с этими данными и подтверждают благоприятный профиль безопасности высокодозовой терапии дорипенемом.
В предыдущих исследованиях при лечении дорипенемом 1,5 г/сут пациентов с нозокомиальной пневмонией (n=223) частота побочных реакций также была низкой (повышение γ-глутамилтрансферазы – 2,7%, тромбоцитопения – 1,8%, диарея – 1,8%, повышение АЛТ и АСТ – 1,8 и 1,3% соответственно).
Оценка профиля безопасности дорипенема, основанная на данных 7 клинических исследований, показала, что частота побочных реакций и досрочной отмены лечения вследствие лекарственно-индуцированных неблагоприятных событий у пациентов, получавших дорипенем, такая же, как и у больных, которым назначали другие антибактериальные препараты – левофлоксацин, меропенем, имипенем и пиперациллин/тазобактам.
Во многих руководствах по ведению пневмонии, в частности в руководстве Японского общества по респираторным заболеваниям (Japanese Respiratory Society, JRS), карбапенемы рекомендуются как препараты первого выбора для лечения больных со среднетяжелой и тяжелой HAP.
Выводы
Таким образом, высокодозовая терапия дорипенемом (Дорибакс®) 3 г/сут показала высокую эффективность и благоприятный профиль безопасности. Эта доза одобрена в Украине для лечения тяжелой нозокомиальной пневмонии, включая пневмонию, связанную с искусственной вентиляцией легких. Препарат назначается каждые 8 ч в виде инфузии длительностью 1 или 4 ч. Четырехчасовая инфузия более предпочтительна для лечения тяжелой пневмонии.
Статья подготовлена и адаптирована Александром Гладким
Адаптировано и переведено согласно оригинальной статье Yatera K. et al. Clinical efficacy and safety of high-dose doripenem in Japanese patients with pneumonia. J Infect Chemother. 2016; 22: 137-142.
UA/DOR/0916/0031