31 травня, 2016
Загальний підхід до медикаментозного лікування пацієнтів похилого та старечого віку

Старіння – фізіологічний процес, який розвивається з віком під впливом екзогенних та ендогенних факторів і проявляється обмеженням адаптаційних можливостей організму, підвищенням вірогідності розвитку захворювань і смерті. За класифікацією Всесвітньої організації охорони здоров’я (2012), виокремлюють такі вікові періоди: від 25 до 44 років – молодий вік; 44-60 років – середній; 60-75 років – літній; 75-90 років – старечий; понад 90 років – вік довгожителів.
Демографічна еволюція призвела до значного збільшення кількості людей віком понад 65 років. Україна належить до демографічно старих країн світу. Частка населення, старшого за працездатний вік, становить 23,4% з прогнозованою тенденцією до подальшого підвищення. За даними Global Age Watch Index 2013, до 2050 р. кількість літніх людей в Україні перевищить 30%. Загальний показник захворюваності літнього населення у 2,6 рази вищий, ніж такий в популяції працездатного віку; загальні показники інвалідності та смертності є більшими відповідно в 1,5 та 8 разів. Серед населення віком ≥70 років 18,3% осіб потребують щоденної соціально-побутової допомоги, 82% постійно приймають ліки.
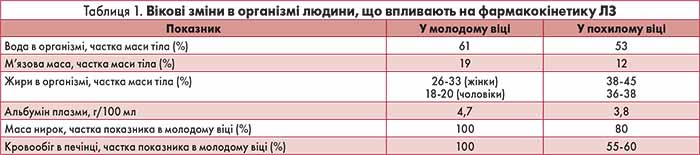
Функціональні здатності більшості систем та органів після 45 років поступово знижуються. Специфіка геріатричної фармакотерапії зумовлена морфологічними та функціональними порушеннями, що виникають в організмі при старінні (табл. 1). Це призводить до вікових змін фармакокінетики лікарських засобів (ЛЗ): усмоктування, розподілу, біотрансформації й елімінації. Водночас при старінні порушується і фармакодинаміка різних груп ЛЗ, яка залежить від онтогенетичних змін кількості фармакорецепторів, їхньої чутливості до ЛЗ (остання може збільшуватися або зменшуватися порівняно з такою у хворих молодого віку), чисельності метаболітів, активності ферментів та ін.
В осіб похилого віку дуже часто виникає потреба в тривалому прийомі медикаментів у зв’язку з хронічним перебігом захворювань. Водночас спостерігається поєднання кількох захворювань (поліморбідність), що підвищує ризик взаємодії ЛЗ in vivo при політерапії. Показано, що 86% населення віком ≥70 років має щонайменш одну хронічну патологію, переважно ураження серцево-судинної системи, ЦНС, опорно-рухового апарату і шлунково-кишкового тракту (ШКТ). Два супутні захворювання відзначаються у 27%, три – в 19%, ≥4 – 24%. Унаслідок медикаментозної взаємодії можуть підвищуватися токсичність або знижуватися фармакологічна активність ЛЗ, розвиватися побічні реакції (ПР). Ризик виникнення ПР у хворих віком понад 60 років у 2-3 рази вищий, ніж у молодих людей і пацієнтів середнього віку. До типових побічних реакцій при проведенні фармакотерапії в людей літнього віку належать (ВООЗ, 2004):
• гострий делірій;
• рухові розлади;
• зміни зорової функції;
• брадикардія;
• аритмія;
• хорея;
• сплутаність свідомості;
• закреп;
• втомлюваність;
• гострий напад глаукоми;
• гіпокаліємія;
• ортостатична гіпотензія;
• парестезія;
• психічні розлади;
• набряк легень; інтенсивна кровотеча;
• дискінезія;
• порушення сечовипускання.
Крім того, для цієї вікової групи характерні зниження рівня психічної активності, зміна як сприйняття та адекватності реакції на рекомендації лікаря, так і можливості їх виконання.
Усі ці аспекти слід враховувати задля підвищення ефективності та безпеки застосування ЛЗ у літніх пацієнтів.
Вікові зміни фармакокінетики
Вікові зміни всмоктування ЛЗ
Вікові зміни всмоктування ЛЗ можуть бути причиною значних змін абсорбції препаратів. У похилому й старечому віці на цей процес суттєво впливають:
• зниження секреторної активності залоз шлунка, кишечнику, підшлункової залози;
• атрофія кишкових ворсинок;
• гіпокінезія шлунка та кишечнику;
• зниження мезентеріального кровообігу;
• наявність запальних захворювань слизової оболонки ШКТ;
• супутня патологія інших органів і систем.
Зміна pH шлункового вмісту значною мірою визначає швидкість та обсяг усмоктування лікарських речовин у тонкій кишці, ступінь розчинності яких залежить від зсуву pH у кислий бік. У людей старечого віку гіпохлоргідрія й ахлоргідрія спостерігаються майже в 50% випадків. Разом з ослабленням кислотоутворення помітно змінюються синтез та активність ферментів. Крім цього, до уповільнення всмоктування призводить гальмування евакуації вмісту шлунка, зниження моторики кишечнику та його випорожнення за рахунок не тільки інволюційних процесів, а й впливу деяких препаратів на абсорбцію. Так, антациди, проносні та антигіпертензивні засоби спричиняють уповільнення випорожнення шлунка і зменшення кровообігу в кишечнику.
Слід зазначити, що, з одного боку, зазначені фактори зменшують надходження ЛЗ у кров та їхній терапевтичний ефект, а з іншого – тривале перебування ЛЗ у шлунку зумовлює зростання їх подразливої дії на слизову оболонку, що супроводжується розвитком диспептичних явищ, болем в епігастральній ділянці, може стати причиною утворення виразок у шлунку та шлункових кровотеч.
Гіпокінезія шлунка та кишечнику сприяє швидшому руйнуванню кислотонестійких препаратів, зниженню терапевтичного ефекту ЛЗ із коротким періодом напіввиведення. Посилення моторики, часті рідкі випорожнення, прийом проносних засобів, прокінетиків зумовлюють зменшення всмоктування препаратів. Разом із тим закрепи в літніх людей із гіпомоторикою кишечнику можуть сприяти збільшенню повноти всмоктування ЛЗ унаслідок тривалого перебування препаратів у ШКТ. У цьому випадку можливі посилення та пролонгування терапевтичної дії ЛЗ, що в поєднанні з уповільненням їхньої елімінації вимагає корекції доз і режимів призначення. Таким чином, у літніх пацієнтів важко точно спрогнозувати рівень абсорбції ЛЗ при пероральному використанні та їх концентрації у сироватці крові.
В осіб літнього віку при підшкірному та внутрішньом’язовому введенні сповільнюється всмоктування ЛЗ у кров унаслідок зниження серцевого викиду, уповільнення кровообігу та зміни проникності стінок судин. Усмоктування трансдермальних ЛЗ порушується через фізіологічне старіння шкіри. Вікові зміни шкіри починаються вже з 40 років, а після 60 років через атрофію та дегенеративні процеси помітно виснажуються всі її шари. Зменшуються також кількість судин і проникність судинних стінок; порушення мікроциркуляції проявляються у вигляді стазу, мікротромбозів, запустіння капілярів.
Вікові зміни розподілу ЛЗ
У літніх хворих швидкість і ступінь розподілу ЛЗ можуть змінюватися внаслідок зниження клітинної маси, заміни метаболічно активних тканин жировими, порушення тканинної архітектоніки, а також через розлади циркуляції (зменшення кількості води в організмі, зміна тканинної проникності тощо).
Зменшення м’язової маси та кількості води призводить до зниження об’єму розподілу гідрофільних ЛЗ і підвищення їхньої концентрації в плазмі крові та тканинах. Зростає небезпека передозування та лікарської інтоксикації. Це стосується аміноглікозидних антибіотиків, серцевих глікозидів, гідрофільних β-адреноблокаторів, Н2-блокаторів. Збільшення кількості жирової тканини в літніх осіб сприяє підвищенню обсягів розподілу та зменшенню концентрації ліпофільних препаратів у тканинах, що супроводжується уповільненням початку та подовженням тривалості дії. Подібні феномени мають місце при прийомі тетрацикліну, бензодіазепінових транквілізаторів, фенотіазинових нейролептиків, барбітуратів.
Важливим аспектом розподілу препарату є його зв’язування з білком. Старіння організму супроводжується зменшенням умісту альбумінів у плазмі крові в середньому на 10-15%. Гіпоальбумінемія призводить до зменшення кількості зв’язаної фракції препарату та зростання концентрації вільної фракції, що підвищує ефективність ЛЗ, збільшує можливість передозування, появи токсичних і побічних реакцій. У хворих похилого віку концентрація в плазмі багатьох препаратів, особливо з низьким терапевтичним індексом, істотно зростає, іноді досягаючи токсичного рівня. Це суттєво для ЛЗ, переважно кислот, що мають високий ступінь зв’язування з білками плазми (понад 80%): β-адреноблокаторів, сульфаніламідів, саліцилатів, серцевих глікозидів, бензодіазепінових транквілізаторів, антикоагулянтів непрямої дії, протидіабетичних засобів, наркотичних аналгетиків, протисудомних препаратів. Водночас у літніх людей спостерігається тенденція до збільшення концентрації α1-кислого глікопротеїну, який зв’язує ЛЗ, переважно основи, що, навпаки, може уповільнювати фармакологічну дію.
Розподіл ЛЗ в осіб літнього віку змінюють також порушення циркуляції: зниження серцевого викиду на 1% щороку, уповільнення та перерозподіл регіонального кровообігу, зміна тканинної проникності. Компенсаторно зростає симпатичний тонус для покращення кровопостачання серця, головного мозку. При цьому страждає периферичний, нирковий і печінковий кровообіг. Зниження печінкового кровообігу призводить до зменшення печінкового кліренсу ЛЗ.
Метаболізм ЛЗ у літніх пацієнтів
Маса печінки в осіб віком понад 65 років знижується на 25%, а печінковий кровообіг – майже на 35-45% порівняно з людьми молодого та середнього віку. Ці суттєві зміни призводять до збільшення біодоступності ЛЗ і підвищення їх концентрації в плазмі. Унаслідок зниження печінкового кліренсу змінюється період напіввиведення для ЛЗ як із швидким, так і з повільним метаболізмом. Ці зміни мають найбільше практичне значення при використанні психотропних препаратів, наркотичних аналгетиків, β-адреноблокаторів, антикоагулянтів, антиаритмічних препаратів, нестероїдних протизапальних засобів (НПЗЗ).
У літніх людей у більшості випадків знижується активність ферментів печінки, що беруть участь в окисленні ЛЗ (у I фазі реакцій детоксикації). Утім, активність гідролізу, навпаки, підвищується. Швидкість реакцій II фази (кон’югація, ацетилювання) не змінюється. У зв’язку із цим у багатьох ЛЗ (наприклад, у пропранололу) подовжується період напіввиведення й уповільнюється кліренс. Порушення метаболізму можуть супроводжуватися утворенням атипових метаболітів ЛЗ, іноді більш токсичних. Крім того, літні хворі більш чутливі до шкідливої дії ЛЗ (парацетамолу, НПЗЗ) на печінку.
Серед мікросомальних ферментів, що здійснюють біотрансформацію ліків, основне місце належить цитохрому Р450. Він має декілька ізоферментів, номенклатура яких визначається подібністю амінокислотних послідовностей. Цими ферментами метаболізується більшість ЛЗ, які використовуються в геріатричній практиці: серцево-судинні (β-адреноблокатори, статини, блокатори рецепторів ангіотензину, блокатори кальцієвих каналів, варфарин); нейротропні засоби; НПЗЗ та ін.
Препарати-індуктори (барбітурати, карбамазепін, фенітоїн, преднізолон, галоперидол, аміназин, амітриптилін, діазепам) підвищують активність цитохрому Р450, унаслідок чого у хворих старших вікових груп може спостерігатися зниження активності одночасно призначених препаратів або утворення токсичних метаболітів. Тривалий (понад 2 тиж) прийом індукторів печінкового метаболізму знижує ефективність непрямих антикоагулянтів, створюючи умови для їх використання в підвищених дозах. При відміні засобів, які прискорюють метаболізм, потрібно обов’язково знижувати дози антикоагулянтів для уникнення геморагічних ускладнень. Ця закономірність справедлива для рифампіцину, амінофеназону, бутадіону. Тривалий прийом індукторів метаболізму може викликати прискорення біотрансформації фолієвої та аскорбінової кислот, вітамінів В6 і D, в осіб старечого віку призводячи до розвитку макроцитозу, мегалобластної анемії, гіперхолестеринемії. Інгібітори цитохрому Р450 уповільнюють метаболізм ЛЗ, унаслідок чого підвищується концентрація останніх у крові та зростає ризик виникнення ПР. До таких ЛЗ належать бензодіазепіни, трициклічні антидепресанти, НПЗЗ, а також деякі інші препарати. Врахування метаболічних характеристик засобів при одночасному їх призначенні допоможе мінімізувати ризик медикаментозної взаємодії.
Із віком знижується інтенсивність не лише системного, а й пресистемного метаболізму: при цьому спостерігається підвищення біодоступності ЛЗ із високим ефектом першого проходження (лабеталол, пропранолол, лідокаїн, нітрати), що зумовлено зниженням метаболізму при першому пасажі, тобто того процесу, під час якого препарат після прийому всередину метаболізується в печінці, ще не досягнувши системного кровообігу.
Зниження знешкоджувальних функцій печінки в літньому віці супроводжується накопиченням в організмі введених ЛЗ і продуктів їх метаболізму. Усе це сприяє виникненню медикаментозної інтоксикації в людей похилого віку. Окрім цього, в даній популяції куріння та прийом алкоголю більшою мірою, ніж у людей молодого віку, впливають на метаболізм ЛЗ.
Екскреція ЛЗ у літніх людей
Головну роль у процесі виведення ЛЗ з організму відіграють печінка та нирки. Також цю функцію виконують кишечник, легені, залози зовнішньої секреції.
Печінка разом із жовчю екскретує як незмінені сполуки, так і метаболіти, які в ній утворилися. При цьому більшість речовин назад не всмоктуються і виводяться кишечником. Однак глюкуроніди та деякі інші парні сполуки, що виділяються з жовчю, можуть гідролізуватися кишковими або бактеріальними ферментами з утворенням ліпідрозчинних речовин, які реабсорбуються й знов потрапляють у кров, підтримуючи в ній і в тканинах свою концентрацію, а потім знову екскретуються з жовчю. У такий спосіб здійснюється ентерогепатична циркуляція. При печінковій недостатності, наявній в осіб похилого та старечого віку, коригувати режим дозування препаратів украй складно, тому на практиці модифікації доз проводять емпірично, ґрунтуючись на клінічних ефектах. За неможливості корекції дозування препарат відміняють, підшукуючи йому заміну.
Для більшості ЛЗ ниркова екскреція є основним, а в багатьох випадках і єдиним шляхом елімінації. Нирковий кровообіг у хворих віком >70 років є удвічі нижчим, ніж в осіб середнього віку. При цьому рівень креатиніну в сироватці не підвищується, оскільки його продукція знижується пропорційно зменшенню м’язової маси. Таким чином, у літніх хворих має місце легка ниркова недостатність. Виведення ліків нирками включає фільтрацію, секрецію та реабсорбцію. Фільтрація ЛЗ у клубочках здійснюється пасивно. Секреція є активним процесом (відбувається із втратою енергії та за участю спеціальних транспортних систем), незалежним від зв’язування препаратів з білками плазми крові. Реабсорбція глюкози, амінокислот, катіонів та аніонів відбувається активно, а жиророзчинних речовин – пасивно.
Здатність нирок до виведення ліків шляхом фільтрації перевіряється за екскрецією ендогенного креатиніну, оскільки обидва процеси відбуваються паралельно з однаковою швидкістю. При оцінці стану нирок в осіб старечого віку слід враховувати невідповідність рівня креатиніну в плазмі крові кліренсу креатиніну, оскільки для визначення істинної функціональної здатності нирок останній є головним показником. Під кліренсом розуміють гіпотетичний об’єм плазми крові, який повністю очищується від ЛЗ за одиницю часу. У нормі кліренс ендогенного креатиніну становить 80-120 мл/хв. Для визначення кліренсу ендогенного креатиніну існують спеціальні нормограми, складені з урахуванням рівня креатиніну в сироватці крові, маси тіла та зросту людини. Визначивши кліренс, лікар користується відповідними рекомендаціями щодо дозування та/або кратності призначення відповідного препарату.
Зазвичай для контролю корекції доз і режиму введення найінформативнішим є визначення рівня ЛЗ у плазмі крові при відомих терапевтичних і токсичних концентраціях речовини, але зробити це не завжди можливо. Крім цього, кількісно елімінацію препарату можна оцінити й за допомогою коефіцієнта елімінації. Він відображає ту частину (у відсотках) ЛЗ, на яку відбувається зменшення його концентрації в організмі за одиницю часу (найчастіше за добу). Зв’язок між об’ємом розподілу та кліренсом речовини виражається періодом напіввиведення (T1/2) – часом, за який її концентрація в плазмі крові знижується наполовину. У разі введення постійної підтримувальної дози при однаковому інтервалі дозування в середньому через 4-5 T1/2 у плазмі крові створюється рівноважна концентрація ЛЗ. Саме у цей час слід починати реагувати на тривалі скарги хворого, тобто треба збільшувати дозу або змінювати препарат. За допомогою показника 4-5 T1/2 можна оцінювати результат терапії після відміни препарату. Нарешті, зникнення більшості небажаних ефектів (крім алергічних) відбувається теж протягом цього часу. Знання та ретельне врахування всіх зазначених вище фармакокінетичних параметрів ЛЗ забезпечують збереження їх концентрації в плазмі крові в межах терапевтичного діапазону.
Зниження ниркової функції призводить до підвищення концентрації препаратів, які екскретуються в незміненому вигляді, й активних чи токсичних метаболітів, а також збільшує Т1/2, створюючи небезпеку кумуляції ЛЗ, передозування та побічних ефектів. У літніх людей необхідна корекція доз ЛЗ із низьким терапевтичним індексом: серцевих глікозидів, аміноглікозидних антибіотиків, а також цефалоспоринів, протидіабетичних, антиаритмічних, урикозуричних засобів, клофеліну, НПЗЗ. Призначення літньому хворому стандартної дози для дорослих може призвести до непропорційно високого вмісту препарату в сироватці крові. Враховуючи неповноцінність печінкового метаболізму та зменшення видільної функції нирок, початкові дози ЛЗ у пацієнтів літнього віку слід знижувати на 30-50%. У літніх осіб унаслідок вікових змін фармакокінетики та супутніх захворювань ефекти ЛЗ можуть посилюватися (табл. 2).
Вікові зміни фармакодинаміки ЛЗ
У більшості випадків при корекції дози ЛЗ з урахуванням зміни фармакокінетичних параметрів необхідно аналізувати додаткові дані щодо чутливості до ЛЗ. Величина ефекту ЛЗ залежить від кількості рецепторів в органах, здатності клітин до відповіді при зв’язуванні молекули ЛЗ із рецептором і контррегулювальних процесів, які підтримують функціональну рівновагу. У літніх людей поряд зі зменшенням кількості рецепторів в органах-мішенях відзначаються функціональне виснаження та зниження реактивності останніх. Це сприяє розвитку важкопрогнозованих, нетипових, неадекватних щодо кількості введеного ЛЗ і навіть парадоксальних реакцій при застосуванні, наприклад, серцевих глікозидів, глюкокортикоїдів, нітратів, адреноміметиків та адреноблокаторів, деяких гіпотензивних препаратів, аналгетиків, барбітуратів, бензодіазепінових анксіолітиків, протипаркінсонічних і протисудомних засобів.
У пацієнтів літнього віку розвиток нетипових реакцій на введення ЛЗ зумовлюють також знижена фізична активність, схильність до закрепів, вітамінна недостатність, погіршення кровопостачання тканин і відносне переважання процесів збудження в нервовій системі. У результаті, наприклад, барбітурати часто спричиняють порушення свідомості або парадоксальне збудження, затримку сечовипускання, а також зниження чутливості до β-адреноблокаторів й α-адреноміметиків. Відзначається також підвищення чутливості до антипсихотичних засобів, що викликають сплутаність свідомості, гіпотонію та затримку сечовипускання. Застосування нітратів і прокаїнаміду супроводжується більш значним, ніж у хворих середнього віку, зниженням артеріального тиску й можливим погіршенням мозкового кровообігу. Виявлено зростання чутливості до непрямих антикоагулянтів. Змінюється з віком і чутливість до наркотичних аналгетиків – при їх уведенні в літніх людей значно швидше, ніж у молодих, розвиваються пригнічення дихального та збудження блювотного центрів.
Слід зазначити, що чинні схеми фармакотерапії розроблені та випробувані без урахування особливостей взаємодії ліків у пацієнтів похилого віку. Неможливо врахувати всі можливі ПР ЛЗ, проте кожен лікар і кожен провізор мають знати клінічно значущі негативні явища. Розглядаючи геріатричний аспект ускладнень фармакотерапії, необхідно брати до уваги такі моменти:
• ризик виникнення ПР ЛЗ у пацієнтів літнього віку в 5-7 разів вищий, ніж у хворих молодших вікових груп;
• осіб літнього віку у 2-3 рази частіше, ніж пацієнтів молодого та середнього віку, госпіталізують у зв’язку з ПР ЛЗ;
• найбільша кількість летальних випадків, пов’язаних з ПР ЛЗ у пацієнтів літнього та старечого віку, припадає на вік 80-90 років;
• при призначенні ≥3 препаратів, прийом яких асоціюється з ПР у старечому віці, ймовірність виникнення останніх збільшується в ≥10 разів.
Найчастіше ПР виникають при призначенні НПЗЗ (27%), антибіотиків (23%), аспірину та інших антикоагулянтів (22%), діуретиків (17%), антигіпертензивних препаратів (β-адреноблокаторів та ІАПФ; 9,4%). У структурі системних ПР у 2008 р. в Україні переважали алергічні реакції (60,0%), серцево-судинні розлади (12,1%) та порушення з боку ШКТ (11,8%). До топ‑10 ЛЗ із найчастішими проявами ПР входять цефтріаксон, амоксицилін та його комбінації з інгібіторами ензимів, диклофенак натрію, розчини електролітів та їх комбінації, пентоксифілін, еналаприл, ципрофлоксацин, декстрин, амлодипін. Вибір препарату – важливий фактор, який впливає на імовірність розвитку ПР. Запропоновано список ЛЗ, призначення яких у літніх пацієнтів слід уникати. Він включає амітриптилін, дизопірамід, доксепін, метилдопу, пентазоцин, алкалоїди беладони й тиклопідин.
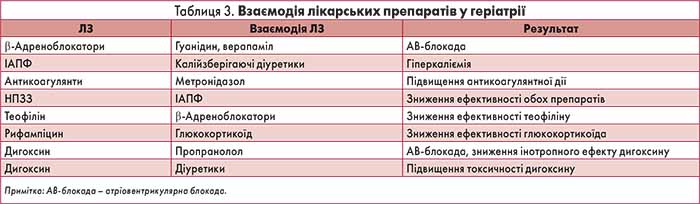
Взаємодія ЛЗ є однією з найважливіших проблем у лікуванні хворих літнього та старечого віку з комплексною хронічною патологією. Частота й тяжкість ПР при взаємодії ліків у цієї категорії хворих корелюють з віком та кількістю призначених препаратів. Прийом 2 ЛЗ призводить до виникнення медикаментозної взаємодії в 6% випадків, 5 – в 50%, 10 – в 66% випадків. Клінічно значущі наслідки медикаментозної взаємодії зареєстровано у 25% амбулаторних та в 46% стаціонарних пацієнтів літнього віку, які отримували одночасно ≥2 ЛЗ. Медикаментозні взаємодії, які найчастіше зустрічаються в геронтологічній практиці, наведено в таблиці 3.
Принципи фармакотерапії у літніх пацієнтів
Єдиних методичних підходів стосовно дозування ЛЗ у геріатрії не існує, тому слід виходити з особливостей фармакокінетики та фармакодинаміки конкретних груп препаратів. У геріатричних пацієнтів слід належно оцінити потребу в медикаментозному лікуванні; кількість препаратів, які приймаються одночасно, має бути зменшено, наскільки це можливо.
Основні принципи призначення ліків у літніх людей є такими.
1. Визначення необхідності призначення ЛЗ:
• не всі хвороби в літніх пацієнтів потребують медикаментозної терапії;
• за можливості необхідно уникати застосування ЛЗ, але обов’язково призначати їх, коли йдеться про якість життя;
• перед початком лікування слід встановити точний діагноз.
2. Ретельне визначення характеру вже проведеного лікування, усіх звичок хворого:
• пацієнт може отримувати рекомендації та перебувати під спостереженням лікарів;
• відомості про лікування, яке вже отримує хворий, дозволять уникнути небажаних лікарських взаємодій;
• куріння, алкоголь, вживання кави можуть призвести до посилення дії ліків.
3. Поінформованість про механізм дії ЛЗ, що призначаються:
• знання про можливість змін у розподілі ЛЗ і відповіді на терапію у літніх хворих;
• призначення добре вивчених ліків.
4. Ініціація терапії з невеликих доз ЛЗ:
• стандартна доза часто завелика для літніх пацієнтів; хворим віком понад 60 років препарати призначають у кількості, що дорівнює 1/2-2/3 дози дорослого. Людям літнього віку потрібно обережно призначати ЛЗ, які підвищують артеріальний тиск, активують серцево-судинну систему, викликають блювання, та проносні засоби. Дози хіміотерапевтичних препаратів не зменшують, натомість вітамінних комплексів – збільшують;
• хоча вплив віку на печінковий метаболізм не завжди передбачуваний, відомо, що ниркова екскреція ліків та їхніх метаболітів знижується з віком;
• літні хворі сприйнятливіші до препаратів, що впливають на ЦНС.
5. Необхідність титрування дози до потрібного ефекту:
• визначають досяжний терапевтичний ефект;
• дозу збільшують до певного терапевтичного результату або можливої межі, після якої можуть виникнути побічні явища;
• в окремих випадках використовують комбіновану терапію як адекватнішу й ефективнішу.
6. Найпростіші режими застосування забезпечують максимальний рівень комплаєнсу. Слід:
• уникати складних режимів дозування (найбільш прийнятним є прийом ліків 1-2 р/добу);
• ретельно інструктувати хворих та їхніх родичів щодо прийому ЛЗ;
• пояснити, з якою метою призначено препарати;
• пропонувати вести записи щодо прийому медикаментів;
• забезпечити постійний контроль виконання призначень літніми хворими.
Похилий вік можна вважати фактором ризику (до того ж, важко прогнозованим) щодо фармакотерапії. Стандартні дози ЛЗ можуть бути зависокими для людей старечого віку, а в літніх пацієнтів – здатні спричиняти гетерогенні реакції. З огляду на це уніфікованих рекомендацій щодо призначення ЛЗ даній групі пацієнтів не існує. Доза має визначатися індивідуально. При цьому особливої уваги потребують корекція дози при зменшенні маси тіла, а також урахування зниження функції нирок в конкретного пацієнта.
Список літератури знаходиться в редакції.
| Медична газета «Здоров’я України 21 сторіччя» № 8 (381), квітень 2016 р. |