25 травня, 2020
Эффективность октреотида в лечении хронического панкреатита
В статье представлены данные исследований о влиянии октреотида (аналога соматостатина) на панкреатическую секрецию, в частности о его положительном действии и эффективности у пациентов с хроническим панкреатитом.
Ключевые слова: хронический панкреатит, соматостатин, болевой синдром, октреотид.
Одной из наиболее сложных задач в лечении хронического панкреатита (ХП) является купирование болевого синдрома. Многокомпонентный механизм развития боли при данном заболевании требует комплексного подхода к лечению. Интенсивный болевой синдром, стойкость его к применяемой терапии, нередко приводят к потере трудоспособности пациента, поэтому важно назначать лечение, действующее на все звенья патогенеза ХП.
Влияние соматостатина на панкреатическую секрецию
Соматостатин– регуляторный гормон, который представляет собой циклический полипептид, существующий в организме человека в двух формах: одна, состоящая из 14 аминокислот, а другая – из 28 [1].
Клетки, которые продуцируют соматостатин‑14, присутствуют в тканях большинства органов и систем (Ben-Shlomo A. et al., 2010), тогда как соматостатин‑28 в основном вырабатывается эпителиальными клетками слизистой оболочки желудочно-кишечного тракта (Van Op den Bosch J. et al., 2009). Этот гормон влияет на многие функции организма: например, он подавляет боль, ингибирует высвобождение гормонов гипоталамуса и гормонов T3/T4 в щитовидной железе. Взаимосвязь между соматостатином и секреторной функцией поджелудочной железы была продемонстрирована во многих исследованиях. Соматостатин уменьшает экспрессию генов инсулина, глюкагона и панкреатического полипептида (PP). Это вызывает снижение секреторной функции эндокринной части поджелудочной железы и ингибирует высвобождение бикарбоната и пищеварительных ферментов из экзокринной ее части (Pinter E. et al., 2006).
Синтетическим аналогом соматостатина является октреотид (Октреотид-МБ). Препарат обладает сходными с соматостатином фармакологическими эффектами, но отличается значительно большей продолжительностью действия.
Эффективность октреотида в лечении хронического панкреатита
ХП – заболевание, которое проявляется болевым синдромом и недостаточностью поджелудочной железы [2, 3]. Заболевание встречается с частотой 27,4 на 100 тыс. человек.
В исследованиях продемонстрировано увеличение количества секретирующих соматостатин δ-клеток и PP-клеток, а также их измененное расположение в островках и паренхиме поджелудочной железы у курящих пациентов с ХП в сравнении с некурящими пациентами и здоровыми лицами [3].
Основной причиной (70-90%) ХП в западных странах является злоупотребление алкоголем. Второй наиболее распространенной формой ХП (25%) является идиопатический панкреатит, который возникает у пациентов без выявленных факторов риска. Численность этой группы неуклонно снижается, а осведомленность о генетических факторах риска растет (Keller J. et al., 2009).
В исследованиях установлено, что ХП ассоциируется со злоупотреблением алкоголем, когда пациент употребляет более 40 г алкоголя в день на протяжении более чем 5 лет. Случаи, которые не могут быть классифицированы в соответствии с вышеуказанными критериями или генетической предрасположенностью, определяют как идиопатический ХП (Sliwinska-Mosson M. et al., 2018).
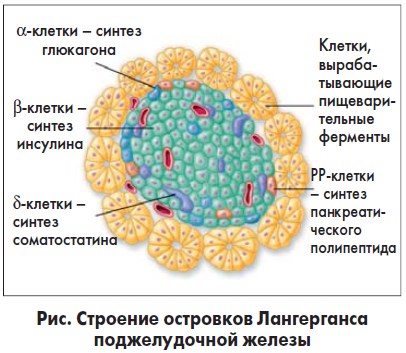 Также исследования показали, что курение сигарет может играть существенную роль в развитии эндокринных нарушений при прогрессировании ХП. Так, у пациентов с ХП, которые курят, по сравнению с некурящими, наряду с увеличением количества соматостатин- и PP-продуцирующих клеток отмечено также изменение их пространственного распределения. Клетки, продуцирующие соматостатин (δ-клетки), в поджелудочной железе здоровых людей расположены в основном по периферии островков (рисунок). У пациентов с ХП δ-клетки расположены по всей площади островков и между фолликулярными клетками в экзокринной части поджелудочной железы. У здоровых людей клетки, секретирующие PP, могут быть обнаружены в островках головки и хвоста поджелудочной железы. У некурящих пациентов с ХП они также могут быть выявлены в теле поджелудочной железы и между фолликулярными клетками, тогда как у курящих – в островках по всей площади железы (головка, тело, хвост) и между фолликулярными клетками. Согласно данным исследований, в поджелудочной железе курильщиков с ХП наблюдаемое количество PP-продуцирующих клеток было в 3 раза больше, чем у здоровых людей, и примерно в 2 раза больше, чем у некурящих пациентов с ХП. Наибольшее их количество было выявлено в головке поджелудочной железы, тогда как у здоровых людей и некурящих пациентов с ХП больше всего их было обнаружено в хвосте. Также у курильщиков наблюдалось уменьшение количества α- и β-клеток. Кроме того, у этих пациентов риск кальцификации поджелудочной железы был на 20% выше по сравнению с некурящими [3].
Также исследования показали, что курение сигарет может играть существенную роль в развитии эндокринных нарушений при прогрессировании ХП. Так, у пациентов с ХП, которые курят, по сравнению с некурящими, наряду с увеличением количества соматостатин- и PP-продуцирующих клеток отмечено также изменение их пространственного распределения. Клетки, продуцирующие соматостатин (δ-клетки), в поджелудочной железе здоровых людей расположены в основном по периферии островков (рисунок). У пациентов с ХП δ-клетки расположены по всей площади островков и между фолликулярными клетками в экзокринной части поджелудочной железы. У здоровых людей клетки, секретирующие PP, могут быть обнаружены в островках головки и хвоста поджелудочной железы. У некурящих пациентов с ХП они также могут быть выявлены в теле поджелудочной железы и между фолликулярными клетками, тогда как у курящих – в островках по всей площади железы (головка, тело, хвост) и между фолликулярными клетками. Согласно данным исследований, в поджелудочной железе курильщиков с ХП наблюдаемое количество PP-продуцирующих клеток было в 3 раза больше, чем у здоровых людей, и примерно в 2 раза больше, чем у некурящих пациентов с ХП. Наибольшее их количество было выявлено в головке поджелудочной железы, тогда как у здоровых людей и некурящих пациентов с ХП больше всего их было обнаружено в хвосте. Также у курильщиков наблюдалось уменьшение количества α- и β-клеток. Кроме того, у этих пациентов риск кальцификации поджелудочной железы был на 20% выше по сравнению с некурящими [3].
Преобладающим симптомом ХП является иррадиирующая в спину острая или тупая боль в эпигастральной области, которая может несколько уменьшаться при наклоне вперед. Болевой синдром часто сопровождается тошнотой и рвотой. Чувствительность в верхней части живота также является распространенным явлением. Из-за боли пациенты часто отказываются от еды, что приводит к значительной потере веса, особенно если у больного наблюдается стеаторея. У трети пациентов развивается клиника явного сахарного диабета, обычно легкой степени тяжести [4].
ХП считается процессом, связанным с избыточной экспрессией фибробластов и факторов роста, повышенной экспрессией интерлейкина‑8 и нарушениями в гомеостазе холецистокинина. Сочетание этих факторов в конечном итоге может привести к необратимому повреждению органов. Применение октреотида было изучено при лечении ХП. Как аналог соматостатина, он ингибирует секрецию поджелудочной железой холецистокинина и, как следствие, значительно снижает его уровень. Первоначально было проведено много небольших краткосрочных исследований, посвященных использованию этого препарата. В метаанализе Gupta V., Toskes P.P. (2005) представлены результаты многоцентрового пилотного исследования, изучавшего различные режимы дозирования октреотида. Исследователи пришли к выводу, что введение 200 мкг октреотида подкожно 3 раза в день было более эффективным, чем плацебо. Также при применении этого препарата наблюдалось значительное снижение интенсивности болевого синдрома, устойчивого к другим формам терапии, у многих пациентов с тяжелым течением ХП.
Изучение влияния ингибирования секреции поджелудочной железы октреотидом на болевой синдром было проведено в двух исследованиях. Первое не показало значительного уменьшения интенсивности боли после трехдневного лечения октреотидом. Второе исследование, в котором октреотид использовался в течение трех недель, продемонстрировало значительное уменьшение болевого синдрома по сравнению с плацебо.
Эффективность октреотида (Октреотид-МБ) в лечении ХП обусловлена целым рядом его свойств, а именно:
- ингибирует эндокринную функцию поджелудочной железы – инсулин, глюкагон, РР;
- ингибирует экзокринную функцию поджелудочной железы – амилаза, трипсин, липаза;
- ингибирует секрецию желудочной кислоты (активированную пентагастрином);
- уменьшает мезентериальный кровоток;
- снижает внутрипротоковое давление;
- модулирует пролиферацию клеток;
- активирует иммунную систему, влияет на пролиферацию лимфоидных клеток и образование иммуноглобулинов и цитокинов;
- уменьшает секрецию эндогенной жидкости в тощей и подвздошной кишках;
- ингибирует не только секрецию, но и рост многих различных типов нейроэндокринных опухолей.
Кроме того, доказано, что октреотид может быть полезен при лечении псевдокист – наиболее распространенного осложнения ХП [5]. В исследовании с участием семи пациентов с ХП, у которых развилась псевдокиста поджелудочной железы, им был назначен октреотид в дозе 300 мкг в день в течение двух недель. Четверо из семи пациентов ответили на лечение немедленно, и средний размер псевдокист уменьшился на 42%. Также у них наблюдалось облегчение болевого синдрома. Другие исследования были проведены при участии пациентов с инфицированными псевдокистами поджелудочной железы. После недели лечения октреотидом в дозе 300 мкг в сутки размер кисты уменьшился в среднем с 8 до 1 см, а суточный объем отделяемого по дренажам – с 200 до 30 мл. Предполагается, что пораженная поджелудочная железа реагирует на соматостатин в меньшей степени. Однако положительные результаты лечения октреотидом у пациентов с ХП указывают на то, что применение ингибирующих секрецию веществ может стать основной концепцией лечения у этой группы пациентов [5, 6].
Таким образом, применение октреотида в лечении ХП способствует уменьшению выраженности его клинических проявлений. Октреотид существенно облегчает болевой синдром, устойчивый к другим формам терапии, у пациентов с тяжелым течением ХП. Он также показал себя эффективным в лечении псевдокист поджелудочной железы. Следовательно, ингибирующее действие октреотида можно рассматривать как новый подход к лечению пациентов с ХП.
Литература
- Liu Y., Lu D., Zhang Y., Li S., Liu X., Lin H. The evolution of somatostatin in vertebrates. Gene 2010; 463:21-8.
- Sebastiano P.D., di Mola F.F., Bockman D.E., Friess H., Büchler M.W. Chronic pancreatitis: the perspective of pain generation by neuroimmune interaction. Gut 2003; 52:907-11.
- Sliwinska-Mosson M., Milnerowicz H., Milnerowicz S., Nowak M., Rabczynski J. Immunohistochemical localization of somatostatin and pancreatic polypeptide in smokers with chronic pancreatitis. Acta Histochem 2012; 114:495-502.
- Bornman P.C., Buckingham I.J. ABC of diseases of liver, pancreas, and biliary system; chronic pancreatitis. BMJ 2001; 322:660-3.
- Büchler M.W., Binder M., Friess H. Role of somatostatin and its analogues in the treatment of acute and chronic pancreatitis. Gut 1994; 35:15-9.
- Sliwinska-Mosson M. et al. The clinical significance of somatostatin in pancreatic diseases. Annals of Endocrinologic 75 (2014) 232-240.
- Подготовили Мария Грицуля, Дмитрий Карасев, Елена Петренчук
- Sliwinska-Mosson M. et al. The clinical significance of somatostatin in pancreatic diseases. Annals of Endocrinologic 75 (2014) 232-240.
Тематичний номер «Хірургія, Ортопедія, Травматологія, Інтенсивна терапія» № 1 (39), 2020 р.


