5 червня, 2020
Ефективність фебуксостату для запобігання розвитку церебральних та серцево-судинних подій при гіперурикемії
Гіперурикемія – підвищений рівень сечової кислоти (СК) у сироватці крові. Цей патологічний стан часто супроводжує подагру, призводить до розвитку артриту, утворення тофусів. Також гіперурикемія асоційована з появою та прогресуванням хронічної хвороби нирок, церебральних, серцево-судинних (СС) подій і підвищенням рівня смертності. Лікарські засоби, що зменшують вміст СК, можуть запобігати рецидиву захворювань, пов’язаних із відкладенням уратів. S. Kojima et al. провели дослідження, в якому порівнювали частоту ниркових, церебральних і СС-ускладнень у пацієнтів із гіперурикемією при лікуванні фебуксостатом та тих, хто отримував стандартну терапію з модифікацією способу життя. До вашої уваги представлено огляд результатів, опублікованих у European Heart Journal (2019; 40: 1778‑1786).
Фебуксостат – непуриновий селективний інгібітор ізоформ ксантиноксидоредуктази, що був затверджений 2011 р. в Японії. Згідно з наявними клінічними даними, фебуксостат чинить потужнішу дію порівняно з алопуринолом щодо зниження сироваткової концентрації СК у крові. Однак докази переваг препарату стосовно СС-подій є суперечливими (Foody et al., 2017; Zhang et al., 2018). У рандомізованому контрольованому дослідженні Febuxostat for Cerebral and CaRdiorenovascular Events PrEvEntion StuDy (FREED) автори мали на меті порівняти частоту ниркових, церебральних та СС-ускладнень у пацієнтів похилого віку з гіперурикемією, що отримували лікування фебуксостатом, та тих, хто застосовував традиційну терапію, супроводжувану модифікацією способу життя (Kojima et al., 2019).
Матеріали й методи дослідження
Дизайн дослідження та популяція пацієнтів
Багатоцентрове проспективне рандомізоване відкрите дослідження із засліпленими кінцевими точками та паралельними групами було проведенe у 141 лікарні Японії. Період спостереження становив 36 місяців. До групи лікування загалом було включено 1070 пацієнтів віком ≥65 років із гіперурикемією (рівень СК >7,0, але ≤9,0 мг/дл), що мали ризик розвитку ниркових, церебральних чи СС-ускладнень. Ризик визначали відповідно до наявних артеріальної гіпертензії / цукрового діабету 2-го типу на даний час або в анамнезі, патології нирок, про яку свідчила розрахункова швидкість клубочкової фільтрації (рШКФ) ≥30, але <60 мл/хв/1,73 м2 протягом трьох місяців до включення у дослідження, а також церебральних чи серцево-судинних захворювань (ССЗ) в анамнезі, що виникли за >3 місяці до початку спостереження. Усі пацієнти надали письмову інформовану згоду на участь у випробуванні.
Хворі були рандомним чином розподілені на дві групи: ті, хто отримував (n=537) та не отримував фебуксостат (n=533). Амбулаторні візити були заплановані на етапах скринінгу, зарахування, рандомізації, через 4, 8, 12, 24 тижні після неї та кожні шість місяців упродовж дослідження. Фебуксостат застосовували перорально один раз на день протягом 36 місяців. Підвищення дози препарату виконували наступним чином:
- початкова доза становила 10 мг/добу;
- на 4-му тижні дозу збільшували до 20 мг/добу;
- на 8-му тижні дозу підвищували до цільової 40 мг/добу.
Середня доза фебуксостату становила 29,1±12,3 мг/добу в кінцевій точці; 67,4% хворих отримували препарат по 40 мг/добу. Група пацієнтів, які не отримували фебуксостат, приймали 100 мг алопуринолу перорально (27,2%), якщо рівень СК у сироватці крові був підвищений упродовж всього періоду, починаючи з моменту включення у дослідження. Дозування обох препаратів коригували для запобігання зменшенню вмісту СК у сироватці крові <2,0 мг/дл. Окрім того, у всіх хворих було проведено модифікацію способу життя, щоб лікування гіперурикемії було більш дієвим. Коморбідні захворювання та небажані явища належним чином контролювалися лікарями шляхом призначення відповідної супутньої терапії. Лікування, розпочате до включення у дослідження, продовжували протягом усього періоду з максимальним дотриманням попереднього режиму. Не розпочинали або не припиняли застосування таких препаратів (без зміни дозування за можливості), як антиагреганти, антигіпертензивні, антидіабетичні та антидисліпідемічні засоби.
Огляд кінцевих точок
Первинна комбінована кінцева точка, визначена у дослідженні, включала:
- смерть через порушення мозкового кровообігу, хворобу нирок чи ССЗ;
- нове або повторюване цереброваскулярне захворювання, як-то інсульт (ішемічний інсульт, внутрішньомозковий/субарахноїдальний крововилив, інсульт неясного ґенезу), транзиторна ішемічна атака;
- нові або повторювані нефатальні коронарні події (інфаркт міокарда, нестабільна стенокардія);
- серцева недостатність, яка потребує госпіталізації;
- атеросклеротична хвороба, яка потребує лікування (аневризма, розшарування аорти та облітерувальний атеросклероз);
- порушення функції нирок: розвиток мікроальбумінурії (≥30, але <300 мг/г креатиніну [Кр]) / легкої протеїнурії (≥0,15, але <0,50 г/л Кр), прогресування до виразної альбумінурії (≥300 мг/г Кр) / протеїнурії (≥0,50 г/л Кр) або погіршення явної альбумінурії, підтверджене двома послідовними лабораторними тестами, проведеними після початку лікування; подвоєння рівня Кр у сироватці крові; прогресування до термінальної стадії ниркової недостатності;
- нова фібриляція передсердь (зокрема пароксизмальна);
- смерть через інші причини.
Вторинна кінцева точка складалася з окремих церебральних, ниркових та СС-ускладнень, жорстка кінцева точка визначалася як сукупність летальних випадків через будь-які причини, цереброваскулярних патологій чи нефатальних коронарних подій. На додачу, в обох групах порівняння оцінювали зміну рівня ШКФ упродовж року. Також аналізували взаємозв’язок між рівнем СК у сироватці крові через 12 тижнів після рандомізації та первинною комбінованою кінцевою точкою. Абсолютні значення та зміни високочутливого С-реактивного білка (вч-СРБ), мозкового натрійуретичного пропептиду (NT-proBNP) та глікованого гемоглобіну (HbA1С), виникнення злоякісних пухлин і венозного тромбозу, що потребував лікування, оцінювали як кінцеву точку дослідження.
Статистичний аналіз
За допомогою ІТТ-аналізу вивчали дані пацієнтів, яким було призначене лікування, і визначали як середнє ± стандартне відхилення (СВ). Також в ІТТ-популяції проводили оцінку безпеки, а міжгрупову різницю у часі щодо рівня СК порівнювали шляхом дисперсійного аналізу з повторним вимірюванням. Зокрема, був оцінений час від рандомізації до виникнення будь-яких ниркових, церебральних і СС-подій чи летальних випадків. Метод Каплана – Мейєра використовували для оцінки частоти ускладнень, а Грінвуда – для обчислення двостороннього 95% довірчого інтервалу (ДІ). Міжгрупові дані порівнювали за допомогою регресії Кокса, вторинні кінцеві точки – моделі небезпеки розподілення Fine та Grey, а різницю між змінами рШКФ та 95% ДІ – тесту Вілкоксона (Kojima et al., 2017).
Результати дослідження
Рівень СК у сироватці крові був порівнянний на початковому етапі між обома групами. У кінцевій точці показник серед пацієнтів, що отримували фебуксостат, виявився значно нижчим, ніж у контрольній групі (4,50±1,52 проти 6,76±1,45 мг/дл, р<0,001). Концентрації СК <6,0 мг/дл упродовж 12 тижнів при лікуванні фебуксостатом досягли понад 85% хворих, тоді як у групі контролю – менш ніж 30% у кінцевій точці. За період дослідження первинна комбінована кінцева точка спостерігалася у 125 пацієнтів (23,3%) у групі фебуксостату та в 153 (28,7%) – контролю. Різниця щодо даного показника між групами виявилася значущою. Результати оцінки первинної кінцевої точки відповідно до кривої Каплана – Мейєра представлені на рисунку.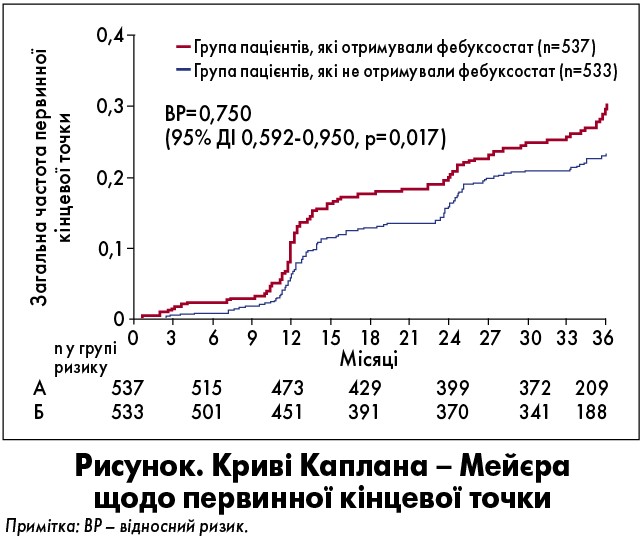
Найчастішим ускладненням в обох групах була ниркова недостатність, що проявлялася розвитком мікроальбумінурії або легкої протеїнурії. Міжгрупові відмінності щодо жорсткої кінцевої точки не простежувалися.
Оцінка зміни рШКФ упродовж року не виявила суттєвої різниці між досліджуваними групами: -0,37 (від -2,32 до 1,44) та -0,69 (від -2,63 до 1,39) мл/хв/1,73 м2 відповідно (р=0,606). Також не спостерігалося значної кореляції щодо сироваткового рівня СК через 12 тижнів після рандомізації та у первинній комбінованій кінцевій точці (n=980, р=0,112). Міжгрупові рівні вч-СРБ та NT-proBNP у кожній вимірюваній та кінцевій точці були зіставними. Однак концентрація HbA1С протягом 30 (р=0,024), 36 місяців (р=0,021) та у кінцевій точці (р=0,035) була суттєво нижчою з-поміж пацієнтів, які отримували фебуксостат, ніж у контрольній групі. В обох групах розвиток злоякісних пухлин (3,9 і 4,7% відповідно; р=0,529) і подагри (1,1 і 2,6% відповідно; р=0,069) був порівнянним, але дещо меншим серед хворих, які лікувалися фебуксостатом. Венозний тромбоз, що потребував лікування, не спостерігався у жодній групі.
Обговорення
Як відомо, процес окислення ксантину до СК може зумовити посилення прогресування атеросклерозу внаслідок індукції пошкодження ендотелію. Таким чином, при терапії гіперурикемії доцільно контролювати сироватковий рівень СК, зокрема фебуксостатом, що сприятиме поліпшенню СС-наслідків. S. Kojima et al. (2019) показали, що зменшення вмісту СК за допомогою фебуксостату сприяло кращому прогнозу щодо первинної комбінованої точки, ніж традиційне лікування, хоча фатальні/нефатальні церебральні та СС-події були подібними. В дослідженні FREED частота порушень функції нирок у первинній комбінованій кінцевій точці при терапії фебуксостатом достовірно знизилася. Препарат зменшував загострення альбумінурії або протеїнурії, тож він, імовірно, чинив кращу ренопротекторну дію, ніж алопуринол (Sezai et al., 2013).
Також, як було зазначено вище, фебуксостат знижував частоту епізодів подагри. Варто зауважити, що сумісне лікування фебуксостатом та інгібіторами інтерлейкіну‑1b може бути корисним не лише для запобігання нападам подагри, але й зменшення ниркових, церебральних і СС-подій (Solomon et al., 2018). У контексті чіткого взаємозв’язку між високим рівнем СК у сироватці крові та розвитком хвороби нирок, лікування фебуксостатом виявилося кращим за алопуринол у пацієнтів із дисфункцією нирок середнього й тяжкого ступеня (Weiner et al., 2008; Obermayr et al., 2008; Shibagaki et al., 2014).
Довідка «ЗУ»
На українському фармринку молекула фебуксостату представлена препаратом Ефстат виробництва ПрАТ «Фармацевтична фірма «Дарниця». Ефстат доступний у таблетованій формі в дозуваннях 80 та 120 мг/добу. Рекомендована доза для терапії подагри становить 80 мг/добу перорально незалежно від приймання їжі. Якщо концентрація сечової кислоти у сироватці крові перевищує 6 мг/дл після 2‑4 тижнів лікування, слід розглянути збільшення дози до 120 мг/добу.
Також Ефстат у дозуваннях 80 та 120 мг використовують для лікування хронічної гіперурикемії при захворюваннях, що супроводжуються відкладанням кристалів уратів, зокрема за наявності тофусів та/або подагричного артриту на даний час чи в анамнезі. Для терапії та профілактики гіперурикемії у дорослих пацієнтів, які проходять курс хіміотерапії з приводу гематологічних злоякісних новоутворень із помірним або високим ризиком розвитку синдрому лізису пухлини, застосовують дозу 120 мг.
Висновки
Результати дослідження FREED продемонстрували, що фебуксостат значно зменшував концентрацію СК у сироватці крові та сповільнював прогресування ниркової дисфункції. Лікування препаратом було пов’язане зі зниженням частоти ниркових, церебральних і СС-подій як основної комбінованої кінцевої точки у пацієнтів віком ≥65 років із гіперурикемією порівняно зі стандартною терапією за модифікації способу життя.
Підготувала Олена Коробка
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (69) 2020 р.


