10 червня, 2020
Лікування артеріальної гіпертензії в особливих клінічних ситуаціях
 Артеріальна гіпертензія (АГ) – найпоширеніше захворювання серцево-судинної (СС) системи серед дорослого населення у світі. Безумовно, своєчасна діагностика та адекватна терапія як первинної, так і вторинної АГ дають можливість досягти стабільної нормалізації артеріального тиску (АТ) і запобігти розвитку СС-ускладнень. У межах Української кардіологічної школи імені академіка М.Д. Стражеска «Діагностика та лікування серцево-судинних захворювань», що пройшла 12‑13 березня у Львові, про сучасні аспекти терапії АГ у нетипових клінічних ситуаціях розповіла науковий керівник відділення гіпертонічної хвороби ННЦ «Інститут кардіології імені М.Д. Стражеска» НАМН України, д. мед. н. Лариса Анатоліївна Міщенко.
Артеріальна гіпертензія (АГ) – найпоширеніше захворювання серцево-судинної (СС) системи серед дорослого населення у світі. Безумовно, своєчасна діагностика та адекватна терапія як первинної, так і вторинної АГ дають можливість досягти стабільної нормалізації артеріального тиску (АТ) і запобігти розвитку СС-ускладнень. У межах Української кардіологічної школи імені академіка М.Д. Стражеска «Діагностика та лікування серцево-судинних захворювань», що пройшла 12‑13 березня у Львові, про сучасні аспекти терапії АГ у нетипових клінічних ситуаціях розповіла науковий керівник відділення гіпертонічної хвороби ННЦ «Інститут кардіології імені М.Д. Стражеска» НАМН України, д. мед. н. Лариса Анатоліївна Міщенко.
У щоденній клінічній практиці актуальною лишається проблема резистентної АГ. Ризик розвитку СС-подій у таких пацієнтів у 2,5 раза вищий, ніж в осіб із контрольованою АГ (Kasiakogias et al., 2018). При цьому незадовільний контроль АТ частіше спостерігається за рахунок стійкого підвищення систолічного АТ (САТ). Зокрема, серед учасників фремінгемського дослідження серця, які лікувалися із приводу АГ, 90% хворих досягали цільового рівня діастолічного АТ (ДАТ) <90 мм рт. ст., але тільки 49% – САТ <140 мм рт. ст. (Lloyd-Jones et al., 2000). Основними предикторами недостатнього контролю АТ були похилий вік, гіпертрофія лівого шлуночка та ожиріння (індекс маси тіла >30 кг/м2).
Згідно з останніми рекомендаціями, розробленими Європейським товариством кардіологів та Європейським товариством гіпертензії (ESC/ESH, 2018), АГ вважається резистентною, якщо не вдається досягти зниження офісних показників АТ <140/90 мм рт. ст. на тлі застосування оптимальних доз трьох і більше антигіпертензивних препаратів (АГП) – інгібіторів ангіотензинперетворювального ферменту (іАПФ) або блокаторів рецепторів ангіотензину ІІ (БРА) у комбінації з блокаторами кальцієвих каналів (БКК) та діуретиками (тіазидними або тіазидоподібними). При цьому неадекватний контроль АТ слід підтвердити результатами добового або домашнього моніторування АТ, а також мають бути виключені різні причини псевдорезистентної та вторинної АГ.
Найчастішою причиною псевдорезистентної АГ є низька прихильність до призначеного лікування, тобто насамперед потрібно з’ясувати, чи приймає пацієнт АГП. Так, метааналіз дев’ятьох клінічних досліджень, де визначали комплаєнс шляхом визначення концентрації АГП у крові або сечі за допомогою методу хроматографії, показав низьку прихильність у 13‑46% випадків та повну відмову від лікування – у 2‑35% (Berra et al., 2016). Лариса Анатоліївна зазначила, що на базі Інституту кардіології всім пацієнтам із підозрою на резистентну АГ призначають потрійну фіксовану комбінацію АГП терміном на три місяці, внаслідок чого у 46% даний діагноз не підтверджується, оскільки АТ вдається нормалізувати.
У разі підтвердження резистентної АГ необхідно провести скринінгові обстеження для виключення основних причин захворювання – первинного альдостеронізму, атеросклеротичного ураження судин, синдрому обструктивного апное сну (СОАС), хронічної хвороби нирок (ХХН) та ін. Щодо ендокринної симптоматичної АГ, найпоширенішою її формою є первинний альдостеронізм (синдром Конна), коли продукція альдостерону клубочковою зоною кори наднирників непропорційно висока.
Найінформативнішим скринінговим тестом первинного альдостеронізму є визначення альдостерон-ренінового співвідношення. Слід зазначити, що з метою отримання достовірного результату тесту за чотири тижні до його проведення варто відмінити ліки, які впливають на натрієво-калієвий обмін та ренін-ангіотензин-альдостеронову систему (РААС) – антагоністи мінералокортикоїдних рецепторів (АМР), іАПФ, діуретики, БРА, дигідропіридинові БКК. Також рекомендовано припинити застосування нестероїдних протизапальних засобів і пероральних контрацептивів. У цей період за потреби антигіпертензивного лікування можна використовувати препарат пролонгованої дії верапаміл та α-блокатори (доксазозин).
Із метою оцінки специфічних симптомів і скарг при СОАС застосовують спеціальні інструменти, найпоширеніший з яких – епвортівська шкала денної сонливості. Золотий стандарт діагностики СОАС – полісомнографічне обстеження, яке включає одночасний запис електроенцефалограми, електроокулограми, електроміограми, дихального потоку, електрокардіограми тощо.
Що стосується реноваскулярної АГ, її найчастішою причиною є атеросклеротичне ураження ниркових артерій. При цьому скринінговим тестом, який дозволяє оцінити розміри нирок і функціональний резерв кровотоку в них, є дуплексна ультрасонографія ниркових судин. Також важливий показник стану функції нирок – оцінка швидкості клубочкової фільтрації (ШКФ).
Якщо розглядати ХХН, найчастіше вона буває діабетичного або змішаного ґенезу. У 70% пацієнтів з АГ та цукровим діабетом дуже важко ефективно контролювати АТ у нічні години. Так, нічна гіпертензія спостерігається в 22% таких хворих, а недостатнє зниження АТ вночі – майже в половини з них (Moye et al., 2013). Крім того, в одному з рандомізованих клінічних досліджень показано, що застосування АГП увечері асоційоване із покращенням прогнозу в осіб із ЦД і ХХН (Hermida et al., 2011).
При цьому, відповідно до європейських рекомендацій, цільовий рівень САТ у даної когорти хворих незалежно від віку повинен бути <140 мм рт. ст., але ≥130 мм рт. ст. Так, за результатами субаналізу дослідження SPRINT, при зниженні САТ <120 мм рт. ст. в осіб із ШКФ ≤60 мл/хв/м2 зростає ризик СС-подій (Pareek et al., 2019). Контроль ШКФ та рівня калію у крові після початку приймання АГП у пацієнтів із ХХН є обов’язковим. У межах ініціальної антигіпертензивної терапії в таких хворих рекомендоване сумісне використання блокатора РААС із БКК або діуретиками. Проте у випробуванні ACCOMPLISH було показано, що комбінація іАПФ та БКК ефективніша щодо зменшення прогресування ХХН у пацієнтів з АГ, ніж іАПФ та діуретика (Bakris et al., 2010).
Посилаючись на європейські рекомендації, спікерка зазначила, що при лікуванні резистентної АГ у разі неефективності потрійної комбінації АГП до вже призначеної терапії необхідно додати спіронолактон у дозі 25‑50 мг або інший діуретик, або α- чи β-блокатори. В дослідженні PATHWAY‑2 доведено, що спіронолактон ефективніше за бісопролол і доксазозин знижує АТ за резистентної АГ (Williams et al., 2015).
Л.А. Міщенко представила власне дослідження, в якому порівнювали ефективність еплеренону, спіронолактону, небівололу та моксонідину в пацієнтів із резистентною АГ (Міщенко та співавт., 2018). Загалом під спостереженням перебували 66 хворих, які отримували стандартну терапію у вигляді фіксованої комбінації блокатора РААС, тіазидного або тіазидоподібного діуретика та БКК у максимально переносимих дозах. Після проведення добового амбулаторного моніторування (ДМАТ) пацієнтам до вказаного вище лікування почергово додавали 25‑50 мг/добу спіронолактону, 25‑50 мг/добу еплеренону, 5‑10 мг/добу небівололу та 0,4‑0,6 мг/добу моксонідину. Тривалість терапії кожним препаратом становила три місяці. Після завершення кожного етапу проводили офісне вимірювання АТ і ДМАТ.
За отриманими даними, АМР мали найвищу антигіпертензивну активність, і достовірної різниці у дієвому зниженні АТ при застосуванні спіронолактону або еплеренону не виявлено. Обидва АМР продемонстрували значну перевагу щодо зменшення амбулаторного САТ упродовж всієї доби, а також ефективніше знижували АТ порівняно із препаратом центральної дії моксонідином та β-блокатором небівололом (рисунок).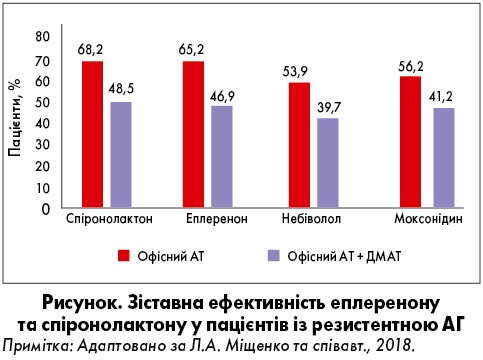
Варто зауважити, що на тлі тривалого приймання спіронолактону часто виникають побічні явища, зокрема гінекомастія та імпотенція в чоловіків, порушення менструального циклу та гірсутизм у жінок. Тому доцільним є призначення еплеренону, який також підтвердив свою ефективність при резистентній АГ, зокрема, у зарубіжних клінічних дослідженнях (Eguchi et al., 2016).
Як відомо, еплеренон – селективний антагоніст альдостеронових рецепторів із мінімальною афінністю до прогестеронових та андрогенових рецепторів. Еплеренон метаболізується переважно в печінці до неактивних метаболітів і має низьку спорідненість (50%) із білками крові. На сучасному вітчизняному фармринку еплеренон представлений препаратом Еплетор у таблетках по 25 і 50 мг (ПАТ НВЦ «Борщагівський хіміко-фармацевтичний завод»). Висока селективність лікарського засобу забезпечує його кращу переносимість, знижує ризик виникнення побічних ефектів і розширює можливості застосування. Крім того, Еплетор – препарат із доведеною біоеквівалентністю оригінальному еплеренону, що дозволяє швидко досягати стійкого антигіпертензивного ефекту в осіб із резистентною АГ і попереджати розвиток СС-ускладнень (Grim et al., 2010).
Одним із найчастіших та небезпечних ускладнень АГ є гостре порушення мозкового кровообігу. Так, серед основних факторів ризику мозкового інсульту провідну позицію займає саме АГ (Otite et al., 2017). Своєю чергою інсульт – важливий предиктор виникнення деменції у майбутньому – розвивається у 20‑35% пацієнтів (Treves et al., 1997).
На додачу, АГ є самостійним фактором ризику судинної деменції за рахунок зниження перфузії мозкових артерій. За несприятливого перебігу АГ повторні гострі епізоди порушення мозкового кровообігу призводять до розвитку дрібних ішемічних вогнищ у мозку (лакун) й ішемічного пошкодження білої речовини. Це являє собою морфологічний субстрат гіпертонічної енцефалопатії та судинної деменції. Водночас цікавими є результати одного з метааналізів, відповідно до яких рівень АТ визначає когнітивне здоров’я людей віком 35‑50 років, а після >70 років підвищений АТ вже не є фактором ризику судинної деменції (Edmin et al., 2016).
Фармакологічною основою лікування деменції різного ґенезу середнього та тяжкого ступеня є препарати, що впливають на нейромедіаторні системи, – інгібітори ацетилхолінестерази (донепезил, ривастигмін, галантамін) та антагоністи N-метил-D-аспартатних рецепторів (мемантин). Проте ці групи ліків не рекомендовані для застосування в рутинній клінічній практиці у пацієнтів із легким та помірним ступенем когнітивних порушень судинного походження.
Що стосується впливу антигіпертензивної терапії на розвиток деменції, метааналіз дев’ятьох досліджень (29 029 пацієнтів) показав практично відсутність будь-якого позитивного впливу АГП на когнітивну функцію головного мозку (van Middelaar et al., 2018). Дані лише одного випробування Syst-Euro засвідчили про зниження ризику виникнення деменції на тлі тривалого застосування препарату нітрендипін (Forrete et al., 2002).
Саме тому на сьогодні актуальний пошук додаткових фармакологічних шляхів покращення когнітивної функції у пацієнтів із судинною деменцією. Як відомо, холінергічна система головного мозку відіграє важливу роль у контролі когнітивних і мнестичних функцій. У зв’язку із цим, доцільним є вивчення впливу препаратів із групи центральних холіноміметиків щодо поліпшення когнітивних функцій в осіб з АГ.
Одним із найбільш поширених та вивчених представників цієї групи є холіну альфосцерат – фізіологічний попередник ацетилхоліну (одного з основних медіаторів нервової системи). Дана молекула стимулює холінергічну нейротрансмісію, внаслідок чого покращуються передача нервових імпульсів та пластичність нейрональних мембран, активується церебральний кровотік та стимулюються процеси метаболізму в ЦНС. В Україні холіну альфосцерат представлений препаратом Центролін (ПАТ НВЦ «БХФЗ») для лікування пацієнтів із цереброваскулярними захворюваннями та когнітивними порушеннями.
На базі Інституту кардіології було проведене дослідження щодо клінічної ефективності та переносимості препарату Центролін в осіб із вторинними проявами цереброваскулярної недостатності. Загалом було залучено 40 пацієнтів віком 55‑75 років з АГ І‑ІІІ стадії, 1‑3-го ступеня та когнітивними порушеннями <26 балів за монреальською шкалою когнітивної оцінки (МоСА). Усі хворі отримували АГП, статини й антитромбоцитарні препарати за наявності показань. Додатково до основної терапії пацієнтам був призначений препарат Центролін внутрішньовенно краплинно по 1 г/добу (4 мл) протягом семи днів і внутрішньом’язово по 1 г/добу (4 мл) упродовж восьми днів. Когнітивну функцію оцінювали на початку та наприкінці дослідження за допомогою шкали МоСА, таблиць Шульте, символ-цифрового тесту та тесту Струпа.
Як зауважила Лариса Анатоліївна, вже через 15 днів застосування препарату Центролін був виявлений позитивний вплив на когнітивну функцію. Зокрема, спостерігалися збільшення кількості балів за шкалою МоСА, поліпшення показників електроенцефалограми та церебрального кровотоку. Також після завершення курсу лікування пацієнти відмічали покращення пам’яті, самопочуття у вигляді зменшення епізодів головного болю та підвищення працездатності (Міщенко та співавт., 2020).
Таким чином, комбінація адекватної антигіпертензивної, антитромбоцитарної терапії, статинів та холіну альфосцерату (Центролін) дає можливість як попередити розвиток судинної деменції, так і ефективно сповільнити її прогресування.
Підготувала Людмила Оніщук
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (69) 2020 р.


