16 червня, 2020
Деякі аспекти рекомендацій NCCN щодо ад’ювантної системної терапії у пацієнтів із меланомою
 Клінічні рекомендації NCCN стосовно меланоми шкіри були істотно переглянуті протягом останніх кількох років у відповідь на нові дані про терапію інгібіторами імунних контрольних точок і BRAF-орієнтовану терапію. У цій статті узагальнено дані та обґрунтування, що підтверджують значні зміни рекомендацій щодо системного ад’ювантного лікування не тільки оперованих пацієнтів, а і тих, у кого виявлено нерезектабельну хворобу або віддалені метастази.
Клінічні рекомендації NCCN стосовно меланоми шкіри були істотно переглянуті протягом останніх кількох років у відповідь на нові дані про терапію інгібіторами імунних контрольних точок і BRAF-орієнтовану терапію. У цій статті узагальнено дані та обґрунтування, що підтверджують значні зміни рекомендацій щодо системного ад’ювантного лікування не тільки оперованих пацієнтів, а і тих, у кого виявлено нерезектабельну хворобу або віддалені метастази.
Деякі рекомендації NCCN щодо розгляду ад’ювантної системної терапії у пацієнтів із меланомою
Для пацієнтів із меланомою I/II стадії не рекомендується ад’ювантне лікування поза клінічними дослідженнями, хоча обґрунтування цієї рекомендації різниться в межах панелі експертів NCCN. Для пацієнтів цієї групи Управлінням з контролю якості харчових продуктів і лікарських препаратів США (FDA) не затверджено лікування інгібіторами імунних контрольних точок або BRAF. За участю пацієнтів, прооперованих з приводу поширеної меланоми, було проведено низку проспективних рандомізованих досліджень, результати яких дозволяють припустити, що інгібітори імунних контрольних точок і BRAF-мішенева терапія є ефективними варіантами ад’ювантного лікування.
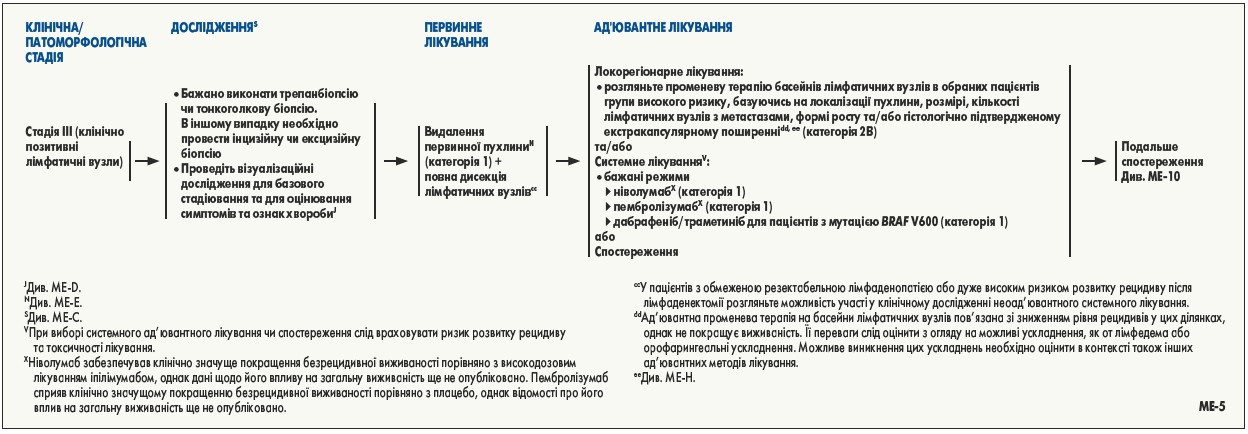
Найважливішим фактором, який слід врахувати при вирішенні питання ад’ювантного лікування, є ризик рецидиву захворювання та/або смерті. Пацієнти з меланомою IIIA стадії є групою найнижчого ризику, для якої NCCN рекомендує розглянути можливість призначення ад’ювантного лікування. Однак важливо зазначити, що критерії включення для багатьох клінічних досліджень на етапі проведення ґрунтувалися на 7-й версії класифікації Американського об’єднаного комітету з раку (AJCC), і відповідно пацієнти із хворобою IIIA стадії, визначеною цією версією класифікації, становлять групу вищого ризику, ніж як це визначено 8-ю версією класифікації AJCC.
Класифікація AJCC 8-ї версії також включає дані щодо товщини пухлини за Бреслоу при III стадії меланоми
Ризик розвитку токсичності – це інший важливий фактор при вирішенні питання про те, чи має пацієнт із захворюванням III стадії отримувати ад’ювантну терапію. Хоча інгібітори білка програмованої клітинної смерті 1 (PD‑1) та BRAF/MEK характеризуються меншою токсичністю, ніж історичні варіанти ад’ювантної терапії (інтерферон альфа, біохімотерапія), небажані події 3-4 ступеня спостерігалися у 25%-41% пацієнтів, які отримували ад’юванте лікування у межах клінічних досліджень [21-23].
У низці проспективних рандомізованих досліджень показано, що інгібітори імунних контрольних точок та BRAF-мішенева терапія є ефективними при нерезектабельній меланомі III та IV стадії [28-43]; ці препарати зараз затверджені FDA та широко застосовуються в цих умовах.
Монотерапія анти-PD‑1-препаратами
Антитіла проти PD‑1 перешкоджають зв’язуванню ліганду Т-клітинним поверхневим рецептором PD‑1, що призводить до посиленої активації Т-клітин [51, 52]. Два антитіла проти PD‑1 – ніволумаб та пембролізумаб – були досліджені як ад’ювантне лікування після видалення меланоми у 2 рандомізованих дослідженнях III фази (CheckMate 238 та KEYNOTE‑054). У дослідженні KEYNOTE‑054 пембролізумаб порівнювали з плацебо у пацієнтів після резекції меланоми III стадії. При медіані спостереження 1,2 року застосування пембролізумабу сприяло покращенню безрецидивної виживаності та зниженню ризику появи віддалених метастазів. Медіана загальної виживаності не була досягнута на час первинного звіту [22]. Незважаючи на те що частка пацієнтів, які перенесли небажану подію будь-якого ступеня, була однаковою у різних групах, небажані події тяжчого ступеня були дещо частішими у групі пембролізумабу. Аналіз даних по підгрупах свідчить, що поліпшення безрецидивної виживаності шляхом використання пембролізумабу (порівняно з плацебо) не пов’язане з експресією PD-L1 або статусом мутації BRAF. Хоча немає даних про проспективні рандомізовані дослідження, у яких би безпосередньо порівнювали ефективність ад’ювантного лікування ніволумабом та пембролізумабом, результати CheckMate 238 та KEYNOTE‑054 дозволяють припустити, що ці агенти мають аналогічну ефективність і безпеку в умовах ад’ювантного лікування [21, 22].
На підставі результатів дослідження KEYNOTE‑054 експерти NCCN рекомендують пембролізумаб як варіант ад’ювантного лікування для пацієнтів із меланомою III стадії. Аналогічно до ніволумабу, вважають експерти NCCN, пембролізумаб в ад’ювантному режимі доцільно призначати для більшої кількості пацієнтів з ІІІ стадією, ніж включена до групи KEYNOTE‑054, але рекомендація категорії 1 доступна лише для конкретних підгруп. Експерти NCCN дійшли згоди, що результати KEYNOTE‑054 дають підстави рекомендувати пембролізумаб як ад’ювантне лікування (категорія 1) для пацієнтів з клінічно виявленими метастазами у лімфатичних вузлах. Для хворих із метастазами у лімфатичних вузлах рекомендація категорії 1 обмежується підгрупою пацієнтів, що були включені у дослідження: IIIA стадія з принаймні одним метастазом у лімфатичному вузлі розміром >1 мм або стадія IIIB/C за з 7-ю версією класифікації AJCC. Пацієнти з транзиторними метастазами були виключені з цього дослідження, тому пембролізумаб в ад’ювантному режимі в цих умовах є варіантом лікування категорії 2А.
Хоча пацієнти з IV стадією не були включені до дослідження KEYNOTE‑054, експерти NCCN подають пембролізумаб в ад’ювантному режимі як варіант категорії 2А для оперованих пацієнтів з IV стадією. Оскільки на сьогодні усі дані проспективних рандомізованих досліджень – і щодо ад’ювантного режиму, і лікування нерезектабельних форм або віддалених метастазів – вказують на те, що пембролізумаб і ніволумаб зіставні за ефективністю та безпекою, експерти NCCN рекомендують пембролізумаб як варіант ад’ювантного лікування, як і ніволумаб.
Кінетика відповіді на лікування пембролізумабом
У клінічних дослідженнях середній час відповіді на застосування пембролізумабу (приблизно 3 місяці) відображає час першої оцінки відповіді на пухлину (12 тижнів), подібно до іпілімумабу, ніволумабу та хіміотерапії [32, 33, 90, 91]. Тривале спостереження у декількох дослідженнях показало, що пізню відповідь на пембролізумаб можна спостерігати більше ніж через 1 рік після початку лікування, і що початкове часткове регресування може з часом ставати повним регресуванням [32, 33, 69, 89, 91]. Об’єднаний аналіз когорти пацієнтів KEYNOTE‑001 з тривалим спостереженням (медіана 43 місяці) продемонстрував, що 16% пацієнтів досягли повного регресування, середній час до повноого регресування становив 12 місяців (від 3 до 36 місяців) [91].
Тривале спостереження під час досліджень також дало змогу виявити, що відповідь на пембролізумаб (2 мг/кг маси тіла через кожні 3 тижні в групі KEYNOTE‑002) дуже довга, її середня тривалість становить від 23 місяців і значно довше (наприклад, не досягнута навіть після 33,9 місяців спостереження у KEYNOTE‑006) [31, 69, 89, 91]. Середня тривалість відповіді становила 6,8 місяця для пацієнтів, які отримували хіміотерапію в дослідженні KEYNOTE‑002 [69]. Об’єднаний аналіз когорти Keynote‑001 з тривалим спостереженням (медіана 43 місяці) показав, що хоч у разі застосування пембролізумабу потрібен певний час для досягнення повного регресування, але воно було досить тривалим (у 88% випадків повне регресування зберігалося після середнього часу спостереження 30 місяців з моменту його фіксації; у 91% час, вільний від хвороби, тривав 24 місяці після повного регресування), навіть серед пацієнтів, яким відмінили пембролізумаб [91].
Список літератури знаходиться в редакції.
Coit D.G., Thompson J.A., Albertini M.R. et al. Cutaneous Melanoma, version 2.2019. Journal of the National Comprehensive Cancer Network. 2019 Apr; 17 (4): 367-402.
Реферативний переклад з англ. Назара Лукавецького
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 2 (63) 2020 р.