21 червня, 2020
Остеоартрит: короткий довідник лікаря
 Що таке остеоартрит?
Що таке остеоартрит?
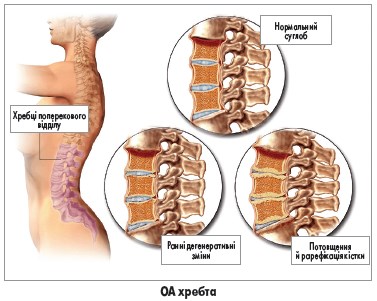
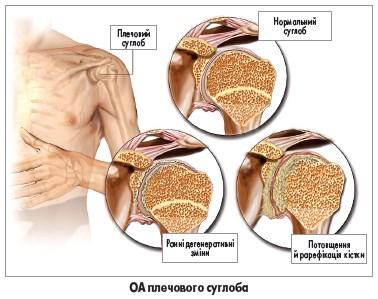
Остеоартрит (ОА) – це дегенеративна хвороба суглобів, яка розвивається внаслідок руйнування суглобового хряща й ушкодження інших тканин суглоба. Якщо безпосередня причина ОА невідома, його називають первинним, або ідіопатичним. Первинний ОА є найпоширенішою формою артриту, що вражає 60% чоловіків і 70% жінок віком понад 65 років. Головні фактори ризику ОА – вік, патологічне навантаження на суглоби, надмірна маса тіла й ожиріння, діабет та інші метаболічні порушення, травми й інфекції суглоба тощо. Фізичні вправи, зокрема біг за відсутності травм, не підвищують ризик розвитку ОА, хрустіння пальцями теж не збільшує ймовірність виникнення цього захворювання. Цікаво, що ОА й остеопороз є практично взаємовиключними патологічними станами: в пацієнтів з ОА майже ніколи не розвивається остеопороз, і навпаки.
Остеоартрит чи остеоартроз?
ОА тривалий час вважали хворобою, зумовленою так званим зношуванням суглобів, яке призводить до втрати хряща. Захворювання розцінювалося виключно як наслідок процесів, які спричиняють підвищення тиску на певний суглоб (наприклад, перевантаження суглобів, які несуть вагу тіла) чи ламкість матриці хряща (генетичні порушення компонентів матриці). Ця позиція ґрунтувалася переважно на тому, що хондроцити – єдиний тип клітин у хрящі – мають дуже низьку метаболічну активність і не здатні відновлювати ушкодження хряща. До того ж, на відміну від усіх інших тканин, суглобовий хрящ у разі ушкодження не може надавати типову запальну відповідь, оскільки в ньому відсутні судини та нерви.
Досягнення молекулярної біології в 1990-х роках докорінно змінили цю теорію. Відкриття того, що різноманітні розчинні медіатори, зокрема цитокіни та простагландини, можуть підвищувати продукцію матричних металопротеїназ хондроцитами, стало, так би мовити, першою цеглинкою в запальній теорії патогенезу ОА. Проте знадобилося аж 10 років, щоби визнати синовіт обов’язковою ознакою ОА. Пізніше експериментальні дослідження продемонстрували, що суттєва роль при ОА може належати субхондральній кістці як механічному амортизатору та джерелу запальних медіаторів, залучених до патогенезу болю й деградації глибокого шару хряща.
На сьогодні доведено, що запальні медіатори є головним чинником виникнення та підтримання остеоартритичного процесу. Джерело цих медіаторів може бути як локальним (клітини суглоба), так і системним (інші тканини). Запальні медіатори, наприклад із жирової тканини, потрапляють у кровообіг і потім досягають суглоба через судини субхондральної кістки. Є свідчення, що ті самі запальні медіатори також сприяють розвитку інших хвороб, пов’язаних із віком або метаболічними порушеннями, зокрема атеросклерозу, хвороби Альцгеймера тощо.
! Яку конструкцію маємо обрати – остеоартрит чи остеоартроз? Відповідь проста: захопливі інтервенційні протизапальні стратегії в першому випадку та фармакологічний нігілізм – у другому (Attur M.G. et al., 2002).
Діагностика
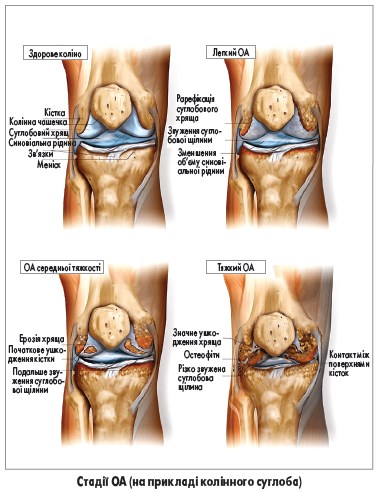
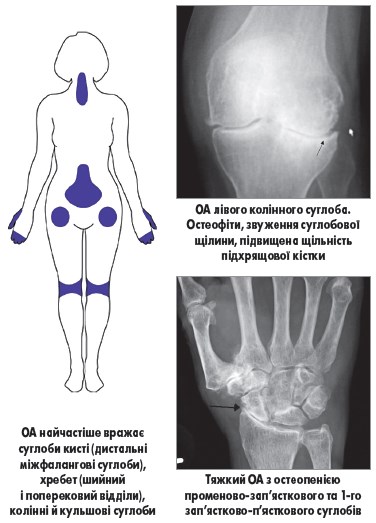
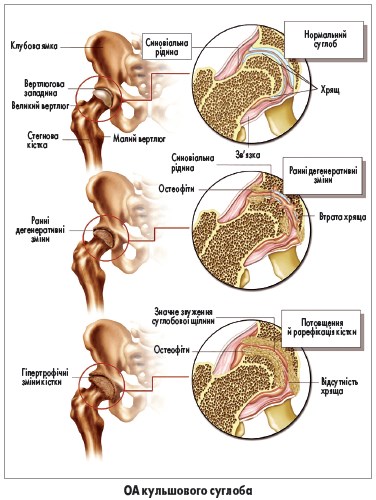
Зазвичай діагноз ОА встановлюється на підставі анамнезу та клінічного обстеження. У сумнівних випадках для підтвердження діагнозу можна застосовувати звичайну рентгенографію; інші методи візуалізації, зокрема магнітно-резонансну томографію, в рутинній практиці використовувати не рекомендується. Типовими рентгенографічними ознаками ОА є звуження суглобової щілини, субхондральний склероз, остеофіти та формування субхондральних кіст. Слід зазначити, що рентгенографічна картина може не корелювати з результатами фізикального огляду чи тяжкістю болю.
Найчастіший симптом ОА – біль, який посилюється під час роботи суглоба та зменшується в спокої. Проте на пізніх стадіях хвороби біль зберігається в спокої та вночі через втрату каркасної функції навколишніх м’язів. Біль у суглобі зазвичай супроводжується вранішньою скутістю і триває менше години. На початкових стадіях пацієнти часто описують феномен так званого стартового болю, пов’язаний із минущою скутістю через «желювання» суглоба. Стартовий біль минає після декількох циклів згинання-розгинання; цей тип болю особливо поширений при ОА суглобів нижніх кінцівок у пацієнтів похилого віку.
Із прогресуванням захворювання пацієнти відзначають зменшення рухливості суглоба, що зумовлено дисконгруентністю суглобових поверхонь, спазмом і контрактурою м’язів, скороченням капсули та механічним блоком, спричиненим остеофітами чи вільними тілами в суглобовій порожнині. Характерними (проте не патогномонічними) ознаками є варусна деформація колінного суглоба внаслідок колапсу медіального компартменту та вузли Гебердена (кісткові нарости на дорсальних поверхнях міжфалангових суглобів пальців рук). Навколо вражених суглобів кисті, стопи, кісточки чи колінного суглоба можуть пальпуватись остеофіти.Діагностика
Зазвичай діагноз ОА встановлюється на підставі анамнезу та клінічного обстеження. У сумнівних випадках для підтвердження діагнозу можна застосовувати звичайну рентгенографію; інші методи візуалізації, зокрема магнітно-резонансну томографію, в рутинній практиці використовувати не рекомендується. Типовими рентгенографічними ознаками ОА є звуження суглобової щілини, субхондральний склероз, остеофіти та формування субхондральних кіст. Слід зазначити, що рентгенографічна картина може не корелювати з результатами фізикального огляду чи тяжкістю болю.
Найчастіший симптом ОА – біль, який посилюється під час роботи суглоба та зменшується в спокої. Проте на пізніх стадіях хвороби біль зберігається в спокої та вночі через втрату каркасної функції навколишніх м’язів. Біль у суглобі зазвичай супроводжується вранішньою скутістю і триває менше години. На початкових стадіях пацієнти часто описують феномен так званого стартового болю, пов’язаний із минущою скутістю через «желювання» суглоба. Стартовий біль минає після декількох циклів згинання-розгинання; цей тип болю особливо поширений при ОА суглобів нижніх кінцівок у пацієнтів похилого віку.
Із прогресуванням захворювання пацієнти відзначають зменшення рухливості суглоба, що зумовлено дисконгруентністю суглобових поверхонь, спазмом і контрактурою м’язів, скороченням капсули та механічним блоком, спричиненим остеофітами чи вільними тілами в суглобовій порожнині. Характерними (проте не патогномонічними) ознаками є варусна деформація колінного суглоба внаслідок колапсу медіального компартменту та вузли Гебердена (кісткові нарости на дорсальних поверхнях міжфалангових суглобів пальців рук). Навколо вражених суглобів кисті, стопи, кісточки чи колінного суглоба можуть пальпуватись остеофіти.
Класифікація
Для градації ОА застосовують низку класифікаційних систем, зокрема індекс WOMAC (ураховує біль, скутість і функціональні обмеження), шкалу Келлгрена-Лоуренса (для ОА колінного суглоба; використовуються лише дані проекційної радіографії), класифікацію Тонніса (ОА кульшового суглоба, також за результатами проекційної радіографії), опитувальники KOOS і HOOS (ОА колінного та кульшового суглоба відповідно).
Залежно від визначених причин захворювання ОА поділяють на первинний і вторинний. Первинний генералізований вузловий ОА й ерозивний, або запальний, ОА є підтипами первинного.
Нефармакологічна терапія
Нефармакологічна терапія є основою лікування ОА й рекомендована всім пацієнтам із цим захворюванням. Надлишкова вага й ожиріння достовірно пов’язані з розвитком і прогресуванням ОА колінного та кульшового суглобів. Навіть невелике зменшення маси тіла знижує ризик захворювання; істотніше зменшення ваги (на 10%) у поєднанні з фізичними вправами може полегшити біль на 50%. Нормалізація маси тіла також допомагає полегшити інші проблеми зі здоров’ям, властиві багатьом пацієнтам з ОА, як-от діабет і підвищений артеріальний тиск.
Отже, помірні фізичні навантаження (аеробні й такі, що тренують місцеві м’язи) рекомендовано всім пацієнтам з ОА незалежно від віку, супутніх захворювань, тяжкості болю та порушення функції.
Фізичні навантаження підвищують рухливість суглобів і силу м’язів, що оточують суглоб. Порівняно з хворими, які ведуть малорухомий спосіб життя, пацієнти, котрі регулярно (принаймні тричі на тиждень) виконують фізичні вправи, незважаючи на ОА, відзначають менший рівень болю та кращу функцію суглобів. Для полегшення симптомів застосовують ортези, шини та різноманітні допоміжні засоби. Важливий компонент нефармакологічного лікування ОА полягає в тому, щоби навчати пацієнта самостійного ведення хвороби, що доведено полегшує біль, покращує функцію, зменшує скутість і втому, а також потребу в лікарських засобах. Під час консультування пацієнту необхідно пояснити природу та принципи ведення захворювання, спростувати поширену хибну думку про неминучість прогресування ОА та наголосити на можливості ефективного лікування.
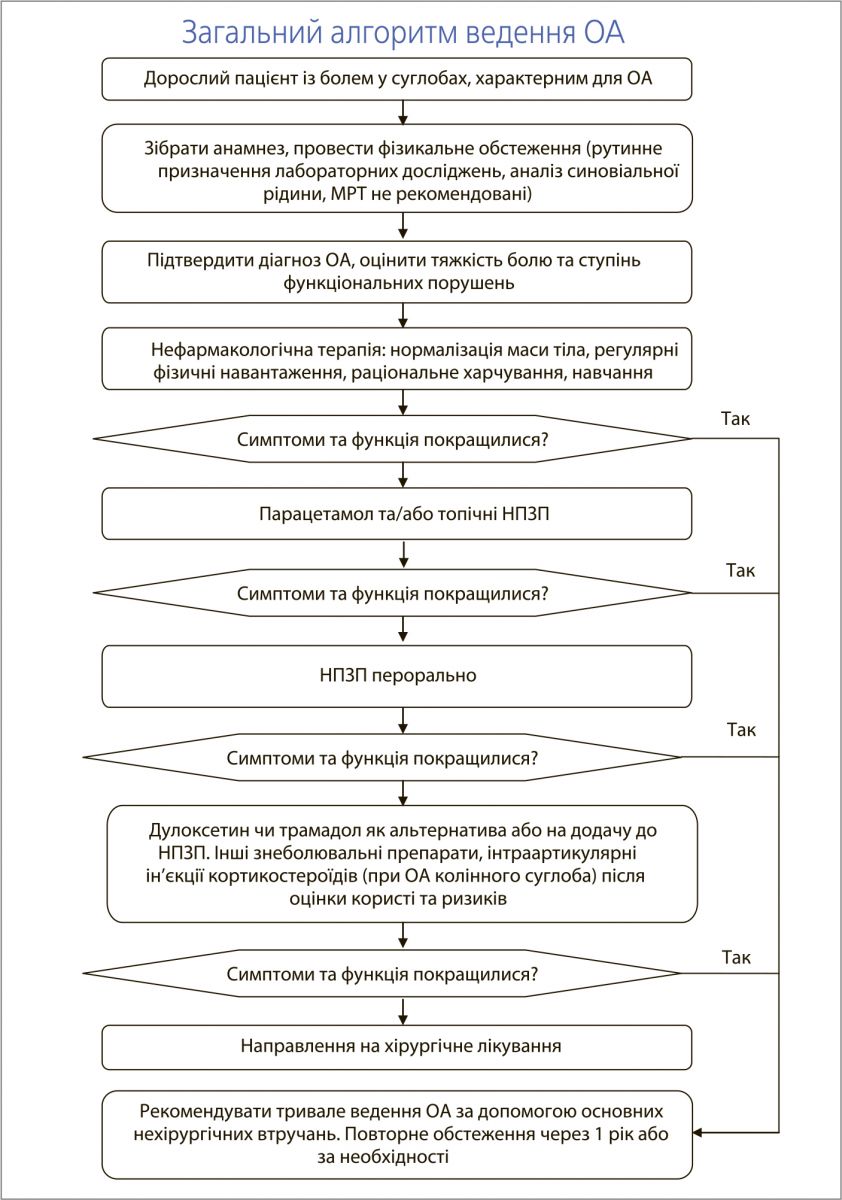
Фармакотерапія
Фармакотерапію ОА доцільно починати з топічних нестероїдних протизапальних препаратів (НПЗП) та/або парацетамолу до 4 г/добу. За наявності середньотяжких і тяжких симптомів пероральні НПЗП можуть бути ефективнішими за парацетамол, однак їх застосування асоціюється з вираженішими побічними ефектами, зокрема з гастроінтестинальною кровотечею. Селективні інгібітори циклооксигенази‑2 (ЦОГ‑2) мають таку саму ефективність, як і неселективні НПЗП, є безпечнішими щодо гастроінтестинальних побічних явищ, натомість частіше пов’язані з кардіоваскулярними подіями, такими як інфаркт міокарда. Особам віком понад 65 років, хворим із пептичною виразкою чи гастроінтестинальною кровотечею в анамнезі, а також пацієнтам, які потребують лікування кортикостероїдами чи антикоагулянтами, доцільно призначати інгібітор ЦОГ‑2, неселективний НПЗП + інгібітор протонної помпи (ІПП) або інгібітор ЦОГ‑2 + ІПП.
У пацієнтів з ОА колінного суглоба, котрі не відповідають на НПЗП або мають протипоказання до їх призначення, можна використовувати дулоксетин. Інтраартикулярні кортикостероїди забезпечують короткочасне (протягом 2-3 тиж) полегшення болю, спричиненого ОА. Останньою лінією фармакотерапії є пероральні опіоїди (трамадол).
У разі неефективності вищезазначених нефармакологічних і фармакологічних втручань слід обговорити з пацієнтом хірургічне лікування (ендопротезування суглоба). Артроскопічні операції не рекомендовані, оскільки вони не покращують перебіг ОА колінного суглоба й асоціюються зі значними ускладненнями.
Медична газета «Здоров’я України 21 сторіччя» № 9 (478), травень 2020 р.