26 липня, 2020
Фізичні навантаження та вправи у пацієнтів з раком легені: чи справдяться очікування?
Раніше хворим на рак рекомендували відпочивати, одужувати й економити енергію, уникаючи втомливих фізичних навантажень. Тим не менше з кінця 1980-х років [1] з’являлися нові дані, підтримуючи уявлення про те, що фізична активність (будь-які тілесні рухи, що виробляються скелетними м’язами та призводять до енерговитрат) і фізичні вправи (включаючи лише заплановану, структуровану та повторювану діяльність, спрямовану на покращення або підтримку одного чи декількох компонентів фізичної форми) можуть забезпечити відповідну користь в онкології. Було повідомлено про обернену кореляцію між фізичною активністю (ФА) та смертю або рецидивом у хворих на рак [2-4]. Більше того, фізичні вправи (ФВ) можуть бути корисними під час та після лікування з приводу онкологічного захворювання, сприяючи клінічно значущому покращенню фізичної підготовки [5-7], якості життя (ЯЖ) [8], зниженню рівня тяжкості пов’язаних із лікуванням побічних ефектів [5, 9] та поліпшенню психологічних наслідків захворювання (тривожність, депресія, рівень самооцінки, енергії та життєвий тонус) [5]. Настанови Американської колегії спортивної медицини щодо ФВ, в основному, призначені для пацієнтів з раком грудної, передміхурової залози, товстої кишки, онкогінекологічних та онгематологічних хворих, а рекомендацій для пацієнтів з раком легені немає.
Незважаючи на значний прогрес у застосуванні інноваційних методів лікування (таких як мішенева терапія та імунотерапія), рак легені залишається пов’язаним із фізичними, психологічними та соціальними труднощами, які чинять негативний вплив на ЯЖ пацієнтів. Крім того, різні ускладнення, зумовлені пухлиною та лікуванням, такі як задишка, втрата м’язової маси, біль, втома, втрата апетиту, зниження фізичної форми та функції легень, можуть ще погіршити стан пацієнтів [12]. Вважається, що усі ці прояви хвороби та її ускладнення можна полегшити застосуванням ФВ, незважаючи на відсутність спеціальних рекомендацій щодо раку легені.
Для пояснення зв’язку між пухлиною та ФВ було запропоновано кілька біологічних механізмів. Основна гіпотеза та докази включають контроль хронічного запалення низького рівня та модуляцію метаболічних дисрегулюючих речовин (наприклад, інсуліну, глюкози й інсуліноподібних факторів росту) та статевих гормонів. Крім того, імовірно, ФА та ФВ можуть впливати на оксидативний стрес і пов’язані з імунітетом функції, змінюючи деякі вирішальні механізми, зумовлені мікросередовищем пухлини (наприклад, ангіогенез, проліферацію та апоптоз) [13].
Матеріали та методи
24 липня 2019 р. було проведено всебічний пошук у базах PubMed та ClinicalTrials.gov для виявлення завершених і поточних досліджень щодо ролі ФА і ФВ при раку легені. Були використані такі ключові слова: вправи, фізична активність, рак легені, недрібноклітинний рак легені, дрібноклітинний рак легені. Для того щоб сформувати всебічну точку зору на цю тему, були розглянуті всі оригінальні статті (дані рандомізованих клінічних досліджень, нерандомізованих контрольованих досліджень і спостережень), що висвітлювали ФА та ФВ при раку легені. У дослідження включали дорослих, хворих на рак легені, яким виконано хірургічне втручання, під час або після медикаментозної терапії; також були розглянуті експериментальні дослідження. Ми розглядали фізичні навантаження (у тому числі також ФВ відповідно до дефініції), визначені як керовані або некеровані, включаючи будь-який тип вправ, що застосовуються у пацієнтів з раком легені і виконуються принаймні 4 тижні.
Результати досліджень щодо ФА та ФВ при раку легені
У низці досліджень вивчали вплив ФА та ФВ на вимірювані результати, такі як кардіореспіраторна витривалість, легенева функція, сила та м’язова маса, втома, якість життя, психологічний статус та якість сну (рис.).
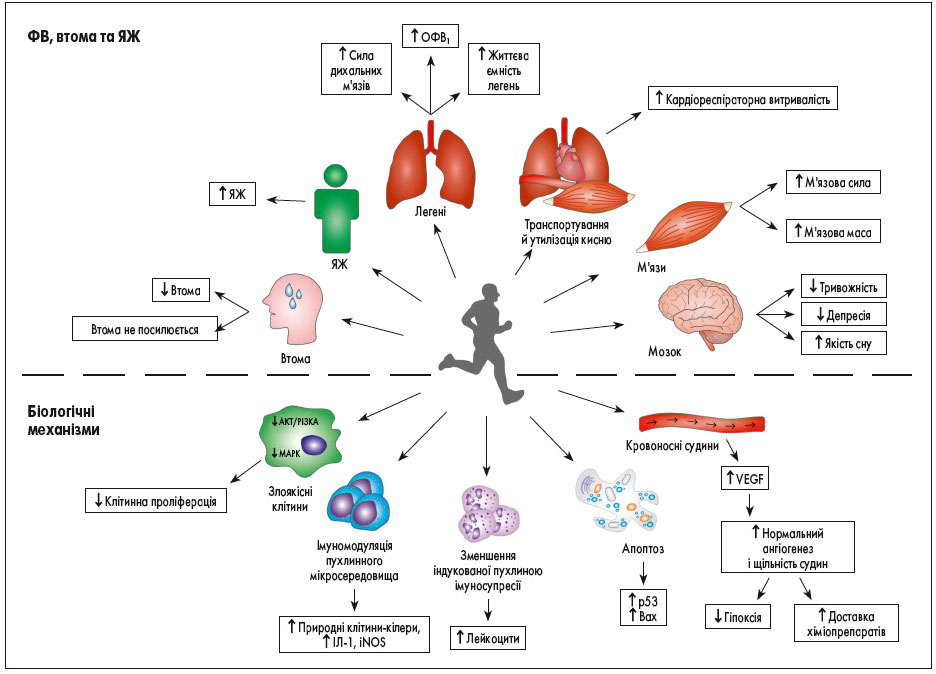 Рис. Результати впливу ФВ на фізіологію, психологію та біологію тіла при раку легені. ОФВ1 – об’єм форсованого видиху за 1 с; VEGF – фактор росту ендотелію судин; ІЛ-1 – інтерлейкін-1
Рис. Результати впливу ФВ на фізіологію, психологію та біологію тіла при раку легені. ОФВ1 – об’єм форсованого видиху за 1 с; VEGF – фактор росту ендотелію судин; ІЛ-1 – інтерлейкін-1
Втома
Втома, пов’язана з раком, визначається як «тривожне стійке суб’єктивне відчуття фізичної, емоційної та/або когнітивної втоми чи виснаження, пов’язане з пухлиною та/або її лікуванням, що не пропорційне недавній діяльності та заважає нормальній активності» [14]. При раку легені приблизно 90% пацієнтів, які проходять хіміотерапію [15], і 57% пацієнтів після хірургічного втручання [16] відзначають цей побічний ефект. Різні генетичні та поведінкові фактори ризику можуть сприяти виникненню втоми у пацієнтів [17], яка має численні прояви, такі як слабкість, порушення сну та зниження концентрації уваги, що в свою чергу негативно впливають на роботу, настрій і соціальні відносини, знижують ЯЖ [17]. Запропоновано кілька факторів як основні механізми, що викликають втому при раку. Серед них збільшення вмісту прозапальних цитокінів (таких як С-реактивний білок, інтерлейкін‑6 і фактор некрозу пухлини) та ангіогенних модуляторів (головним чином фактор росту ендотелію судин), анемія, змінений метаболізм серотоніну в мозку та дефект регенерації аденозинтрифосфату, імовірно, відіграють вирішальне значення [18, 19].
Модулюючи ці біологічні механізми, ФА може поліпшити керованість пов’язаної з раком втоми за рахунок зменшення вираженості симптомів. Було показано, що ФА допомагає протистояти втомі у пацієнтів з різними типами злоякісних новоутворень (наприклад, грудної, передміхурової залози, товстої кишки тощо) та тих, що перебувають на спостереженні після лікування [8]. Більше того, нещодавно проведений метааналіз дав змогу виявити, що ФВ і психологічне втручання є більш ефективними, ніж фармакологічний підхід для протидії такому дистресу [20]. За даними обсерваційних досліджень, що стосувалися раку легені, наявна зворотна кореляція між ФА та симптомами втоми [21‑23]. Незважаючи на те що ці результати підтвердили користь ФВ для спричиненої раком легені втоми, в інших дослідженнях відмічено відсутність змін рівня втоми після цільової програми ФВ [29-32]. Однак залучення до програми ФВ ніколи не було пов’язане із загостренням втоми. Потрібні подальші дослідження, щоб остаточно з’ясувати реальний вплив фізичних вправ на втому, пов’язану з раком легені.
Якість життя
ЯЖ визначається суб’єктивною та багатовимірною концепцією, яка включає фізичну, психологічну й соціальну сфери та виявляє прогностичний вплив при раку легені [33, 34]. Всесвітня організація охорони здоров’я характеризує ЯЖ як сприйняття людиною свого становища в житті, в контексті культурних і ціннісних систем, у яких вона перебуває, і ставлення до своїх цілей, очікувань, стандартів та проблем [35]. Пацієнти з раком легені мають тривале порушення ЯЖ порівняно зі здоровими людьми, особливо щодо фізичного стану здоров’я, як після операції, так і після хіміотерапії або променевої терапії [36-38]. Тим не менше рівень зниження ЯЖ також може залежати від стадії захворювання, прогнозу та локалізації пухлини [39].
Комплексний систематичний огляд літератури, що включав 16 рандомізованих контрольованих досліджень, які стосувалися різних типів раку (грудної, передміхурової залози, легені, колоректального раку, лімфоми), продемонстрував, що ФВ значно покращують ЯЖ (середня різниця 5,55; 95% довірчий інтервал – ДІ – 3,16‑7,90; p <0,001) під час та після лікування. Більше того: під час лікування спостерігалося поліпшення як психологічних, так і фізичних змінних, тоді як після завершення терапії було виявлено поліпшення лише фізичних аспектів [41]. Фокусуючись на дослідженнях, що включають лише хворих на рак легені, не виявлено переконливої переваги щодо ЯЖ після застосування програми ФВ [29, 31, 32, 42-49].
У рандомізованому контрольованому дослідженні намагалися оцінити вплив ФВ на ЯЖ 81 пацієнта, який переніс торакотомію. Незважаючи на те що дослідження було припинено передчасно через запровадження відеоторакоскопічної хірургії, після 12 тижнів вправ та під час періоду спостереження було зареєстровано дуже високий показник виходу із дослідження (8/23 пацієнтів в активній групі та 11/25 у контрольній групі виконали функціональний тест) без зміни рівня ЯЖ та посилення болю в активній групі [50]. Наявні результати досліджень, які свідчать про покращення ЯЖ після навчання [25, 51-55]. Зокрема у дослідженні за участю 40 пацієнтів з недрібноклітинним раком легені I-IIIA стадії показано значне поліпшення загальної ЯЖ (p=0,0032), емоційного самопочуття (p <0,0001), психічного компонента здоров’я (p=0,0004) та зменшення тривожності, депресії та дистресу після 12 тижнів мультидисциплінарних вправ, включаючи ФА (аеробні, силові вправи та природні дії), дієтичні поради, соціальне консультування та інше (наприклад, консультування щодо відмови від куріння) [51]. Враховуючи суперечливий зв’язок між ФВ та ЯЖ при лікуванні раку легені, для уточнення потрібні подальші дослідження з надійним дизайном та адекватним розміром вибірки.
Функція легень
Оцінка функції дихання за допомогою спірометрії є важливим кроком для визначення терапевтичних перспектив при раку легені. Зокрема, прогнозований післяопераційний об’єм форсованого видиху за 1 с (ОФВ1) та дифузійна здатність оксиду вуглецю (DLCO) найширше використовуються як параметри для оцінки хірургічного ризику [56] і пов’язані з прогнозом у пацієнтів з раком легені [57, 58]. Хірургічні втручання, хіміотерапія, променева терапія та супутні захворювання (наприклад, хронічне обструктивне захворювання легень – ХОЗЛ) можуть бути шкідливими для легеневої системи, знижуючи функціональність дихання [59-61]. Завдяки будові дихальна система може витримувати велике фізичне навантаження, тому тренування не потребують значної адаптації легень здорових осіб [62]. Однак роль ФВ при легеневих захворюваннях все ще суперечлива. ФВ у пацієнтів із ХОЗЛ широко досліджуються, зокрема, нещодавно виконано метааналіз, що включив 21 рандомізоване контрольоване дослідження щодо впливу ФВ на легеневу функцію у дорослих із хронічними захворюваннями легень (переважно ХОЗЛ). Результати продемонстрували невелике, але значне покращення показників спірометрії в групі ФВ порівняно з контрольною. Це дозволяє припустити, що за певних умов дихальна система може адаптуватися у відповідь на тренування [63].
Вплив ФВ на легеневі параметри при раку легені досліджували за попередньо підтвердженими даними [43, 64-67]. Індивідуальне навчання під контролем (3 рази на тиждень, 60 хв на сеанс) було запропоновано 17 пацієнтам із недрібноклітинним раком легені І-ІІІА стадії. Після 8 тижнів тренувань спостерігалось підвищення фізичних можливостей (первинний результат) без істотного поліпшення інших параметрів, таких як сила, ЯЖ, втома, тривожність, депресія та показники легеневої функції [43]. Однак у перший рік після операції у пацієнтів зазвичай спостерігається збільшення легеневих параметрів [68], що можна пояснити дією компенсаторних механізмів, таких як розширення залишкових часток легень і судинної тканини [69]. У контексті післяопераційних результатів у дослідженнях впливу різних тренувальних програм послідовно виявляють покращення сили дихальних м’язів та/або функціональність [42, 52, 70]. У ретроспективному дослідженні оцінили результати впливу різнобічних реабілітаційних заходів на легеневу функцію у 82 хворих на рак легені (IIB-IV стадія). Програма включала період розслаблення (принаймні 1 раз на день), дихальні тренування (принаймні 1 раз на день до операції), тренування проти кашлю (принаймні 1 раз на день до операції), відновлення повсякденної активності (після операції) та ФВ для нижньої кінцівки (високоінтенсивну аеробіку, 5 днів на тиждень по 45 хв). На 8-10-му тижні було виявлено значне збільшення форсованої життєвої ємності легень (ФЖЄЛ) – на 6,4% (p=0,0096) та ОФВ1 (+10,4%; p <0,0001), тоді як DLCO знизилася. Навіть в активних або колишніх курців спостерігалось поліпшення ОФВ1, тоді як у пацієнтів із порушеннями дихання спостерігалося збільшення як ФЖЄЛ (+13,9%; p=0,0025), так і ОФВ1 (+22,5%; p <0,0001) [71]. У сукупності ці результати слід трактувати обережно, оскільки в деяких дослідженнях відсутня контрольна група, і кілька аспектів потребують подальшого визначення, головним чином щодо потенційної ролі ФВ у компенсаторних механізмах після хірургічного втручання.
Кардіореспіраторна витривалість
Пікове споживання кисню (VO2peak) та 6-хвилинний тест із ходьбою (6MWT) найчастіше застосовуються для оцінювання кардіореспіраторної витривалості при раку легені. Кардіореспіраторна витривалість відображає можливість вдихання, транспортування та використання кисню, це важливий показник функціональності, здоров’я та довголіття. Як і легенева функція, VO2peak може надати клінічно важливу діагностичну та прогностичну інформацію. Він обернено пов’язаний з періопераційними та післяопераційними ускладненнями і є незалежним фактором виживаності [72]. На сьогодні вивчено зв’язок між кардіореспіраторною витривалістю та виживаністю при раку легені у 3 дослідженнях [73-75]. Jones та співавт. проспективно встановили, що кожні 50 м поліпшення 6MWT були пов’язані зі зниженням ризику смерті на 13% у пацієнтів з метастатичним недрібноклітинним раком легені. Крім того, порівняно з пацієнтами, що мали найнижчі результати 6МВТ, відзначено загальне зниження ризику смерті разом із збільшенням функціональної здатності легень (з 39 до 52%) [75]. Кардіореспіраторна витривалість у пацієнтів з раком легені була порушена порівняно зі здоровими учасниками (середня різниця 0,87 мл × кг-1 × хв-1; 95% ДІ від -12,1 до -5,3; р <0,001) [76], і це порушення не покращилося після лікування. П’ятдесят пацієнтів з недрібноклітинним раком легені (I-IIIB стадія) спостерігали протягом 6 місяців, починаючи з діагностування (попереднього лікування), наступні 10 тижнів (під час лікування) та 6 місяців (зазвичай після закінчення терапії). Результати 6МВТ значно знизилися від діагностування до лікування (-42,7 м; 95% ДІ від -71,4 до 14,0; р <0,01) і продовжували знижуватися через 6 місяців (-77,9 м; 95% ДІ від -144,3 до 11,4; p=0,02) [77].
Кардіореспіраторна витривалість передбачає кілька послідовних складників, включаючи дихальну та серцево-судинну системи, кров і скелетні м’язи. У здорових людей найважливішим фактором, що обмежує здатність до фізичних навантажень, є серцевий м’яз [62], але при злоякісних пухлинах легень багато чинників, пов’язаних із раком, одночасно зменшують кардіореспіраторну витривалість [78]. По-перше, наявність пухлинної маси, а також відповідні хірургічні процедури можуть впливати на дихальну систему за рахунок зменшення дифузійної здатності. По-друге, при поширеному раку легені оксидативна здатність скелетних м’язів порушується зі зменшенням капіляризації та мітохондріальної щільності. Крім цього, хіміотерапевтичні засоби та променева терапія можуть завдати шкоди серцю, популяції клітин крові та функції судин [78].
Хоча при захворюваннях легень дихальна система може відігравати головну роль у зменшенні здатності до фізичних навантажень, у пацієнтів, у яких після пульмонектомії минув тривалий час (середнє значення – 5,5 року), було припущено, що вона в основному обмежується за рахунок серцево-судинної системи [79]. Тим не менше ФВ можуть пом’якшити ці порушення і поліпшити кардіореспіраторну витривалість при раку легені. У рандомізованому контрольованому дослідженні вивчали вплив тренувань високої інтенсивності та силових вправ на кардіореспіраторну витривалість як основний результат. Шістдесят одного пацієнта з недрібноклітинним раком легені (I-IV стадія) було зараховано до програми ФВ (60 хв 3 рази на тиждень). Через 20 тижнів при рівні дотримання протоколу 88% автори виявили у групі ФВ збільшення кардіореспіраторної витривалості на 4,5±3,4 мл × кг-1 × хв-1, тоді як у контрольній групі відзначили її зниження на 0,6±2,7 мл × кг-1 × хв-1 [52].
У нещодавно проведеному дослідженні, що включало пацієнтів з недрібноклітинним раком (I-II стадія) після хірургічної резекції, виявлено значне збільшення VO2peak у групі ФВ порівняно з контрольною [42]. Загалом вважається (хоча у деяких дослідженнях не зафіксовано значної зміни функціональних можливостей після тренувального періоду [27, 29, 45, 47-49, 55, 64, 65]), що тренування чинять сприятливий вплив на кардіореспіраторну витривалість [22, 25, 31, 42-44, 46, 50, 52, 53, 66, 67, 70, 80].
Сила та м’язова маса
Сила та склад м’язів (маса чи розмір м’язів) – найбільш точні параметри для оцінки їх функції. Пацієнти з раком легені можуть мати порушення функції м’язів через захворювання, пов’язані з обміном речовин, методами онкологічного лікування, фізичною бездіяльністю та неправильним харчуванням [81]. Зміни м’язової маси, що виникають під час онкологічного захворювання, визначаються такими патологічними станами, як кахексія (мультифакторний синдром, який характеризується тяжкою втратою м’язової маси, неправильним харчуванням і системним запаленням) та саркопенія (зниження м’язової маси). У більшості пацієнтів із поширеним раком легені виникає кахексія (69%) або саркопенія (47%) [82], що свідчить про поганий прогноз [12, 81, 83]. Враховуючи, що сила тісно пов’язана з м’язовою масою, пацієнти з раком легені можуть також мати відповідні порушення цього параметра. Дійсно, пацієнти з недрібноклітинним раком легені (I-IIIA стадія) мали значно нижчу міцність рукостискання, ніж порівняно здорові особи (середня різниця – 6 кг; p=0,023) [76]. М’язова сила – важливий параметр, у здорових осіб вона є предиктором загальної смертності [84]. У дослідженні, яке стосувалося впливу сили на виживаність, виявлено, що сила рукостискання є незалежним прогностичним фактором у пацієнтів з недрібноклітинним раком легені та раком органів шлунково-кишкового тракту (поширеним та метастатичним) [85].
ФВ, особливо тренування опору, є потужним модулятором скелетних м’язів і може протидіяти м’язовій дисфункції у пацієнтів з раком легені. У більшості інтервенційних досліджень, що включали оцінку сили у вторинних результатах, виявлено позитивний ефект ФВ [31, 44, 47, 48, 52, 53, 64, 66, 80], проте у деяких із них не зафіксовано відповідний ефект [43, 46, 55]. Однак порівняно небагато досліджень стосувалися впливу ФВ на м’язову масу при раку легені. Salhi та співавт. досліджували вплив реабілітаційної програми на м’язову масу та силу у 45 хворих на рак легені (I-III стадія), які пройшли радикальне онкологічне лікування (хірургічне втручання та/або променеву та/або хіміотерапію). Реабілітація складалася з початкової розминки (20 хв) із подальшим тренуванням на опір м’язів верхньої та нижньої кінцівки, звичайні тренування з опором або вібрацією всього тіла 3 дні на тиждень протягом 12 тижнів після завершення лікування. Значне зменшення площі поперечного перерізу м’язів та сили квадрицепсів із збереженням маси без жиру, вимірюваної біоелектричним імпедансом, спостерігалося після лікування. Після 12-тижневої програми реабілітації було виявлено повне відновлення сили та маси м’язів в основній групі, тоді як у контрольній спостерігалося подальше зниження від початкового рівня [86].
Як було запропоновано в контексті доклінічних досліджень, аеробіка та силові тренування можуть бути корисними при раковій кахексії [87, 88]. У дослідженні MENAC тестували мультимодальний підхід з метою послаблення та/або запобігання раковій кахексії. Цей підхід включав використання протизапальних препаратів, пероральних харчових добавок, дієтичні консультації та програми ФВ у пацієнтів із раком легені та підшлункової залози. Домашні ФВ включали аеробіку (30 хв 2 рази на тиждень) та 6 індивідуальних силових вправ (3 рази на тиждень). Через 6 тижнів було показано, що втручання є безпечним і здійсненним, рівень дотримання протоколу застосування протизапальних препаратів – 76%, ФВ – 60% та харчових добавок – 48%. Не зафіксовано жодних істотних змін ФА, м’язової маси та сили, втоми та харчового статусу, ймовірно, через малий розмір вибірки [89]. Когорта ІІІ фази дослідження MENAC, до складу якої увійдуть 240 пацієнтів, наразі залучає учасників (NCT02330926) для уточнення ефективності цього мультимодального підходу.
Висновки
Як зазначено вище, багато питань досі залишаються відкритими щодо оптимального призначення ФВ і реального впливу ФВ та ФА на рівень виживаності, пов’язані з лікуванням побічні ефекти та ЯЖ пацієнтів з раком легені. Незважаючи на те що наявні докази дають вагоме обґрунтування для подальшого вивчення цих аспектів як з клінічної, так і з дослідницької точки зору, поточні результати залишаються неповними через методологічні обмеження, включаючи невелику кількість пацієнтів (в основному з початковою стадією раку легені) і недостатність спеціалізованих програм ФВ, у яких враховано індивідуальні умови пацієнта, супутні захворювання та вподобання.
Теоретично доцільно припускати, що поведінкові та психологічні втручання чи консультування можуть посилити мотивацію та дотримання протоколу, потенційно сприяючи неухильному виконанню індивідуальних програм ФВ. Поради щодо харчування можуть допомогти протидіяти саркопенії та втраті м’язової маси, тим самим зробити ФВ більш ефективними у підтримці м’язової маси та збільшенні сили. Більше того, за даними метааналізу поєднання ФВ та психологічного впливу є ефективнішим, ніж фармакологічний підхід, для протидії втомі [8]. Комплексний підхід, що включає ФВ, рекомендації щодо дієти, соціальне консультування та відмову від куріння [51], сприяє покращенню ЯЖ, емоційного самопочуття та психічного здоров’я, зменшуючи при цьому тривожність, депресію та дистрес. Загалом вплив ФА та ФВ на ЯЖ є більш глибоким, коли його застосовують як частину багатовимірного, всебічного підходу до фізичного, харчового та психологічного благополуччя.
Список літератури знаходиться в редакції.
А. Avancini, G. Sartori, A. Gkountakos et al. Physical Activity and Exercise in Lung Cancer Care: Will Promises. Be Fulfilled? The Oncologist. 2020; 25: e555-e569.
Переклав з англ. Назар Лукавецький
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 3 (64) 2020 р.


