31 липня, 2020
Применение метиленового синего в терапии инфекций мочевыводящих путей: современный взгляд
 В статье представлен обзор современных научных источников, описывающих фармакологические эффекты метиленового синего при лечении инфекций мочевыводящих путей. В частности, применение метиленового синего открывает большие возможности его влияния на патогенную микрофлору без использования традиционных антибактериальных препаратов.
В статье представлен обзор современных научных источников, описывающих фармакологические эффекты метиленового синего при лечении инфекций мочевыводящих путей. В частности, применение метиленового синего открывает большие возможности его влияния на патогенную микрофлору без использования традиционных антибактериальных препаратов.
Ключевые слова: инфекции мочевых путей, метиленовый синий.
Инфекции мочевыводящих путей: этиология, эпидемиология, современные проблемы терапии
Инфекции мочевыводящих путей (ИМП) широко распространены в мире, характеризуются высоким риском осложнений и формирования хронических воспалительных процессов. Это одна из наиболее частых причин применения антибиотиков, а также значительных финансовых затрат для системы здравоохранения. Являясь одними из самых распространенных бактериальных инфекций, ИМП способствовали формированию иммунозависимых/иммунонезависимых защитных реакций в человеческом организме. Однако и микробные патогены выработали ряд факторов вирулентности: ингибирование миграции нейтрофилов в очаг воспаления, возможность снижения иммунного ответа при реинфекции, а также выживания внутри макрофага и формирования устойчивости к антибиотикам [1].
Согласно клиническим рекомендациям Американского общества инфекционных болезней (Infectious Diseases Society of America, 2009), терапия ИМП строго регламентирована и должна осуществляться последовательно, с применением как антибактериальных, так и препаратов других фармакологических групп. Катетер-ассоциированная бактериурия (КAБ) является одной из наиболее распространенных в мире причин формирования антибиотикорезистентности, значительных экономических затрат в учреждениях здравоохранения, а также одним из наиболее распространенных расстройств здоровья у пожилых лиц, нуждающихся в постороннем уходе [2]. Ежегодно регистрируется до 900 тыс. случаев госпитальной КAБ, что составляет до 40% в структуре внутрибольничной бактериурии [3]. Согласно общемировым данным, уретральный катетер используется у 15-25% пациентов в лечебных учреждениях общего профиля; в домах престарелых эта цифра составляет от 5 до 10%, а общее число лиц, имеющих постоянный мочевой катетер, в США составляет более 1 млн человек [4-6]. Хотя средняя длительность катетеризации мочевых путей составляет не более 2-4 дней, нередко необходимо продолжительное использование мочевого катетера [7].
Симптоматическая ИМП встречается реже, чем респираторные и кожные инфекции, а также инфекции мягких тканей [4].
Из-за формирования резистентности микробиоты мочевых путей к антибактериальным средствам актуальным остается поиск препаратов для лечения и профилактики ИМП, которые стали бы альтернативной антибиотикам. К признанным в настоящее время неантибактериальным методам лечения ИМП относят коррекцию привычек (регуляция актов мочеиспускания, особенностей половой жизни, пищевых привычек, питьевого режима, физических нагрузок и т.д.), использование пищевых добавок и лекарственных препаратов (фитопрепараты, неспецифические противовоспалительные средства, про- и пребиотики, препараты D-маннозы, метенамина гиппурата; местные эстрогены; внутрипузырное введение гликозаминогликанов; иммунотропные средства, вакцины, бактериофаги и т.д.) [8, 9].
Пациенты после урологических операций и манипуляций, лица с постоянными мочевыми катетерами, пожилые пациенты мужского пола, а также с рецидивирующим течением хронических заболеваний имеют высокий риск развития ИМП. Все бактериальные ИМП должны лечиться вне зависимости от наличия у пациента мочевого катетера. В первую очередь антимикробная терапия показана при симптоматических ИМП, однако устойчивость патогенных микроорганизмов мочевыделительной системы к распространенным антибиотикам в настоящее время является предметом активного научного поиска [11, 12].
ИМП у детей обходятся системе здравоохранения США в более чем 180 млн долл. в год и являются причиной более чем 1,5 млн визитов к врачу [13].
По мнению экспертов, одной из основных современных проблем терапии ИМП у детей является повышение устойчивости штаммов группы Enterobacteriaceae к цефалоспоринам 3-го поколения, что обусловливает необходимость применения альтернативных групп уросептиков. Любые клинические протоколы применения эмпирической терапии антибиотиками широкого спектра действия требуют регулярного обновления в соответствии с локальными данными по антибиотикорезистентности [14]. Это же касается диагностики и лечения ИМП у пожилых людей, особенно при необходимости долгосрочной терапии [15].
В современной диагностике и лечении ИМП существуют следующие проблемы, связанные с антибиотикотерапией:
- широкое использование эмпирической терапии способствовало формированию антибиотикорезистентности грамотрицательных штаммов;
- сокращение вариантов лечения и повышение экономических затрат;
- постепенно в клиническую практику вводятся новые диагностические методы (тест амплификации нуклеиновых кислот, масс-спектрометрия, биосенсоры, капельная микрофлюидика) [16, 17];
- в ряде стран антибиотики широко используют как безрецептурные препараты без учета региональных особенностей антибиотикочувствительности микробиоты.
Успешное решение данных вопросов будет способствовать повышению эффективности лечения ИМП [18].
Принимая во внимание широкую лекарственную устойчивость патогенных грамотрицательных бактерий к противомикробным препаратам, а также высокий социальный запрос, Руководящая группа по проблеме резистентности к антибактериальным препаратам (ARLG) провела проспективные когортные и интервенционные исследования для улучшения результатов лечения пациентов. Фонд наблюдательных исследований CRACKLE (консорциум по устойчивости к карбапенемам – Klebsiella pneumoniae и других энтеробактерий) представил результаты многоцентровых исследований, описывающие факторы риска и клинические исходы при наличии у пациентов медицинских учреждений США устойчивых к карбапенемам энтеробактерий. Результаты исследований были предложены для включения в практические рекомендации по лечению инфекций, вызванных Acinetobacter baumannii и/или Pseudomonas aeruginosa, карбапенем-резистентными штаммами Enterobacteriaceae у больных, перенесших трансплантацию твердого органа, энтеробактериями, продуцирующими бета-лактамазу; научные исследования активно продолжаются [19].
Метиленовый синий: новые возможности применения
Метиленовый синий (МС) является давно известным медицинским антисептическим веществом. Его впервые синтезировал в 1876 г. Генрих Каро, работавший на крупнейший в мире химический концерн Badische Anilin und Soda Fabrik (BASF), что положило начало развитию химии фенотиазинов [2]. Как продукт анилинового производства, получаемый из N,N-диметиланилина, МС может поступать в сточные воды и в больших концентрациях загрязнять водные ресурсы в регионах химической промышленности [20, 21].
На данный момент МС применяется гораздо реже, чем в начале ХХ века, его коммерческие препараты до недавнего времени в нашей стране отсутствовали. Согласно обзорам иностранной литературы, использование препаратов МС имеет широкие перспективы в контексте использования в случаях резистентности микробной флоры к антибактериальным препаратам.
МС продолжает оставаться признанным антисептиком, применяемым в промышленности и медицине, что подтверждается целым рядом современных научных исследований [22-26]. В урологической практике использование МС традиционно заключалось в обработке им дефектов кожи в качестве антисептика, а также в введении препарата внутривенно при хромоцистоскопии, с визуальной оценкой интенсивности окраски струи мочи, выделяющейся из мочеточниковых устьев. Последний метод имеет историческое значение, поскольку его заменили более точные визуализационные технологии (эндоскопические, МРТ). Препараты МС (метилтиониния хлорид, хромосмон) традиционно использовали с целью детоксикации при острых отравлениях цианидами, окисью углерода, сероводородом, метгемоглобинобразующими ядами, а также при амилоидозе и гиперпаратиреоидизме в качестве акцептора и донатора ионов водорода в организме. Также ранее были проведены исследования, посвященные оценке эффективности селективного окрашивания опухолей мочевого пузыря при внутрипузырном введении 0,1% раствора МС, что способствовало улучшению их эндоскопической идентификации при отсутствии окрашивания нормального уротелия, участков воспаления и гиперплазии [28]
В настоящее время ось интересов к эффектам МС сместилась в сторону перспектив его применения у лиц с дизурией, которая часто сопровождает уропатии инфекционного и неинфекционного генеза. Под дизурией традиционно понимают чувство дискомфорта, жжения или ощущение боли во время мочеиспускания (симптомы нижних мочевых путей – СНМП). Даже с учетом значительного нарушения качества жизни пациентов с дизурией и высокого риска формирования осложнений, нередко проводится только патогенетическое лечение дизурии, а проявления основного заболевания остаются без должного внимания [29-36].
Коммерческие фенотиазиновые красители – МС (метилтиониния хлорид) и толуидиновый синий (ТС) являются эффективными фотосенсибилизирующими агентами для инактивации патогенных организмов, включая вирусы, бактерии и грибы [37]. Бактерицидные свойства МС используются в различных отраслях медицины, в частности при инактивации различных вирусов в процессе криоконсервации плазмы крови доноров [38, 39], в качестве антифунгицидного и антибактериального веществ [40-43]. Было установлено, что лимфоциты, которые могут содержать вирусы и вызывать заболевания при переливании крови, чувствительны к фотоинактивации диметил-метиленовым синим [44]. В существующих исследованиях сравнительного бактерицидного эффекта МС и ТС установлено, что оба красителя сопоставимы по эффектам фотоповреждения различных видов аденовирусов [45], вирусов везикулярного стоматита и простого герпеса, пародонтопатогенных бактерий (грамположительных и грамотрицательных) и грибов Kluyveromyces fragilis и Candida аlbicans [46]. MС эффективен против вирусов Influenza и Helicobacter [47]. Хотя фенотиазиновые красители имеют большой потенциал в лечении бактериальных, грибковых и вирусных заболеваний, в литературе содержится не много исследований, посвященных данной теме, и они разрознены [47-50].
Патогенетические механизмы действия метиленового синего
В исследовании бактерицидной активности суспензии Staphylococcus aureus, Streptococcus pneumoniae, Enterococcus faecalis, Hemophilus influenzae, Escherichia coli и Pseudomonas aeruginosa в физиологическом растворе обрабатывали растворами МС и ТС. Оба красителя уничтожили все исследованные бактерии под лазерным излучением. Полная фотодеструкция микроорганизмов была достигнута при концентрациях ТС в 1,5-7 раз ниже, чем у МC. ТC проявляет большую бактерицидную активность, чем МC, против большинства бактерий в темноте и на свету. В основном эти результаты согласуются с соответствующими коэффициентами распределения красителей [51]. Спектрофотометрически было установлено, что между красителями и бактериями произошла метахроматическая реакция, а бактерии вызывали дополнительную димеризацию МС и ТС. Грамотрицательные бактерии индуцировали димеризацию красителя более интенсивно, чем грамположительные. Эти результаты подтверждают важную роль димеров красителей в бактериальном фотоповреждении [52].
Как ТС, так и МС образуют метахроматические комплексы с липополисахаридами (ЛПС). Высокую фотобактерицидную эффективность ТС можно объяснить его сродством к ЛПС. ЛПС в основном участвуют в процессе фотосенсибилизации, опосредованном ТС, в то время как белки наружной мембраны, вероятно, в большей степени задействованы в фотокиллинге, индуцированном МС [53].
Роль МС в фотодинамической терапии против классических микробных штаммов и грибов Candida albicans хорошо известна. В настоящее время была установлена способность МС эффективно ингибировать рост Mycobacterium tuberculosis. Установлено, что МС в дозе 15,62 мкг/мл способен вызывать мембранное возмущение с усиленным образованием активных форм кислорода и повреждением ДНК у микобактерий. В исследовании указывается эффективность антимикробного действия МС на Candida и Mycobacterium [54].
Эффект противогрибкового влияния МС заключается в развитии митохондриальной дисфункции, нарушении окислительно-восстановительного и мембранного потенциала в клетках C. albicans и двух видов Candida. Было установлено, что МС ингибирует переход дрожжей в гиф у C. albicans, что является одним из основных признаков вирулентности и указывает на высокую перспективность применения его в стратегиях лечения Candida [56].
Перспективы применения метиленового синего при доброкачественной гиперплазии предстательной железы
Отдельно следует рассмотреть перспективы применения препаратов МС, в частности метилтиониния хлорида, при доброкачественной гиперплазии предстательной железы (ДГПЖ) – распространенном заболевании мужской половой сферы, с преимущественным проявлением у лиц после 50 лет. ДГПЖ возникает у мужчин в возрасте 30 лет и старше (в среднем у 20% мужчин в возрасте 40 лет и у 90% – в возрасте 90 лет), однако клинические проявления в виде СНМП появляются после 45-50 лет [57]. Увеличение частоты впервые возникших случаев ДГПЖ на протяжении последнего десятилетия является актуальной проблемой современной урологии.
К СНМП традиционно относят:
- вялую струю мочи;
- императивные позывы к мочеиспусканию днем и ночью;
- ощущение неполного опорожнения мочевого пузыря;
- выделение мочи в виде капель в конце акта;
- недержание при переполнении мочевого пузыря;
- острую задержку мочи. Острая задержка мочи (частота 3,0/1000 пациентов в год в возрасте 40-49 лет и 34,7/1000 – в возрасте 70-79 лет) является состоянием, требующим немедленного вмешательства, в отличие от хронической ретенции мочи [58].
Закономерным следствием срыва защитных механизмов компенсации при повреждении стенки мочевого пузыря на почве хронической ретенции мочи при ДГПЖ является нарушение процессов репарации слизистой оболочки. Воспалительно-дистрофические процессы в слизистой при указанных условиях протекают на фоне гипоксии и выраженного оксидативного стресса в подслизистом слое, с последовательными процессами гипертрофии, а затем атрофии детрузора. Такие условия исключают эффективный физиологический механизм элиминации бактерий из мочевого пузыря с током мочи, формируя условия развития и персистенции очагового бактериального воспаления. Хроническая ретенция мочи создает предпосылки и для возникновения пузырно-мочеточникового рефлюкса, усугубляя его рецидивирующий воспалительный процесс с повреждением защитного слоя гликозаминогликанов и формированием условий для адгезии уропатогенов с последующим образованием биопленок [59].
Признаки ИМП при хронической задержке мочи на фоне ДГПЖ наблюдаются в среднем у 29,2-36,4% пациентов [60], в то время как бессимптомная бактериурия выявляется значительно чаще – у 44,7-45% (доля уропатогенных штаммов E. coli составляет от 48 до 71%) [61].
Бессимптомная бактериурия как фактор риска развития ИМП представляет огромный интерес, поскольку может повлиять на течение и прогноз заболевания у больных ДГПЖ. Необходимость профилактической санации мочевых путей перед выполнением трансуретральной резекции простаты или трансуретральной простатэктомии отражена в рекомендациях как Европейской [58], так и Американской ассоциации урологов. Следует отметить, что тактика ведения пациентов с бессимптомной бактериурией перед оперативным вмешательством продолжает обсуждаться, и применение метилтиониния хлорида можно рассматривать как инструмент подготовки ДГПЖ к хирургическому вмешательству.
Метилтиониния хлорид обладает всеми свойствами, необходимыми в данной клинической ситуации, а именно:
- способен проникать в толщу уротелия и биопленок благодаря малому молекулярному весу;
- обладает уросептическим бактерицидным эффектом по отношению к грамотрицательным микроорганизмам (группа Enterobacteriaceae с ведущим штаммом E. coli);
- облегчает экстернализацию, а также элиминацию микробного агента (устранение возбудителя, находящегося в глубоких слоях уротелия на границе c подслизистым слоем) (рисунок), что особенно важно для предупреждения рецидивов ИМП.
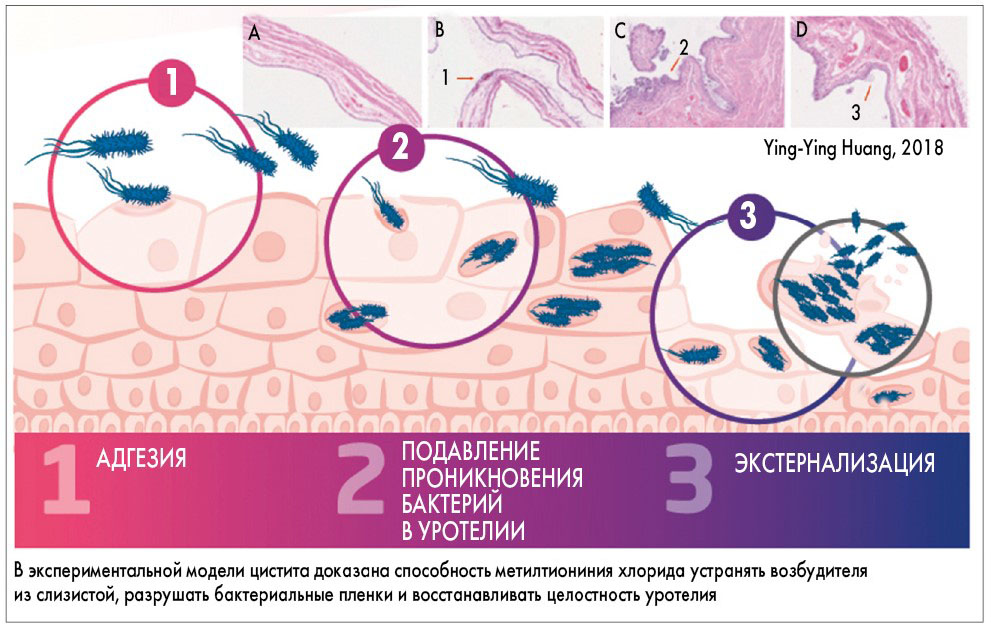 Рис. Противомикробное действие метилтиониния хлорида при экспериментальном цистите (адапт. по Huang Y., Wintner A., Seed P.C. et al. Sci Rep 8, 7257 (2018))
Рис. Противомикробное действие метилтиониния хлорида при экспериментальном цистите (адапт. по Huang Y., Wintner A., Seed P.C. et al. Sci Rep 8, 7257 (2018))
Применение МС в случаях ИМП открывает большие возможности влияния на патогенную микрофлору без использования традиционных антибактериальных препаратов. В настоящее время в Украине единственным средством, содержащим метилтиониния хлорид, остается Пембина-Блю (компания Creo Pharm). Механизм фармакологического действия Пембина-Блю заключается в способности при контакте с микробной клеткой вызывать энергозависимое мембранное возмущение ее структур с усиленным образованием активных форм кислорода и повреждением ее ДНК. Образование указанных малорастворимых комплексных соединений с мукополисахаридами и белками бактериальной клетки в верхних и нижних мочевыводящих путях способствует гибели или резкому снижению жизнеспособности различных патогенных микроорганизмов, а растительные компоненты (шалфей) способны потенцировать уросептический эффект МС.
Список литературы находится в редакции.
Тематичний номер «Урологія. Нефрологія. Андрологія» №2 (19), 2020 р.


