11 серпня, 2020
Индуцированный гипоксией фактор для лечения анемии при хронической болезни почек
Хроническая болезнь почек (ХБП) – это нарушение структуры и функции почек, присутствующее в течение ≥3 мес. ХБП является огромной проблемой общественного здравоохранения во всем мире, частота новых случаев существенно возрастает.
По данным исследования Global Burden of Disease [1], опубликованного в 2015 г., смертность от ХБП за последние 10 лет увеличилась на 31,7%. Это заболевание занимает 17-е место среди причин летальных исходов [2].
ХБП приводит к различным системным расстройствам, включая анемию, которая начинает проявляться при скорости клубочковой фильтрации (СКФ) <60 мл/мин/1,73 м2 (стадия III) [3]. При ХБП анемия встречается в 2 раза чаще (15,4%), чем в основной популяции (7,6%). Ее распространенность возрастает с каждой стадией ХБП: I стадия – 8,4%, II стадия – 14,6%, III-IV стадии – 26,4% и V стадия – 53,4% [4]. Анемия у пациентов с ХБП может быть вызвана одним фактором или комбинацией нескольких. К ним относятся дефицит эритропоэтина (ЭПО), потеря крови, снижение продолжительности жизни эритроцитов, хроническое воспаление, инфекционные заболевания, гемолитическая болезнь, повышение уровня гепсидина, вторичный гиперпаратиреоз, гипотиреоидизм, гемолиз эритроцитов, неполноценное питание (дефицит витамина В12, фолиевой кислоты, железа), повышение уровня воспалительных цитокинов. Симптомами анемии являются усталость, бледность кожи, одышка, головокружение, учащенное сердцебиение. До 1990 г. для лечения тяжелой анемии, особенно у пациентов с терминальной стадией хронической почечной недостаточности, использовали препараты на основе железа, андрогены (нандролон) и переливание крови. К сожалению, это приводило к осложнениям в виде трансфузионных реакций, сенсибилизации и перенасыщения организма железом [5]. Последний может проявлять токсичность, неблагоприятное стимулирующее действие на рост бактерий, а также прямо влиять на клетки, вызывая их повреждение [6]. Существенным недостатком препаратов железа является образование реактивных форм кислорода – гидроксильных радикалов (окисление Fe2+ → Fe3+).
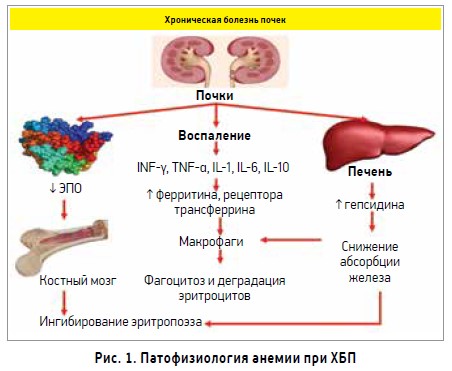
Основными причинами анемии при ХБП считается относительный дефицит продуцирования ЭПО, недостаток железа и воспаление [7] (рис. 1).
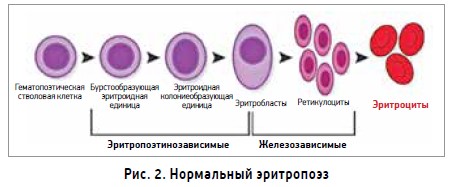
ЭПО, один из гормонов почек, представляет собой гликопротеин (40% углеводного компонента) с м. м. 34 кДа, который стимулирует выработку эритроцитов. Его роль заключается в том, чтобы контролировать продукцию эритроцитов, регулируя дифференциацию и пролиферацию эритроидного предшественника клеток в костном мозге (рис. 2).
В последние три десятилетия при недостатке ЭПО применяют эритропоэзостимулирующие агенты (ЭСА), обычно в комбинации с железом. Их классификация представлена в таблице 1.
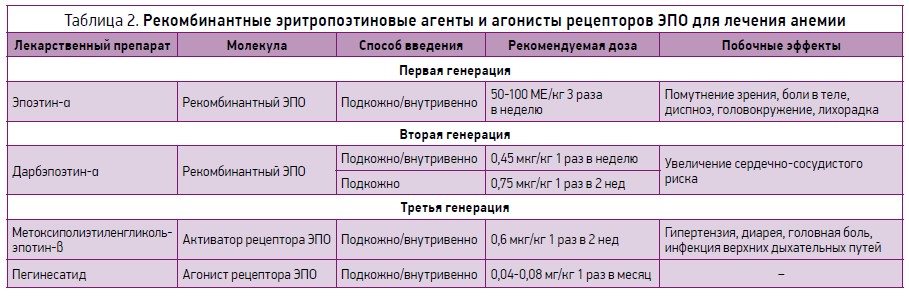
Впервые ЭПО был идентифицирован как медиатор клеточного ответа на гипоксию в середине XX века [8]. После очистки ЭПО из 2550 л мочи пациентов с анемией [9] была идентифицирована его 165-аминокислотная последовательность [10], что позволило эффективно клонировать ген ЭПО в 1985 г. [11, 12]. Рекомбинантный человеческий эритропоэтин (рчЭПО) был одобрен Управлением по контролю качества продуктов питания и лекарственных средств США (FDA) в 1989 г. [13, 14]. В исследованиях было показано, что использование рчЭПО способствует повышению уровня гемоглобина (Hb), уменьшению необходимости в переливании крови и улучшению качества жизни [15]. В последнее время появились новые возможности лечения анемии у пациентов с ХБП, которые включают использование эритропоэтиновых агентов длительного действия, а также агонистов рецептора ЭПО (табл. 2) [16].
Наиболее частыми побочными реакциями, связанными с терапией ЭСА, являются гипертензия и тромбоэмболические осложнения [17, 18]. У пациентов отмечались головная боль, тахикардия, отек, одышка, тошнота, рвота, диарея, местные реакции на инъекцию. Целью исследователей было найти «святой Грааль», то есть целевые агенты для терапии анемии, которые не имели бы побочных эффектов. Как показали научные исследования, проводимые на протяжении последних лет, такими лекарственными препаратами могут стать ингибиторы фермента пролилгидроксилазы.
Индуцированный гипоксией фактор
ЭСА, применяющиеся для лечения анемии при ХБП, имеют большое количество недостатков и могут спровоцировать неблагоприятные события, такие как повышенный риск тромбоза, сердечно-сосудистые осложнения, инфаркт миокарда, тромбоэмболия и смерть [19, 20]. Новые научные исследования показали, что в ответ на снижение напряжения кислорода в крови продуцируются факторы, которые регулируют экспрессию генов, участвующих в эритропоэзе. Так, в 1992 г. был идентифицирован продуцируемый гипоксией фактор (HIF), а в 1995 г. это соединение выделено в чистом виде [21, 22]. HIF представляет собой гетеродимерный белок, состоящий их двух компонентов: лабильной HIF‑α и стабильной HIF‑β cубъединиц. HIF‑α имеет три субъединицы – HIF‑1α, HIF‑2α, HIF‑3α. В синтезе ЭПО первая из них принимает участие в эмбриональном состоянии и теряет свои функциональные свойства после рождения. HIF‑1α также принимает участие в процессах ангиогенеза, опосредуемых фактором роста эндотелия сосудов (VEGF), и в анаэробном метаболизме глюкозы. HIF‑2α является наиболее важной субъединицей, которая экспрессируется в больших количествах в клетках организма, включая эндотелиальные клетки, гепатоциты, кардиомиоциты, глиальные клетки, пневмоциты и перитубулярные интерстициальные клетки почек. HIF‑2α отвечает за контроль синтеза ЭПО у взрослых и метаболизм железа.
Механизм действия HIF
Активность HIF регулируется путем гидроксилирования двух пролиновых остатков (в положении 402 и 564) при помощи фермента пролилгидроксилазы из семейства HIF-PH – пролилгидроксилазного домена (PHD), который состоит из PHD1, PHD2 и PHD3 [23, 24].
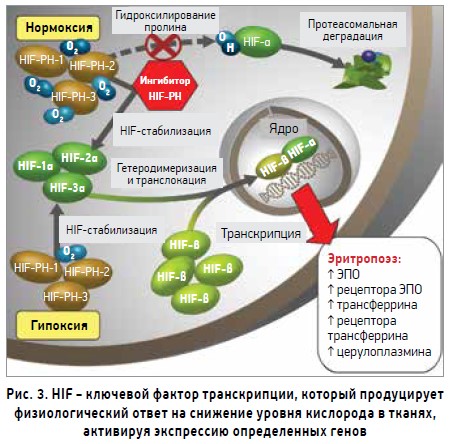
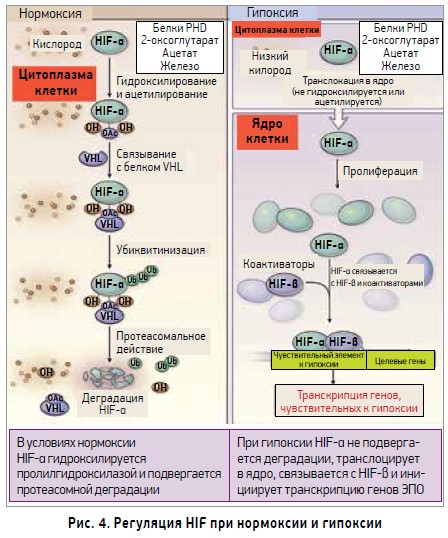
При нормоксии HIF‑2α не задействован, поэтому он инактивируется гидроксилированием через протеасомный процесс деградации, индуцированный пролилгидроксилазой. Напротив, в условиях гипоксии, когда необходимо увеличить количество эритроцитов для улучшения транспорта кислорода, стабилизация HIF‑2α осуществляется через ингибирование пролилгидроксилазы. В ряде исследований показано, что HIF‑2α является главной субъединицей, участвующей в регуляции экспрессии гена ЭПО и транспорте железа при гипоксии [25-27]. HIF активирует продуцирование ЭПО, трансферрина, церулоплазмина и рецептора трансферрина, что способствует увеличению транспорта железа из плазмы к тканям (рис. 3). HIF‑1α играет решающую роль в регуляции клеточного цикла гемопоэтических стволовых клеток, которые локализованы при гипоксии в нишах костного мозга. В ответ на стресс, каким является кровопотеря, гемопоэтические стволовые клетки быстро дифференцируются для регенерации эритроцитов. Стабилизация HIF‑1α при действии HIF-PH стимулирует гемопоэз через влияние на стволовые клетки костного мозга in vivo, которые не зависимы от ЭПО. Поэтому ингибиторы HIF-PH в отличие от обычных ЭСА могут способствовать повышению уровня Hb.
HIF‑2α экспрессируется в перитубулярных фибробластах, которые считаются основным местом продуцирования ЭПО в почках, и является ключевым фактором ответа на гипоксию. Однако в определенных ситуациях HIF‑1α контролирует ранний ответ на гипоксию. Убиквитинлигаза связывается с супрессором опухолевого белка Гиппеля – Линдау (VHL) вместе с куллином 2, элонгином C, RBX1 и распознает HIF‑1α, подготавливая ее для протеасомного разрушения. PHD1, PHD2 и PHD3 представляют собой негеможелезосодержащие диоксигеназы, для которых необходим кислород, 2-оксоглутарат как косубстраты и железо, аскорбат как кофакторы для проявления их ферментативной активности. Кроме того, активность PHD может модулироваться рядом метаболических промежуточных продуктов, включая реактивный кислород, аскорбат, сукцинат, фумарат и оксид азота. Кислородозависимая регуляция HIF в основном связана с деградацией субъединиц HIF‑α, которая начинается с гидроксилирования ферментами HIF-PH [28]. Поскольку для регуляции HIF ферментами HIF-PH требуется кислород, то при снижении его уровня пролилгидроксилирования не происходит. Это приводит к димеризации HIF‑α с HIF‑β и их аккумулированию в ядре для регуляции HIF целевых генов [29] (рис. 4).
Ингибиторы HIF‑пролил‑4-гидроксилазы являются соединениями, обратимо ингибирующими каталитическую активность PHD. Это новый перспективный класс лекарственных препаратов, которые активируют HIF и повышают уровень эндогенного ЭПО, одновременно стимулируя метаболизм железа [30] (табл. 3).
Роксадустат (FG‑4592)
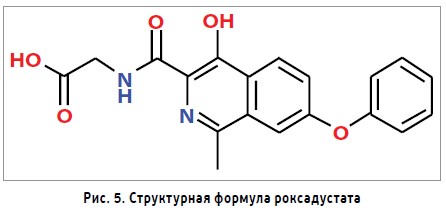
Представляет собой первую в своем классе небольшую молекулу, которая является ингибитором пролилгидроксилазы. Сейчас проходит клинические исследования III фазы для лечения анемии при ХБП [31]. Это совместная разработка компаний Fibrogen Inc., Astellas Pharma и Astra Zeneca [32]. Молекула роксадустата – это аналог 2-оксоглутарата, который стабилизирует HIF‑α (рис. 5).
Фармакодинамика
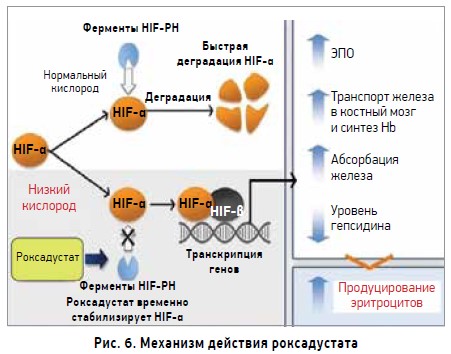
Роксадустат ингибирует деградацию HIF‑α, после чего HIF‑α димеризуется с HIF‑β и транслоцируется в ядро, где происходит активирование транскрипционного ответа на гипоксию путем активации эритропоэза (рис. 6). В клинических исследованиях I и II фаз было показано, что роксадустат стимулирует эритропоэз с продуцированием эндогенного ЭПО и подавлением гепсидина как непрямого регулятора абсорбции железа. При супрессии гепсидина увеличивается всасывание железа из тонкой кишки и происходит его выделение из мест хранения.
Фармакокинетика
Роксадустат вводится перорально, период его полувыведения составляет 12 ч. Для оценки действия препарата проводилось измерение эндогенного ЭПО и таких показателей железа, как общая железосвязывающая способность сыворотки (ОЖСС), степень насыщения трансферрина железом (СНТЖ) и уровни гепсидина. При введении роксадустата в дозе 1,0 или 2,0 мг/кг 2 или 3 раза в неделю эндогенный ЭПО увеличивался в течение 4 ч от момента введения и достигал пика через 10 ч. К исходному уровню эндогенный ЭПО возвращался через 24-48 ч независимо от полученной дозы. После 6-недельного наблюдения отмечалось снижение СНТЖ и увеличение ОЖСС, а также значительное снижение уровня гепсидина [33].
Клинические исследования Лечение анемии у пациентов с ХБП, не проходящих гемодиализ
В фазе II рандомизированного плацебо-контролируемого исследования [34] была проведена оценка лечения роксадустатом у пациентов с ХБП III-IV стадий: СКФ – 15-59 мл/мин/1,73 м2 с анемией (Hb ≤11,0 г/дл). Пациенты были рандомизированы для получения роксадустата в дозах 0,7; 1,0; 1,5 и 2,0 мг/кг или плацебо дважды в неделю в течение 4 нед или трижды в неделю в течение 26 дней. Последующие 12 нед после лечения проводилось наблюдение. Пациенты не получали аналоги ЭПО, железо внутривенно, андрогены или трансфузию эритроцитов. Было отмечено увеличение Hb ≥1 г/дл c первого дня и в последующие 2 нед. Всего были рандомизированы 117 пациентов с сопоставимыми исходными данными. Наблюдалось увеличение Hb (в зависимости от вводимой дозы) у пациентов, получавших роксадустат по сравнению с плацебо. При введении дозы роксадустата 1,5-2,0 мг/кг трижды в неделю зафиксирован более быстрый ответ Hb по сравнению с группами, получавшими препарат дважды в неделю. В отчетах сообщалось о 52 побочных действиях. Серьезные побочные реакции, такие как сосудистые события, перелом шейки бедра, боли в груди некардиального характера и одышка, зарегистрированы у 5% пациентов, получавших роксадустат, и у 4% – плацебо. Не отмечено случаев сердечно-сосудистого поражения или тромбоэмболии. Общими побочными эффектами для роксадустата были диарея, головная боль, боли в спине и усталость.
Лечение анемии у пациентов с ХБП, находящихся на гемодиализе
В открытом рандомизированном исследовании изучали действие роксадустата и экзогенного железа на анемию у пациентов, находящихся на гемодиализе [35]. В исследование были включены 60 пациентов. Из них 24 проходили гемодиализ и не получали дополнительно экзогенного железа, 12 пациентов были на гемодиализе, 12 – на перитонеальном диализе и получали железо перорально, еще 12 – на гемодиализе и получали железо внутривенно. Средняя доза перорального железа составляла 71±50 мг, внутривенного – 50 или 62,5 мг в неделю. Роксадустат в дозе 4-4,3 мг/кг вводили 3 раза в неделю. Средний возраст пациентов, включенных в исследование, – 50±15 лет, 52% составляли мужчины. Среднее время от начала первого гемодиализа – 2,2±0,9 мес, базовый уровень Hb – 8,3±1 г/дл. Среднее значение Hb увеличилось на ≥2 г/дл в течение 7 нед. Кроме того, общее среднее изменение от базовой линии Hb составило 3,1±0,2 г/дл. Ответ Hb был выше у пациентов, получавших железо, чем у тех, кто железо не получал. Реакция была одинаковой независимо от пути введения железа. Уровни гепсидина снизились во всех группах. При этом наибольшее снижение (80%) наблюдалось у пациентов на гемодиализе, не получавших железа. Неблагоприятные события отмечались у 50% больных (характерны для лиц, находящихся на гемодиализе). Наиболее частыми неблагоприятными событиями были гипертензия (10%) и снижение СНТЖ (6,7%). Имели место два смертельных исхода, которые не были связаны с роксадустатом.
Лечение анемии у пациентов с ХБП, находящихся на гемодиализе, которые ранее принимали эпоэтин-α
В фазе II рандомизированного открытого исследования оценивали безопасность и эффективность роксадустата у пациентов на поддерживающей диализной терапии, которым внутривенно вводился эпоэтин-α. Часть I исследования длилась 6 нед с последующим 8-недельным наблюдением и оценкой роксадустата, применяемого в дозах 1,0; 1,5; 1,8 и 2,0 мг/кг 3 раза в неделю, по сравнению с ЭПО. Часть II длилась 19 нед с последующим 4-недельным наблюдением у 90 пациентов в 6 когортах с различными стартовыми дозами роксадустата для сравнения с аналогами ЭПО, равными 90 Ед/кг/нед. В части I исследования у пациентов, получавших самую низкую дозу роксадустата (1,0 мг/кг трижды в неделю), наблюдалась сопоставимая скорость ответа Hb от -0,5 г/дл или выше от базовой линии по сравнению с аналогами ЭПО. У пациентов, получавших пулированный роксадустат, среднее увеличение Hb от исходного составило 0,3 г/дл по сравнению с аналогами ЭПО. В части II исследования пациенты, получавшие роксадустат, достигли необходимого уровня Hb в течение 4 нед из 19 нед лечения по сравнению с аналогами ЭПО. Таким образом, роксадустат был более эффективен по сравнению с аналогами ЭПО для поддержания уровня Hb у пациентов с терминальной стадией почечной недостаточности, не получавших внутривенно железа в дозе 1,5 мг/кг 3 раза в неделю. Профили безопасности препаратов были сопоставимы.
Продолжающиеся клинические исследования
В настоящее время проводятся 9 клинических исследований III фазы с целью изучения безопасности, эффективности и долгосрочных эффектов роксадустата у пациентов с различными стадиями ХБП, включая пациентов на гемодиализе и не проходящих его. Сравнивается применение роксадустата с плацебо, дарбэпоэтином-α и эпоэтином-α. Эти исследования должны оценить роль роксадустата в возникновении побочных эффектов при сердечно-сосудистых событиях и злокачественных образованиях.
Вададустат (AKB‑6548)
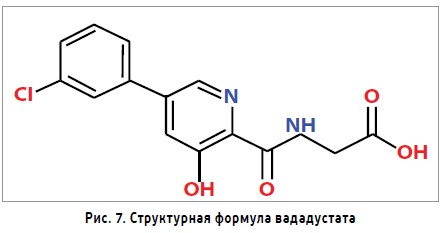
Представляет собой молекулу, которая является мощным ингибитором индуцируемого гипоксией фактора пролилгидроксилазы (HIF-PH) (рис. 7).
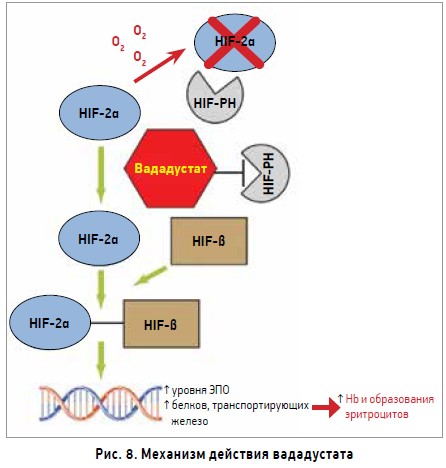
Механизм действия вададустата заключается в ингибировании HIF-PH, что способствует стабилизации и увеличению HIF. В свою очередь, HIF повышает продуцирование Hb и эритроцитов, сохраняя при этом нормальные уровни ЭПО (рис. 8). Этот дифференцированный механизм действия более безопасный, чем у инъекционных рекомбинантных стимуляторов ЭПО, что позволяет избежать супрафизиологических уровней последнего и насыщения ЭПО‑рецепторов в течение длительного периода времени. Стабилизация HIF‑2α отмечается при пероральном применении вададустата 1 раз в день.
Клинические исследования
Участники исследования (недиализные пациенты) с ХБП (n=93) были рандомизированы для приема возрастающих доз вададустата (240, 370, 500, 630 мг) или плацебо 1 раз в день в течение 6 нед [36]. Все участники получали 50 мг перорального железа ежедневно. Вададустат значительно увеличивал уровни Hb дозозависимым образом по сравнению с плацебо. В группе 630 мг 78% участников достигли ответа Hb ≥1 г/дл в течение 6 нед. Кроме того, индексы железа изменились в сторону повышения эритропоэза дозозависимым образом через снижение гепсидина и ферритина и увеличение общей железосвязывающей способности. На последующей стадии IIb двойного слепого плацебо-контролируемого исследования участники были рандомизированы на три когорты, получающие титруемые дозы вададустата (начальная доза – 450 мг) или плацебо 1 раз в день в течение 20 нед [37]. В конце 20-й недели большинство участников, получающих вададустат, достигли первичной конечной точки (средний уровень Hb ≥11,0 г/дл или увеличение Hb ≥1,2 г/дл от исходного уровня) по сравнению с плацебо (53,9% против 10,3%; р<0,001). В исследовании II фазы была отмечена хорошая переносимость препарата, а побочные реакции сравнимы с типичными проявлениями при ХБП. Вададустат находится на этапе III фазы клинических исследований, которая состоит из двух программ – «недиализные пациенты» (PRO2TECT; около 3100 участников) и «пациенты на диализе» (INNO2VATE; около 2600 участников), где одним из компонентов является дарбэпоэтин-α [38].
Дапродустат (GSK‑1278863)
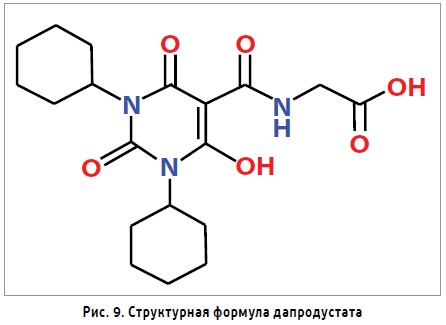
Представляет собой молекулу для ингибирования HIF-PH (рис. 9). Образовывает прочные связи с ферментом и подвергается окислительному метаболизму в печени при действии CYP2C8 с периодом полувыведения 4 ч в дозе 100 мг. Дапродустат продемонстрировал дозозависимое увеличение различных фармакодинамических маркеров, таких как ЭПО, абсолютное количество ретикулоцитов, уровень Hb, ОЖСС, и дозозависимое снижение уровней гепсидина, ферритина.
Клинические исследования
В доклинических исследованиях было показано, что дапродустат ингибирует PHD2 и PHD3 и таким образом стабилизирует как HIF‑1α, так и HIF‑2α in vitro [39]. В фазе I c возрастающей дозой дапродустата до 300 мг проводились исследования у пациентов с анемией и ХБП III-IV стадий, а также у здоровых пациентов [40]. Концентрации Hb и эндогенного ЭПО увеличивалась дозозависимо. Кроме того, лечение дапродустатом ассоциировалось с дозозависимыми изменениями эритропоэза и снижением уровня гепсидина в сыворотке без изменения уровней VEGF у пациентов на гемодиализе и не получавших гемодиализ с ХБП III-V стадий [41]. Эти результаты были подтверждены в двух исследованиях фазы IIа [42]. Пациенты были разделены на негемодиализных и гемодиализных и получали дапродустат в течение 4 нед в дозах 0,5; 2,0 и 5 мг для оценки безопасности и эффективности. В первом, «недиализном», исследовании пациенты с III-V стадиями ХБП не использовали рчЭПО в течение последних 7 нед. Во втором исследовании (группа пациентов на гемодиализе) участники получали диализ 3 раза в неделю и адекватно реагировали на рчЭПО. В группе «недиализных» пациентов были рандомизированы 73 участника, из которых 59 (81%) завершили исследование в последующие 5 и 54 нед. Исходно 100% «недиализных» пациентов имели сердечно-сосудистые факторы риска, включая гипертензию (97%), гиперлипидемию (76%) и диабет (69%). В исследовании с участием больных на гемодиализе были рандомизированы 83 пациента, из которых 70 (84%) завершили исследование с последующим наблюдением. Сердечно-сосудистые факторы риска, включая гипертензию (95%), гиперлипидемию (57%) и диабет (45%), имели 95% участников на гемодиализе. В течение 4 нед лечения в исследовании «недиализных пациентов» среднее наблюдаемое изменение от исходного уровня скорости повышения Hb для дапродустата в дозе 0,5; 2,0 и 5 мг составило 0,121; 0,121 и 0,951 г/дл соответственно по сравнению с -0,15 г/дл в группе плацебо. Было отмечено 5 нежелательных явлений у лиц, получавших дапродустат: тошнота у 2 пациентов в «недиализной» группе и анемия у 3 пациентов из «гемодиализной» группы. Однако побочные явления, связанные с действием препарата, в этих исследованиях не были четко различимы. Несмотря на это, случаи смерти в обеих группах не зафиксированы.
Молидустат (BAY 85-3934)
Является новым ингибитором HIF-РН, который стимулирует образование ЭПО и эритроцитов (рис. 10).
Клинические исследования
В исследовании фазы IIb 121 пациент с ХБП III-V стадий, не находящиеся на гемодиализе, лечились по одной из пяти схем дозирования молидустата, при котором варьировали доза и частота введения (n=101), или плацебо (n=20) [43]. Молидустат увеличивал уровни ЭПО в сыворотке в зависимости от дозы после 16-недельного периода исследования. В другой фазе 124 пациента, получавших стабильное лечение дарбэпоэтином, были рандомизированы для перехода на молидустат (начальная доза – 25, 50 и 75 мг) или остались на дарбэпоэтине в течение 16 нед. Средний уровень Hb был повышен в большей степени у пациентов, получавших молидустат [44]. Молидустат, как правило, хорошо переносился, его профиль неблагоприятных событий сопоставим с таковым плацебо. Наиболее распространенными неблагоприятными явлениями были инфекции, расстройства со стороны желудочно-кишечного тракта, сосудистые и ренально/уренальные расстройства.
Другие ингибиторы HIF-PH
В настоящее время активно проводятся исследования препаратов для лечения анемии у пациентов с ХБП такими компаниями, как Japan Tobacco Inc. (молекула JTZ‑951), Janssen Pharmaceuticals (молекула JNJ‑42905343) и Akros Pharma Inc. (молекула NCT0197164) [45].
Выводы
Понимание процессов кислородозависимой регуляции эритропоэза и взаимосвязи между ЭПО, содержанием железа, хроническим воспалением открывает возможности для внедрения в практическую медицину новых препаратов для лечения анемии у пациентов с ХБП. Этими средствами в самое ближайшее время могут стать ингибиторы HIF-PH. Пероральный путь введения данных препаратов является существенным преимуществом перед ЭСА, которые требуют внутривенного/подкожного введения. Хотя результаты многочисленных клинических исследований свидетельствуют о том, что стратегия стабилизации HIF для стимулирования эритропоэза у пациентов с заболеванием почек клинически эффективна, существует несколько проблем относительно безопасности. К ним относятся проангиогенное действие препаратов, неблагоприятные сердечно-сосудистые и метаболические эффекты, которые необходимо тщательно оценить в долгосрочных исследованиях. Еще одной проблемой, связанной с длительным использованием этих агентов, является воздействие на опухоль, поскольку активация HIF в условиях гипоксии «помогает» уже существующей опухоли выживать и продолжать рост. Знания о влиянии системной активации HIF на физиологию и патофизиологию человека все еще являются ограниченными.
Список литературы находится в редакции.