26 червня, 2015
Урогенітальний мікоплазмоз, викликаний Mycoplasma genitalium: погляд на питання лікування в практиці лікаря

 Відомо, що Mycoplasma genitalium є облігатним патогеном урогенітального тракту людини і беззаперечним збудником інфекцій, що передаються переважно статевим шляхом (ІПСШ), як у чоловіків, так і у жінок [1]. Тому визначитися з показаннями до лікування урогенітального мікоплазмозу, викликаного саме M. genitalium, досить просто. Так, показаннями до призначення антибактеріальної терапії є підтверджена M. genitalium-інфекція будь-якої локалізації чи наявність M. genitalium у статевого партнера.
Відомо, що Mycoplasma genitalium є облігатним патогеном урогенітального тракту людини і беззаперечним збудником інфекцій, що передаються переважно статевим шляхом (ІПСШ), як у чоловіків, так і у жінок [1]. Тому визначитися з показаннями до лікування урогенітального мікоплазмозу, викликаного саме M. genitalium, досить просто. Так, показаннями до призначення антибактеріальної терапії є підтверджена M. genitalium-інфекція будь-якої локалізації чи наявність M. genitalium у статевого партнера.
Вважається, що виявлення зазначеного мікроорганізму в особи навіть за відсутності клінічних проявів ураження урогенітального тракту вимагає лікування як цього пацієнта, так і всіх його статевих партнерів [2].
Починаючи з 1990-х рр., з моменту впровадження в клінічну практику виявлення M. genitalium методом полімеразної ланцюгової реакції, з’явилося багато наукових робіт щодо ролі M. genitalium у розвитку патології урогенітального тракту людини та методів лікування запальних уражень урогенітального тракту, зумовлених цим збудником [3-5].
Під час вибору тактики лікування урогенітального мікоплазмозу, викликаного M. genitalium, питання необхідності призначення адекватної антибактеріальної терапії перед лікарем не стоїть. Але питання вибору базового антибіотика, його дози і тривалості прийому залишається актуальним. Крім того, слід окремо розглядати питання застосування комплексного підходу до лікування пацієнта, а саме – необхідність та доцільність включення до схем терапії інших груп лікарських засобів, зокрема імуномодуляторів, ферментних препаратів та ін. Так, існує думка про те, що лікування урогенітального мікоплазмозу має бути комплексним і включати не лише засоби, які впливають на збудник, а й препарати, що стимулюють неспецифічну опірність організму [6].
За період вивчення різних груп антибіотиків, дозування та режимів їх призначення при лікуванні урогенітального мікоплазмозу накопичено досить велику кількість даних щодо їх ефективності. Узагальнену інформацію щодо переліку антибіотиків, режимів дозування і тривалості лікування урогенітального мікоплазмозу наведено в оглядовій роботі Н.Д. Хальневича [7] (табл.).
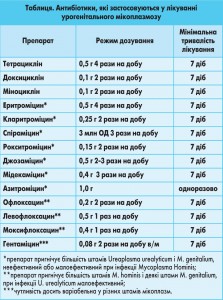
В останній час для лікування мікоплазменних інфекцій переважно використовуються антибіотики тетрациклінового ряду, макроліди та фторхінолони [8]. При виборі базового антибіотика для лікування усіх збудників ІПСШ загалом і M. genitalium зокрема лікарю необхідно орієнтуватися в першу чергу на рекомендації ВООЗ щодо критеріїв вибору антибактеріального препарату:
• ефективність не менше 95%;
• доступна ціна;
• добра переносимість і мала токсичність;
• можливість одноразового застосування;
• пероральний прийом;
• можливість застосування під час вагітності;
• повільний розвиток резистентності мікроорганізмів до засобів терапії.
Ефективність є найважливішим критерієм відбору схем лікування. Схеми з гарантією виліковування <95% необхідно використовувати з обережністю, тому що така терапія сприяє селекції стійких штамів і, таким чином, зменшує ефективність лікування пацієнтів у подальшому. Застосування схем лікування, ефективність яких нижча 85%, неприпустимо.
Ще одним важливим питанням при лікуванні ІПСШ є питання безпеки, яка залежить від ступеня токсичності застосовуваних лікарських засобів. Контингент хворих з ІПСШ нерідко схильний до зараження не одним, а кількома збудниками, що вимагає застосування кількох препаратів. Зараження може відбутися і на тлі вагітності, що змушує з особливою увагою ставитися до безпеки плода.
Питання доступності лікування зумовлено тим фактом, що ІПСШ належать до так званих соціопатологій, тобто захворювань, які мають не тільки медичне, а й соціальне значення. Тому лікування має бути ефективним незалежно від того, де воно проводиться (у центральному або периферичному лікувальному закладі), а також від того, до якого прошарку суспільства належить пацієнт.
Можливість одноразового використання та пероральний прийом є факторами, що зумовлюють комплаєнтність (прихильність до лікування) – зручність для пацієнта. Для окремих категорій хворих з низьким рівнем прихильності саме цей критерій відбору антибіотика необхідно розглядати як пріоритетний.
На сьогоднішній день на чільне місце виходить питання розвитку резистентності збудників ІПСШ до популярних засобів терапії, що призводить як до значного зниження ефективності лікування окремого пацієнта, так і до поширення резистентних до відомих антибіотиків штамів збудників ІПСШ, у тому числі M. genitalium.
Тривалий час «універсальними» антибіотиками для лікування урогенітальних мікоплазмозів вважалися тетрацикліни, які демонстрували високу ефективність як in vitro, так і in vivo [9-12]. Препарати зазвичай добре переносяться, рідко викликають алергічні реакції та токсичні ефекти. Як недолік слід розцінити неможливість їх використання для лікування вагітних і дітей. Необхідно пам’ятати, що тетрациклінові препарати слід з обережністю призначати в літній сезон через імовірність фотодинамічних реакцій, а також не поєднувати тетрацикліни із засобами, які викликають їх інактивацію, а саме з препаратами кальцію, заліза, антацидами, молочними продуктами та ін. При тривалому використанні препарати тетрациклінового ряду можуть спричиняти дисбактеріози і кандидози. Найбільш популярним і застосовуваним препаратом із групи тетрациклінів є доксициклін. Він краще, ніж тетрациклін, всмоктується при прийомі всередину, вживання їжі не впливає на його біодоступність; препарат характеризується в 2-3 рази більш тривалим періодом напіввиведення, забезпечує більш високі тканинні концентрації діючої речовини, краще переноситься пацієнтами [13]. Проте в останні роки з’явилося багато публікацій щодо низької ефективності препаратів доксицикліну саме при урогенітальних запальних ураженнях, зумовлених M. genitalium.
Так, результати низки клінічних досліджень ефективності 7-денного курсу доксицикліну при уретритах, викликаних M. genitalium, показали повне виліковування в середньому лише в 31% випадків [14-16]. В той же час саме доксициклін входить до першої лінії препаратів, рекомендованих Центрами з контролю і профілактики захворювань США (CDC) при синдромному веденні чоловіків та жінок із запальними ураженнями органів сечостатевого тракту [17]. Крім того, доксицикліну моногідрат по 100 мг 2 рази на добу протягом 10 днів рекомендовано як препарат вибору для лікування запальних захворювань урогенітальної сфери, викликаних M. genitalium, у останніх російських клінічних рекомендаціях з ведення хворих з ІПСШ та урогенітальними інфекціями (2012) [8].
Зважаючи на те що препарати доксицикліну є відносно недорогими, а у випадку застосування моногідрату – ще й досить безпечними, призначення при урогенітальному мікоплазмозі, викликаному M. genitalium, доксицикліну моногідрату по 100 мг 2 рази на добу протягом 10 днів є доречним в якості першої лінії антибактеріальної терапії, особливо у пацієнтів з гострими явищами запальних уражень нижніх відділів сечостатевої системи та першим епізодом ІПСШ в анамнезі. Не слід забувати про обмеження застосування препаратів тетрациклінового ряду під час вагітності та у дітей.
Серед макролідних антибіотиків найбільш популярними для лікування урогенітального мікоплазмозу, викликаного M. genitalium, на сьогоднішній день є азитроміцин та джозаміцин.
Що стосується ефективності використання азитроміцину в дозі 1 г одноразово для лікування M. genitalium (табл.), за останні роки накопичилося досить багато даних. Одним із найбільш відомих досліджень з порівняння ефективності доксицикліну та азитроміцину є рандомізоване дослідження, проведене на базі відділення інфекційних хвороб Медичного центру Університету Міссісіпі (м. Джексон, США) [14]. Саме на результати цього дослідження посилаються більшість спеціалістів, які займаються вивченням ефективності різних схем лікування урогенітального мікоплазмозу. Результати лікування 78 чоловіків з уретритом, викликаним M. genitalium, азитроміцином 1 г одноразово або 100 мг доксицикліну 2 рази на добу протягом 7 днів свідчать про вищу ефективність саме азитроміцину. Хоча інше рандомізоване дослідження продемонструвало клінічну ефективність азитроміцину 1 г одноразово лише 66,7% (у групі пацієнтів, які приймали доксициклін 7 днів за загальноприйнятою схемою, клінічна ефективність становила 74,5%) [18]. Низка інших досліджень показала, що використання азитроміцину в дозі 1 г одноразово для лікування чоловіків та жінок з позитивними результатами аналізів на M. genitalium забезпечувало частоту клінічного одужання у 79-87% епізодів [19, 20]. У будь-якому випадку клінічна ефективність азитроміцину у дозі 1 г одноразово не відповідає вимогам критеріїв ВООЗ щодо вибору антибактеріального препарату за показником ефективності (не менше 95%). В той же час саме одноразовий прийом азитроміцину є дуже зручним для пацієнтів і має найвищий рівень комплаєнтності. Саме тому ця методика терапії є найбільш популярною в схемах синдромного підходу до лікування пацієнтів із синдромом «виділення з уретри» у чоловіків та «вагінальних виділень» у жінок [21].
Відносно низька клінічна та мікробіологічна ефективність азитроміцину в режимі лікування 1 г одноразово багатьма дослідниками пояснюється наростанням резистентності окремих штамів збудників ІПСШ (в тому числі і M. genitalium) до антимікробних препаратів групи макролідів. Така резистентність штамів M. genitalium розвивається в штамах, що містять 23sRNA генну мутацію [22-24]. Цікавим є той факт, що в останній час з’являється дедалі більше доказів того, що саме одноразове застосування азитроміцину для лікування уражень урогенітального тракту, викликаних патогенними мікоплазмами, є причиною появи цієї мутації, яка зумовлює стійкість збудників до антибактеріальних препаратів групи макролідів [25-26]. Зважаючи на те що в Україні вивчення резистентності циркулюючих в країні штамів збудників ІПСШ до різних груп антибактеріальних препаратів в останній час системно не проводиться, а також досить широко в клінічній практиці застосовувалися схеми одноразового лікування азитроміцином, зазначена інформація щодо наростання резистентності збудників ІПСШ до макролідів має насторожувати практикуючих лікарів при виборі схеми базової антибактеріальної терапії пацієнтів з ІПСШ.
У той самий час накопичені дослідниками дані щодо ефективності азитроміцину для лікування пацієнтів з виявленим інфікуванням M. genitalium в пролонгованих курсах терапії свідчать про значно кращі результати. Вже при режимі призначення азитроміцину за схемою 1 г в перший день та повторно 1 г через 5-7 днів ерадикація M. genitalium спостерігалася у 74% випадків [27].
На сьогодні найбільш ефективною схемою призначення азитроміцину для лікування урогенітального мікоплазмозу, асоційованого з M. genitalium, вважається тривалий курс: 0,5 г у 1-й день та по 0,25 г на добу протягом 4 днів. Дослідники вважають, що саме таке дозування азитроміцину не викликає антимікробної резистентності збудника до макролідів [27, 28]. Використання продовженого 5-денного режиму терапії азитроміцином після встановленої неефективності лікування доксицикліном підвищує частоту одужання до 96% випадків [28]. Але отримати такий високий результат ефективності цієї схеми лікування урогенітальних патологій, викликаних M. genitalium, можливо лише за умови відсутності у пацієнтів штамів збудника, який є резистентним до макролідів, що прогнозувати у практиці лікаря досить важко.
В схемах лікування урогенітальних мікоплазмозів також може використовуватися інший макролід – джозаміцин. Найбільш відомим рекомендованим режимом призначення джозаміцину при урогенітальних запальних захворюваннях, викликаних M. genitalium, є 0,5 г препарату 3 рази на добу протягом 7 днів (табл.). Але на сьогодні більшість науковців та дослідників рекомендують продовження курсу лікування до 10 днів, що знайшло своє відображення і в останніх російських клінічних рекомендаціях [8]. Серед наукових досліджень оцінки ефективності та безпечності джозаміцину при урогенітальних інфекціях, асоційованих з M. genitalium, заслуговує на увагу відкрите багатоцентрове не порівняльне дослідження «Оценка эффективности джозамицина при УГИ, ассоциированных с M. genitalium, в РФ», яке показало як клінічну, так і бактеріологічну ефективність джозаміцину (по 0,5 г всередину 3 рази на добу протягом 10 днів) у чоловіків з негонококовим уретритом та у жінок із цервіцитом, викликаними M. genitalium – 96% [29].
Важливим аспектом призначення джозаміцину є можливість його застосування у вагітних жінок [30]. Висока ефективність (91,5%) і відмінна переносимість (побічних ефектів не зареєстровано) джозаміцину були, зокрема, продемонстровані в дослідженні, яке включало 47 вагітних жінок (термін вагітності 24-32 тиж) зі змішаною хламідійно-уреаплазменною інфекцією [31]. У 2001 р. джозаміцин було рекомендовано Європейським керівництвом з ІПСШ для лікування хламідійної інфекції у вагітних. Російські клінічні рекомендації 2012 р. розглядають саме джозаміцин як препарат вибору для лікування вагітних жінок з діагностованою M. genitalium – по 0,5 г 3 рази на добу протягом 10 днів.
Альтернативними препаратами є фторхінолони, а саме левофлоксацин та офлоксацин. Вивчення ефективності препаратів цієї групи щодо мікоплазм показало, що найбільш ефективним є левофлоксацин [32]. Окремі дослідження ефективності фторхінолонів вказують на непогані результати їх використання при урогенітальних інфекціях, у тому числі і M. genitalium [33-35]. Але більшість науковців вважають, що зазначені препарати необхідно розглядати в якості альтернативних за наявності протипоказань до призначення доксицикліну або макролідів [8, 36].
Окремо необхідно розглянути місце моксифлоксацину в лікуванні урогенітального мікоплазмозу, зумовленого M. genitalium. Досвід вивчення ефективності моксифлоксацину у чоловіків та жінок при ураженні M. genitalium не великий, але всі дослідники вказують на його високу ефективність [37, 38]. При невдачі ерадикації M. genitalium іншими схемами лікування європейські спеціалісти рекомендують використовувати моксифлоксацин по 0,4 г на добу протягом 10 днів, але через ризик швидкого розвитку резистентності та побічних ефектів ця терапія є виключно альтернативною [39].
Інші схеми терапії, які були представлені в таблиці, на сьогодні в лікуванні урогенітальних запальних процесів, зумовлених M. genitalium, практично не розглядаються.
Зазвичай при призначенні лікування конкретному пацієнту, у якого в процесі лабораторного обстеження виявлено M. genitalium, лікар повинен не лише орієнтуватися на дані різноманітних досліджень щодо ефективності того чи іншого режиму антибактеріальної терапії, а й враховувати індивідуальні особливості пацієнта. І хоча системних досліджень з доведеною ефективністю застосування в комплексному лікуванні урогенітального мікоплазмозу імуномодуляторів, ферментних препаратів тощо немає, рішення щодо їх призначення приймає лише лікар, враховуючи особливості конкретного пацієнта.
Але необхідно пам’ятати, що більшість невдач у лікуванні урогенітальних мікоплазмозів пов’язані з:
• використанням неадекватної антибіотикотерапії;
• порушенням режиму лікування;
• прийомом під час антибіотикотерапії алкоголю, а також несумісних лікарських засобів або харчових продуктів (див. характеристику тетрациклінів);
• відновленням статевих контактів з нелікованим партнером; наявністю у пацієнта інших ІПСШ (трихомоніазу та інших) або ендогенної інфекції сечостатевого тракту (пієлонефрити та ін.).
Саме індивідуальний комплексний підхід до призначення терапії для кожного пацієнта на основі науково-обґрунтованих методик є запорукою успішного лікування урогенітального мікоплазмозу, асоційованого з M. genitalium.
Література
1. Глобальная стратегия профилактики инфекций, передаваемых половым путем, и борьбы с ними. 2006-2015 гг. / ВОЗ, Женева – 2006.
2. Курбанова А.А. Урогенитальные инфекционные заболевания, вызванные генитальными микоплазмами. Клинические рекомендации / А.А. Курбанова, М.Р. Рахматулина // Vestn. Dermatol. Venerol. – 2009. – № 3. – С.78-83.
3. Jensen J.S., Orsum R., Dohn B. et al. Mycoplasma genitalium: a cause of male urethritis? // Genitourin. Med. – 1993. – № 69. – P. 265-369.
4. Taylor-Robinson D., Horner P.J. The role of Mycoplasma genitalium in nongonococcal urethritis // Sex. Transm. Infect. – 2001. – № 77. – P. 229-331.
5. Horner P.J., Gilroy C.B., Thomas B.J. et al. Association of Mycoplasma genitalium with acute nongonococcal urethritis // Lancet. – 1993. – № 342. – P. 582-585.
6. Прилепская В.Н., Абуд И.Ю. Урогенитальный микоплазмоз. Тезисный доклад. – М., 2001. – С. 21-23.
7. Хилькевич Н.Д. К вопросу о генитальных микоплазменных инфекциях / Н.Д. Хилькевич // Военная медицина. – 2012. – № 2.– С. 128-133.
8. Кубанова А.А. и соавт. Клинические рекомендации. – М.: Деловой Экспресс, 2012. – 112 с.
9. Дискутабельные вопросы клинического значения генитальных микоплазм / Кисина В.И., Прилепская В.Н., Соколовский Е.В. и др. // Клин. дерматология и венерология. – 2005. – № 4. – С.120-125.
10. К вопросу о роли микоплазм в урогенитальной патологии / Прилепская В.Н., Кисина В.И., Соколовский Е.В. и др. // Гинекология. – 2007. – Т. 9, № 1. – С. 31-38.
11. Mycoplasma genitalium in males with nongonococcal urethritis: prevalence and clinical efficacy of eradication / D. Gambini, I. Decleva, L. Lupica et al. // Sex Transm. Dis. – 2000. – Vol. 27, № 4. – P. 226-229.
12. Mucopurulent cervicitis and Mycoplasma genitalium / L.E. Manhart, C.W. Critchlow, K.K. Holmes et al. // J. Infect.Dis. – 2003. – Vol. 187, № 4. – P. 650-657.
13. Сухорукова М.В. Особенности диагностики и лечения Mycoplasma genitalium-ассоциированых инфекций у мужчин. Современные подходы к терапии / М.В. Сухорукова, А.В. Гущин, Д.Л. Вознесенский и др. // Фарматека. – 2008. – Cпецвыпуск: Урология, № 1. – С. 22-28.
14. Mena L.A., Mroczkowski T.F., Nsuami M., Martin D.H. A randomized comparison of azithromycin and doxycycline for the treatment of Mycoplasma genitalium-positive urethritis in men / Clin Infect Dis. Jun. – 2009. – № 48(12) – Р. 1649-1654.
15. Schwebke J.R., Rompalo A., Taylor S. et al. Re-evaluating the treatment of nongonococcal urethritis: emphasizing emerging pathogens – a randomized clinical trial / Clin Infect Dis. – Jan. – 2011. – № 52(2) – Р. 163-170.
16. Manhart L.E., Gillespie C.W., Lowens M.S. et al. Standard treatment regimens for nongonococcal urethritis have similar but declining cure rates: a randomized controlled trial / Clin Infect Dis. – Apr 2013. – № 56(7). – Р. 934-942.
17. Workowski K.A., Berman S. (2010) Sexually transmitted diseases treatment guidelines, 2010. MMWR Recomm Rep 59: 1-110.
18. Schwebke J.R. et al. Re-Evaluating the Treatment of Nongonococcal Urethritis: Emphasizing Emerging Pathogens – A Randomized Clinical Trial / Clin. Infect Dis. – 2011. – № 52(2). – Р. 163-170.
19. Bjornelius E., Anagrius C., Bojs G., Carlberg H., Johannisson G. et al. Antibiotic treatment of symptomatic Mycoplasma genitalium infection in Scandinavia: a controlled clinical trial / Sex Transm Infect. – 2008. – № 84. – Р. 72-76.
20. Jernberg E., Moghaddam A., Moi H. Azithromycin and moxifloxacin for microbiological cure of Mycoplasma genitalium infection: an open study / Int J STD AIDS. – 2008. – № 19. – Р. 676-679.
21. Guidelines for the management of sexually transmitted infections (Руководство по лечению инфекций, передающихся половым путем). ВОЗ. Женева. 2003. – 91 с.
22. Sena A.C., Lensing S., Rompalo A., Taylor S.N., Martin D.H., Lopez L.M. et al. Chlamydia trachomatis, Mycoplasma genitalium, and Trichomonas vaginalis infections in men with nongonococcal urethritis: predictors and persistence after therapy / Journal of Infectious Diseases. – 2012. – № 206(3). – Р. 357-65.
23. Manhart L.E., Gillespie C.W., Lowens M.S., Khosropour C.M., Colombara D.V., Golden M.R. et al. Standard Treatment Regimens for Nongonococcal Urethritis Have Similar but Declining Cure Rates: A Randomized Controlled Trial / Clinical Infectious Diseases. – 2013. – № 56(7). – Р. 934-42.
24. Schwebke J.R., Rompalo A., Taylor S., Sena A.C., Martin D.H., Lopez L.M. et al. Re-evaluating the treatment of nongonococcal urethritis: emphasizing emerging pathogens – a randomized clinical trial / Clinical Infectious Diseases. – 2011. – № 52(2). – Р. 163-70.
25. Anagrius C., Lorе B., Jensen J.S. Treatment of Mycoplasma genitalium. Observations from a Swedish STD Clinic. PLoS ONE. – 2013. – № 8(4) – e61481.
26. Bradshaw C.S., Jensen J.S., Tabrizi S.N., Read T.R., Garland S.M., Hopkins C.A. et al. Azithromycin failure in Mycoplasma genitalium urethritis / Emerging Infectious Diseases. – 2006. – № 12(7). – Р. 1149-1152.
27. Jernberg E., Moghaddam A., Moi H. Azithromycin and moxifloxacin for microbiological cure of Mycoplasma genitalium infection: an open study / Int. J. STD AIDS. – 2008. – № 19. – Р. 676-679.
28. Bjornelius E., Anagrius C., Bojs G., Carlberg H., Johannisson G., Johansson E. et al. Antibiotic treatment of symptomatic Mycoplasma genitalium infection in Scandinavia: a controlled clinical trial / Sexually Transmitted Infections. – 2008. – № 84(1). – Р. 72-76.
29. Гущин А.Е. Мониторинг лечения пациентов с инфекцией, вызванной Mycoplasma genitalium, с помощью методов ПЦР и НАСБА в реальном времени / А.Е. Гущин, О.А. Бурцев., П.Г. Рыжих и соавт. // Клиническая дерматология и венерология. – 2009. – № 4. – C. 58-63.
30. Czeizel A.E., Rockenbauer M., Olsen J. et al. A case control teratological study of spiramycin, roxithromycin, oleadomycin and josamycin / Acta Obstet Gynecol Scand. – 2000. – № 79(3). – Р. 234-237.
31. Юцковский А.Д. К проблеме урогенитальных инфекций у беременных: опыт лечения вильпрафеном / А.Д. Юцковский, Я.А. Юцковская, Е.А. Ивашков // Российский журнал кожных и венерических болезней. – 2002. – № 6. – С. 67-70.
32. Руденко М.А. Применение Локсофа в терапии урогенитального микоплазмоза у мужчин / Здоровье мужчины. – 2005. – № 1. – С. 35-39.
33. Немченко О.И., Уварова Е.В. Урогенитальный микоплазмоз (обзор литературы) // Гинекология. – 2007. – Т. 9, № 6. – С. 9-16.
34. Раковская И.В. Микоплазмы и микоплазменные инфекции // Вестн. дерматологии и венерологии. – 2008. – № 5. – С. 60-65.
35. Савичева А.М., Башмакова М.А. Генитальные микоплазмы и вызываемая ими патология // Леч. врач. – 2008. – № 11. – С. 11-16.
36. Sexually Transmitted Diseases Treatment Guidelines, 2014 / Kimberly A. Workowski, MD; Gail Bolan, MD et al. – 2014. – 270 р.
37. Bebear C.M., de Barbeyrac B., Pereyre S., Renaudin H., Clerc M., Bebear C. Activity of moxifloxacin against the urogenital mycoplasmas Ureaplasma spp., Mycoplasma hominis and Mycoplasma genitalium and Chlamydia trachomatis / Clinical Microbiology & Infection. – 2008. – № 14(8). – Р. 801-805.
38. Hamasuna R., Jensen J.S., Osada Y. Antimicrobial susceptibilities of Mycoplasma genitalium strains examined by broth dilution and quantitative PCR / Antimicrobial Agents & Chemotherapy. – 2009. – № 53(11). – Р. 4938-4939.
39. Ross J.D., Jensen J.S. Mycoplasma genitalium as a sexually transmitted infection: implications for screening, testing, and treatment / Sex Transm Infect. – 2006. – № 82. – Р. 269-271.


