29 листопада, 2016
Метастатичні ураження кісток та методи їх лікування

Метастатичне ураження скелета є серйозною проблемою для пацієнтів із поширеним пухлинним процесом. Цей тип ураження, як правило, супроводжується гострим тривалим болем, виснажує пацієнта і призводить до значного погіршення якості життя. Біль, що супроводжує метастази в кістки, залежить від таких факторів, як хімічна стимуляція больових рецепторів цитокінами, які вивільняються з пухлинних клітин, розростання пухлинних мас, гіперкальціємія, нестабільність скелета, утворення мікропереломів, розвиток патологічних переломів. Компресія спинного мозку або нервових корінців, пов’язаних із метастатичним ураженням скелета, викликають больовий синдром і можуть значно обмежувати функціональний стан хворого, при цьому пацієнтам необхідна госпіталізація та хірургічне втручання для їх корекції. Переломи хребців на тлі метастатичного ураження призводять до нерухомості хворого та функціональних порушень з боку тазових органів. Особливо пацієнтів виснажують переломи ребер, які супроводжуються сильним болем, неможливістю виконувати звичні дії, при цьому часто потрібна постійна допомога медичного персоналу. Ці ускладнення метастатичного ураження кісток зазвичай об’єднують словосполученням «skeletal-related events» (SREs), тобто «події, пов’язані зі скелетом». За даними рентгенографії, більша частина метастазів у кістки мають остеолітичний характер і близько третини випадків становлять змішані остеолітичні й остеобластичні ураження.
Метастази в кістках зустрічаються у 80% пацієнтів, хворих на рак молочної залози (РМЗ) і на рак передміхурової залози (РПЗ), і у 40% пацієнтів із раком легенів (РЛ). Середній проміжок часу між хірургічним видаленням первинної пухлини та появою метастазів становить 38 місяців, а середня тривалість життя пацієнтів при РМЗ із метастатичним ураженням кісток коливається від 19 до 25 місяців, із гормонозалежним РПЗ – від 30 до 35 місяців.
Недрібноклітинний рак легенів (НДКРЛ) становить більшу частину всіх пухлин легенів (75-80%), причому на момент встановлення діагнозу в більшості пацієнтів спостерігається поширений процес. Віддалені метастази зустрічаються у 11-36% пацієнтів, найчастіше ураження кісток представлено переважно остеолітичними вогнищами. На момент встановлення діагнозу місцево-поширений процес виявляється приблизно у 20% пацієнтів із нирково-клітинним раком (НКР), віддалені метастази – у 25% хворих. Частота, з якою зустрічається метастатичне ураження кісток, серед усіх первинних пацієнтів з НКР коливається від 17 до 50%. Середня тривалість життя пацієнтів із метастатичним НКР становить усього 6-12 місяців.
Велика частина клінічних проявів множинної мієломи (ММ) пов’язана з остеолітичною деструкцією кісток. Так, під час аналізу перебігу хвороби понад тисячі пацієнтів із ММ остеолітичні вогнища було виявлено приблизно у 67% первинних пацієнтів, а з перебігом захворювання остеолітичні ураження спостерігалися у 84% хворих. На момент встановлення діагнозу явища остеопорозу були у 23% пацієнтів, больовий синдром різного ступеня вираженості – у 58%, патологічні переломи – у 26%, компресійні переломи – у 22% хворих. Середня тривалість життя пацієнтів із ММ становить 33 місяці, причому цей показник дещо вищий у пацієнтів у віці 65-70 років – 40,5 місяця.
Прогноз при метастазах у кістки залежить від низки факторів, серед яких, зокрема, агресивне зростання первинної пухлини; короткий часовий проміжок між лікуванням первинної пухлини і появою метастазів (безрецидивний період), відсутність рентгенологічних ознак склерозу кістки в ділянці метастазу до і після проведення системної терапії; множинність метастазів, особливо в поєднанні з ураженням вісцеральних органів, великий об’єм метастатичної пухлини; незадовільний загальний стан хворого.
В основі сучасних підходів до лікування метастатичних пухлин кісток лежить використання комбінованих і комплексних методів лікування, які дозволяють значно поліпшити якість життя цього контингенту хворих.
Під час вибору тактики лікування хворих на злоякісні новоутворення з метастатичними ураженнями скелета слід ураховувати загальний стан пацієнта, тип пухлини та її радіочутливість, стадію процесу, включаючи середню тривалість життя хворого, попередню терапію, неврологічний статус, термін від появи перших симптомів ураження скелета, поширеність ураження скелета.
Лікування метастазів у частини хворих з онкопатологією може бути радикальним, однак у переважної більшості пацієнтів – лише паліативним. Основними завданнями терапії є зменшення вираженості больового синдрому, запобігання розвитку патологічних переломів, підвищення рухливості та функціональної активності хворих і, якщо можливо, збільшення тривалості їхнього життя. Все це можливо лише за умови застосування комплексу заходів, який включає: локальну дію (хірургічне лікування, променева терапія); системну терапію (хіміотерапія; гормонотерапія; препарати, що впливають на обмін кісткової тканини, – бісфосфонати), підтримувальну терапію (так зване supportive care – аналгетики, психологічна та соціальна допомога).
Під час паліативного лікування хворих із метастазами в кістки, особливо остеолітичного характеру, безперечні перспективи має використання бісфосфонатів (золендронова кислота, памідронова кислота тощо) – синтетичних аналогів неорганічного компонента кісткового матриксу. Застосування бісфосфонатів дає змогу у хворих з множинними остеолітичними метастазами в короткі терміни зменшити больовий синдром, кількість патологічних переломів, поліпшити їхнє самопочуття.
Бісфосфонати мають здатність до стримування резорбтивних процесів у кістках шляхом зниження активності остеокластів. Пригнічуючи резорбцію кістки, бісфосфонати гальмують росткові чинники, тим самим блокують зворотний зв’язок із пухлинними клітинами, що сприяє зниженню активності проліферації пухлинних клітин.
Бісфосфонати також здатні знижувати адгезію пухлинних клітин до кістки, що робить її менш доступною для них, стримуючи появу нових метастатичних вогнищ.
У комбінації зі стандартною протипухлинною терапією бісфосфонати уповільнюють прогресування кісткових метастазів, стабілізують зміни в кістках, що сприяє розвитку в цих ділянках остеосклерозу.
Променева терапія (ПТ) є традиційним засобом знеболення при метастатичному ураженні скелета. Пацієнтам із поодинокими метастатичними вогнищами в кістках, ураженням хребців та основи черепа (включаючи епідуральне поширення процесу) показано проведення ПТ. Крім того, навіть у пацієнтів із множинними метастазами ПТ на «ключові» ділянки дозволяє значно знизити потребу в наркотичних аналгетиках й істотно поліпшити якість життя хворого. Проведення локальної радіотерапії сприяє зменшенню вираженості больового синдрому приблизно у 80% хворих, понад 50% пацієнтів відзначають повне зникнення болю в ділянці опромінення вогнища метастатичного характеру. Крім того, ПТ дозволяє досягти консолідації (ремінералізації) патологічних переломів і є ефективним засобом боротьби з компресійним синдромом. Деякі автори рекомендують проведення курсів специфічної ад’ювантної поліхіміотерапії (ПХТ) у комплексному лікуванні метастатичних уражень кісток. Як хіміотерапію I-II лінії при лікуванні метастатичного РМЗ застосовують переважно чотири препарати: циклофосфамід, 5-фторурацил, метотрексат і доксорубіцин; при монохіміотерапії застосовують, як правило, тільки доксорубіцин. Основними схемами ПХТ I-II лінії при лікуванні метастазів РМЗ у кістки є такі: CMF (циклофосфамід, метотрексат, 5-фторурацил); CA (циклофосфамід, доксорубіцин); CAF (циклофосфамід, доксорубіцин, 5-фторурацил); CAMF (циклофосфамід, доксорубіцин, метотрексат, 5-фторурацил); CAP (циклофосфамід, доксорубіцин, цисплатин). Крім того, у схемах ПХТ застосовують гемцитабін, а також схеми з таксанами, в яких використовують доцетаксел або паклітаксел. Як ПХТ III-IV лінії застосовують мітоксантрон, мітоміцин, вінорельбін у комбінаціях: МММ (мітоміцин, мітоксантрон, метотрексат) або комбінації мітоміцина з вінорельбіном. При гормонозалежному РМЗ, у тому числі з метастатичним ураженням кісток, застосовують гормонотерапію: тамоксифен, летрозол, анастрозол, екземестан, фулвестрант.
Основним методом лікування метастазів РПЗ у кістки є гормонотерапія. Максимальна андрогенна блокада передбачає виконання хірургічної або хімічної кастрації у поєднанні із застосуванням антиандрогенів. Антиандрогени розрізняють за будовою і механізмом дії і поділяють на дві групи – нестероїдні та стероїдні. До нестероїдних антиандрогенів належать флутамід, нілутамід, бікалутамід, а до стероїдних – ципротерон і мегестрол ацетат. Упровадження в практику агоністів гонадотропін-рилізинг-гормона, таких як гозерелін, 3,6 мг 1 раз на 4 тиж, або гозерелін 10,8 мг 1 раз на 12 тиж, лейпрорелін 3,75 мг 1 раз на 4 тиж дозволило замінити хірургічну орхіектомію хімічною кастрацією. У випадках вичерпаних можливостей антиандрогенів можливе використання інгібіторів ароматази. Лікування за схемою максимальної андрогенної блокади практично ліквідувало терапію естрогенами: гексестрол, фосфестрол, хлортрианізен, поліестрадіол тощо. ПХТ малоефективна при метастазах РПЗ у кістки і переваг перед гормональною терапією немає, її використовують переважно при генералізованому процесі, при поєднанні з метастазами в інші органи і при низькодиференційованих формах. Найбільш часто застосовують схеми: CAF (циклофосфамід, доксорубіцин, 5-фторурацил); САР (циклофосфамід, доксорубіцин, цисплатин).
При метастазах дрібноклітинного раку легенів (ДКРЛ) найчастіше проводять хіміотерапію (ХТ) з широким поєднанням таких препаратів, як доксорубіцин, циклофосфамід, метотрексат, вінкристин, 5-фторурацил, етопозид, цисплатин тощо.
За останнє десятиріччя стандартом для лікування хворих із ДКРЛ стала комбінація ЕР або ЕС (етопозид з цисплатином або карбоплатином), яка замінила популярні раніше комбінації CAV (циклофосфамід, доксорубіцин, вінкристин), АСЕ (доксорубіцин, циклофосфамід, етопозид), САМ (циклофосфамід, доксорубіцин, метотрексат) та інші комбінації.
Доведено, що комбінації ЕР (етопозид, цисплатин) і ЕС (етопозид, карбоплатин) мають протипухлинну активність при поширеному ДКРЛ у 61-78% пацієнтів (повний ефект у 10-32% хворих). Медіана виживання становить від 7,3 до 11,1 місяця.
Розвиток хіміотерапії в останнє десятиріччя сприяв подвоєнню середньої тривалості життя пацієнтів із IV стадією НДКРЛ з 4 до 8-10 місяців, а також збільшенню майже втричі показника трирічної виживаності (з 11-14 до 32-37%). При НДКРЛ застосовують курси ПХТ із використанням схем на основі цисплатину (цисплатин і гемцитабін або доцетаксел і цисплатин). Як монохіміотерапію застосовують капецитабін.
Метастази раку нирки (РН) іноді зумовлюють перші клінічні прояви прихованого перебігу пухлини нирки. За наявності поодиноких віддалених метастазів лікування доцільно починати з видалення первинної пухлини, а тоді вирішувати питання про хірургічне або консервативне лікування метастазу залежно від його локалізації. Під час консервативного лікування найчастіше використовують локальну ПТ на тлі гормональних препаратів: антиестрогенів (тамоксифен), інгібіторів ароматази, прогестинів або кортикостероїдів. У разі поєднання кісткових і легеневих метастазів найбільшого поширення набуло лікування альфа-інтерфероном. Найчастіше ХТ (5-фторурацил) поєднують із ПТ на ділянку окремих метастатичних вогнищ із найбільшою больовою симптоматикою або загрозою переломів. Для таргетної терапії застосовують сорафеніб.
На сьогодні сучасна протипухлинна терапія онкологічних хворих має низку істотних недоліків, одним із яких є «емпіричний характер» її призначення, оскільки не існує «абсолютних» ознак чутливості/резистентності пухлини до цитостатиків. Призначення протипухлинної терапії базується на основних фенотипічних характеристиках пухлини і поширеності пухлинного процесу, ускладнюється відсутністю прямих прогностичних факторів ефективності та токсичності лікування.
Ще більшою є проблема лікування хворих у разі рецидивів хвороби і/або резистентності пухлин до протипухлинних агентів. При цьому часто рецидивні пухлини, які, як правило, метастазують, відрізняються від вихідної пухлини чутливістю до препаратів. В такому випадку застосовують конверсії одних схем ПХТ на інші, але досить часто і такі кроки не дають позитивних результатів або доводиться витрачати багато часу на підбір ефективних протипухлинних препаратів. Саме тому дослідження чутливості пухлинних клітин (із клінічного матеріалу) до різних класів протипухлинних препаратів і встановлення прямої цитотоксичної дії є надзвичайно актуальною темою як у фундаментальному, так і в практичному аспектах.
Таким чином, терапевтичні можливості лікування метастазів злоякісних пухлин у кістки за останні 10-15 років істотно зросли. Для метастазів пухлин, які мають ознаки гормональної чутливості, основною лікувальною ланкою є гормональна терапія. При кісткових метастазах пухлини без ознак гормональної чутливості, особливо з низьким ступенем диференціювання, або в поєднанні із метастазами в інші органи найбільш ефективною вважається системна ПХТ.
За останнє десятиріччя в клінічній практиці для лікування больового синдрому при метастатичних пухлинах почали використовувати деякі радіофармпрепарати (РФП), які є тропними до кісткової тканини. До них належать 89Sr-хлорид (стронція хлорид), 135Sm-оксабіфор (самарій), 186Re-ГЕДФК (гідроксиетилдифосфонова кислота) і деякі інші.
З-поміж перерахованих радіонуклідів найбільше застосування отримав 89Sr-хлорид. Цей радіонуклід є чистим бета-випромінювачем, і його можна застосовувати в амбулаторних умовах. Ефективність використання РФП доведена у хворих на РПЗ із метастазами в кістки.
За даними літератури, метастатичне ураження скелета є третьою за частотою локалізацією після метастатичного ураження легенів та печінки. Причому в скелеті ураження хребта злоякісними пухлинами зустрічається у 70% хворих, кісток таза і кінцівок – у 40%, ділянки кульшового суглоба – у 25% пацієнтів. Ризик виникнення патологічних переломів у довгих трубчастих кістках корелює зі ступенем деструкції кортикального шару. Перелом стає можливим у разі ураження кортикального шару більш ніж на 50%. Патологічні переломи, що потребують хірургічного лікування, зустрічаються у 9% хворих із метастазами в кістки.
У літературі повідомляється, що головними показаннями до хірургічного лікування метастатичного ураження кісток є солітарні метастази, явний больовий синдром, патологічний перелом або загроза його виникнення, але застосування тільки хірургічних методів лікування призводить до 45,6% рецидивів пухлини.
Хірургічне лікування, яке є паліативним методом у комбінованій терапії метастазів у кістки, відіграє важливу роль в адаптації хворих і полегшує їм проведення певних маніпуляцій. На цей час у світовій онкоортопедії хірургічні методи представлені ендопротезуванням, інтрамедулярним та накістковим остеосинтезом, кюретажем пухлини з використанням кісткового цементу, черезкістковим позавогнищевим остеосинтезом і стабілізуючими оперативними втручаннями на хребті.
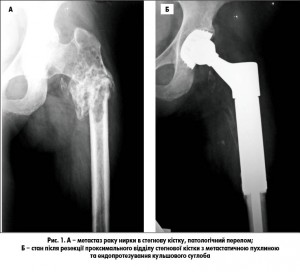
Ендопротезування суглобів практично завжди обґрунтовано і є методом вибору при метастатичному ураженні суглобових сегментів кістки, проте використання ендопротезів, що заміщують 2/3 або цілу кістку при ураженні діафізу кістки, доволі травматично й виправдано тільки при солітарних метастазах або первинних кісткових пухлинах, коли воно спрямоване на лікування хворого (рис. 1, А, Б).
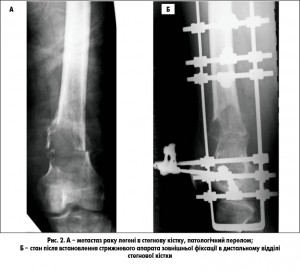
Черезкістковий остеосинтез (рис. 2, А, Б) характеризується тривалістю лікування, яке часто перевищує тривалість життя хворого з IV стадією онкологічного процесу, використанням об’ємних конструкцій, які обмежують амплітуду рухів у суглобах, високою ймовірністю розвитку запальних ускладнень – до 40,8% у попередньо ослаблених хворих, проте є ефективним при множинних ураженнях, коли відбувся патологічний перелом кістки. При використанні васкуляризованих аутотрансплантатів не завжди можливо замістити значні кісткові дефекти. Цей метод потребує виконання додаткового втручання, збільшується обсяг крововтрати, розширюється обсяг хірургічного втручання. При застосуванні васкуляризованих трансплантатів необхідне спеціальне обладнання і володіння мікрохірургічною технікою.
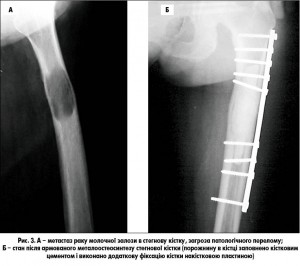
Спосіб алопластики також не вирішує проблеми заміщення великих дефектів кістки, що зумовлено високим відсотком розвитку ускладнень, тривалою функціональною реабілітацією хворих, особливо у випадках, коли необхідно виконувати великі резекції згідно з вимогами онкологічного радикалізму. З огляду на те, що більшість онкологічних хворих є ослабленими пацієнтами, можливість застосування малоінвазивних (кістковий цемент) методів лікування кісткових метастазів на сьогодні є актуальним питанням, але використання кісткового цементу при патологічних переломах довгих трубчастих кісток на тлі метастатичного характеру при великому ураженні кістки по довжині не завжди є достатнім. Цементна вставка при навантаженнях втрачає зв’язок із кісткою, що призводить до перелому, тому необхідний додатковий металоостеосинтез: накістковий або інтрамедулярний, що підсилює конструкцію і сприяє опороздатності та функції кінцівки, особливо при поодиноких метастазах і коли проведено передопераційне лікування (ПТ на вогнище ураження в кістці), а також отримано позитивну відповідь на застосування бісфосфонатів і ПХТ (рис. 3, А, Б).
В основі хірургічного лікування при метастатичному ураженні хребта лежать два види втручань: декомпресуючі і декомпресуючо-стабілізуючі операції. Суть декомпресуючої операції полягає у видаленні дужок уражених хребців, унаслідок чого відбувається декомпресія спинного мозку з подальшою фіксацією хребта жорстким або м’яким корсетом. Але більш ефективні декомпресуючо-стабілізуючі операції, при яких стабілізація хребта відбувається за рахунок фіксації заднього опорного комплексу за допомогою транспедикулярних фіксаторів типу Харрінгтона, USS (універсальна спінальна система) або переднього опорного комплексу за допомогою протезів тіл хребців, ауто- і алотрансплантатів, вуглецевих композитних імплантатів, пластин (CSLP – cervical spine locking plate, тораколюмбальної пластини). В літературі також повідомляється про застосування малоінвазивного методу пластики хребців за допомогою кісткового цементу. Проведення хірургічного лікування при метастатичному ураженні хребта дозволяє зменшити больовий синдром, ліквідувати компресію спинного мозку та зменшити неврологічні порушення, при хірургічних втручаннях на довгих трубчастих кістках у разі метастатичного ураження вдається поліпшити опороздатність та функцію кінцівки, поліпшити якість життя хворих і в найближчому післяопераційному періоді проводити додаткову специфічну терапію (ПХТ, гормонотерапію, бісфосфонати тощо). Все вищезазначене свідчить про те, що комплексне лікування метастатичних уражень кісток, яке включає хірургічне лікування, ПТ, ПХТ, гормонотерапію, імунотерапію, застосування бісфосфонатів та радіонуклідів має найбільший позитивний ефект лікування та сприяє поліпшенню якості життя хворого.