1 квітня, 2016
Хирургические аспекты лечения обструктивных заболеваний панкреатодуоденальной зоны. Методики оперативных вмешательств
Патологические образования панкреатодуоденальной зоны (ПДЗ) объединяет прогрессирующая обструкция панкреатического, общего желчного протоков и большого дуоденального сосочка (БДС) с развитием механической желтухи, реже – стеноз просвета двенадцатиперстной кишки (ДПК) с развитием дуоденальной непроходимости. Обструктивные патологические процессы включают злокачественные и доброкачественные заболевания, куда входят опухоли головки поджелудочной железы (ПЖ), БДС и периампулярной зоны, опухоли и стриктуры терминального отдела холедоха, хронический панкреатит (ХП) с преимущественным фиброзом, кальцинозом и кистами в области головки ПЖ.
При обструктивных заболеваниях ПДЗ выполняются радикальные, условно радикальные, паллиативные и симптоматические оперативные вмешательства. К радикальным оперативным вмешательствам относится панкреатодуоденальная резекция (ПДР), тотальная панкреатэктомия, к условно радикальным – трансдуоденальная папиллэктомия, парциальная панкреатодуоденальная резекция, к паллиативным – резекционные методики в объеме R1, R2, к симптоматическим – различные варианты билиодигестивных анастомозов, гастроэнтероанастомоз, направленные на купирование механической желтухи, дуоденальной непроходимости.
При предоперационной оценке степени резектабельности опухолевого процесса ПДЗ главными задачами являются: определение размеров опухоли ПДЗ, определение стадии опухолевого процесса, оценка взаимоотношения опухоли и магистральных сосудов.
Оценка края резекции необходима для определения полноты ПДР. Все резекции ПЖ следует классифицировать по резидуальному признаку (R): R0 – отсутствие в краях разреза макроскопических и микроскопических признаков заболевания; R1 – микроскопические признаки заболевания (микроскопически наличие опухолевых клеток в крае разреза); R2 – макроскопические признаки заболевания в крае резекции.
По рекомендации Европейской группы по изучению протоковой аденокарциномы железы (ESPAC), в зависимости от объема вмешательства R0-резекции при раке головки ПЖ подразделены на стандартную, радикальную, расширенную радикальную ПДР.
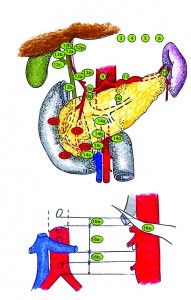
Japanese Pancreatic Society (JPS) в 1993 г. предложена подробная классификация групп абдоминальных лимфатических узлов, которая широко используется при стадировании рака ПЖ: правые паракардиальные лимфоузлы (1), левые паракардиальные лимфоузлы (2), малой кривизны желудка (3), большой кривизны желудка (4), привратниковые лимфоузлы (5), подпривратниковые лимфоузлы (6), левой желудочной артерии (7), общей печеночной артерии (8a, 8p); чревные лимфоузлы (9) – вокруг чревного ствола; лимфоузлы ворот селезенки (10); селезеночные лимфоузлы (11), лимфоузлы печеночно-двенадцатиперстной связки (12h, 12a1, 12a2, 12b1, 12b2, 12p1, 12p2, 12c); задние поджелудочно-двенадцатиперстные лимфоузлы (13a, 13b), верхние брыжеечные лимфоузлы (14a, 14b, 14c, 14d, 14v), средние ободочные лимфоузлы (15), парааортальные лимфоузлы (16a1, 16a2, 16b1, 16b2), передние поджелудочно-двенадцатиперстные лимфоузлы (17a, 17b), лимфоузлы нижнего края тела и хвоста поджелудочной железы (18). Объем лимфоаденэктомии при ПДР показан на рисунке 1.
Стандартная ПДР подразумевает выполнение регионарной лимфаденэктомии вокруг ДПК и ПЖ. Блоком резецируются лимфоузлы следующих групп:
– группы 12b1, 12b2, 12c – лимфатические узлы правой стороны гепатодуоденальной связки;
– группы 13a, 13b – задние поджелудочно-двенадцатиперстные лимфоузлы;
– группы 14a, 14b – лимфоузлы по правой стороне верхней брыжеечной артерии от устья этой артерии на аорте до устья нижней поджелудочно-двенадцатиперстной артерии;
– группы 17a, 17b – передние поджелудочно-двенадцатиперстные лимфоузлы.
Отдельно резецируются лимфоузлы группы 8a – передне-верхней зоны общей печеночной артерии.
Радикальная ПДР подразумевает выполнение регионарной лимфаденэктомии вокруг ДПК и ПЖ, скелетизацию общей печеночной артерии и верхней брыжеечной артерии (между ее устьем на аорте и нижней поджелудочно-двенадцатиперстной артерией), а также чревного ствола; иссечение фасции Герота и клетчатки между аортой и нижней полой веной. Блоком резецируются лимфоузлы, удаляемые при «стандартной» операции, а также лимфоузлы:
– группы 8 (8a, 8p) – общие печеночные и собственно печеночные лимфоузлы;
– группы 9 – лимфоузлы чревного ствола;
– группы 12 – все лимфоузлы левой и правой сторон гепатодуоденальной связки;
– группы 14 – циркулярная скелетизация верхней брыжеечной артерии между аортой и нижней поджелудочно-двенадцатиперстной артерией;
– группы 16a2, 16b1 – все лимфоузлы передне-боковой поверхности аорты и нижней полой вены, дополненные иссеченной фасцией Герота, расположенные между чревным стволом и нижней брыжеечной артерией.
Расширенная радикальная ПДР подразумевает выполнение лимфаденэктомии как при стандартной, так и радикальной операции с дополнительной лимфодиссекцией в области передней поверхности брюшной аорты между ее диафрагмальным отверстием и бифуркацией общих подвздошных артерий. Блоком резецируются лимфоузлы, удаляемые при стандартной и радикальной операции, а также лимфоузлы следующих групп: группы 16 (16a1, 16a2, 16b1, 16b2) – диссекция всей клетчатки и лимфатических сосудов, которая начинается справа на 3 см кнаружи от ДПК до средней трети левой почечной вены, и сверху – от нижней поверхности печени и диафрагмального отверстия аорты, вокруг чревного ствола и до бифуркации общих подвздошных артерий.
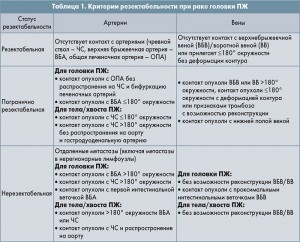
Критерии резектабельности при раке головки поджелудочной железы (NCCN Guidelines Version 2.2015 Pancreatic Adenocarcinoma) представлены в таблице 1.
ПДР относится к разряду наиболее сложных оперативных вмешательств, сопровождающихся большим числом послеоперационных осложнений.
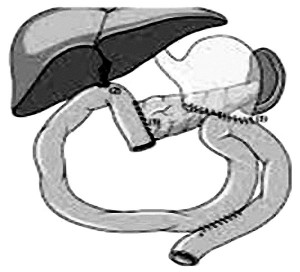
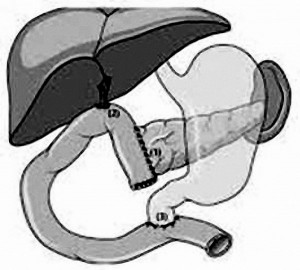
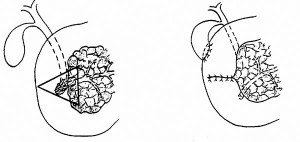
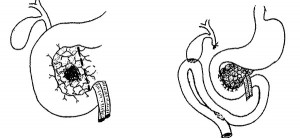
Наиболее распространенной методикой является ПДР по Kausch-Whipple (рис. 2). При локализации опухоли в области БДС, в терминальном отделе гепатохоледоха и крючковидном отростке головки ПЖ без поражения пилорических и верхних панкреатических лимфоузлов чаще выполняется пилоросохраняющая ПДР по Traverso-Longmire (рис. 3) [2, 3, 7].
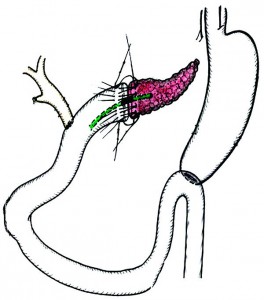
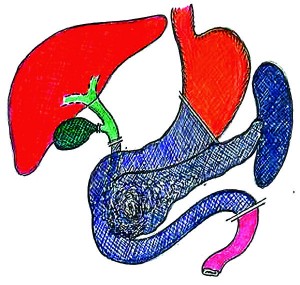
У нас в клинике применяются 3 варианта реконструктивного этапа ПДР: первый – с наложением панкреатоеюноанастомоза (ПЕА), билиодигестивного анастомоза, позадиободочного гастроэнтероанастомоза на одной петле тощей кишки с дополнительным выполнением энтероэнтероанастомоза (n=166), второй – с наложением ПЕА, билиодигестивного анастомоза, впередиободочного гастроэнтероанастомоза на одной петле тощей кишки без энтероэнтероанастомоза (n=45), третий – с наложением анастомозов на изолированных петлях тощей кишки (n=9) [1]. При мягкой, «сочной» ПЖ и высоком риске развития несостоятельности ПЕА применяется первый вариант методики (рис. 4).
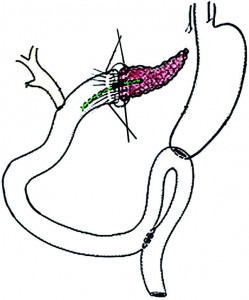 Рис. 4. Реконструктивный этап ПДР (ПЕА, холедохоеюноанастомоз, гастроэнтероанастомоз, энтероэнтероанастомоз)
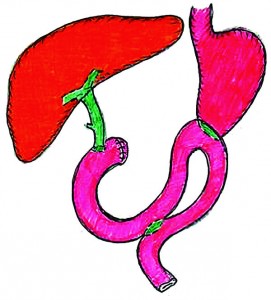
Рис. 4. Реконструктивный этап ПДР (ПЕА, холедохоеюноанастомоз, гастроэнтероанастомоз, энтероэнтероанастомоз)В последние годы чаще обращаемся к варианту реконструктивного этапа ПДР, при котором формируются ПЕА, гепатикоеюноанастомоз, впередиободочный гастроэнтероанастомоз на единой петле тощей кишки, при этом энтероэнтероанастомоз не выполняется (рис. 5).
Третий вариант реконструктивного этапа ПДР, разработанный на кафедре, заключается в наложении ПЕА, гепатикоеюноанастомоза и гастроэнтероанастомоза на изолированных петлях тощей кишки, что позволяет уменьшить риск их несостоятельности.
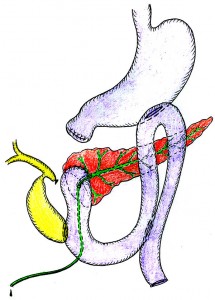
При выполнении реконструктивного этапа ПДР накладывался ПЕА с петлей тощей кишки, затем выполнялось пересечение тощей кишки на расстоянии 40-50 см от ПЕА с формированием гепатикоеюноанастомоза с межкишечным соустьем по Ру (на расстоянии 60 см от гепатикоеюноанастомоза). Затем накладывался гастроэнтероанастомоз (на расстоянии 30-40 см от межкишечного соустья) на петлю тощей кишки, идущей от гепатикоеюноанастомоза (патент України № 97936) (рис. 6).
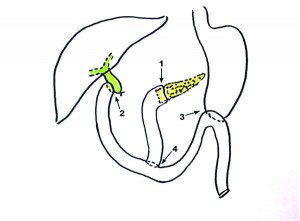 Рис. 6. Реконструктивный этап ПДР с изолированным наложением ПЕА, гепатикоеюноанастомоза и гастроэнтероанастомоза: 1 – ПЕА; 2 – гепатикоеюноанастомоз; 3 – гастроэнтероанастомоз; 4 – энтероэнтероанастомоз
Рис. 6. Реконструктивный этап ПДР с изолированным наложением ПЕА, гепатикоеюноанастомоза и гастроэнтероанастомоза: 1 – ПЕА; 2 – гепатикоеюноанастомоз; 3 – гастроэнтероанастомоз; 4 – энтероэнтероанастомозВ исследовании М. Hirota было высказано предположение, что пальпация периампулярной опухоли с целью ревизии, мобилизация ДПК по Кохеру и осуществление тракции за головку ПЖ по ходу мобилизации панкреатодуоденального комплекса повышает частоту появления метастазов в печени, и это подтолкнуло М. Hirota к разработке no-touch ПДР, главным отличием которой является выполнение мобилизации ДПК по Кохеру как завершающего этапа ПДР уже после полной перевязки всех артерий, вен, лимфатических протоков и пересечения связки крючковидного отростка.
В настоящее время применяется техника no-touch ПДР по Nagai, более широко известная в Японии как «Jichi method». Эта технология так же подразумевает отказ от мобилизации ДПК по Кохеру до полной перевязки всех артерий, вен, лимфатических протоков панкреатодуоденального комплекса и пересечения связки крючковидного отростка. Основным отличием Jichi method от методики, предложенной М. Hirota, является завершение операции не стандартной мобилизацией ДПК по Кохеру, а так называемой «реверсированной кохеризацией» – мобилизацией комплекса в направлении от верхних брыжеечных сосудов (слева направо) [4].
Совершенствование современных хирургических технологий и разумного онкологического подхода привело к внедрению лапароскопических технологий, роботохирургии в лечении опухолей панкреадодуоденальной зоны [5].
В нашей клинике выполнено 220 ПДР больным с обструктивными заболеваниями ПДЗ. Возраст больных варьировал от 31 до 76 лет. При раке головки ПЖ ПДР выполнена 179 (81,4%) больным, при раке БДС – 25 (11,4%), при раке дистального отдела холедоха – 6 (2,7%), при хроническом головчатом псевдотуморозном панкреатите – 10 (4,5%) пациентам.
Выбор варианта панкреатодигестивного анастомоза при ПДР. Ключевым моментом ПДР считается выбор оптимального способа обработки культи ПЖ и наложения панкреатодигестивного анастомоза, однако до сих пор нет методики, которая бы давала абсолютно надежный результат. В настоящее время используют различные методы включения культи ПЖ в пищеварительный тракт или наоборот, полного выключения ее из пищеварения: панкреатогастростомия, панкреатоеюностомия, наружное дренирование протока ПЖ, лигирование либо окклюзия протока. Выбор того или иного метода зависит от состояния культи ПЖ, ширины протока, а также от предпочтений оперирующего хирурга [1, 4, 7].
Наиболее распространенными являются две методики панкреадигестивного анастомоза: ПЕА и панкреатогастроанастомоз (ПГА). Преимуществом ПГА по сравнению с ПЕА некоторые авторы называют отсутствие напряжения линии швов при его выполнении и активации ферментов панкреатического секрета желудочным соком.
При выполнении разнообразных панкреатодигестивных анастомозов далеко не всегда удается избежать экстравазации панкреатического секрета, поступления в брюшную полость и забрюшинное пространство агрессивной смеси секрета с тонкокишечным содержимым, воздействия ее на окружающие ткани с последующим возникновением вторичных, нередко фатальных осложнений [2, 5].
Поэтому в качестве более безопасного способа обработки дистальной культи ПЖ при ее проксимальной резекции, позволяющего при правильном техническом выполнении предотвратить развитие панкреатогенного перитонита и парапанкреатита и одновременно сохранить функцию островкового аппарата оставшейся части железы, некоторыми авторами рассматривалось формирование наружного свища ее главного протока. При этом наложение панкреатикостомы дополняется наложением заднего ряда будущего ПЕА, который окончательно формируют спустя 4-5 мес, проводя панкреатикостомическую трубку в просвет ранее подшитой к железе кишечной петли через небольшой прокол в стенке последней и накладывая узловые швы на переднюю стенку соустья [6, 7].
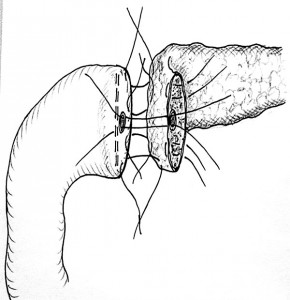
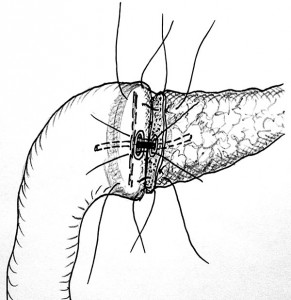
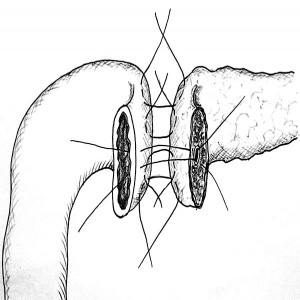
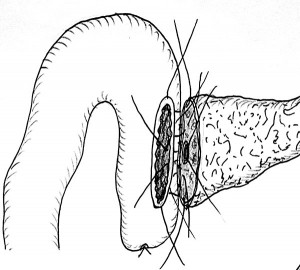
Выбор методики панкреатоеюноанастомоза. Выбор типа ПЕА при ПДР зависит, прежде всего, от размеров поперечника культи ПЖ и диаметра просвета тощей кишки, а также состояния паренхимы ПЖ и главного панкреатического протока. При соответствии этих параметров чаще всего накладывается «телескопический» ПЕА «конец в конец» (рис. 7), при несоответствии применяется погружной анастомоз «конец в бок» (рис. 8). При этом ПЕА выполняется как на внутреннем «скрытом» стенте, так и без него [1].
Панкреатоеюноанастомоз – «ахиллесова пята» реконструктивного этапа ПДР. Неблагоприятными факторами являлась мягкая, «сочная», жирная ПЖ, более благоприятными – фиброзно измененная, плотная, бугристая ПЖ. При оценке просвета главного панкреатического протока неблагоприятным фактором являлось наличие узкого, тонкостенного вирсунгового протока диаметром до 1-2 мм, более благоприятными факторами – средний (2-3 мм) и широкий панкреатический проток диаметром более 3 мм с утолщенной стенкой.
Телескопический инвагинационный дуктоеюнальный ПЕА (рис. 9-10) выполняется как с применением скрытого («потерянного») дренажа (длиной до 4,5-5,0 см с перфоративными отверстиями и диаметром 2-5 мм в зависимости от диаметра вирсунгового протока), так и без применения стента.
При мягкой, «сочной» железе применяется методика вшивания по всему периметру культи ПЖ внутренним непрерывным швом с обязательным раздельным захватом стенок главного панкреатического протока и наложением второго ряда погружных инвагинирующих швов без применения «потерянного» стента (рис. 11). Считаем ошибкой наложение ПЕА без дифференцировки главного протока ПЖ, даже если он очень узкий (менее 1 мм). Наиболее грубой ошибкой с тяжелыми последствиями является зашивание узкого протока при наложении швов по периметру среза ПЖ. При несоответствии (кишка уже культи) применялся погружной анастомоз «конец в бок» (рис. 12).
При мягкой, «сочной» ПЖ нами разработан способ, при котором накладывался прецизионный инвагинационный ПЕА на внутреннем стенте и обворачивающей пластикой линии анастомоза серповидной связкой печени. Серповидной связкой печени в виде манжеты обворочивается и фиксируется по периметру как задняя, так и передняя губа ПЕА, затем применяются инвагинирующие П-образные швы (патент Украины № 92410) (рис. 13).
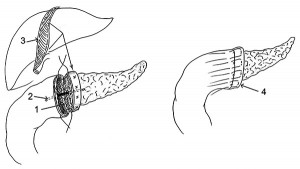 Рис. 13. Прецизионный ПЕА на внутреннем стенте с обворачивающей пластикой линии анастомоза серповидной связкой печени: 1 – линия ПЕА (задняя губа); 2 – внутренний стент; 3 – серповидная связка печени; 4 – п-образные швы по линии анастомоза.
Рис. 13. Прецизионный ПЕА на внутреннем стенте с обворачивающей пластикой линии анастомоза серповидной связкой печени: 1 – линия ПЕА (задняя губа); 2 – внутренний стент; 3 – серповидная связка печени; 4 – п-образные швы по линии анастомоза.Выбор методики билиодигестивного анастомоза при ПДР. Билиодигестивный анастомоз на реконструктивном этапе ПДР чаще выполняется в виде гепатикоеюноанастомоза, холедохоеюноанастомоза и реже накладывается холецистоеюноанастомоз. Кроме выбора варианта билиодигестивного анастомоза, имело важное значение определение расстояния между анастомозами, которое лимитировано расположением культи гепатохоледоха и культи ПЖ [1].
Использование желчного пузыря для наложения билиодигестивного соустья считаем нецелесообразной и в ряде случаев порочной методикой. Длительно существующий при такой методике замедленный желчеотток через пузырный проток и желчный пузырь приводит к формированию сладжей и конкрементов в желчном пузыре и печеночных протоках, приступам холангита, которые мы наблюдали у 3 больных, что и потребовало повторных операций с выполнением холецистэктомии, гепатиколитотомии, наложения гепатикоеюноанастомоза.
У большинства больных, как поступающих с признаками желчной гипертензии, так и без признаков желчной гипертензии, но с достаточной шириной гепатикохоледоха (более 7-8 мм), выполнялась холецистэктомия, наложение билиодигестивного анастомоза в объеме холедохоеюноанастомоза или гепатикоеюноанастомоза. Показаниями к выполнению холедохоеюноанастомоза явились наличие небольшой опухоли в области БСДК и головки ПЖ, отсутствие увеличенных лимфоузлов в области гепатодуоденальной связки, наличие псевдотуморозного головчатого панкреатита. Показаниями к выполнению гепатикоеюноанастомоза и более проксимальной резекции гепатикохоледоха явились: опухоли в области головки поджелудочной железы более 4 см, наличие опухоли дистального отдела холедоха [1].
Короткое расстояние между двумя прецизионными анастомозами приводит к высокому риску развития их несостоятельности, особенно в условиях послеоперационного пареза при одновременном выделении достаточно больших объемов панкреатического сока и желчи.
При мягкой, «сочной» ПЖ и большом риске развития послеоперационного панкреатита, частичной или полной несостоятельности ПЕА нами предложено «выпускать» более свободной петлю тонкой кишки длиной 15-17 см для наложения гепатикоеюноанастомоза ниже поворота ее в сторону брыжеечного «окна». Такой вариант расположения гепатикоеюноанастомоза создает лучшие условия для оттока желчи, снимая напряжение с начальной анастомотической петли кишечника в зоне панкреатоеюноанастомоза (рис. 14).
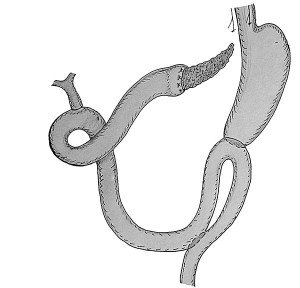 Рис. 14. Модифицированный вариант реконструктивного этапа ПДР с увеличением расстояния между ПЕА и гепатикоеюноанастомозом
Рис. 14. Модифицированный вариант реконструктивного этапа ПДР с увеличением расстояния между ПЕА и гепатикоеюноанастомозомВыбор метода резекции желудка при ПДР. Наиболее частые применяемые варианты резекции желудка при ПДР: резекция 1/2 желудка, антрумэктомия (гемиантрумэктомия) в сочетании с ваготомией, пилоросохраняющая ПДР.
Одним из наиболее частых осложнений ПДР является послеоперационный гастростаз, особенно после пилоросохраняющих ПДР. Причинами гастростаза после ПДР явились: «веретенообразная» деформация мобилизованного выходного отдела желудка при наложении гастроеюноанастомоза, любой перифокальный инфильтрат вследствие просачивания панкреатических ферментов в окружности ПЕА, затянувшийся выраженный парез культи желудка, особенно при одновременной ваготомии. В нашей клинике чаще применяется резекция 1/2 желудка или экономная резекция желудка в виде антрумэктомии с селективной ваготомией.
Профилактикой рефлюкса желчи в желудок является выполнение энтероэнтероанастомоза на реконструктивном этапе ПДР, при котором хорошо разгружается приводящая петля и создается хороший отток желчи и панкреатического сока в кишечник.
Для профилактики гастростаза и нарушения пассажа по приводящей петле на реконструктивном этапе ПДР наряду с ПЕА, билиодигестивным соустьем накладывается впередиободочный гастроэнтероанастомоз без межкишечного соустья. Такое расположение гастроэнтероанастомоза позволяет максимально удалить его от влияния возможного панкреатического инфильтрата, который может развиться из-за послеоперационного панкреатита культи ПЖ [1].
При пилоросохраняющей ПДР, перевязывая кровеносные сосуды при ПДР с сохранением привратника, хирург должен всегда помнить о многочисленных вариантах кровоснабжения ДПК для того, чтобы сохранить адекватное кровоснабжение ее культи и таким образом успешно сформировать анастомоз.
Тотальная панкреатэктомия. При распространении опухолевого процесса на перешеек и тело ПЖ, больших размерах опухоли показано выполнение тотальной панкреатэктомии. Показаниями для тотальной панкреатэктомии являются: мультифокальные локализации опухоли в железе, наличие опухолевой ткани в срезе железы при ПДР, нейроэндокринные опухоли; злокачественные муцинозные цистаденомы и внутрипротоковые папиллярно-муцинозные опухоли (IPMN) с тотальным поражением железы; рыхлый и «стеариновый» характер дистальной части железы (рис. 15-16).
Целесообразность выполнения панкреатэктомии при раке ПЖ:
– панкреатэктомия в сочетании с лимфодиссекцией является приоритетной с онкологической точки зрения;
– тенденция рака к мультицентрическому поражению железы и внутрипротоковому распространению опухоли;
– отсутствие необходимости в ПЕА, что уменьшает вероятность послеоперационных осложнений;
– наличие резидуальной опухоли в краях резекции или локальный рецидив рака после выполненной резекции.
Операция тотальной панкреатэктомии не сложнее ПДР при условии отсутствия инвазии в сосуды чревного ствола, так как не нуждается в наложении ПЕА, но, как правило, сопровождается спленэктомией. Объем панкреатэктомии включает удаление единым блоком большого сальника, ПЖ, ДПК, общего желчного протока, желчного пузыря, селезенки и части желудка [7, 9].
Одной из основных причин неудовлетворительных результатов панкреатэктомии является развитие в послеоперационном периоде инсулин-зависимого диабета.
Условно радикальные оперативные вмешательства. Выделяют различные варианты папиллэктомии БДС: трансдуоденальная типичная и расширенная папиллэктомия, а также эндоскопическая папиллэктомия. Эндоскопическая папиллэктомия выполняется с применением электрокоагуляции и электросварки с последующей установкой эндобилиарного стента [2, 6].
В нашей клинике применяется модифицированная методика расширенной трансдуоденальной папиллэктомии (ТДПЭ), которая выполняется при наличии или подозрении на опухолевую инвазию у основания БДС в стенку ДПК и близлежащие ткани головки ПЖ у пациентов с высоким операционным риском ПДР, высоким риском деструктивных, инфекционных и тромбоэмболических осложнений и сомнительной переносимостью более радикальной операции.
Методика расширенной ТДПЭ заключалась в более широком иссечении тканей ДПК у основания БДС с захватом до 1,5-2,0 см от БДС, иссечении прилежащих тканей головки ПЖ на глубину до 1,5-2,0 см с выделением интрапанкреатической части общего желчного протока (ОЖП) и главного панкреатического протока, пересечением и перевязкой ОЖП на уровне супрадуоденальной его части для более глубокого удаления прилежащей ткани головки ПЖ [1].
При небольших опухолях БДС и периампулярной зоны головки ПЖ выполняются методики парциальной панкреатодуоденальной резекции: по Н.С. Макохе (рис. 17), В.А. Михайличенко (рис. 18), по А.А. Шалимову, В.М. Копчак (рис. 19).
Нами разработана методика экономной парциальной верхнелокальной ПДР, которая позволяла более широко иссечь ткани ПЖ с верхним отделом нисходящей части ДПК. Затем последовательно перевязывался ОЖП, вшивался вирсунгов проток в нисходящую часть культи ДПК на стенте, выведенном наружу в виде микродуоденостомы, зашивалась наглухо культя верхней горизонтальной части ДПК, накладывался последовательно холедохоеюноанастомоз, гепатикоеюноанастомоз по Петерсону на длинной петле с энтероэнтероанастомозом по Брауну и выполнялась селективная ваготомия (рис. 20).
Таким образом, у больных пожилого и старческого возраста при раке БДС и периампулярной зоны головки ПЖ с выраженной сопутствующей патологией и высоким периоперационным риском выполнения ПДР трансдуоденальная расширенная папиллэктомия и парциальная резекция головки ПЖ являются операциями выбора [1].
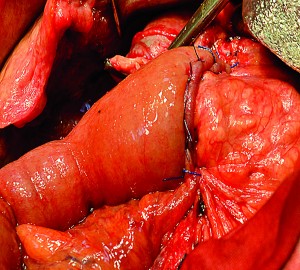
Сосудистые реконструкции при ПДР. Возможность выполнения радикальной ПДР при опухолях головки ПЖ нередко лимитирована местным распространением опухоли с инвазией в ВБВ, ВВ и селезеночную вены. Вовлечение перипанкреатических сосудов в опухолевый процесс – один из важнейших критериев, определяющих потенциальную резектабельность опухоли при раке ПЖ. При этом на успешность выполнения операции влияют опыт оперирующего хирурга и его умение выполнить адекватную реконструкцию венозных сосудов, которые резецируются и удаляются вместе с опухолью. ПДР с одновременным удалением участка ВБВ, ВВ позволяет выполнить радикальное оперативное вмешательство даже при IVа стадии рака с высокой частотой благоприятных исходов.
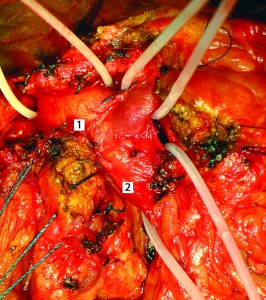 Рис. 21. Опухоль головки ПЖ прорастает воротную вену; воротная, верхнебрыжеечная, селезеночная вены взяты на турникеты (1 – зона прорастания опухолью воротной вены, 2 – воротная вена)
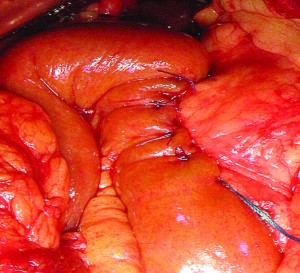
Рис. 21. Опухоль головки ПЖ прорастает воротную вену; воротная, верхнебрыжеечная, селезеночная вены взяты на турникеты (1 – зона прорастания опухолью воротной вены, 2 – воротная вена)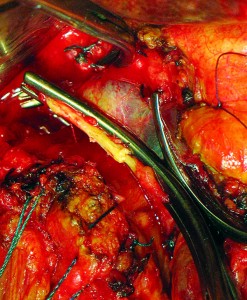 Рис. 22. Выполнена краевая резекция воротной вены (сосудистые зажимы на воротной вене, верхнебрыжеечной вене, селезеночной вене)
Рис. 22. Выполнена краевая резекция воротной вены (сосудистые зажимы на воротной вене, верхнебрыжеечной вене, селезеночной вене)Дополнительная к радикальной операции резекция вены повышает шансы выполнить R0-резекцию, существенно не влияя на число осложнений, летальность и выживаемость. В зависимости от степени инвазии опухоли в стенки крупных сосудов выполняется краевая резекция, циркулярная резекция с формированием анастомоза «конец в конец», протезирование синтетическим протезом, аутопротезирование большой подкожной веной [1, 3, 8].
При частичном краевом прорастании на небольшом протяжении ВВ и ВБВ, применяется линейная (тангенциальная) резекция вены, дефект в ее стенке продольно ушивается непрерывной атравматической нитью (5-0) (рис. 21-23).
В случаях, когда продольное ушивание может сопровождаться чрезмерным сужением ее просвета, дефект стенки вены устраняют путем вшивания «заплаты» из стенки другой аутовены, взятой у этого же пациента. После сегментарных резекций, если расхождение (диастаз) краев пересеченной вены не превышает 2,0-4,0 см, непрерывность сосуда восстанавливают путем сшивания его концов. При дефектах, имеющих большую протяженность, для восстановления кровотока в системе ВВ используются вставки из аутовены или сосудистые протезы.
Удлинение реконструктивного этапа восстановления кровотока в бассейне воротной вены за счет технической сложности выполнения сосудистых венозных анастомозов чревато развитием ряда осложнений, самыми грозными из которых являются острый тромбоз воротной вены и некроз печени.
В нашей клинике при инвазии опухоли головки ПЖ в крупные магистральные сосуды для выполнения ПДР R0 выполнено 10 (4,7%) больным сосудистые реконструкции: венозные резекции – 9 (4,2%), артериальная резекция – 1 (0,5%) больному. Выполнены следующие венозные резекции: резекция верхнебрыжеечной вены выполнена у 2 (22,2%), линейная (тангенциальная) резекция воротной вены – у 6 (66,7%), циркулярная резекция воротной вены – у 1 (11,1%) больного. При линейной резекции воротной вены протяженность составляла от 2,0 до 4,0 см, при циркулярной резекции воротной вены выполнен анастомоз «конец в конец». У 1 больного была произведена ПДР с резекцией участка верхнебрыжеечной артерии и восстановлением кровотока путем анастомоза «конец в конец».
При выполнени ПДР с лимфодиссекцией применялись современные методы электрокоагуляции: аппарат Патона с режимами рассечения, коагуляции, сварки (ЕК 300М1), аппарат LigaSure.
Таким образом, радикальным оперативным вмешательством в лечении обструктивных заболеваний ПДЗ опухолевого генеза является ПДР, в то же время при прорастании опухолью магистральных сосудов показано выполнение R0-резекции и сосудистой реконструкции.
У больных пожилого и старческого возраста при раке БДС и периампулярной зоны головки ПЖ с выраженной сопутствующей патологией и при высоком периоперационном риске выполнения ПДР трансдуоденальная расширенная папиллэктомия и парциальная резекция головки ПЖ являются операциями выбора.