28 листопада, 2016
Можливості відеоторакоскопічного видалення новоутворень середостіння на прикладі клінічного випадку
Пухлини середостіння є одним із найбільш складних розділів у торакальній хірургії та онкології. Незважаючи на те що пухлини середостіння трапляються рідко (близько 3-7% у структурі пухлинних захворювань грудної клітки), вони продовжують залишатися цікавою діагностичною і терапевтичною проблемою для торакальних хірургів (О.М. Білий, 2004; Akshatha Rao Aroor, 2014). Актуальність проблеми зумовлена тим, що ембріо- та гістогенетична різноманітність пухлин середостіння, їх топографо-анатомічні особливості, своєрідність клінічної картини ускладнюють діагностику й уточнення нозологічної належності патологічних процесів цієї ділянки (З.О. Мачаладзе, 2008; S. Juanpere et al., 2013).
Дані щодо співвідношення добро- та злоякісних новоутворень неоднозначні. Так, за даними M. Vaziri та співавт. (2009), Akshatha Rao Aroor та співавт. (2014), злоякісні пухлини середостіння більш поширені, ніж доброякісні, і становлять 60 і 68,57% випадків відповідно, тоді як у більш ранніх повідомленнях ця частота фіксувалась на рівні 25-49% (K.S. Azarow et al., 1993; M. Wongsangiem et al., 1996). Щодо більшої поширеності доброякісних пухлин зазначалося у дослідженнях, проведених R.D. Davis і співавт. (1987) та V.O. Adegboye і співавт. (2003), – 58 і 57% відповідно.
За останні десятиліття спостерігається збільшення кількості пухлин середостіння майже вдвічі, переважно за рахунок зростання кількості лімфатичних пухлин (В.С. Шавлохов, 2009; N. Pearce та співавт., 2005).
У лікуванні пухлин середостіння тривалий час застосовували і застосовують дотепер стандартні методи оперативних втручань, які проводять через стернотомічний чи торакотомічний доступи. Вони вважаються досить травматичними й супроводжуються значною кількістю післяопераційних ускладнень, що пов’язано з топографо-анатомічними особливостями переднього середостіння. На сьогодні в лікуванні середостіння дедалі більшої популярності набуває мініінвазивний метод відеоторакоскопічної хірургії, який за підсумками численних досліджень був визнаний ефективною діагностичною і терапевтичною альтернативою (L.M. Cirino et al., 2000; R.D. Shah, T.A. D’Amico, 2014; Gonzalez-Rivas, 2016). Торакоскопія (особливо відеоторакоскопія) дає змогу детально візуалізувати медіастінальну пухлину, визначити її поширеність, зв’язок з оточуючими органами і тканинами, виконати прицільну біопсію її різних відділів і встановити морфологічний діагноз у понад 90,0% досліджень (Т.Н. Борисова и др., 2014).
Засновником торакоскопії як ендоскопії внутрішньої порожнини грудної клітки вважають H.C. Jacobaeus, який у 1910 році використав модифікований цитоскоп для зменшення спайок у плевральній порожнині та колапсу легені при туберкульозі. Два важливих наукових прориви наступних десятиліть дали змогу покращити хірургічну техніку. Перший – запровадження у 1960-ті роки окремої вентиляції легень, що дало змогу проводити процедури з невентильованою легенею, і другий – використання відеокамери до хірургічної оптики, що забезпечило передачу зображення на екран телевізора у збільшеному вигляді. Відтоді в торакальній хірургії за кордоном почали використовувати абревіатуру VATS (video-assisted thoracoscopic surgery) і ВТСХ (відеоторакоскопічна хірургія) – у нашій країні (J.B. Brodsky та співавт., 2000; J. Deslauriers та співавт., 2002).
Спершу, в період між 1992 і 2002 роками, показаннями до VATS були діагностичні процедури (плевроскопія, медіастеноскопія, біопсія легень, плевральна біопсія, медіастенальна біопсія) і малі торако-хірургічні процедури (симпатектомія, пневмоторакальна хірургія, Nuss-хірургія). З 2002 року техніку VATS широко використовують не лише для діагностики середостіння, легень і плевральних захворювань, а й для виконання великих торакальних хірургічних процедур, таких як резекція стравоходу або всієї легені (лобектомія, пневмонектомія, езофагектомія, тімектомія).
Розвиток мініінвазивної хірургії сприяв тому, що в країнах західної Європи та США почала зростати кількість мініінвазивних втручань: за даними різних авторів, кількість відеоторакоскопічних операцій сягнула 25-30% серед хворих, що потрапляють у торакальні відділення (D.M. Hansell et al., 2009; R.D. Shah et al., 2014).
Відеоторакоскопічні втручання дозволяють досягти майже 100% верифікації діагнозу в пацієнтів з пухлинами середостіння (L.M. Cirino et al., 2000), а кількість післяопераційних ускладнень під час використання відеоторакоскопії становить усього 2,7-4% (M.P. Lochowski, J. Kozak, 2014). Ускладнення після VATS можуть статися під час операції і, як правило, пов’язані з основним захворюванням, тоді як ускладнення в післяопераційному періоді найчастіше пов’язані із самим методом (J. LoCicero, 1993). Ускладнення процедур VATS можуть відбуватися зі змінною частотою при різних захворюваннях. Найбільш частим ускладненням є тривалий післяопераційний витік повітря. Іншими значними ускладненнями є кровотечі, інфекції, післяопераційні болі та рецидиви. Найбільш важливими факторами ризику тривалого витоку повітря є емфізема, пневмоторакс, вік старше 70 років, чоловіча стать і обсяг форсованого видиху за 1 с (ОФВ1) <70% (A. Brunelli et al., 2004). До факторів ризику інфекції після процедури VATS належать наявність пухлини, пригнічення імунітету, наявність інфекції до початку лікування VATS, тривале перебування в стаціонарі до операції, наявність центрального катетера (D.N. Nan et al., 2011), а також хронічні обструктивні захворювання легень і ОФВ1 <70% (A. Imperatori et al., 2008). Рецидив є ускладненням, що строго пов’язаний із хірургічною технікою. Ризик виникнення цього ускладнення збільшується при лікуванні мезотеліоми, метастазів саркоми або меланоми та злоякісного плеврального випоту у VATS. Використання коагуляції рани знижує ризик розвитку цього ускладнення (K. Parekh et al., 2001).
Відповідно до класифікації D. Dindo, N. Demartines, P.A. Clavien (2004) ускладнення поділяють на 5 категорій. Перші дві категорії включають незначні ускладнення: I – не становлять небезпеки для життя, не потребують лікування і не подовжують тривалість госпіталізації у середньому більш ніж удвічі, II – потенційно небезпечні для життя, потребують лікарської терапії, парентерального харчування або переливання. У III категорії – пацієнти з небезпечними для життя ускладненнями, потребують госпіталізації, діагностичних ендоскопічних процедур або повторної операції. До IV категорії належать серйозні загрозливі для життя ускладнення із залишковою або тривалою непрацездатністю. V категорія – смерть пацієнта.
Зазначимо, що, незважаючи на велику кількість типів ускладнень, вони зустрічаються рідко і їх можна уникнути за рахунок правильного підбору пацієнтів і володіння відповідною хірургічною технікою (M.P. Lochowski, J. Kozak, 2014).
Розвиток мініінвазивних хірургічних втручань сприяв застосуванню VATS при таких розладах, як грудні пухлини середостіння і рак стравоходу.
У разі патології середостіння VATS найчастіше застосовують до нейрогенних пухлин, лімфатичних вузлів і пухлин переднього середостіння. Діагностичні процедури зазвичай здійснюють, коли інші діагностичні методи є негативними. Ускладнення після цих процедур є рідкісними. Привертає увагу лімфорея, яка трапляється в 1% випадків після процедур VATS у середостінні. Близько 50% випадків лімфореї можуть бути припинені шляхом застосування консервативного лікування: дренування плевральної порожнини та використання дієти з низьким умістом тригліцеридів (A. Imperatori et al., 2008). Якщо таке лікування виявиться неефективним, тактикою вибору є перев’язка грудної протоки через праву плевру. Лікування можливе з використанням техніки VATS (A. Watanabe et al., 2007).
Як зазначають M.R. Asgary та співавт. (2014), серед пацієнтів з пухлиною середостіння незначно переважають чоловіки (56,4%), більшість із них перебувають між третьою і п’ятою декадами життя. Зазначені автори виявили неходжкінську лімфому у 30,7%, тімому – у 13,8% і лімфому Ходжкіна – у 12,9% випадків. 78,2% пухлин локалізувались у передньому середостінні, а далі в порядку зменшення частоти – в задньому і середньому середостінні. Дослідження показало, що лімфома і тімома були більш поширені в передньому середостінні, а нейрогенні пухлини – в задньому середостінні. Найбільш поширеними в порядку зменшення частоти симптомами були кашель, задишка і лихоманка (M.R. Asgary et al., 2014).
Вищенаведені дані свідчать про те, що застосування відеоторакоскопічних втручань є актуальним вирішенням питань більш ефективного та безпечного лікування, а також діагностики захворювань середостіння.
Клінічний випадок
Пацієнтка А., 1966 р.н., госпіталізована у НІХТ ім. О.О. Шалімова зі скаргами на дискомфорт за грудиною, відчуттям нестачі повітря. З анамнезу відомо, що в 2014 році пацієнтка скаржилася на болі в грудному та шийному відділі хребта, у зв’язку з чим їй було виконано МРТ-дослідження грудного та шийного відділу хребта, під час якого і було діагностовано новоутворення середостіння. В умовах клініки хворій проведено обстеження.
Загальний аналіз крові: еритроцити – 4,98×1012/л, гемоглобін – 135 г/л, кольоровий показник – 0,8, лейкоцити – 4,5×109/л, тромбоцити – 139×109/л, ШОЭ – 6 мм/год.
Біохімічний аналіз крові: загальний білок – 78,7 г/л, загальний білірубін – 8,1 мкмоль/л, прямий білірубін – 2,1 мкмоль/л, аланінамінотрансфераза – 19 мОд/л, аспартатамінотрансфераза – 23 мОд/л, a-амілаза – 49 мОд/л, сечовина – 4,0 ммоль/л, креатинін – 68,6 мкмоль/л, глюкоза – 6,7 ммоль/л.
Коагулограма: протромбіновий час – 11,0 с, протромбіновий індекс – 95%, міжнародне нормалізоване співвідношення – 1,0; фібриноген – 4,4 г/л.
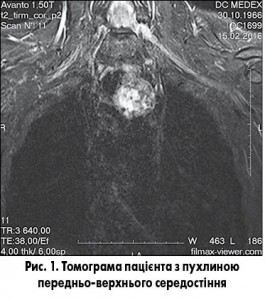
МРТ: Загрудинно на рівні верхнього середостіння візуалізується об’ємний утвір гетерогенної структури, що неоднорідно накопичує гадолінієвий агент та має у своїй структурі включення гіперінтенсивного МР-сигналу на T1WI (кальцинати?), розміри 37,7×31,6×36,4 мм. Утвір розташований ліворуч від трахеї, дислокуючи її, і прилягає до дуги аорти (рис. 1).
Прийнято рішення про виконання відеоторакоскопічного видалення пухлини передньо-верхнього середостіння.
Хід операції. Виконано інтубацію трахеї двопросвітною інтубаційною трубкою 35F. Розпочато однолегеневу вентиляцію. У грудну клітку зліва введено 4 троакари: у VIII міжребер’я – 15 мм, у VII міжребер’я – 10 мм, у V міжребер’я – 5 мм, у IV міжребер’я – 5 мм. Під час ревізії явної органічної патології в лівій половині грудної клітки не виявлено. Після розтину медіастинальної плеври нижче рівня діафрагмального нерва, вище дуги аорти виявлено щільно-еластичне пухлиноподібне утворення до 4 см у діаметрі в капсулі, розташоване на судинах дуги аорти (лівої підключичної і лівої загальної сонної артерій). Тупим шляхом і за допомогою ультразвукового скальпеля Harmonic утворення мобілізовано і видалено в єдиному блоці з капсулою. Контроль гемостазу по ходу операції – сухо. Пухлина видалена з грудної порожнини в контейнері. Дренування плевральної порожнини зліва. Легеня розправилась. Пошарові шви ран. Асептичні пов’язки. Одразу після оперативного втручання оглянули препарат макроскопічно (рис. 2, А, Б).
Патогістологічний висновок: ектопія тканин щитоподібної залози з ознаками макро- та мікрофолікулярного колоїдного зобу.
Післяопераційний період протікав відповідно до обсягу оперативного втручання. На 4-ту добу після операції пацієнтку було виписано в задовільному стані.
Висновки та перспективи подальших розробок
Відеоторакоскопічне видалення новоутворень середостіння – безпечний та ефективний метод лікування хворих такого контингенту, що дає змогу скоротити перебування пацієнта в стаціонарі й зменшити кількість післяопераційних ускладнень після торакальних оперативних втручань.
Прагнення спеціалістів – науковців і практиків – розширити показання відеоторакоскопічного методу й обґрунтувати доцільність його застосування в різних розділах торакальної хірургії зумовлене зростанням популярності мініінвазивної хірургії у зв’язку зі значно меншою його травматичністю порівняно із загальноприйнятою торакотомією, яка нерідко перевищує сам етап видалення пухлини.
Література
- Білий О.М. Оптимізація діагностики та лікування пухлин середостіння, що зустрічаються найчастіше: автореф. дис. на здобуття наук. ступеня к.мед.н.: спец. 14.01.07 «Онкологія» / О.М. Білий. – Донецьк, 2004. – 20 с. 2.
- Клинические рекомендации по диагностике и лечению больных опухолями средостения и вилочковой железы [Электронный ресурс] / [Борисова Т.Н., Бредер В.В., Горбунова В.А. и др.]. – Москва, 2014. – 64 с. – Режим доступа: http://www.oncology.ru/association/clinical-guidelines/2014/48.pdf.
- Мачаладзе З.О. Опухоли средостения (дифференциальная диагностика и лечение): автореф. дис. на соискание уч. степени д-ра мед. наук: спец. 14.00.14 «Онкология» / З.О. Мачаладзе. – М., 2008. – 51 с. 4.
- Шавлохов В.С. Хирургические вмешательства в диагностике и терапии лимфатических опухолей средостения и легких: автореф. дис. на соискание уч. степени д-ра мед.наук: спец. 14.00.29 «Гематология и переливание крови», 14.00.27 «Хирургия» / В.С. Шавлохов. – Москва, 2009. – 40 с. 5.
- A diagnostic approach to the mediastinal masses / Sergi Juanpere, Noemі Canete, Pedro Ortuno [et al.] // Insights Imaging. – 2013. – Vol. 4 (1). – P. 29-52.
- A Study of Clinical Characteristicsof Mediastinal Mass / Akshatha Rao Aroor, Rama Prakasha S., Shubha Seshadri [et al.] // J. Clin. Diagn. Res. – 2014. – Vol. 8 (2). – P. 77-80.
- Brodsky J.B. Video-assisted thoracic surgery / J.B. Brodsky, E. Cohen // Curr. Opin. Anaesthesiol. – 2000. – Vol. 13. – P. 41-5.
- Davis R.D. Primary cysts and neoplasms of the mediastinum: recent changes in clinical presentation, methods of diagnosis, management, and results / R.D. Davis, H.N. Oldham, D.C. Sabiston // Ann. Thorac. Surg. – 1987. – Vol. 44. – P. 229-37.
- Deslauriers J. Thoracoscopy for diagnosis and staging. Pearson’s thoracic & esophageal surgery / J. Deslauriers, C. Sirois. – Philadelfia: Churchill Livingstone, 2002. – P. 103-15.
- Diagnosis and treatment of mediastinal tumors by thoracoscopy / L.M. Cirino, J.R. Milanez de Campos, A. Fernandez [et al.] // Chest. – 2000. – Vol. 117 (6). – P. 1787-92.
- Diagnosis and Treatment of Mediastinal Tumors by Thoracoscopy / Luіs Marcelo Inaco Cirino, Josе Ribas Milanez de Campos, Angelo Fernandez [et al.] // Chest. – 2000. – Vol. 117, Issue 6. – P. 1787-1792.
- Dindo D. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey / D. Dindo, N. Demartines, P.A. Clavien // Ann. Surg. – 2004. – Vol. 240. – P. 205-13.
- Epidemiology of Mediastinal Tumors during Six Years (2006-2012) in Rasht City / M.R. Asgary, M. Aghajanzadeh, H. Hemmati, M. Jafari // Emergencias. – 2014. – Vol. 2. – P. 88-94.
- Imaging of Diseases of the Chest / D.M. Hansell, D.A. Lynch, H. Page McAdams, A.A. Bankier [5th edition]. – 2009. – 1208 p.
- Lochowsk M.P. Video-assisted thoracic surgery complications / M.P. Lochowski, J. Kozak / Wideochir. Inne Tech. Maloinwazyjne. – 2014. – Vol. 9 (4). – P. 495-500.
- Lochowski M.P. Video-assisted thoracic surgery complications / M.P. Lochowski, J. Kozak // Wideochir. Inne Tech. Maloinwazyjne. – 2014. – Vol. 9 (4). – P. 495-500.
- LoCicero J. 3rd credentialing issues and complications of video-assisted thoracic surgery / J. LoCicero // Semin. Thorac. Cardiovasc. Surg. –1993. – Vol. 5. – P. 303-4.
- Nosocomial infection following video-assisted thoracoscopic surgery / D.N. Nan, M. Fernаndez-Ayala, C. Farinas-Alvarez [et al.] // Rev. Esp. Quimioter. – 2011. – Vol. 24. – P. 217-22.
- Pearce N. Agricultural exposures and non-Hodgkin’s lymphoma / N. Pearce, D. McLean // Scand. J. Work Environ. Health. – 2005. – Vol. 31 (Suppl 1). – P. 18-25.
- Peri-operative complications of video-assisted thoracoscopic surgery / A. Imperatori, N. Rotolo, M. Gatti [et al.] // Int. J. Surg. – 2008. – Vol. 6 (suppl 1). – S. 78-81.
- Predictors of prolonged air leak after pulmonary lobectomy / A. Brunelli, M. Monteverde, A. Borri [et al.] // Ann. Thorac. Surg. – 2004. – Vol. 77. – P. 1205-10.
- Presentation of primary mediastinal masses in Ibadan / V.O. Adegboye, A.O. Ogunseyinde, M.O. Obajimi [et al.] // East African Medical. Journal. – 2003. – Vol. 80. – P. 484-7.
- Primary mediastinal masses. A comparison of pediatric populations / Azarow K.S., Pearl R.H., Zurcher R. [et al.] // J. Thorac. Cardiovasc. Surg. – 1993. – Vol. 106. – P. 6772.
- Shah R.D. Modern impact of video assisted thoracic surgery / R.D. Shah, T.A. D’Amico / J. Thorac. Dis. – 2014. – Vol. 6 (Suppl 6). – S. 631-636.
- Shah R.D. Modern impact of video assisted thoracic surgery / R.D. Shah, T.A. D’Amico // J. Thorac. Dis. – 2014. – Vol. 6 (Suppl 6). – S. 631-6. doi: 10.3978/j.issn.2072-1439.2014.08.02.
- Supradiaphragmatic thoracic duct clipping for chylothorax through left-sided video-assisted thoracoscopic surgery / A. Watanabe, T. Koyanagi, S. Nakashima, T. Higami // Eur. J. Surg. – 2007. – Vol. 31. – P. 313-4.
- Uniportal thoracoscopic surgery: from medical thoracoscopy to non-intubated uniportal video-assisted major pulmonary resections / Diego Gonzalez-Rivas // Annals of Cardiothoracic Surgery. – 2016. – Vol. 5 (2). – P. 85-91.
- VATS port site recurrence: a technique dependent problem / K. Parekh, V. Rusch, M. Bains [et al.] // Ann. Surg. Oncol. – 2001. – Vol. 8. – P. 175-8. VATS port site recurrence: a technique dependent problem / K. Parekh, V. Rusch, M. Bains [et al.] // Ann. Surg. Oncol. – 2001. – Vol. 8. – P. 175-8.
- Vaziri M. Mediastinal masses: Review of 105 cases / M. Vaziri, A. Pazooki, L. Zahedi-Shoolami // Acta Medica Iranica. – 2009. – Vol. 47. – P. 297-300.
- Wongsangiem M. Primary tumours of the mediastinum: 190 cases analysis (1975-1995) / M. Wongsangiem, A. Tangthangtham // J. Med. Assoc. Thai. – 1996. – Vol. 79. – P. 689-97.