28 листопада, 2016
Современная концепция этиопатогенеза язвенной болезни и хирургические методы лечения осложненных гастродуоденальных язв

Проблему совершенствования хирургических методов лечения осложненной язвенной болезни (ЯБ) двенадцатиперстной кишки (ДПК) и желудка нельзя рассматривать в отрыве от научных достижений последних десятилетий в этиопатогенезе и консервативном лечении ЯБ. Австралийскими учеными B.J. Marchall и J.R. Warren была сформулирована новая бактериальная теория этиопатогенеза ЯБ, за которую в 2005 г. они были награждены Нобелевской премией, а Helicobacter pylori (H. pylori) безоговорочно признан основным фактором риска в возникновении этого заболевания.
Известный с 1910 г. классический постулат австрийского хирурга K. Schwartzа «нет кислоты – нет язвы» был дополнен другим постулатом знаменитого американского хирурга-гастроэнтеролога D.Y. Graham – «нет H. рylori – нет язвы» [41]. Однако позднее стало появляться все больше работ о так называемой H. рylori-негативной ЯБ. Было доказано, что в 25-30% случаев имеет место ЯБ, при которой H. pylori не выявляется [18, 32].
Появился новый постулат: «нет H. рylori – нет H. рylori-ассоциированной ЯБ» [49]. Установлено, что хеликобактерная инфекция широко распространена во всем мире: до 60% населения планеты инфицированы H. рylori начиная с детского возраста. Путь передачи – фекально-оральный, особенно при диарее, орально-оральный и эндоскопический. Бессимптомными бактерионосителями являются 70% зараженных H. рylori, и лишь 12-15% инфицированных страдают ЯБ. В неблагоприятных условиях происходит трансформация спиралевидных (вегетативных) форм H. рylori в кокковидные с резким снижением обмена веществ и репродуктивной способности, но с сохранением потенциальной реверсии.
В большинстве случаев H. рylori является «комменсалом» (от франц. commensal – «сотрапезник») и частью микробиоценоза желудка человека, комфортно существуя тысячелетиями в своей экологической нише и не причиняя никакого вреда [27, 28, 31]. В определенных условиях, особенно на фоне антибиотикотерапии, эти «комменсалы» начинают выступать в роли патогенов. Следование стратегии «test and treat», подкрепленной лозунгом «хороший H. рylori – только мертвый H. рylori», приводило во многих случаях к мутациям и трансформации H. рylori в патоген с цитотоксическими свойствами.
К настоящему времени стало известно, что в процессе эволюции H. рylori появляются «островки патогенности» (РАI), в которых находятся гены цитотоксичности: Cag A, Vac A, Ice A и Bab A, способные вызывать патологические изменения в слизистой желудка [42].
Одновременно с этим практически всеми специалистами признается роль кислотно-пептического фактора – второго важнейшего агрессивного предиктора в возникновении ЯБ. В разработку вопросов патогенетической роли кислотно-пептического фактора, нейрогуморальной регуляции желудочной секреции и обоснования применения ваготомии большой вклад внесли работы А.А. Шалимова, В.Ф. Саенко, А.С. Лаврика, Б.С. Полинкевича, В.Т. Зайцева, П.Д. Фомина, В.В. Бойко, С.Д. Гройсмана и других авторов [14, 17, 21, 24, 26, 29].
На последнем Всеукраинском съезде гастроэнтерологов была озвучена принятая за рубежом современная гипотеза этиопатогенеза ЯБ: «нет цитотоксических штаммов H. рylori и кислоты – нет язвы» (О.Я. Бабак, Г.Д. Фадеенко, С.М. Ткач). Однако при наличии цитотоксических штаммов и высокой кислотности не всегда возникает ЯБ.
В 1990-е годы сотрудники нашей клиники (И.Б. Брикульский, К.М. Курбанов, К. Шамун) провели исследование иммунного статуса тканей желудка и ДПК [1, 19, 20]. Иммуноферментным и гистохимическим методами исследовано содержание секреторных иммуноглобулинов А, G и E. Было доказано наличие местной иммунной системы желудка и обнаружено отклонение от нормы всех показателей в зоне язвенного поражения. По материалам этих работ нами сделаны следующие выводы:
- желудок – первый секреторный орган желудочно-кишечного тракта, встречающий внешнюю агрессивную среду в виде поступающих в организм нестерильных, наполненных чужеродными белками и различными химическими соединениями пищевых продуктов;
- желудок имеет свой местный защитный механизм в виде локальной иммунной системы, являющейся частью общей иммунной системы организма, которая в силу различных причин может оказаться ослабленной и не способной к самозащите, тогда желудочная микрофлора, в первую очередь H. рylori, проявляет себя как патоген.
Фундаментальные работы последних лет убедительно продемонстрировали, что цитотоксические штаммы H. рylori проявляют себя лишь в случае снижения иммунного статуса [27-28, 34-35].
В настоящее время выделены 3 основных фенотипа заболеваний, вызываемых H. рylori: І – простой (доброкачественный) гастрит (75-80%); II – дуоденальная язва (15%); III – рак желудка (1-2%). I и II фенотипы перекликаются с забытой воспалительной гастритической теорией J. Konyetzni (1925), а III – характеризуется мультифокальной атрофией слизистой, гипо- и ахлоргидрией и часто переходит в онкопроцесс [45]. Примечательно, что больные с язвой ДПК (по II фенотипу) фактически защищены от развития рака желудка.
В работах последнего десятилетия уделяется большое внимание роли генетических факторов человека при болезнях, вызванных H. рylori. Люди с группой крови 0(I), генотипами IL-1β Т31C и 2/2 IL1RN с высоким содержанием ФНО подвержены более высокому риску развития гипохлоргидрии и атрофии желудка в ответ на инфицирование H. рylori. Эти генотипы повышают риск кишечной и диффузной форм рака желудка, но не кардиального отдела, не эзофагеальной аденокарциномы и не эзофагеального плоскоклеточного рака [35-38].
На основании сказанного нами предлагается следующий постулат этиопатогенеза ЯБ: «без цитотоксических штаммов H. рylori, кислоты и снижения иммунитета – нет язвы».
При этом также следует учитывать индивидуальную генетическую предрасположенность.
Остаются не полностью раскрытыми механизмы образования H. рylori-негативных язв. При этом, по данным разных источников (С.М. Ткач, 2012; О.Я. Бабак и Г.Д. Фадеенко, 2014), следует выделять 2 группы H. рylori-негативных язвенных поражений: 1 – нестероидные противовоспалительные препараты (НПВП) и ацетилсалициловая кислота (АСК) – индуцированные язвы; 2 – идиопатические H. рylori-негативные язвы (механизм патогенеза не раскрыт). Ко второй группе следует отнести стрессорные язвы, развивающиеся остро в ответ на стресс, травму, тяжелую эндогенную интоксикацию (могут осложняться кровотечениями и перфорацией).
Первая группа язвенных поражений сопровождается НПВП и АСК-гастропатиями, требующими применения гастропротекторов (лучше, на наш взгляд, селективный ингибитор протонной помпы – ИПП – пантопразол), а при образовании язвы – классических схем лечения. Идиопатические H. рylori-негативные язвы часто сопровождаются кишечной метаплазией и дисплазией, рассматриваемой как предраковый процесс. Следует помнить, что именно H. рylori официально признан Международной ассоциацией по изучению рака (IARC) канцерогеном I класса, доказана его роль в развитии атрофии и дисплазии слизистой, железодефицитной и В12-дефицитной анемии, МАЛТ-лимфомы и рака желудка.
На основании сказанного необходимо сделать два важных практических вывода:
- следует чаще выполнять тест на H. рylori (во время эндоскопии);
- при наличии H. рylori-негативной язвы желудка обязательно проводить мультифокальную биопсию (не менее 6 биоптатов) из краев и дна язвы. По данным A. Misumi (2000), одиночная биопсия может быть не только бесполезной, но и вредной.
Доказано, что большинство желудочных малигнизирующих язв изначально являются первично-язвенной формой рака. При этом может наблюдаться даже процесс временного заживления, как правило, неполный. Большинство ведущих терапевтов-гастроэнтерологов считают, что современные схемы лечения (Маастрихт 2-4) с эрадикацией H. рylori способствуют успешному заживлению язв, предотвращению рецидивов, что дает право рассматривать ЯБ как сугубо терапевтическое заболевание. Однако, по данным ведущих клиник Европы, наблюдается 8-10% неудачных результатов консервативной терапии с развитием острых и хронических осложнений ЯБ, требующих применения хирургического лечения. К этому числу следует добавить еще больший процент больных, которые попадают на операционный стол с острыми осложнениями ЯБ без язвенного анамнеза (чаще всего при перфорациях). Поэтому полностью исключить хирургическое вмешательство в лечении ЯБ невозможно, однако следует признать, что число операций и показаний к ним существенно сократилось.
Хирургическому лечению в настоящее время подлежат лишь осложненные формы ЯБ: перфорации, кровотечения (профузные, повторные), пенетрации (обширные, глубокие), гигантские язвы, органические стенозы, длительно незаживающие желудочные и дуоденальные язвы, малигнизации. Операции при осложненной ЯБ должны основываться на органосохраняющих или органощадящих методиках. При этом, по нашему мнению, обязательным элементом органосохраняющих операций (ОСО) должно быть удаление язвенного субстрата с адекватным восстановлением просвета, а также проведение кислотоснижающей процедуры (оперативной или медикаментозной ваготомии).
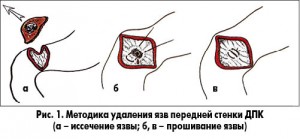
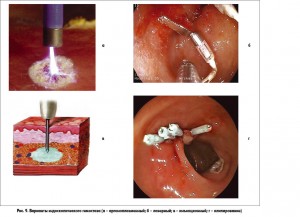
Методика удаления язв передней стенки ДПК и желудка не представляет большой сложности, известна давно и часто используется при перфоративных язвах в сочетании с дуодено- или пилородуоденопластикой, ваготомией или без нее, что в последнее время встречается намного чаще (рис. 1). При этом после иссечения производится ревизия задней стенки ДПК, где часто (15-18% случаев) обнаруживается вторая – потенциально кровоточащая язва, требующая также соответствующей обработки (при небольших размерах – до 1см – достаточно прошивания).
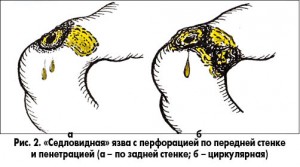
Наибольшую сложность представляют варианты атипично расположенных перфоративных язв. Прежде всего, довольно часто встречается так называемая седловидная язва с перфорацией по передней стенке и пенетрацией по боковой и задней стенкам, а также циркулярные язвенные поражения (рис. 2). Такие язвы при обработке только передней прободной части чаще всего осложняются реперфорацией и кровотечением.
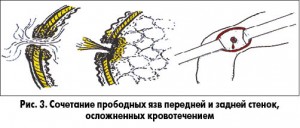
В 12-15% случаев имеются сочетания отдельно расположенных прободной язвы передней стенки и кровоточащей язвы задней стенки (рис. 3). Поэтому ушивание одной язвы передней стенки в таких случаях опасно и недопустимо.
Поскольку при перфоративной язве, сопровождающейся распространенным перитонитом, практически всегда в послеоперационном периоде применяются антибиотики, мы рекомендуем кроме аминогликозидов (для подавления кишечной микрофлоры) включать кларитромицин, амоксициллин (амоксициллина клавуланат) и метронидазол (лучше – орнидазол) для одновременной эрадикации H. рylori-инфекции. При этом аминогликозиды спустя 3-4 сут при благоприятном течении послеоперационного периода можно отменить, а эрадикацию следует продлить до 7 сут.
Если не проводилась ваготомия, то с первых суток послеоперационного периода следует применять современные ингибиторы желудочной секреции, вначале внутривенные препараты – лучше селективный ингибитор пантопразол (Контролок®).
Вторым наиболее частым осложнением ЯБ являются кровотечения, общая частота которых превышает количество случаев перфораций. Однако с точки зрения хирургии наиболее актуальными являются массивные профузные кровотечения, которые трудно остановить консервативно и приходится проводить операции «на высоте кровотечения». Хирургическая тактика при язвенных кровотечениях на протяжении последнего столетия имела ряд изменений: от выжидательной (в начале XX в.) до активно-выжидательной (середина XX в.) и активной (2-я половина XX в.). С начала 80-х годов прошедшего столетия за счет широкого внедрения фиброгастродуоденоскопии появилась возможность составлять индивидуальный эндоскопический прогноз и проводить хирургическую тактику, которую мы назвали «индивидуально активной», а А.И. Горбашко – «индивидуализированно активной» тактикой [3, 12]. Суть индивидуально активной тактики заключается во введении в арсенал хирургии отсроченных операций (кроме экстренных и ранних плановых). Отсроченные операции должны выполняться в течение 1-2 сут от начала кровотечения, несмотря на его остановку. Показаниями к отсроченным операциям служат неустойчивый гемостаз и высокий риск рецидива кровотечения. Эффективность гемостаза определялась по трем параметрам:
- неэффективный гемостаз – продолжающееся кровотечение (F-1А, F-1В по классификации Forrest);
- неустойчивый гемостаз – высокий риск рецидива кровотечения (F-2А, F-2В, F-2С);
- устойчивый гемостаз (F-3).
Доказана корреляция между использованием ИПП (в/в) и снижением частоты повторных язвенных кровотечений (C.J. van Rensburg et al. Pantoprazole for the Treatment of Peptic Ulcer Bleeding and Prevention of Rebleeding Clinical Medicine Insights: Gastroenterology 2012; 5: 51-60). Так, по результатам исследования N.J. Chahin и соавт., при использовании оригинального пантопразола (Контролок®) в сочетании с эндоскопическим гемостазом удается существенно снизить частоту повторных язвенных кровотечений, необходимость хирургических вмешательств и длительность госпитализации. Причем эти показатели существенно лучше, чем при использовании омепразола. Частота повторных кровотечений в исследовании при использовании пантопразола и омепразола составила 3,7 vs 10,2% соответственно. (N.J. Chahin, M. Meli, F. Zaca, P. Gilbertini. Can J Gastroenterol 2006; 20, Suppl A: 112).
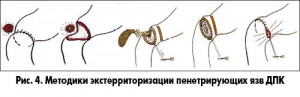
Наибольшую трудность представляла разработка методов локального удаления пенетрирующих язв. К 1982 г. нами были разработаны, внедрены в клиническую практику и защищены авторскими свидетельствами основные методики удаления пенетрирующих язв ДПК [7, 8, 10]. Суть этих разработок заключалась в выведении пенетрирующей язвы за пределы просвета ЖКТ, методика была названа «экстерриторизацией» язвы с последующей субциркулярной или сегментарной дуоденопластикой (рис. 4).
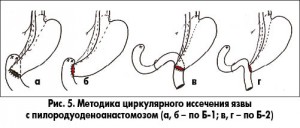
Предложена методика циркулярного иссечения с пилородуоденоанастомозом по Б-1 и пилороэнтероанастомозом по Б-2 [11] (рис. 5).
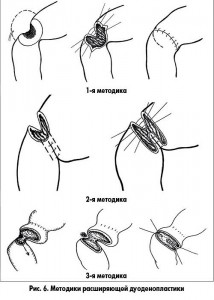
При сочетании пенетрирующей язвы с органическим стенозом предложены три методики расширяющей дуоденопластики [10] (рис. 6).
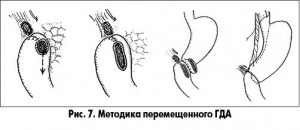
В дальнейшем были разработаны методики перемещенного гастродуоденоанастомоза (ГДА) [23] (рис. 7), низкий ГДА, антирефлюксные и некоторые другие методики. Все они объединены одной общей идеей – выведения пенетрирующей язвы (экстерриторизация, экстрадуоденизация) за пределы ЖКТ, где эта «язва» – просто участок фибрина – рубцовой ткани, не представляющий никакой опасности для организма.
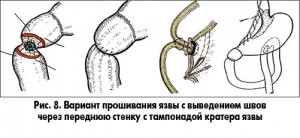
При низких постбульбарных кровоточащих язвах предлагается вариант прошивания язвы с выведением швов через переднюю стенку с тампонадой кратера язвы, ваготомией и гастроэнтероанастомозом (ГЭА) (рис. 8).
К настоящему времени по разработанным методикам нами выполнено более 2500 операций с практически нулевой несостоятельностью швов в зонах дуоденопластики и пилородуодено- или пилороэнтероанастомоза при плановых операциях и минимальным количеством осложнений (4-5%) при ургентных вмешательствах.
В последние годы произошли значительные изменения в консервативном лечении язвенных кровотечений. В схему гемостаза введены современные ингибиторы желудочной секреции – прежде всего ИПП. Созданы их внутривенные формы. В Лондоне (2010) достигнут консенсус по дозировкам и эффективности ИПП (пантопразол, рабепразол, эзомепразол); определены уровни ингибирования кислотопродукции (рН >6), при которых не разрушается формирующийся тромб; сделан вывод о недостаточности блокаторов Н2-рецепторов. В схему гемостатической терапии введены препараты транексамовой кислоты и соматостатина (октреотид), производные вазопрессина – терлипрессин и др. В последние годы наметился заметный прогресс в эндоскопическом гемостазе. Практически повсеместно используются орошения и пленкообразующие жидкости. Шире стал применяться инъекционный гемостаз, а также коагуляционный, аргоноплазменный и лазерный гемостазы, клипирование (рис. 9 а-г). Эти достижения вносят изменения в хирургическую тактику. С нашей точки зрения она должна оставаться индивидуально активной, но с усилением консервативной части с целью достижения стойкого гемостаза и сокращения числа операций на высоте кровотечения.
Неоспоримым показанием для оперативного лечения являются органические стенозы. Общее правило: декомпенсированный стеноз является абсолютным показанием к операции, субкомпенсированный – условно абсолютным, а компенсированный – относительным. Во всех случаях должен быть индивидуальный подход с исключением затянувшейся терапии и недооценки степени тяжести стеноза.
Работы сотрудников Национального института хирургии и трансплантологии им. А.А. Шалимова и нашей клиники показали, что при сохранившемся тонусе желудочной стенки, даже при декомпенсированном стенозе, можно успешно выполнять ОСО. Декомпенсированные стенозы следует разделять на две группы: с сохраненным мышечным тонусом желудочной стенки (показаны ОСО); со сниженным или отсутствующим (дилатация) мышечным тонусом, когда преимущественно применяются резекционные методы.
При органических стенозах часто встречается как гастроэзофагеальная рефлюксная болезнь, так и патологический дуоденогастральный рефлюкс. Причинами этой сопутствующей патологии могут быть грыжи пищеводного отверстия диафрагмы, дуоденостаз, недостаточность кардиального и пилорического жома, конституционно-генетические особенности, недифференцированная дисплазия соединительной ткани и другие факторы. Такая сочетанная патология может быть успешно скорригирована симультанными операциями, направленными на устранение язвенного субстрата и ликвидацию рефлюксной болезни [5-6]. Во многих случаях эти вмешательства, а также операции по поводу язвенных кровотечений и перфораций, можно выполнять видеолапароскопическими методами [2, 4, 15-16].
Отдельно следует рассматривать рецидивные послеоперационные язвы. Чаще всего встречаются рецидивы после ушивания перфоративной язвы без иссечения и без ваготомии. Реже – пептическая язва ГЭА, язвы ГДА (после методики Джабулея), а также низкие постбульбарные и юкстапапиллярные рецидивные язвы. Как правило, больные с такой осложненной формой ЯБ требуют лечения в специализированных хирургических центрах.
Таким образом, несмотря на значительное снижение общего числа хирургических вмешательств (особенно за счет плановых операций), осложненная язвенная патология не стала проще, а осложнения ЯБ – не менее опасны. Хирургические методы при ЯБ должны сочетаться с современными терапевтическими средствами (ИПП, эффективными гемостатиками, препаратами для эрадикации H. рylori и др.). Вследствие резкого сокращения количества операций при ЯБ к подготовке хирургов выдвигаются более высокие требования, что накладывает большую ответственность на центры, где еще работают специалисты с опытом ургентной хирургии ЯБ, которая имела место в течение предыдущих десятилетий, а также центры, продолжающие научные разработки и внедряющие современные технологии в такой сложный раздел хирургии, каким является осложненная ЯБ.
Литература
- Брикульский И.Б. Влияние хирургического лечения язвенной болезни двенадцатиперстной кишки на состояние местного иммунитета желудка и двенадцатиперстной кишки. Автореф. дис. кан. мед. наук. Харьков. – 1993. – 24 с.
- Велигоцкий Н.Н. Выбор метода пластики при выполнении симультанных антирефлюксных операций у больных с осложненными формами язвенной болезни двенадцатиперстной кишки / Н.Н. Велигоцкий, В.В. Комарчук, А.В. Горбулич, Е.В. Комарчук // Харківська хірургічна школа. – 2014. – № 1(64). – С. 11-15.
- Велигоцкий Н.Н. Обоснование необходимости иссечения кровоточащей хронической язвы двенадцатиперстной кишки и желудка / Н.Н. Велигоцкий и соавт. // Хирургия. – 1989. – № 4. – С. 18-20.
- Велигоцкий Н.Н. Опыт лечения перфоративной язвы двенадцатиперстной кишки с учетом кислотопродуцирующей функции желудка / Н.Н. Велигоцкий, В.В. Комарчук, А.С. Трушин, А.В. Горбулич и соавт. // Харківська хірургічна школа. – 2012. – № 3(54). – С. 47-49.
- Велигоцкий Н.Н. Опыт лечения язвенной болезни двенадцатиперстной кишки в сочетании с рефлюксной болезнью / Н.Н. Велигоцкий, В.В. Комарчук, А.С. Тpушин, С.С. Раззадорин // Вісник Української медичної стоматологічної академії. Актуальні проблеми сучасної медицини. – 2011. – Т. 11, вип. 1(33). – С. 34-36.
- Велигоцкий Н.Н. Опыт лечения язвенной болезни двенадцатиперстной кишки в сочетании с рефлюксной болезнью / Н.Н. Велигоцкий, В.В. Комарчук, А.С. Тpушин, С.С. Раззадорин // Вісник Української медичної стоматологічної академії. Актуальні проблеми сучасної медицини. – 2011. – Т. 11, вип. 1(33). – С. 34-36.
- Велигоцкий Н.Н. Органосохраняющие методы хирургического лечения острокровоточащих язв желудка и двенадцатиперстной кишки / Н.Н. Велигоцкий, В.Ф. Саенко, П.Г. Кондратенко, В.П. Хохоля // Методические рекомендации МЗ СССР. – 1985. – 20 с.
- Велигоцкий Н.Н. Органосохраняющие операции при кровоточащей язве двенадцатиперстной кишки / Н.Н. Велигоцкий, В.Т. Зайцев // Клин. Хирургия. – 1982. – № 4. – С. 9-13.
- Велигоцкий Н.Н. Органосохраняющий подход в реконструктивной хирургии рецидивных послеоперационных язв двенадцатиперстной кишки / Н.Н. Велигоцкий, А.Н. Велигоцкий, Г.Ю. Бука, В.В. Комарчук и соавт. // Харківська хірургічна школа. – 2008. – № 2(29). – С. 31-34.
- Велигоцкий Н.Н. Расширяющая пилородуоденопластика в хирургическом лечении кровоточащих и стенозирующих язв двенадцатиперстной кишки / Н.Н. Велигоцкий и соавт. // Хирургия. – 1985. – № 2. – С. 34-36.
- Велигоцкий Н.Н. Способ хирургического лечения кровоточащих низких постбульбарных язв двенадцатиперстной кишки // Авторское свидетельство № 3617451 от 08.07.83.
- Велигоцкий Н.Н. Хирургическая тактика при осложнении язвенной болезни кровотечением в сочетании с перфорацией / Н.Н. Велигоцкий и соавт. // Клин. Хирургия. – 1985. – № 8. – С. 48-50.
- Горбашко А.И. Диагностика и лечение кровопотери (руководство для врачей) / А.И. Горбашко // Москва: Медицина. – 1982. – 224 с.
- Гройсман С.Д. Влияние ваготомии на моторику желудка / С.Д. Гройсман // Моторная функция желудочно-кишечного тракта. – Киев. – 1965. – С. 67-68.
- Грубник В.В. Результаты лечения язвенной болезни ДПК, сочетанной с гастроэзофагеальной рефлюксной болезнью, с применением лапароскопических технологий / В.В. Грубник, О.Н. Загороднюк // Харківська хірургічна школа. – 2003. – № 1. – С. 11.
- Грубник В.В. Роль селективной проксимальной ваготомии при лапароскопической фундопликации по Тупе / В.В. Грубник, А.В. Малиновский, Ш.Т. Гиуашвили, М.А. Кидадзе // Эндоскопическая хирургия. – 2011. – № 3. – С. 24-26.
- Зайцев В.Т. Нарушение моторно-эвакуаторной функции желудка у больных после органосохраняющих операций с ваготомией / В.Т. Зайцев, В.В. Бойко, А.Е. Ладога, Г.О. Григорян и соавт. // Хирургия. – 1992. – № 2. – С. 9-13.
- Исаков В.А. Хеликобактериоз / В.А. Исаков, И.В. Домарадский // М. Медпрактика. – М. – 2003. – 412 с.
- Шамун К. Состояние защитного слизистого барьера и хеликобактериоз при язвенных пилородуоденальных стенозах: Дис… канд. мед. наук / ХИУВ. – Х. – 1997. – 125 с.
- Курбанов К.М. Органосохраняющие методы в хирургии постбульбарных язв двенадцатиперстной кишки. – Харьков. – 1990. – 24 с.
- Лаврик A.C. Выбор метода хирургического лечения хронической язвенной болезни желудка: Автореф. канд. мед. наук. – Киев. – 1988. – 22 с.
- Маев И.В. Важные практические результаты и современные тенденции в изучении заболеваний желудка и двенадцатиперстной кишки / И.В. Маев, А.А. Самсонов, Н.Г. Андреев, Д.Н. Андреев // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. – 2012. – № 4. – С. 17-26.
- 23. Пат. 24597 А Україна, МПК6 А 61В17/00. Спосіб хірургічного лікування ускладнених виразок дванадцятипалої кишки / Велигоцький М.М., Комарчук В.В., Трушин О.С., Сербул М.М.; заявник і патентовласник Харківський інститут удосконалення лікарів. – № 97063138. Заявл. 26.06.97; опубл. 30.10.98. Бюл. № 5.
- Полинкевич Б.С. Влияние ваготомии на интрамуральные нервные сплетения желудка, проблема реиннервации желудка после ваготомии / Б.С. Полинкевич, М.П. Ковальский, С.Д. Гройсман // Клин. хирургия. – 1990. – № 8. – С. 24-26.
- Ткач С.М. Современные подходы к оптимизации терапии инфекции Helicobacter pylori /С.М. Ткач // Сучасна гастроентерологія. – Харків; Дніпропетровськ. – 2012. – № 5. – С. 83-90.
- Фомін П.Д. Спосіб селективної проксимальної ваготомії / П.Д. Фомін, Є.М. Шепетько, О.А. Повч, Г.М. Шепетько // Промислова власність. Офіційний бюлетень. – 1998. – № 3. – С. 31-41.
- Циммерман Я.С. Гастроэнтерология / Я.С. Циммерман // М.: ГЭОТАР – Медиа. – 2012. – 800 с.
- Циммерман Я.С. Нерешенные и спорные проблемы современной гастроэнтерологии (Unsolved and Debatable Issues of Modern Gastroenterology). – М.: МЕДпресс-информ. – 2013. – 224 с.
- Шалимов A.A. Хирургия желудка и двенадцатиперстной кишки / A.A. Шалимов, В.Ф. Саенко. – Киев: Здоровье. – 1972. – 388 с.
- Amieva M.R., El-Omar E.M. Host-bacterial interactions in Helicobacter pylori infection. Gastroenterology. 2008 Jan; 134(1): 306-23. doi: 10.1053/j.gastro.2007.11.009.
- Blaser M.J. (1998) Helicobacters are indigenous to the human stomach: duodenal ulceration is due to changes in gastric microecology in the modern era. Gut 43: 721-727.
- Bytzer P. Helicobacter pylori – negative duodenal ulcers: Prevalence, clinical characteristics and prognosis: Results from a randomized trial with 2-year fallow-up / P. Bytzer, P.S. Taglbjaerd // Am. J. Gastroenterol. – 2001. – Vol. 96. – Р. 1409-1416.
- Cheng H., Hu F., Zhang L., Yang G., Ma J., Hu J. et al. Prevalence of Helicobacter pylori infection and identifi cation of risk factors in rural and urban Beijing, China. Helicobacter. 2009; 14: 128-33.
- El-Omar E.M., Oien K., Murray L.S., et al. (2000) Increased prevalence of precancerous changes in relatives of gastric cancer patients: critical role of H. pylori. Gastroenterology 118: 22-30.
- El-Omar E.M., Carrington M., Chow W.H., et al. Interleukin-1 polymorphism associated with increased risk of gastric cancer (erratum appears in Nature 2001; 412: 99). Nature 2000; 404: 398-402.
- El-Omar E.M., Chow W.H., Gammon M.D., et al. Pro-inflammatory genotypes of IL-1B, TNFa and IL-10 increase risk of distal gastric cancer but not of cardia or esophageal adenocarcinoma. Gastroenterology 2001; 120 (suppl): A86.
- El-Omar E.M., Chow W.H., Rabkin C.S. Gastric cancer and H. pylori: host genetics open the way. Gastroenterology 2001; 121: 1002-4.
- El-Omar E.M., You W.C., Chow W.H., et al. IL-1β and IL-10 genotypes in a high gastric cancer risk province in China. Gastroenterology 2001; 120: A 3994.
- Ford A.C., Axon A.T. Epidemiology of Helicobacter pylori infection and public health implications. Helicobacter. 2010; 15 (Suppl. 1): 1-6.
- Go M.F. Review article: natural history and epidemiology of Helicobacter pylori infection. Aliment. Pharmacol. Ther. 2002; 16: 3-15.
- Graham D.Y. Campylobacter pylori and peptic ulcer disease // Gastroenterology. – 1989. – Vol. 96. – Р. 615-625.
- Laine L. Therapy for Helicobacter pylori in patients with nonulcer dyspepsia: A meta-analysis of randomized, controlled trials / L. Laine; P. Schoenfeld; M.B. Fennert// Mar 6 2001 In: Annals of Internal Medicine. 134, 5, P. 361-369.
- Marshall B.J., Warren J.R. Unidentifi ed curved bacilli in the stomach of patients with gastritis and peptic ulceration. Lancet. 1984; 1(8390): 1311-5.
- Misumi A., Misumi K., Murakami A. et al. Endoscopic diagnosis for minute, small and flat early gastric cancers. Endoscopy., 1989; 21: 159-164.
- Naylor G.M., Gotoda T., Dixon M., Shimoda T., Gatta L., Owen R., Tompkins D., Axon A. Why does Japan have a high incidence of gastric cancer? Comparison of gastritis between UK and Japanese patients. Gut 2006; 55: 1545-52.
- Ruggiero P. Helicobacter pylori infection: what’s new. Curr. Opin. Infect. Dis. 2012; 25(3): 337-44.
- Salih B.A. Helicobacter pylori infection in developing countries: The burden for how long? Saudi J. Gastroenterol. – 2009. – 15(3): 201-7.
- Tonkic A., Tonkic M., Lehours P., Megraud F. Epidemiology and diagnosis of Helicobacter pylori infection. Helicobacter. 2012; 17 (Suppl. 1): 1-8.
- Tytgat G.N. Endoscopic transmission of H. pylori // Aliment. Pharmacol. Ther. 1995. Vol. 9(2). P. 105-110.