31 жовтня, 2021
Реальна ефективність бригатинібу у пацієнтів з ALK+ метастатичним недрібноклітинним раком легені, які раніше вже отримували лікування
Результати дослідження UVEA-Brig
Недрібноклітинний рак легені (НДРЛ) становить приблизно 85% усіх випадків діагностованого раку легені [1]. Це одне із найпоширеніших онкологічних захворювань, основним фактором ризику розвитку якого, як відомо, є куріння. НДРЛ включає такі основні гістологічні форми, як аденокарцинома, плоскоклітинний рак і великоклітинний (недиференційований) рак. Підходи до лікування НДРЛ залежать від його стадії, гістологічного типу та загального стану пацієнта. Протягом останнього десятиріччя у хворих на метастатичний НДРЛ все ширше застосовують інноваційні засоби таргетної терапії, які дозволяють прицільно впливати на пухлини з певними молекулярно-генетичними характеристиками. Саме використання таргетної терапії наразі вважається найбільш персоналізованим і перспективним напрямом онкології.
Приблизно у 3-5% пацієнтів з НДРЛ спостерігаються перебудови гена кінази анапластичної лімфоми (ALK) [2, 3]. Незважаючи на те що цей відсоток на перший погляд видається відносно невеликим, визначення наявності транслокації гена ALK насправді є надзвичайно важливим, оскільки у пацієнтів із цією мутацією найефективнішим буде саме застосування таких таргетних препаратів, як інгібітори ALK. Слід зазначити, що прогноз у пацієнтів з ALK+ поширеним НДРЛ традиційно вважається несприятливим: наприклад, у дослідженні III фази частота об’єктивної відповіді у пацієнтів з ALK+ НДРЛ, котрі отримували хіміотерапію, складала 45% (95% довірчий інтервал – ДІ – 37-53), а медіана виживаності без прогресування (ВБП) – лише 7,0 міс (95% ДІ 6,8-8,2) [4]. Більше того, пацієнти з ALK+ НДРЛ становлять групу високого ризику метастазування у центральну нервову систему (ЦНС): повідомляється, що частота виявлення у них метастазів у ЦНС протягом перебігу захворювання складає 60-90% [5, 6].
Проте нові підходи до лікування ALK+ НДРЛ продовжують швидко розвиватися, і на цьому шляху вже є вагомі досягнення. Кризотиніб – інгібітор ALK першого покоління – став першим препаратом, який був схвалений саме для лікування цієї популяції пацієнтів і продемонстрував здатність достовірно покращувати частоту досягнення відповіді та ВБП порівняно із хіміотерапією [7, 8]. Однак у більшості пацієнтів, які отримують кризотиніб, на жаль, розвивається резистентність до нього, а його обмежена здатність проникати в головний мозок означає, що у багатьох пацієнтів відзначається прогресування захворювання з формуванням метастазів у головному мозку [9-12].
Тому згодом було розроблено та схвалено низку більш потужних інгібіторів ALK другого покоління, які характеризуються кращим проникненням у ЦНС, до них належать церитиніб, алектиніб і бригатиніб [10, 13-16]. При ALK+ НДРЛ ці препарати рекомендовані для застосування у першій та/або другій лінії [17]. П’ятий за рахунком інгібітор ALK – лорлатиніб – показаний для використання у пацієнтів, у яких відзначається прогресування захворювання після лікування інгібіторами ALK другого покоління [17]. Також повідомляється про його вищу ефективність порівняно із кризотинібом у разі застосування у першій лінії терапії [18]. Однак профіль переносимості лорлатинібу відрізняється від такого інших інгібіторів ALK [19, 20]. Шостий інгібітор ALK – енсартиніб – також нещодавно засвідчив свою вищу ефективність порівняно з кризотинібом у пацієнтів з поширеним ALK+ НДРЛ, які раніше не отримували лікування інгібіторами ALK [21].
Послідовне призначення інгібіторів ALK істотно вплинуло на результати лікування пацієнтів з ALK+ метастатичним НДРЛ: у ретроспективних дослідженнях із застосуванням спочатку кризотинібу як препарату першої лінії, а потім щонайменше ще одного іншого інгібітору ALK було зафіксовано досягнення медіани загальної виживаності (ЗВ) до 89 міс [22-24].
Інгібітор ALK другого покоління бригатиніб є високоселективним потужним лікарським засобом, який проявляє активність проти пухлин із широким спектром мутацій ALK та онкогенними мутаціями (злиттями) гена ROS1 [25]. Він також продемонстрував активність проти ширшого спектра мутацій резистентності, ніж кризотиніб та деякі інші інгібітори ALK [25]. У дослідженні II фази ALTA, котре стало основою для схвалення застосування бригатинібу після кризотинібу, у пацієнтів з ALK+ НДРЛ, у яких відзначалося прогресування захворювання на тлі попереднього лікування кризотинібом, частота відповіді становила 56%, медіана ВБП – 16,7 міс, а медіана ЗВ – 34,1 міс [26, 27]. У пацієнтів із метастазами у ЦНС частота відповіді з боку внутрішньочерепних метастазів (інтракраніальної відповіді) на лікування бригатинібом дорівнювала 67%, а медіана ВБП на тлі початкового метастатичного ураження ЦНС («інтракраніальної» ВБП) – 18,4 міс [27]. Подальше дослідження III фази ALTA‑1 продемонструвало, що бригатиніб достовірно покращував результати лікування порівняно з кризотинібом у пацієнтів з ALK+ НДРЛ, які не отримували попередню терапію інгібітором ALK: згідно з висновком комітету з незалежної оцінки у сліпому режимі (BIRC), медіана ВБП склала 24,0 порівняно з 11,0 міс (відношення ризиків – ВР – 0,49; 95% ДІ 0,35-0,68; логрангове значення p <0,0001) [14, 28]. У цьому дослідженні частота інтракраніальної відповіді складала 78% [28]. Сьогодні застосування бригатинібу у режимі монотерапії схвалено для лікування пацієнтів з поширеним ALK+ НДРЛ, які раніше не отримували інгібіторів ALK, а також для тих хворих, яким раніше призначали кризотиніб [26, 29].
У 2016 р. за участі 9 країн Європи була ініційована Глобальна програма розширеного доступу (EAP) до лікування бригатинібом ще до його схвалення Європейським агентством з лікарських засобів (EMA) [29]. Однак аналіз ефективності бригатинібу не входив у сферу уваги EAP, оскільки збір даних у рамках цієї програми охоплював лише тривалість лікування бригатинібом, про яку повідомлялося як про непрямий показник переносимості й ефективності. Тому для збору детальної інформації про реальну ефективність терапії бригатинібом у пацієнтів, які отримували лікування ним у рамках глобальної програми EAP у Європі, було сплановане спеціальне дослідження UVEA-Brig (Use Via Expanded Access to Brigatinib). За дизайном воно було ретроспективним аналізом відомостей із медичних карт (без препарату порівняння), розробленим для збору клінічних даних про пацієнтів з ALK+ місцево-поширеним та/або метастатичним НДРЛ, які раніше отримували щонайменше один інгібітор ALK і надалі лікувалися бригатинібом. Результати дослідження UVEA-Brig були вперше надруковані міжнародною групою дослідників (S. Popat et al.) на сторінках авторитетного спеціалізованого видання Lung Cancer у липні цього року, і вони, безумовно, становлять значний інтерес для лікарів-онкологів, які займаються веденням пацієнтів з раком легені.
Загалом до дослідження UVEA-Brig було включено 104 дорослі пацієнти з гістологічно або цитологічно підтвердженим місцево-поширеним чи метастатичним НДРЛ з мутацією ALK (у тому числі пацієнти з ураженням головного мозку), що отримували бригатиніб у рамках програми EAP на базі клінічних центрів Італії (n=56; 13 центрів), Норвегії (n=13; 2 центри), Іспанії (n=14; 5 центрів) та Великої Британії (n=21; 4 центри). Додатковими критеріями включення стали непереносимість або резистентність як мінімум до одного попередньо застосовуваного інгібітору ALK та оцінка функціонального статусу ≤3 бали за критеріями Східної об’єднаної онкологічної групи (ECOG). Клінічні центри вважалися придатними для участі у дослідженні UVEA-Brig, якщо у них щонайменше два пацієнти отримували лікування бригатинібом у рамках EAP і при цьому не проводилося жодне конкуруюче дослідження. Збір даних розпочато у січні 2018 р., а припинено у вересні 2019 р. Медіана тривалості періоду подальшого спостереження за включеними у дослідження пацієнтами склала 16,5 міс.
Первинна мета дослідження UVEA-Brig полягала в описі клінічної картини захворювання, застосовуваних режимів лікування та клінічних результатів у пацієнтів, які отримували лікування бригатинібом з приводу ALK+ місцево-поширеного або метастатичного НДРЛ у рамках EAP. Вторинні цілі включали опис характеристик пацієнтів, клінічної картини захворювання, застосовуваних режимів лікування та клінічних результатів залежно від того, у якій саме лінії лікування призначали терапію бригатинібом. Були оцінені початкові характеристики пацієнтів, а також схеми лікування до терапії бригатинібом та після її припинення. Оцінки пухлини та клінічних показників лікуючі лікарі здійснювали під час лікування бригатинібом, а також після застосування кожної лінії терапії до та після лікування цим препаратом. Оцінювали такі результати лікування:
- ЗВ (час від початку лікування бригатинібом до настання смерті пацієнта);
- ВБП (час від початку лікування бригатинібом до першої констатації факту прогресування захворювання/рецидиву або смерті; дані пацієнтів, у яких не відзначалося прогресування захворювання, або тих пацієнтів, які залишалися живими, були цензуровані на дату останньої оцінки/сканування);
- тривалість відповіді (ТВ; час від найкращої відповіді на лікування бригатинібом до прогресування захворювання, переривання лікування або смерті);
- час до припинення лікування (ЧДП; час від початку терапії бригатинібом до її припинення, останнього візиту у рамках періоду подальшого спостереження або смерті, без цензурування даних);
- тривалість лікування бригатинібом (ТЛ; час від початку терапії бригатинібом до її припинення, останнього візиту у рамках періоду подальшого спостереження або смерті, без цензурування даних);
- частота переривання лікування через розвиток небажаних явищ (НЯ).
Для відображення характеристик пацієнтів та схем лікування використовували описову статистику. ЗВ, ВБП, ТВ, ЧДП і ТЛ визначали за допомогою аналізу методом Каплана – Меєра для кожної лінії терапії бригатинібом. Показники частоти повної відповіді, часткової відповіді, стабілізації перебігу захворювання та прогресування захворювання були розраховані залежно від лінії терапії, у рамках якої було розпочато застосування бригатинібу. Відповідь на терапію визначали як зменшення розмірів пухлини або її зникнення (за можливості здійснювали оцінку із використанням Критеріїв оцінки об’єктивної відповіді при солідних пухлинах – RECIST v1.1).
Про дослідження UVEA-Brig
Медіана віку пацієнтів на момент встановлення діагнозу дорівнювала 53 роки (діапазон 29-80 років); 57% становили жінки. Частка пацієнтів з оцінкою функціонального статусу за критеріями ECOG, рівною 1, 2 та 3 бали, складала 41; 10 та 5% відповідно; 63% пацієнтів мали метастази у головному мозку/ЦНС.
До призначення бригатинібу пацієнти отримали до 6 ліній системної терапії (медіана – 2 лінії). Загалом 41 (39,4%) пацієнт отримав ≥3 попередніх ліній терапії (табл. 1).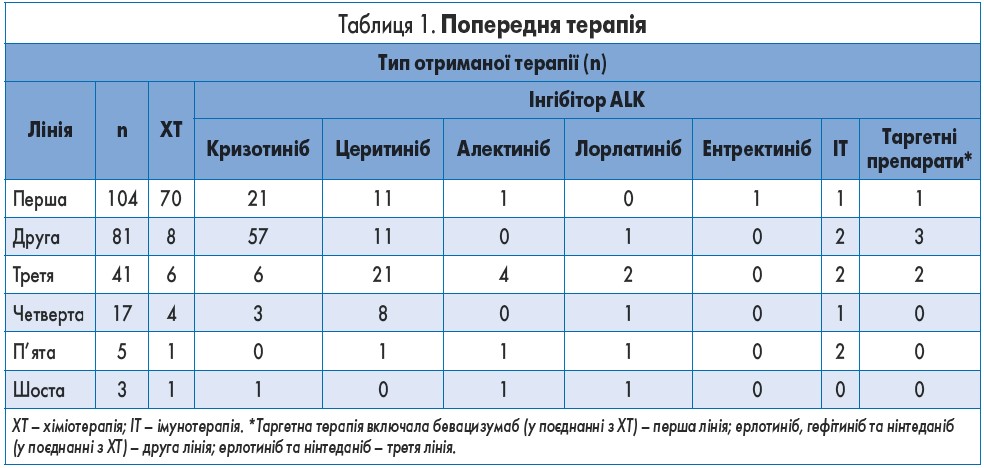
Пацієнти отримали до 5 попередніх ліній терапії інгібіторами ALK (медіана – 1 лінія); у 87 (83,6%) пацієнтів застосували попередню терапію кризотинібом в одній із цих ліній, у 52 (50,0%) – церитинібом, у 7 (6,7%) – алектинібом, у 5 (4,8%) – лорлатинібом та в 1 (1,0%) – ентректинібом.
Зі 104 включених до дослідження пацієнтів, всі з яких отримували попередню терапію першої лінії, 34 (33%) пацієнти приймали як препарат першої лінії інгібітор ALK (кризотиніб – 21, церитиніб – 11, алектиніб – 1, ентректиніб – 1). Більшість тих пацієнтів, які не використовували інгібітор ALK у першій лінії, як першу лінію отримували ХТ (табл. 1). Загалом 102 зі 104 пацієнтів мали доступні дані оцінки відповіді на терапію першої лінії, при цьому 1 (1,0%), 35 (34,3%) та 34 (33,3%) пацієнти досягли повної відповіді (ПВ), часткової відповіді (ЧВ) та стабілізації перебігу захворювання (СПЗ) відповідно (частота контролю захворювання – 67,3%).
З тих пацієнтів, які отримали щонайменше 2 лінії системної терапії перед призначенням бригатинібу (n=81), 69 (85%) хворих отримували у другій лінії інгібітор ALK (кризотиніб – 57, церитиніб – 11, лорлатиніб – 1; табл. 1). Із 77 осіб, які мали доступні дані про оцінку відповіді на терапію другої лінії, в 1 (1,3%), 33 (42,9%) та 21 (27,3%) пацієнта було досягнуто ПВ, ЧВ та СПЗ відповідно (частота контролю захворювання – 71,4%). Крім того, 74 (71%) зі 104 пацієнтів отримували попередню променеву терапію. Найчастіше зоною опромінення був головний мозок/ЦНС (59% усіх призначених курсів променевої терапії).
Зі 104 включених у дослідження пацієнтів 93 (89,4%) отримували бригатиніб у стандартній дозі 180 мг 1 раз на добу після 7-денного вступного прийому у дозі 90 мг 1 раз на добу. З інших 11 пацієнтів 8 (7,7%) осіб застосовували бригатиніб у дозі 90 мг 1 раз на добу протягом усього періоду лікування, 1 пацієнт – у дозі 180 мг на добу протягом усього періоду лікування та ще 1 пацієнт – у дозі 90 мг 1 раз на добу протягом 2 днів, після чого доза була знижена до 30 мг 1 раз на добу протягом 5 днів, 90 мг 1 раз на добу протягом 12 днів, а потім – 180 мг 1 раз на добу. Інформація щодо одного пацієнта була втрачена.
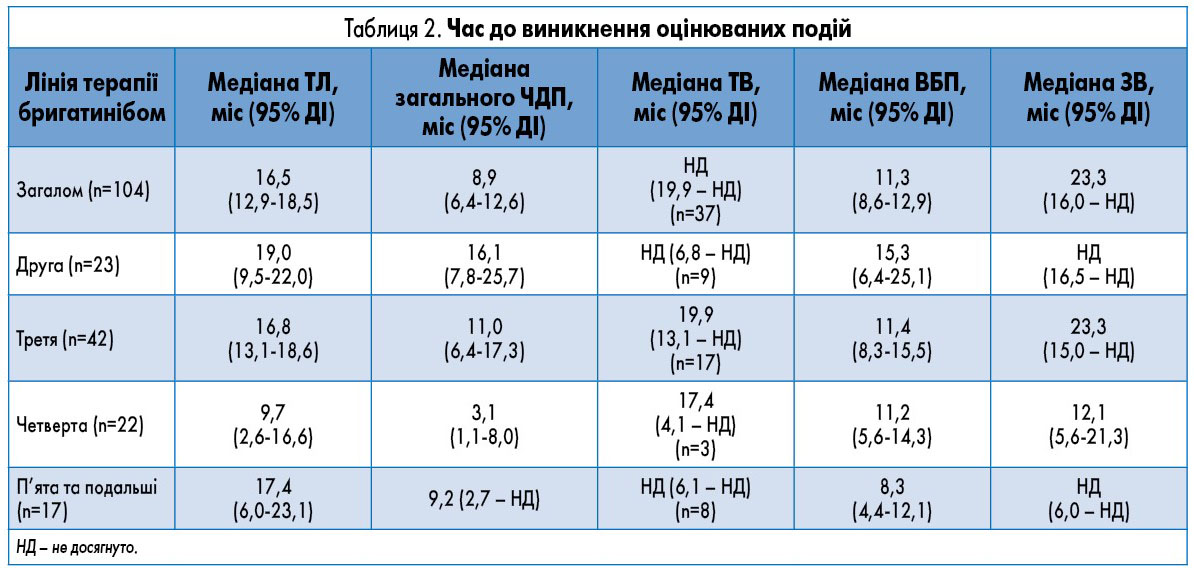
Загальна медіана тривалості терапії бригатинібом складала 16,5 міс (95% ДІ 12,9-18,5); 27 пацієнтів продовжували отримувати бригатиніб на момент припинення збору даних. Тривалість терапії бригатинібом залежно від лінії лікування відображена у таблиці 2.
Дані про оцінку найкращої відповіді на терапію бригатинібом були доступні у 93 пацієнтів; частота відповіді складала 39,8%, а частота контролю захворювання – 55,9% (табл. 3).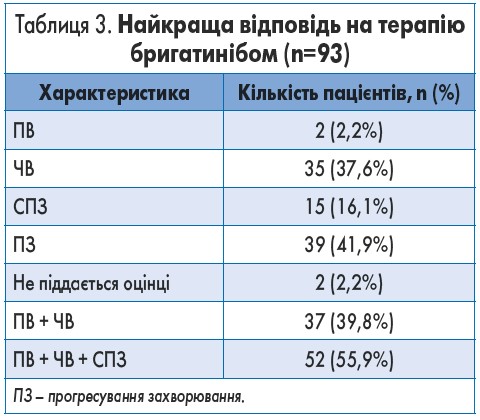
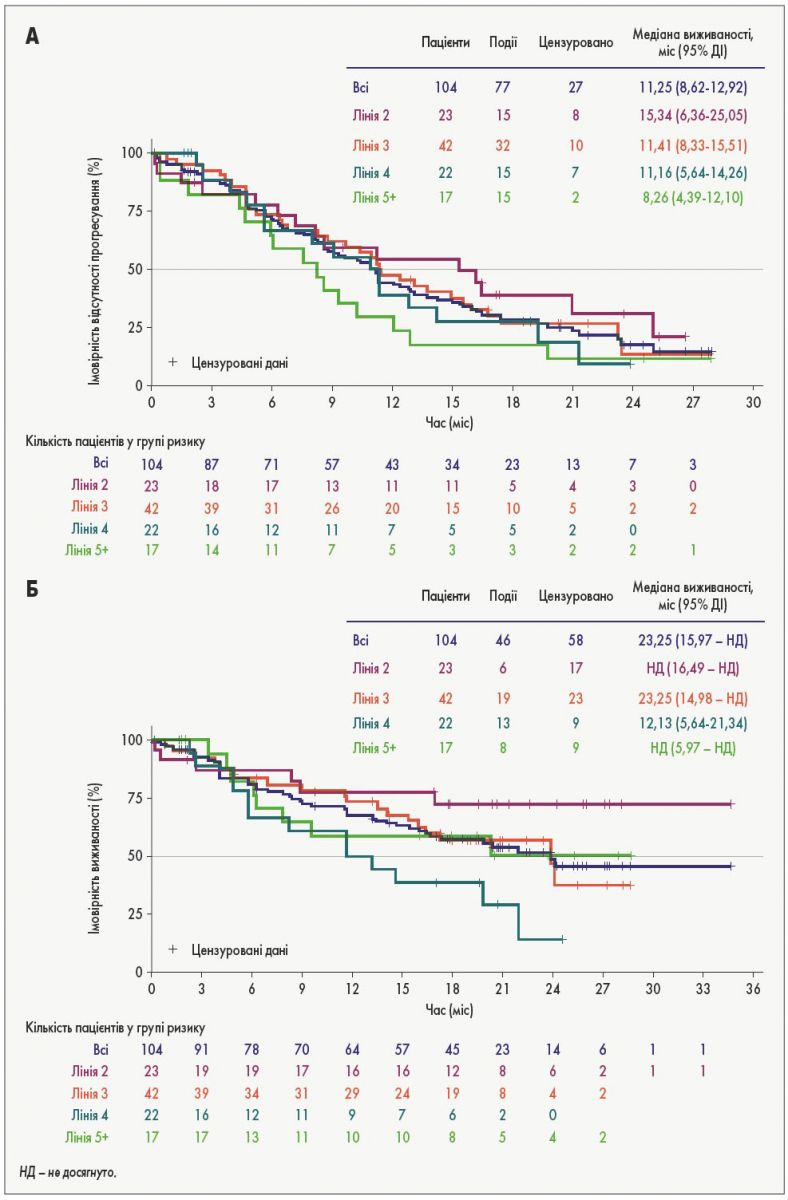
Ці оцінки були зроблені на підставі критеріїв RECIST у версії 1.1 (42% оцінок), оцінки дослідника (33%) та клінічної оцінки (20%). Загальна медіана тривалості відповіді не була досягнута (n=37; табл. 2). Медіана ВБП у 104 включених у дослідження пацієнтів склала 11,3 міс (95% ДІ 8,6-12,9), а медіана ЗВ – 23,3 міс (95% ДІ 16,0 –НД; табл. 2; рис.).
Явища, пов’язані з ПЗ, спостерігали у 77пацієнтів (17 випадків смерті та 60 випадків прогресування захворювання). З 60 пацієнтів, у яких було зафіксовано ПЗ, у 46 (76,7%) відзначали прогресування наявних уражень, у 3 (5,0%) – лише розвиток нових уражень, у 11 (18,3%) – як прогресування наявних вогнищ ураження, так і появу нових уражень. Прогресування наявних уражень було виявлено переважно у головному мозку/ЦНС (25,9% з 85 уражень), легенях (18,8%), печінці (12,9%), лімфатичних вузлах (12,9%) і кістках (10,6%). Медіана ВБП та ЗВ загалом зменшувалася з лінією терапії, у котрій застосовувався бригатиніб (рис.).
Рис. Криві Каплана – Меєра залежно від лінії початку терапії бригатинібом: А – ВБП, Б – ЗВ
Дані про відповідь на лікування були доступні у 57 з 65 пацієнтів з метастазами у головному мозку/ЦНС. Із цих 57 пацієнтів 23 (40,4%) мали найкращу ЧВ, а 8 (14,0%) – СПЗ. Медіана ВБП і ЗВ у цих пацієнтів складала 10,4 (95% ДІ 6,6-12,4) та 21,3 міс (95% ДІ 13,1 – НД) відповідно. Найкращими відповідями у пацієнтів без метастазів у головному мозку/ЦНС (n=39) були ЧВ (33,3%) та СПЗ (19,4%), у той час як медіана ВБП та ЗВ складали 11,4 (95% ДІ 8,3-16,5) та 23,4 міс (95% ДІ 14,5 – НД) відповідно.
Також виконано окремий аналіз даних 15 пацієнтів з оцінкою функціонального статусу за критеріями ECOG 2 або 3 бали. З 10 осіб із наявними оцінками відповіді 4 (40%) та 2 (20%) пацієнти мали найкращу відповідь у вигляді ЧВ і СПЗ відповідно. Медіана ВБП і ЗВ у цих пацієнтів складала по 5,6 міс (95% ДІ 0,5-6,4 та 0,8-7,6 відповідно). Найкращими відповідями у пацієнтів з оцінкою функціонального статусу за критеріями ECOG 0/1 бал (n=86) були ПВ (2,5%), ЧВ (37,5%) та СПЗ (16,3%); медіана ВБП складала 12,4 міс (95% ДІ 11,0-15,5), а медіана ЗВ не була досягнута (95% ДІ 19,3 – НД).
Профіль безпеки бригатинібу у дослідженні UVEA-Brig
На момент проведення цього аналізу терапія бригатинібом була припинена у 77 пацієнтів, медіана часу до переривання лікування складала 8,9 міс (95% ДІ 6,4-12,6) (табл. 2). У 4 пацієнтів (5,2%) лікування було припинено через НЯ, у той час як більшість учасників припинили лікування через прогресування захворювання або відсутність відповіді (n=55; 71,4%) та інші причини (n=18; 23,4%). До припинення терапії бригатинібом призвели такі НЯ:
- один випадок пневмоніту 2 ступеня тяжкості, який розвинувся через 7,7 міс після початку застосування бригатинібу у другій лінії терапії;
- один випадок пневмоніту 3 ступеня тяжкості, який розвинувся через 4 дні після прийому першої дози бригатинібу у рамках четвертої лінії терапії через 5 міс після завершення попереднього лікування;
- один випадок астенії/стомлюваності 2 ступеня тяжкості, що виникла через 0,7 міс після початку четвертої лінії терапії;
- один випадок підвищення рівня амілази та креатинкінази 3 ступеня тяжкості, який був зафіксований через 10,4 міс від початку третьої лінії терапії.
Результати оцінки безпеки були аналогічними у пацієнтів з наявністю метастазів у головному мозку/ЦНС та у хворих без них, хоча серед учасників з метастазами у головному мозку/ЦНС було менше пацієнтів, які припинили терапію через прогресування захворювання/відсутність відповіді (67,3 порівняно з 78,6%). Два пацієнти з метастазами у головному мозку/ЦНС вибули з дослідження через НЯ (пневмоніт 2 ступеня тяжкості та астенія/стомлюваність 2 ступеня тяжкості).
З 15 пацієнтів з оцінкою функціонального статусу за критеріями ECOG 2/3 бали один хворий припинив терапію через НЯ (пневмоніт 2 ступеня тяжкості), а 7 – через ПЗ або відсутність відповіді.
Висновки
Таким чином, дослідження UVEA-Brig надає дуже важливі для клініцистів дані щодо ефективності та безпеки використання терапії бригатинібом у клінічній практиці у пацієнтів з ALK+ поширеним НДРЛ, які раніше вже отримували як мінімум одну лінію лікування на основі інгібіторів ALK у рамках програми EAP у Європі. Ці дані свідчать про значну активність та хорошу переносимість цього препарату при його застосуванні у повсякденній клінічній практиці для лікування пацієнтів з ALK+ місцево-поширеним або метастатичним НДРЛ, які отримували навіть інтенсивнішу попередню терапію, ніж хворі, включені у клінічні дослідження. Ці результати також цілком узгоджуються з іншими наявними на сьогодні даними щодо застосування бригатинібу у клінічній практиці та підтверджують дані клінічних досліджень, що демонструють ефективність цього інноваційного препарату у пацієнтів з ALK+ місцево-поширеним або метастатичним НДРЛ [14, 27, 28, 31].
Список літератури знаходиться в редакції.
За матеріалами Popat S., Brustugun O.T., Cadranel J., Felip E., Garassino M.C., Griesinger F., Helland A., Hochmair M., Perol M., Bent-Ennakhil N., Kruhl C., Novello S. Real-world treatment outcomes with brigatinib in patients with pretreated ALK+ metastatic non-small cell lung cancer. Lung Cancer. 2021 Jul; 157: 9-16. doi: 10.1016/j.lungcan.2021.05.017. Epub 2021 May 24. PMID: 34051652.
Підготувала Вікторія Новікова
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 4 (71) 2021 р.