3 листопада, 2021
2-й Міжнародний флебологічний мітинг: у фокусі – хронічні захворювання вен
За матеріалами конференції
У серпні цього року відбувся 2-й Міжнародний флебологічний мітинг, присвячений останнім новинам флебології, за підтримки компанії «Серв’є». Провідні вітчизняні та міжнародні експерти представили сучасні погляди щодо патогенезу хронічних захворювань вен, діагностики й лікування, оновленої класифікації СЕАР, поділилися власним клінічним досвідом лікування пацієнтів із тазовими венозними розладами.
Ключові слова: хронічні захворювання вен, варикозне розширення вен, лікування ХЗВ, класифікація СЕАР, венозна гіпертензія, зміни мікроциркуляції.
Віце-президент Асоціації судинних хірургів, флебологів та ангіологів України, головний науковий співробітник Національного інституту хірургії і трансплантології ім. О.О. Шалімова НАМН України, доктор медичних наук, професор Лариса Михайлівна Чернуха у доповіді «Патогенез хронічних захворювань вен нижніх кінцівок. Від теорії до практики» представила найсучасніші дані щодо патогенезу хронічних захворювань вен (ХЗВ).
 Доповідач наголосила, що ХЗВ – одне з найпоширеніших порушень венозної системи нижніх кінцівок, де стійка амбулаторна венозна гіпертензія призводить до різних патологічних станів. За даними популяційних епідеміологічних досліджень у різних країнах, телеангіектазії та сітчасті вени наявні приблизно у 80% чоловіків та 85% жінок, а варикозне розширення вен – у 25-32% жінок та 7-40% чоловіків. Поширеність відкритої та загоєної венозної виразки спостерігається приблизно в 1% населення.
Доповідач наголосила, що ХЗВ – одне з найпоширеніших порушень венозної системи нижніх кінцівок, де стійка амбулаторна венозна гіпертензія призводить до різних патологічних станів. За даними популяційних епідеміологічних досліджень у різних країнах, телеангіектазії та сітчасті вени наявні приблизно у 80% чоловіків та 85% жінок, а варикозне розширення вен – у 25-32% жінок та 7-40% чоловіків. Поширеність відкритої та загоєної венозної виразки спостерігається приблизно в 1% населення.
Відсутність лікування ХЗВ призводить до розвитку больового синдрому, варикозного розширення вен, набряку, появи гіперпігментації, ліподерматосклерозу, венозної екземи, білої атрофії шкіри, виразок на ногах та тромбозу вен. При цьому у значної частини пацієнтів із неускладненим варикозним розширення вен (С2) захворювання може перейти у вищі клінічні класи згідно класифікації СЕАР (С3-С6).
Незважаючи на постійний прогрес у розумінні молекулярних аспектів ХЗВ, терапія варикозного розширення вен спрямована на анатомічні та механічні втручання. Але ці підходи не повністю усувають причини ХЗВ. Краще розуміння патогенезу цього захворювання є важливим кроком у визначенні нових потенційних терапевтичних цілей і сучасних стратегій лікування та персоналізованої терапії.
Повсякденна клінічна практика показує, що можлива ситуація, коли відсутні початкові ознаки ХЗВ (навіть підсилений венозний малюнок), а результати інструментального обстеження венозної системи нижніх кінцівок реєструють «легкий» рефлюкс у поверхневій венозній системі наприкінці робочого дня та після статичних навантажень, і при цьому пацієнт скаржиться на біль та важкість у нижніх кінцівках. Chiesa та співавт. (2007) показали, що приблизно 80% пацієнтів без видимих ознак венозного захворювання, включаючи відсутність варикозу, скаржаться на симптоми. Згідно з результатами досліджень, кожен п’ятий пацієнт на стадії С0s має сильний больовий синдром без клінічних ознак. Це свідчить про те, що зміни відбуваються не лише на макро-, а й на мікросудинному рівні.
Патогенез хронічних захворювань вен
Точний механізм розвитку ХЗВ залишається неясним. Ранні теорії припускали, що варикозне розширення вен виникає внаслідок функціональної неспроможності венозних клапанів і венозної гіпертензії. На сьогодні недостатньо даних про конститутивні аномалії клапанів при первинних венозних захворюваннях. Крім того, варикозні розширення стовбурів часто зустрічаються за нормально функціонуючих клапанів.
Ось чому за останні десятиліття відбувся перехід від початкових теорій, заснованих виключно на механічних чинниках – включаючи зміну гідростатичного тиску, неспроможність клапанів, обструкцію глибоких вен, неефективну функцію м’язової помпи гомілки, до теорій та гіпотез, які акцентують увагу на підвищеній проникності капілярів, ендотеліальній дисфункції, активації лейкоцитів, мікротромбозі капілярів, складних молекулярних змінах, що призводять до ХЗВ.
Венозна гіпертензія, яка є основною причиною ХЗВ, із часом призводить до екстравазації макромолекул у шкірний інтерстицій і до хронічного запалення венозної стінки. Також через гіпертензію вени розширюються, що веде до деформації стулок клапанів та втрати їхніх функцій. Збій у роботі клапанів, у свою чергу, призводить до турбулентного току, застою крові та розвитку рефлюксу, що також провокує місцеві запальні та тромботичні реакції.
Ці події спонукають до вироблення протромботичних агентів (моноцитарний хемоаттрактантний білок 1 та молекула адгезії судинних клітин 1) та агентів, що стимулюють ріст (ангіотензин II, ендотелін 1 та фактор росту, що походить від тромбоцитів), міграцію лейкоцитів та нейтрофілів і сприяють апоптозу.
Згідно з даними досліджень, внаслідок венозної гіпертензії, що супроводжує ХЗВ, виникають зміни у венозних судинах, а саме:
- нерегулярне потовщення інтими;
- фіброз між інтимою та адвентицією;
- атрофія та порушення еластичних волокон;
- потовщення окремих колагенових волокон;
- дезорганізація м’язових шарів, які гетерогенно розподілені по великій підшкірній вені та її притоках.
Розтяжність венозної стінки контролюється клітинами колагену, еластину та гладкої мускулатури. Її структурні зміни сприяють патологічному ослабленню і призводять до розширення вен. Надмірне вироблення колагену І типу негативно впливає на еластинові волокна й порушує розташування клітин гладкої мускулатури, а головне – знижує синтез колагену ІІІ типу, який визначає розтяжність та еластичність кровоносних судин. Тому зміни співвідношення між колагеном І та ІІІ типів можуть негативно вплинути на цілісність стінки вени й призвести до її ослаблення та варикозного розширення.
Роль ендотелію та глікокаліксу в патогенезі хронічних захворювань вен
При ХЗВ помітно змінюється структура глікокаліксу, через ушкодження якого виникає ендотеліальна дисфункція, що супроводжується появою запальних клітин та запалення. Ендотелій та глікокалікс за допомогою спеціалізованих рецепторів реагують на зміни напруги зсуву (розтягнення судин при гіпертензії) та експресують молекули адгезії, що дозволяє активувати лейкоцити. Активовані лейкоцити прикріплюються до ендотелію як венозної стінки, так і клапанів, потім відбуваються процеси діапедезу, які призводять до ушкодження венозної стінки та накопичення запальних клітин. Активація ендотелію, стимуляція захоплення лейкоцитів та вивільнення ряду факторів росту можуть призводити до потовщення гладком’язових клітин судин, утворення неоінтими, зменшуючи просвіт венозної судини.
Крім факторів росту у результаті запалення активуються також матричні металопротеїнази (ММП). ММП – це сімейство щонайменше 25 цинкозалежних ендопептидаз, здатних руйнувати широкий спектр субстратів, включаючи компоненти позаклітинного матриксу, такі як колаген.
Лейкоцити є важливим джерелом ММП, тому активація молекул адгезії й подальша адгезія та інфільтрація лейкоцитів у стінці вени можуть збільшити вироблення та вивільнення ММП. У свою чергу, експресія та активність ММП може бути пов’язана з прогресуванням ХЗВ.
Патогенез больового синдрому при хронічних захворюваннях вен
N. Danziger (2007) у своїй статті про патогенез венозного болю підкреслює, що капілярний і венулярний застій активує ендотеліальні клітини. Це призводить до синтезу й місцевого вивільнення таких медіаторів запалення, як брадикінін, та інших факторів, що активують тромбоцити. У свою чергу, ці медіатори запалення активують С-ноцицептори у стінках капілярів і вен, що призводить до появи дифузного болю, який часто описується як дискомфорт, стиснення або важкість у ногах. Пацієнти з такими симптомами, що вже свідчать про розвиток захворювання, не завжди звертаються до лікаря. Як наслідок, лікарі спілкуються з пацієнтами, у яких уже розвинулися зовнішні ознаки захворювання, із прогресуванням яких симптоми можуть нівелюватися або залишатися «у тіні» домінуючих ознак.
Доповідач наголосила, що для початку терапії не потрібно чекати появи об’єктивних ознак захворювання. На стадії, коли у пацієнта вже виявлено незначний рефлюкс та наявний біль, може бути призначене патогенетичне лікування із застосуванням мікронізованої очищеної флавоноїдної фракції (МОФФ). Згідно з результатами досліджень, застосування МОФФ зменшує інфільтрацію лейкоцитів у судинній стінці та клапанах, пригнічуючи експресію молекул адгезії, розриває порочне коло запалення при ХЗВ. Також МОФФ підвищує тонус вен, покращує мікроциркуляцію та підсилює лімфатичний відтік.
Лікування хронічних захворювань вен
Протягом останнього десятиліття у керівних принципах, оглядах та консенсусних висновках щодо ХЗВ з’являється постійне повідомлення: веноактивні препарати, зокрема МОФФ, ефективні для контролю симптомів на всіх стадіях захворювання, включно з найбільш ранньою стадією хронічних венозних розладів (С0s), коли пацієнти не мають видимих або відчутних ознак венозного захворювання. Роль веноактивних препаратів у менеджменті ХЗВ у настановах 2014-2018 років описується як «центральна та унікальна». Ці керівні принципи також виступають за зміну способу життя у пацієнтів із С0s.
Бесіда з пацієнтом, порівняння отриманих даних клінічного обстеження та інструментальних досліджень й – обов’язково – активне медичне мислення є ключем до встановлення правильного діагнозу та визначення оптимальних підходів до лікування, коли за появи перших симптомів можна уповільнити або запобігти розвитку хвороби, а тим більше її тяжких форм.
 У продовження теми мікросудинних змін при ХЗВ професор Державного університету Ріо-де-Жанейро (Бразилія) Eliete Bouskela у доповіді «Аналіз зміни мікроклапанів та оцінки ефективності лікування МОФФ в експериментальній моделі венозної гіпертензії» представила результати власних досліджень. За допомогою ортогональної поляризаційної спектральної візуалізації із застосуванням цитоскану дослідники визначили, який малюнок мають капіляри в нормі та на різних стадіях ХЗВ:
У продовження теми мікросудинних змін при ХЗВ професор Державного університету Ріо-де-Жанейро (Бразилія) Eliete Bouskela у доповіді «Аналіз зміни мікроклапанів та оцінки ефективності лікування МОФФ в експериментальній моделі венозної гіпертензії» представила результати власних досліджень. За допомогою ортогональної поляризаційної спектральної візуалізації із застосуванням цитоскану дослідники визначили, який малюнок мають капіляри в нормі та на різних стадіях ХЗВ:
- норма – у центрі дермального сосочка незмінений капіляр, розширення вен відсутнє;
- С1 – морфологія капілярів порушена, наявні телеангіектазії;
- С2-3 – дуже змінені капіляри, присутній набряк;
- С4 – крім змін капілярів та набряку присутнє потемніння дермальних сосочків;
- С5 – капіляри виглядають як клубочки, дермальні сосочки ще більш темні.
Також автори визначали функціональну щільність капілярів (кількість капілярів), діаметр дермального сосочка, найбільший діаметр капіляра в основній частині, середній діаметр усіх капілярів та морфологію капілярів.
При прогресуванні ХЗВ, особливо вище стадії С4, відбувалося зменшення функціональної щільності капілярів, що відповідало гіпоксії тканин. Діаметр дермального сосочка, навпаки, із розвитком ХЗВ збільшувався вже на стадії С3. Діаметр основи капіляра також починав збільшуватися на стадії С3. При цьому середній діаметр капілярів збільшувався вже починаючи зі стадії С2. Так само із цієї стадії починала збільшуватись кількість різних типів капілярів.
Професор із командою також оглядали пацієнтів із ХЗВ на безсимптомній стадії С0 (30 жінок) та симптоматичній C0s (20 жінок) і з’ясували, що у хворих вже є зміни мікроциркуляції навіть на стадії С0. Чим більше змін відзначалося на мікроциркуляторному рівні, тим гіршим був перебіг і тяжчими симптоми.
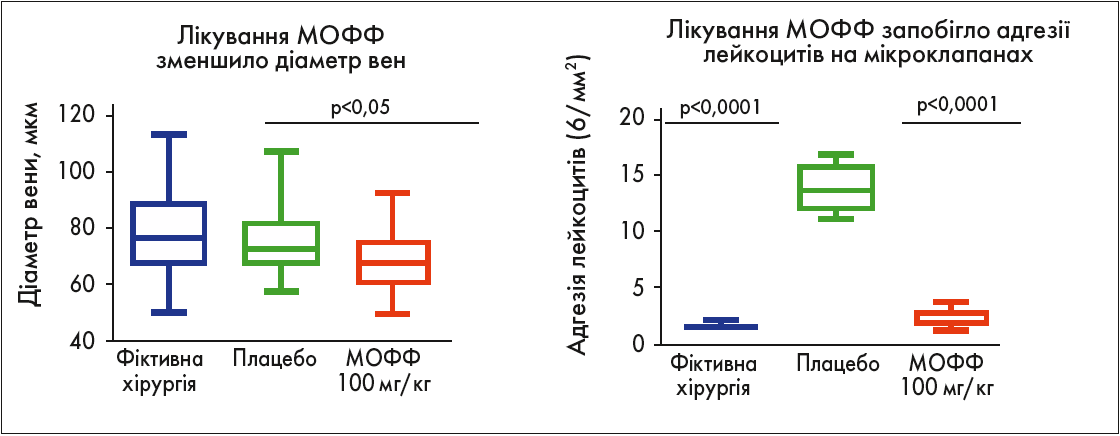
Також під час дослідження була створена експериментальна модель ХЗВ для оцінки ефективності веноактивних препаратів. Застосування МОФФ зменшує набряк, запобігає збільшенню діаметра вен та знижує щільність капілярів, а також зменшує кількість лейкоцитів та їх наближення до стінок капілярів (рисунок).
Рис. Вплив МОФФ на діаметр вен та адгезію лейкоцитів в експериментальній моделі ХЗВ
Терапія із застосуванням МОФФ майже повністю запобігла адгезії лейкоцитів на мікроклапанах (p<0,0001) і зменшила венозний діаметр (p<0,05) порівняно з контрольною групою (плацебо). Венозна протизапальна та венотонізуюча дія МОФФ була продемонстрована на рівні мікроклапанів, що вказує на її здатність запобігати прогресуванню венозного захворювання.
Професор Івано-Франківського національного медичного університету, доктор медичних наук Ростислав Васильович Сабадош у доповіді «Класифікаційна система СЕАР як стандарт звітності, перегляд 2020» презентував головні зміни нового перегляду системи СЕАР. Насамперед доповідач наголосив на важливості розмежування двох основних термінів класифікації – «хронічні венозні розлади» та «хронічні венозні захворювання».
у доповіді «Класифікаційна система СЕАР як стандарт звітності, перегляд 2020» презентував головні зміни нового перегляду системи СЕАР. Насамперед доповідач наголосив на важливості розмежування двох основних термінів класифікації – «хронічні венозні розлади» та «хронічні венозні захворювання».
- Термін «хронічні венозні розлади» (ХВР) включає у себе увесь спектр морфологічних та функціональних порушень венозної системи.
- Термін «хронічні захворювання вен» (ХЗВ) позначає будь-які довготривалі морфологічні та функціональні порушення венозної системи, що проявляються венозними скаргами й/або об’єктивними симптомами, які потребують обстеження й/або лікування хворого.
Отже, ХЗВ є складовою частиною ХВР і включає у себе всі клінічні класи за класифікацією СЕАР, крім С0а, натомість як ХВР може мати місце і при клінічному класі С0а. Тривало існуючі ХВР переростають у ХЗВ, як тільки починають проявлятися венозними скаргами або об’єктивними симптомами.
Венозні скарги включають поколювання, печіння, свербіж шкіри, ломоту, біль, м’язові судоми, набряк, відчуття пульсації, тяжкість у ногах, втомлюваність ніг, синдром неспокійних ніг (посилюються під вечір та за високої зовнішньої температури й зменшуються після відпочинку та підняття ніг догори).
Об’єктивні венозні симптоми (за СЕАР) – це телеангіектазії, ретикулярні або розширені вени, набряк ніг, трофічні зміни шкіри, гіперпігментація, екзема, біла атрофія шкіри, соrоnа phlebectatica, виразки.
Оновлення класифікації СEAP
Як відомо, кожна літера класифікації СEAP має своє значення, а саме: С – клінічна картина, E – етіологія, A – анатомія, P – патофізіологія. Правильна ідентифікація ХЗВ за цією класифікацією дозволяє покращити комунікацію між лікарями різних спеціальностей і підібрати коректне лікування.
Критерій С (Clinical)
Критерій С зазнав важливих змін. Зокрема, були додані дескриптори, що дозволяють позначити рецидиви ХЗВ:
- С2r – повторне варикозне розширення вен;
- С6r – повторна активна венозна виразка.
Також з’явився дескриптор С4с для позначення сorona phlebectatica, і цей стан було віднесено до тяжких проявів хронічних венозних проблем. Однак через назву дескриптора С4с можливе хибне уявлення, що ця проблема більш тяжка, ніж ліподерматосклероз (С4b) чи екзема (С4a).
Також дуже важливо після виставлення дескриптора С вказати, яким є перебіг захворювання – симптоматичним (s) чи асимптомним (а).
Критерій E (Ethiologic)
Внесено зміни щодо критерію E. Так, вторинне ХЗВ було розділено на інтравенозне (Esi) та екстравенозне (Ese).
- Вторинне інтравенозне – ушкодження стінок вен і/або клапанів, що виникає внаслідок будь-яких внутрішньовенозних захворювань: тромбозу глибоких вен (ТГВ), травматичних артеріовенозних нориць, первинної внутрішньовенозної саркоми або інших внутрішньопросвітних змін вен.
- Вторинне екстравенозне – немає ушкоджень венозної стінки або клапанів, проте симптоми є внаслідок стану, що впливає на гемодинаміку вен, місцево чи системно: центральна венозна гіпертензія (ожиріння, застійна серцева недостатність, «синдром Лускунчика», синдром тазового повнокрів’я), зовнішня компресія (позавенна пухлина та місцевий фіброз, зокрема ретроперитонеальний) або дисфункція м’язової помпи внаслідок рухових порушень (параплегія, артрит, хронічна нерухомість, адгезивний капсуліт або постійне сидяче положення).
- Дескриптор Ес так само призначений для позначення природженого ХВР (етіологічні чинники присутні з народження і пов’язані з порушеннями розвитку венозної системи).
- Дескриптором Ep позначають первинний ХЗВ (немає ознак, які могли б класифікувати ХЗВ як вторинний чи природжений). Первинний ХЗВ – це дегенеративний процес венозного клапана й/або венозної стінки, що призводить до слабкості та розширення клапана й/або стінки вени, зумовлюючи розвиток патологічного рефлюксу, виявленого за допомогою візуалізаційних методів;
- Дескриптор En залишився для позначення ХЗВ невстановленої етіології.
У новому перегляді класифікації СEAP можна вказувати кілька етіологічних чинників. Наприклад, первинне варикозне розширення вен (Ер) може мати місце до тромбозу глибоких вен (ТГВ). Якщо після ТГВ виникає посттромботичний синдром (Еsі), то етіологія ХВР у такого пацієнта має бути описана як «Еpsi» (тобто первинна «р» і вторинна інтравенозна «si»).
Критерій А (Anatomic)
Щодо критерію А також внесено зміни. Раніше уражені вени у класифікації потребували відповідного цифрового позначення, яке зараз змінено на абревіатури. Також до класифікації було додано притоку малої підшкірної вени – передню додаткову велику підшкірну вену, однак дотепер немає можливості відобразити всі притоки вен. Що стосується глибоких вен, то було деталізовано осьові міжм’язові вени гомілки: малогомілкові, передньо- та задньовеликогомілкові (раніше всі ці вени мали одне цифрове позначення). Також були деталізовані внутрішньом’язові вени гомілки – литкові та камбалоподібні (також раніше позначалися однією цифрою).
Критерій Р (Pathophysiologic)
Критерій Р майже не зазнав змін. Дескриптор Pr позначає рефлюкс, Po – оклюзію, Pro – рефлюкс з оклюзією, Pn – відсутність ідентифікованих патофізіологічних змін. Після кожного значення критерію Р повинні вказуватися не цифри, а нові скорочення відповідних уражених вен.
У класифікації СЕАР також обов’язково вказується дата (у круглих дужках після всіх дескрипторів СЕАР), права або ліва уражена кінцівка (квадратні дужки перед дескрипторами СЕАР) та рівень обстеження (після дати у круглих дужках).
Рівні обстеження пацієнтів
- рівень I (L І): фізикальне обстеження пацієнта (скарги, анамнез, огляд), яке може включати використання портативного доплер-сканера;
- рівень ІI (L ІІ): неінвазивне дослідження судин, яке включає колірне дуплексне (триплексне) сканування й, за бажанням, плетизмографію;
- рівень IIІ (L III): інвазивні або більш складні візуалізаційні дослідження, включаючи висхідну та низхідну флебографію, вимірювання венозного тиску, комп’ютерно-томографічну флебографію або магнітно-резонансну томографію.
Відмінності між базовим і вдосконаленим варіантами класифікації СЕАР
Після позначення клінічного класу С у базовому варіанті слід вказувати лише один, найвищий, дескриптор, а у вдосконаленому – усі. Наприклад, у пацієнта з варикозним розширенням вен, набряком та гіперпігментацією у базовому варіанті необхідно записати «С4а», а у вдосконаленому – «С2, 3, 4а».
У базовому варіанті класифікації СЕАР після позначення патофізіологічного діагнозу не вказують абревіатури конкретних уражених вен чи їхніх сегментів.
Третє засідання 2-го Міжнародного флебологічного мітингу було присвячено тазовим венозним розладам.

Спеціаліст з ультразвукової діагностики, асистент кафедри оперативної хірургії з топографічною анатомією Львівського національного медичного університету ім. Данила Галицького Марія Глібівна Орел у доповіді «УЗД тазових венозних розладів» зосередила увагу на перевагах ультразвукового дуплексного сканування (УЗДС), яке є неінвазивним методом, що дозволяє успішно провести обстеження вен заочеревинного простору та ділянки таза. Доповідач представила результати власних спостережень, під час яких було виявлено істотну різницю в діаметрах вен параметрія для всіх груп вагітних обстежуваних порівняно з невагітними. Також діаметр вен параметрія справа істотно зростав відповідно до терміну вагітності. При цьому УЗДС було ефективним методом для виявлення компресії лівої загальної клубової вени біфуркацією аорти та лівою загальною клубовою артерією (синдром Мея – Тернера).

Завідувач кафедри хірургії № 2 Львівського національного медичного університету ім. Данила Галицького, доктор медичних наук, професор Ігор Іванович Кобза представив доповідь «Сучасні підходи до лікування синдрому Nutcracker», у якій поділився власним клінічним досвідом. Спікер показав, що транспозиція лівої ниркової вени в нижню порожнисту вену демонструє свою ефективність як у ранньому, так й у віддаленому післяопераційному періоді і є золотим стандартом лікування «синдрому Лускунчика» з тяжкою тривалою симптоматикою.

Завідувач кафедри госпітальної хірургії Запорізького державного медичного університету, доктор медичних наук, професор Андрій Олександрович Ніконенко у доповіді «Власний досвід лікування хворих із тазовим венозним порушенням» наголосив на важливості дотримання протоколу обстеження в діагностиці хронічного тазового з болю з метою виключення супутньої патології. Також він зауважив, що планування хірургічного втручання має ґрунтуватися на даних УЗД, мультиспіральної комп’ютерної томо- та флебографії з урахуванням патологічного венозного кровотоку.

Професор Лариса Михайлівна Чернуха та керівник Аngiology expert centre Verum, кандидат медичних наук Олена Анатоліївна Власенко представили спільну доповідь «Лікування тазових венозних розладів. Коли і що робити? Що говорять сучасні рекомендації?», у якій зазначили, що комп’ютерна томографія не може бути остаточним методом підтвердження «синдрому Лускунчика». Необхідно провести флебографію з вимірюванням градієнта тиску в лівій нирковій та нижній порожнистій венах. Якщо підтверджується «синдром Лускунчика», синдром Мея – Тернера або післятромботичний синдром, стентування або реконструктивну операцію проводять відповідно до рекомендацій. Лікування цих синдромів слід проводити у спеціалізованих центрах. У разі недостатності клапанів гонадних вен у чоловіків та жінок із відповідними клінічними ознаками методом вибору є ендоваскулярне та ендовенозне лікування із застосуванням спіралей та ендовенозних термічних методик. Перші результати застосування останніх у лікуванні синдрому хронічного тазового венозного повнокрів’я, викликаного недостатністю клапанів гонадних вен, є обнадійливими. Протягом тривалого періоду (до 6 років) рецидивів болю та варикозного розширення вен параметрія не спостерігалося.
Своєчасне лікування, спрямоване на нормалізацію порушеної структури венозного кровотоку та хронічного запалення, які лежать в основі ХЗВ, може зменшити симптоми й ознаки цієї патології. Краще розуміння патогенезу венозного захворювання, зокрема його молекулярних механізмів, дозволить обрати патогенетично спрямоване фармакологічне лікування та персоналізовану тактику хірургічного втручання.
Читати продовження >>
Підготувала Анастасія Романова
CVD-NonP-C1(2021-2022)-1