18 лютого, 2022
20-річний досвід лікування пацієнтів із хворобою Гоше 1 типу
За даними Національної дитячої спеціалізованої лікарні «Охматдит», на хворобу Гоше (ХГ) страждають 70 українців. Це найчастіша орфанна лізосомальна хвороба накопичення, що успадковується за автосомно-рецесивним типом. Захворювання може проявитися з раннього віку та суттєво вплинути на функцію багатьох органів, тому своєчасне патогенетичне лікування є основою збереження якості життя пацієнта. 23 грудня на науково-практичній конференції, присвяченій діагностиці та лікуванню гематологічних захворювань, старший науковий співробітник ДУ «Інститут гематології та трансфузіології НАМН України» (м. Київ), кандидат медичних наук Олена Анатоліївна Кисельова поділилася результатами 20-річного досвіду лікування ХГ іміглюцеразою (Церезим® 400 ОД)* у світі.
ХГ – захворювання, спричинене дефіцитом ферменту кислої β-глюкозидази, що зумовлює накопичення в лізосомах глюкозилцераміду. Виокремлюють 3 різновиди ХГ: тип 1 – ненейропатичний, тип 2 – гострий нейропатичний, тип 3 – хронічний нейропатичний. ХГ із часом може поступово знижувати якість життя та спричиняти вісцеромегалію, тобто прогресуюче збільшення внутрішніх органів (гепатомегалію, спленомегалію), затримку росту, початку статевого дозрівання в дітей, біль у кістках, остеонекроз, переломи, тромбоцитопенію, коагулопатію, анемію. Гематологічні зміни клінічно проявляються кровотечами, утворенням синців і втомлюваністю. Слід зазначити, що в багатьох пацієнтів можуть бути рентгенологічні ознаки захворювання кісток за відсутності вісцеромегалії та гематологічних симптомів.
Діагностика
Для встановлення діагнозу ХГ слід провести аналіз активності ферменту глюкоцереброзидази крові; цей аналіз призначається після виключення всіх можливих гематологічних злоякісних новоутворень (наприклад, лейкемії, лімфоми, множинної мієломи), імунної тромбоцитопенічної пурпури, портальної гіпертензії, що виникла як наслідок захворювання печінки. Натомість пацієнтам, у яких діагностовано ідіопатичну спленомегалію, тромбоцитопенію, що не піддається лікуванню, гіперферитинемію з нормальним насиченням трансферину, появу синців або кровотечу невідомої етіології, необхідно провести аналіз рівня ферменту глюкоцереброзидази. Зниження вмісту цього ферменту дозволяє встановити діагноз ХГ.
Лікування
Оптимальне лікування ХГ передбачає як специфічну патогенетичну, так і симптоматичну терапію. Для усунення симптомів застосовують знеболювальні засоби, біфосфанати, препарати заліза. Пацієнту також може бути запропоноване хірургічне лікування. Патогенетичне лікування базується на ферментнозамісній та субстрат-знижувальній терапії. Поєднання цих двох підходів дозволяє максимально довго зберігати оптимальну якість життя пацієнта. Відносно нещодавно на фармацевтичному ринку з’явилися препарати для субстрат-редукуючої терапії, яка проводиться перорально та запобігає накопиченню субстрату в лізосомах клітин. Однак наразі в Україні препарати з таким механізмом дії не зареєстровані, тому на сьогодні основна роль у лікуванні пацієнтів із ХГ належить ферментнозамісній терапії. Її підхід полягає у внутрішньовенному введенні з певними часовими проміжками біологічних лікарських засобів. Застосування препаратів з таким механізмом дії дозволяє заміщувати недостатню ферментну активність, таким чином коригуючи первинну патофізіологію та попереджаючи вторинну патологію. Як ферментозамісне лікування широкого використання набула іміглюцераза. Це єдиний схвалений в Європейському Союзі препарат для лікування ХГ 3 типу. Задокументований досвід застосування іміглюцерази при 150 вагітностях переконливо доводить її безпечність для плода. Терапія із застосуванням іміглюцерази прередбачає індивідуалізований підхід, оскільки його доза визначається індивідуально для кожного хворого.
Дослідження впливу іміглюцерази на перебіг ХГ
За 20 років Міжнародною групою співпраці щодо ХГ (ICGG) зареєстровано 6446 пацієнтів, які страждають на цю патологію. Для порівняння даних за 10 і 20 років із даними на вихідному рівні (до початку лікування) здійснено аналіз серед пацієнтів із ХГ 1 типу, що отримували алглюцеразу/іміглюцеразу протягом ≥17 років (475 пацієнтів). У процесі дослідження вплив іміглюцерази на гематологічні показники визначався за вмістом гемоглобіну (г/дл), кількістю тромбоцитів (×109/л), наявністю анемії та тромбоцитопенії, а оцінка вісцеральних показників – за об’ємом печінки та селезінки (наявністю гематомегалії, спленомегалії). Визначення впливу лікування іміглюцеразою на кісткову систему оцінювалося за показниками наявності болю в кістках і кісткових кризів. Окрім того, в дослідженні враховувалися антропометричні дані пацієнтів (зріст, маса тіла, індекс маси тіла).
Результати гематологічних і вісцеральних показників після лікування іміглюцеразою
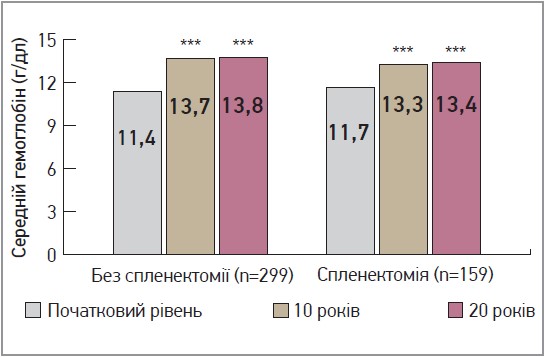
- При застосуванні іміглюцерази концентрація гемоглобіну підвищилася до нормального рівня через 10 років і залишалася в межах норми через 20 років (≥12 г/дл для чоловіків, 11 г/дл для жінок) (рис. 1).
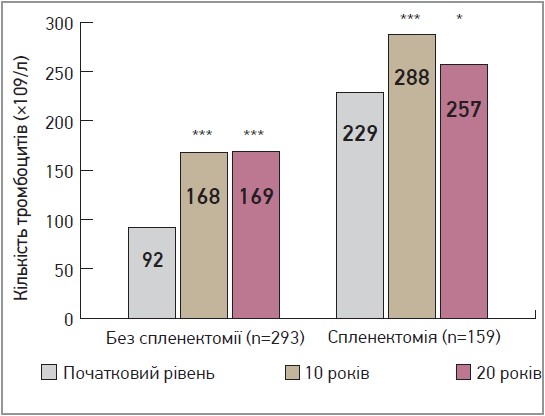
- Рівень тромбоцитів підвищився до значення норми (180-320×109/л) в пацієнтів зі збереженою селезінкою через 10 років, а в хворих після спленектомії цей показник залишався в межах норми через 10 років. Загалом в усіх пацієнтів рівень тромбоцитів залишався в межах норми через 20 років (рис. 2).
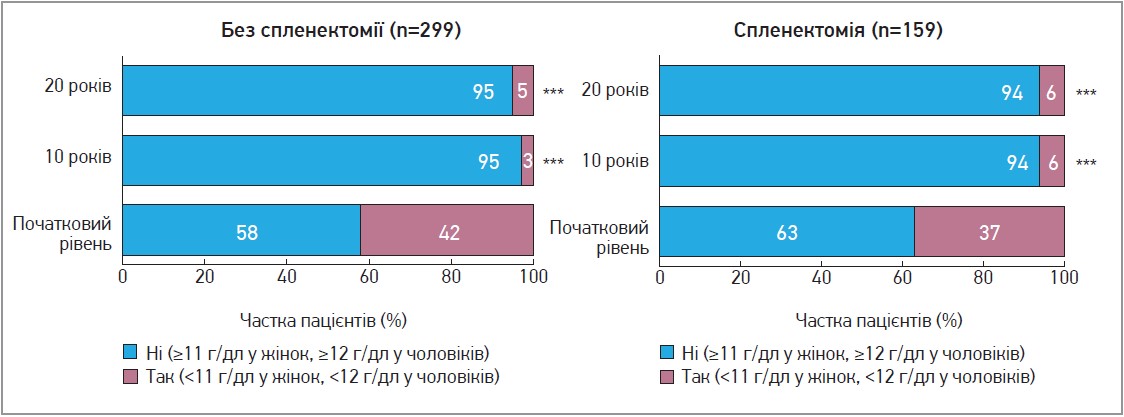
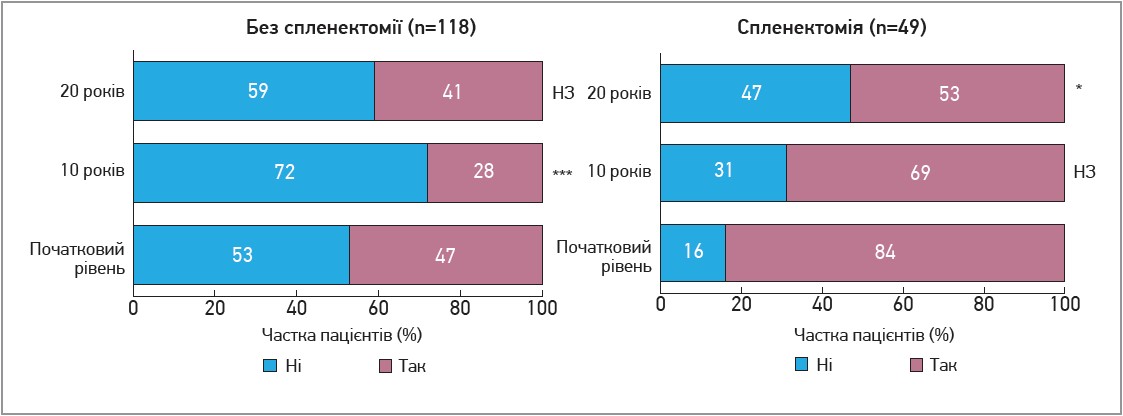
- Частка пацієнтів з анемією зменшилася через 10 років і залишилася низькою через 20 років (рис. 3).
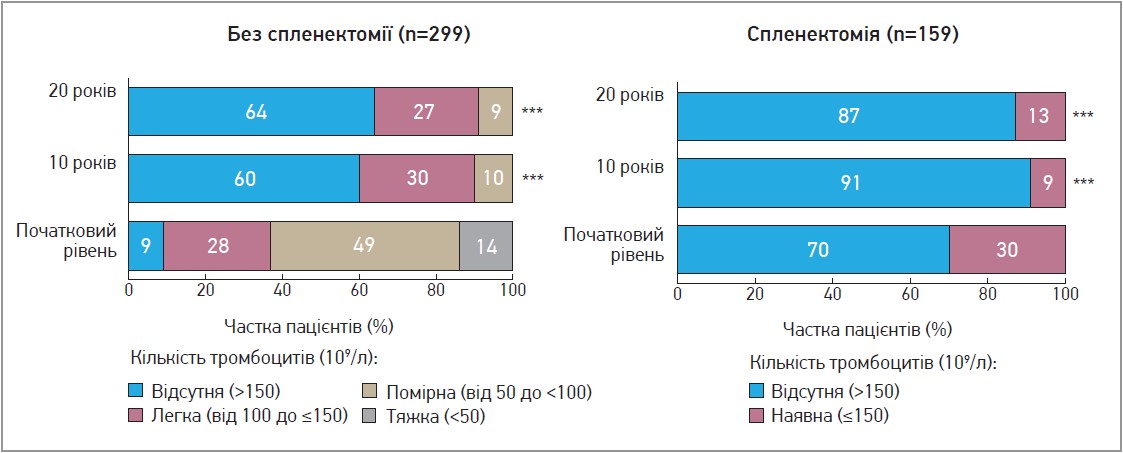
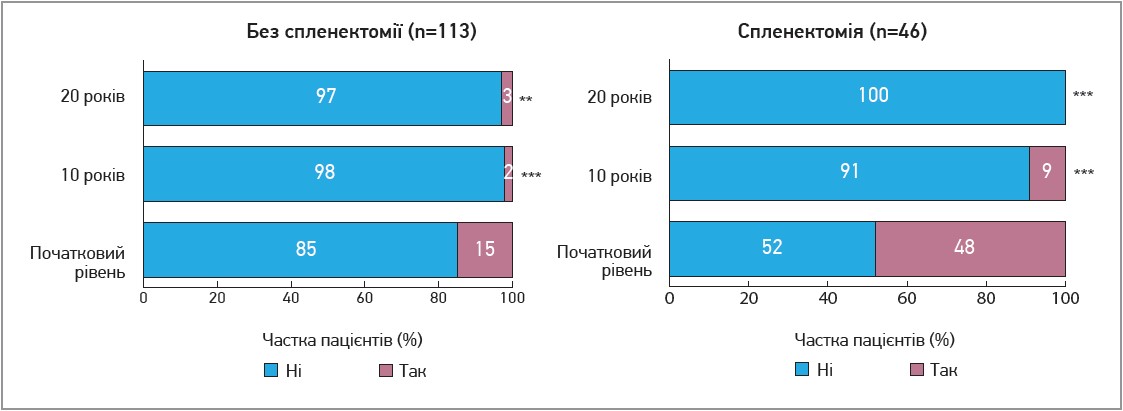
- Відсоток пацієнтів із тромбоцитопенію та ступінь тяжкості тромбоцитопенії знизилися через 10 років і залишалися низькими через 20 років (рис. 4).
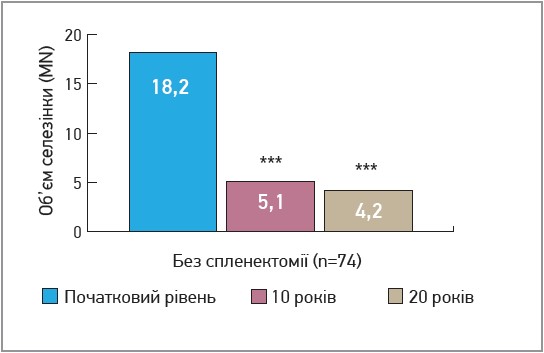
- Розмір селезінки значно зменшився через 10 років і його нормальний показник зберігався через 20 років (рис. 5).
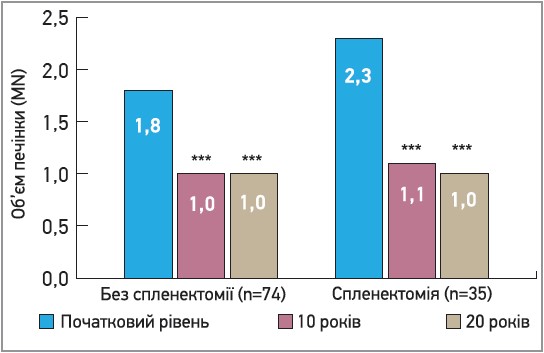
Розмір печінки відновився до норми чи майже до норми через 10 років і це покращення зберігалося через 20 років (рис. 6).
Показники стану кісткової системи після лікування іміглюцеразою
У клінічних дослідженнях, а також за результатами аналізу реєстру хворих із ХГ (ICGG) за 20 років зібрано значний масив доказових даних щодо іміглюцерази, при застосуванні якої було показано поліпшення основних параметрів з боку кісток, таких як біль, кісткові кризи, прояви аваскулярного некрозу та остеопенії (рис. 7, 8).
- Кістковий біль зменшився через 10 та 20 років у пацієнтів після спленектомії. Відзначено статистично незначимі результати щодо пацієнтів зі збереженою селезінкою.
- При застосуванні іміглюцерази не спостерігалося розвитку кісткових кризів навіть у пацієнтів після спленектомії, які мали кризи до початку лікування. Вони значно зменшилися через 10 років; у цих пацієнтів поліпшення тривало й через 20 років.
- Кількість пацієнтів із кістковим болем в анамнезі була меншою через 10 та 20 років лікування, ніж на вихідному рівні.
- При застосуванні іміглюцерази в пацієнтів, у яких лікування було розпочато в дитинстві, нормалізувалися зріст, маса тіла, індекс маси тіла.
- Загалом у групах пацієнтів із ХГ легкого, середнього та тяжкого ступенів на тлі прийому іміглюцерази спостерігали значне покращення гематологічних, вісцеральних, кісткових показників через 10 і 20 років порівняно з вихідним рівнем.
Іміглюцераза (Церезим® 400 ОД*) вважається препаратом, який є найбільш дослідженим і вже протягом 20 років демонструє свою ефективність. Клінічно значимі покращення результатів з боку кровотворення, внутрішніх органів і кісток досягаються вже в перші роки терапії іміглюцеразою та зберігаються протягом 10 і 20 років лікування.
Рис. 1. Результати лікування іміглюцеразою; гематологічні показники: середня концентрація гемоглобіну (г/дл) на початковому етапі, через 10 (±1,5 року) та 20 років спостереження (±3,0 року) в когорті пацієнтів із наявністю/відсутністю селезінки
Рис. 2. Середня кількість тромбоцитів (×109/л) на початковому етапі, через 10 і 20 років спостереження в когортах пацієнтів із наявністю/відсутністю селезінки
Рис. 3. Частка пацієнтів з анемією та без неї у когортах пацієнтів із наявністю/відсутністю селезінки
Примітки: MN кратне нормі; * p<0,01; ** p<0,001; *** p<0,0001.
Рис. 4. Частка хворих із тромбоцитопенією та без неї у когортах пацієнтів, розподілених на групи за наявністю/відсутністю селезінки
Рис. 5. Результати лікування іміглюцеразою; вісцеральні показники: середній об’єм селезінки (кратність нормі) в пацієнтів без спленектомії
Рис. 6. Результати лікування іміглюцеразою; вісцеральні показники: середній об’єм печінки (кратність нормі) на початковому етапі, через 10 і 20 років із розбивкою за статусом спленектомії
Примітки: MN кратне нормі; *** p<0,0001.
Рис. 7. Частка пацієнтів із болем у кістках та без нього, розподілених на групи за наявністю/відсутністю селезінки
Рис. 8. Частка пацієнтів із кістковими кризами та без них, про які повідомлялося протягом кожного періоду спостереження, з розподілом на групи за наявністю/відсутністю селезінки
Примітки: НЗ – незначимий; * p<0,01; ** p=0,001; *** p<0,001; **** p<0,0001.
* Лікарський засіб Церезим® 400 ОД, порошок для приготування концентрату для розчину для інфузій по 400 ОД, зареєстрований в Україні. Р.П. № UA/8659/01/02. Наказ МОЗ № 1504 від 16.08.2018, зміни внесено Наказ МОЗ № 938 від 14.05.2021.
** Інструкція для медичного застосування лікарського засобу Церезим® 400 ОД, порошок для приготування концентрату для розчину для інфузій по 400 ОД. Р.П. № UA/8659/01/02. Наказ МОЗ № 1504 від 16.08.2018, зміни внесено Наказ МОЗ № 938 від 14.05.2021.
Підготувала Олеся Андронік