20 липня, 2022
Новий гравець – нові можливості: пероральні цефалоспорини в епоху антибіотикорезистентності
 У листопаді 2021 року у форматі онлайн відбувся IV Міжнародний конгрес Antibiotic resistance STOP, час проведення якого збігався з Всесвітнім тижнем поінформованості про антибіотики. Захід об’єднав провідних спеціалістів медичної галузі для розробки стратегії щодо контролю над розвитком антибіотикорезистентності. У рамках робочої програми конференції провідний науковий співробітник ДУ «Національний інститут фтизіатрії і пульмонології ім. Ф.Г. Яновського НАМН України (м. Київ), доктор медичних наук Ярослав Олександрович Дзюблик представив доповідь, присвячену місцю группи цефалоспоринових антибактеріальних препаратів у лікуванні бактеріальних інфекцій.
У листопаді 2021 року у форматі онлайн відбувся IV Міжнародний конгрес Antibiotic resistance STOP, час проведення якого збігався з Всесвітнім тижнем поінформованості про антибіотики. Захід об’єднав провідних спеціалістів медичної галузі для розробки стратегії щодо контролю над розвитком антибіотикорезистентності. У рамках робочої програми конференції провідний науковий співробітник ДУ «Національний інститут фтизіатрії і пульмонології ім. Ф.Г. Яновського НАМН України (м. Київ), доктор медичних наук Ярослав Олександрович Дзюблик представив доповідь, присвячену місцю группи цефалоспоринових антибактеріальних препаратів у лікуванні бактеріальних інфекцій.
Ключові слова: цефдінір, цефалоспорини, антибіотикотерапія, алергія на пеніцилін, пероральні антибіотики.
 Іще в 1945 р. італійським професором Джузеппе Бротцу був виділений плісневий гриб Cephalosporium acremonium, в якого виявилася здатність пригнічувати розмноження Salmonella typhi. Із цього гриба було синтезовано антибіотик (АБ) цефалоспорин C. Він широко застосовується в клінічній практиці і став прародичем класу АБ, відомого як цефалоспорини.
Іще в 1945 р. італійським професором Джузеппе Бротцу був виділений плісневий гриб Cephalosporium acremonium, в якого виявилася здатність пригнічувати розмноження Salmonella typhi. Із цього гриба було синтезовано антибіотик (АБ) цефалоспорин C. Він широко застосовується в клінічній практиці і став прародичем класу АБ, відомого як цефалоспорини.
На прикладі представлених нижче клінічних випадків розглянемо проблему вибору антибактеріального препарату залежно від конкретної клінічної ситуації.
Клінічний випадок 1
Пацієнт, 67 років, звернувся за медичною допомогою зі скаргами на задишку під час незначного фізичного навантаження, інтенсивність якої суттєво збільшилась, на підвищення температури тіла до 37,4 °C, кашель із виділенням мокротиння темно-жовтого кольору, відчуття скутості в грудній клітці, пітливість і слабкість. Хворіє 3 дні, після перевтоми і переохолодження на риболовлі. В анамнезі – куріння протягом 30 років (до 2015 року). 2008 року встановлено діагноз – хронічне обструктивне захворювання легень (ХОЗЛ). Натепер для лікування отримує сальметерол/флутиказон у дозах 50/500 мкг по 1 інгаляції двічі на добу; тіотропій у дозі 18 мкг 1 інгаляція 1 р./добу, сальбутамол – за потреби. Перкуторно над легенями коробковий звук. Аускультативно дифузно різко послаблене дихання, розсіяні сухі низькотональні хрипи на видиху. ПЛР тест на SARS-CoV-2 негативний. Рентгенологічно: дифузний пневмосклероз, явища емфіземи, вогнищевих та інфільтративних змін не виявлено. За даними спірометрії (ОФВ1 = 46%, ФЖЄЛ = 87,5%, ОФВ1/ФЖЄЛ = 0,43) пацієнта було віднесено до групи GOLD 2. Таким чином, у пацієнта було встановлено діагноз ХОЗЛ, фаза інфекційного загострення.
Клінічний випадок 2
Пацієнт, 33 роки, індекс маси тіла 31,3 кг/м2, захворів гостро – із підвищенням температури тіла до 39,2 °C, кашлем із виділенням мокротиння коричнево-сірого кольору, болем у правій половині грудної клітки, зі слабкістю і пітливістю. Хворіє 5 днів, застосовував парацетамол, німесулід, вітамін С та інгаляцій із декаметоксином без ефекту. В анамнезі – алергія на пеніцилін, також відомо, що пацієнт отримав курс антихелікобактерної терапії (амоксицилін, кларитроміцин) 2 міс тому з приводу виразки 12-палої кишки. Об'єктивно: АТ 150/90 мм рт. ст.; ЧСС 100/хв; SpO2 96%. Над легенями аускультативно послаблене везикулярне дихання над правою легенею і крепітація у 3-4-му міжребер’ї по сосковій лінії справа. У загальному аналізі крові незначний лейкоцитоз зі зсувом формули ліворуч і підвищена ШОЕ (45 мм/год). Комп’ютерна томографія підтвердила наявність інфільтрації в правій легені. Був встановлений діагноз – негоспітальна пневмонія (НП) верхньої частки правої легені, нетяжкого перебігу, 2-га клінічна група.
В обох пацієнтів були показання для проведення антибіотикотерапії. Підхожим варіантом лікування цих пацієнтів виявився препарат ІІІ покоління цефалоспоринів цефдінір, який нещодавно з’явився на українському фармацевтичному ринку під назвою 3-Дінір.
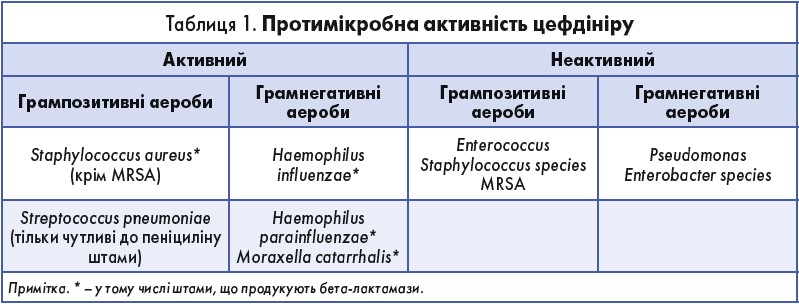
Препарат цефалоспоринів ІІІ покоління – цефдінір (препарат 3-Дінір виробництва ТОВ «АРТЕРІУМ ЛТД», Україна) містить амінотіазольну і вінілову групи. Амінотіазольна група підвищує афінність молекули АБ до пеніцилін-зв’язувального білка бактерій, вінілова група полегшує всмоктування препарату без етерифікації, а тому біодоступність АБ не залежить від прийому їжі. Крім цього перевагою цефдініру є стійкість до більш як 13 основних бета-лактамаз розширеного спектра (табл. 1).
Біодоступність цефдініру становить 16-21% і знижується в разі застосування більших доз препарату і вживання його з жирною їжею.
Максимальної концентрації в крові препарат досягає через 2-4 год після прийому.
Цефдінір не проникає крізь гематоенцефалічний бар’єр, але може подолати плацентарний бар’єр. Дані щодо виділення в грудне молоко відсутні, тому застосування цефдініру не рекомендовано для жінок, які годують груддю.
Препарат практично не зазнає метаболізму і виводиться з організму із сечею переважно в незміненому вигляді (при прийомі 300 мг і 600 мг препарату – відповідно 18,4% і 11,6% прийнятої дози). Період напіввиведення становить 1,7 (±0,6) год, це дає можливість використовувати препарат двічі або один раз на добу, що покращує комплаєнс.
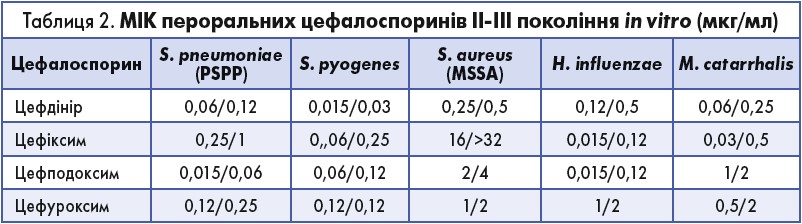
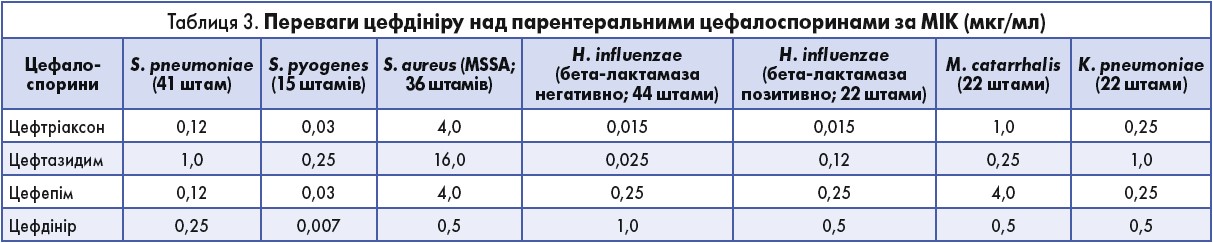
За величиною мінімальної інгібувальної концентрації (МІК) цефдінір має хорошу активність щодо S. pneumoniae, хоча дещо поступається цефподоксиму, але за ефективністю проти Streptococcus pyogenes, Moraxella catarrhalis і Staphylococcus aureus значуще перевершує інші цефалоспорини (табл. 2). Ба більше, активність цефдініру вища за таку парентеральних цефалоспоринів (табл. 3). Таким чином, препарат має суттєві переваги навіть над парентеральними цефалоспоринами і є активним щодо широкого кола збудників.
Отже, 3-Дінір можна застосовувати для лікування інфекцій нижніх дихальних шляхів (ІНДШ), зокрема негоспітальних (спричинених пневмококом, гемофільною паличкою і Moraxella catarrhalis), інфекцій ЛОР-органів (риносинусити, тонзиліти), уражень шкіри і м’яких тканин.
У терапії інфекційних загострень ХОЗЛ або хронічного бронхіту можна застосовувати препарат у дозі 300 мг 2 р./добу або 600 мг 1 р./добу, у разі пневмонії – у дозі 300 мг 2 р./добу.
Можливе застосування З-Дініру в педіатричній практиці, є спеціальна форма випуску – порошок для оральної суспензії для дітей. Так, наприклад, американське товариство педіатрів рекомендує цефдінір для лікування середнього отиту як препарат першої лінії в дітей з алергією на пеніцилін.
Товариство педіатричних інфекційних хвороб і Американське товариство інфекціоністів пропонує застосовувати цефдінір для лікування НП, спричиненої Haemophilus influenzaе, у дітей з алергією на пеніцилін як препарат другого ряду (Bradley et al., 2011).
Відомо, що 50% дітей відмовляються приймати препарати, 75% із них – через неприємний смак, а 90% американських педіатрів називають гіркий смак препарату основною причиною відмови дітей від лікування, тож комплаєнс у цій віковій когорті педіатричної популяції варіює від 11 до 93% (Batchelor and Marriott, 2015; Milne and Bruss, 2008). І в цьому плані вибір – за цефдініром, оскільки він має доволі приємний смак на відміну від більшості дитячих форм АБ, зокрема якщо порівнювати з азитроміцином, ко-тримоксазолом, кларитроміцином, ко-амоксиклавом та ін. – смакова привабливість у порядку спадання: цефдінір >цефіксім >азитроміцин >котримоксазол кларитроміцин > амоксицилін/клавулонат > цефподоксим > цефуроксим (Sader and Jones, 2007).
Отже, дитяча форма 3-Дініру характеризується зручністю дозування, незалежністю від прийому їжі, можливістю однократного застосування, приємними органолептичними властивостями, що в комплексі сприяє кращій прихильності до лікування.
У численних публікаціях підтверджується застосування цефдініру як альтернативи парентеральним цефалоспоринам для лікування ІНДШ, інфекційних уражень шкіри тощо (Anzueto, Bishai and Pottumarthy, 2007; Chatterjee, Moland and Thomson, 2005; Guay, 2002; Sader and Jones, 2007).
За даними дослідження стійкості мікроорганізмів – збудників бактеріальних інфекцій ДШ SOAR, яке проводилося в Україні в період із 2011 до 2018 року, пневмокок має хорошу чутливість до цефдініру (73,3%), те саме стосується й гемофільної палички (100%) (Feshchenko et al., 2016; Torumkuney et al., 2018; Torumkuney et al., 2020).
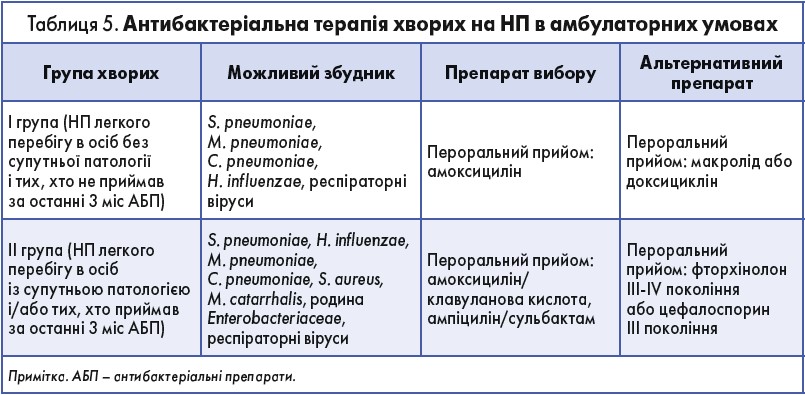
Повертаючися до наведених клінічних випадків, пацієнтові із загостренням ХОЗЛ було рекомендовано цефалоспорини як другу лінію лікування (табл. 4); хворий на НП також мав показання для лікування цефалоспоринами, зважаючи на наявність в анамнезі алергії на пеніциліни і попередню антихелікобактерну терапію (табл. 5).
Отже, перевагами цефдініру (3-Дініру від Артеріум) є можливість його застосування:
- як альтернативи препаратам першої лінії (у тому числі для терапії загострень ХОЗЛ / хронічного бронхіту та пневмонії);
- у пацієнтів із тяжкими захворюваннями печінки;
- за наявності алергії на пеніциліни;
- як пероральний компонент ступеневої терапії.
А з огляду на важливість прийнятного смаку ліків для педіатричної практики, органолептична привабливість дитячої форми випуску цефдініру (3-Дініру) гарантує прихильність маленьких пацієнтів до лікування.
Література
- Anzueto A., Bishai W.R. & Pottumarthy S. (2007). Role of oral extended-spectrum cephems in the treatment of acute exacerbation of chronic bronchitis. Diagnostic microbiology and infectious disease, 57(Suppl 3), 31-38S. https://doi.org/10.1016/j.diagmicrobio.2006.12.003
- Batchelor H.K. & Marriott J.F. (2015). Formulations for children: problems and solutions. British journal of clinical pharmacology, 79(3), 405-418. https://doi.org/10.1111/bcp.12268
- Chatterjee A., Moland E.S. & Thomson K.S. (2005). Cefdinir: an oral alternative to parenteral cephems. Diagnostic microbiology and infectious disease, 51(4), 259-264. https://doi.org/10.1016/j.diagmicrobio.2004.11.015
- Feshchenko Y., Dzyublik A., Pertseva T., Bratus E., Dzyublik Y. et al. (2016). Results from the Survey of Antibiotic Resistance (SOAR) 2011-13 in Ukraine. The Journal of antimicrobial chemotherapy, 71 Suppl 1(Suppl 1), i63-i69. https://doi.org/10.1093/jac/dkw068
- Guay D.R. (2002). Cefdinir: an advanced-generation, broad-spectrum oral cephalosporin. Clinical therapeutics, 24(4), 473-489. https://doi.org/10.1016/s0149-2918(02)85125-6
- Milne C.P. & Bruss J.B. (2008). The economics of pediatric formulation development for off-patent drugs. Clinical therapeutics, 30(11), 2133-2145. https://doi.org/10.1016/j.clinthera.2008.11.019
- Sader H.S. & Jones R.N. (2007). Cefdinir: an oral cephalosporin for the treatment of respiratory tract infections and skin and skin structure infections. Expert review of anti-infective therapy, 5(1), 29-43. https://doi.org/10.1586/14787210.5.1.29
- Torumkuney D., Bratus E., Yuvko O., Pertseva T. & Morrissey I. (2020). Results from the Survey of Antibiotic Resistance (SOAR) 2016-17 in Ukraine: data based on CLSI, EUCAST (dose-specific) and pharmacokinetic/pharmacodynamic (PK/PD) breakpoints. The Journal of antimicrobial chemotherapy, 75(Suppl 1), i100-i111. https://doi.org/10.1093/jac/dkaa087
- Torumkuney D., Pertseva T., Bratus E., Dziublik A. et al. (2018). Results from the Survey of Antibiotic Resistance (SOAR) 2014-16 in Ukraine and the Slovak Republic. The Journal of antimicrobial chemotherapy, 73 (suppl 5), v28-v35. https://doi.org/10.1093/jac/dky069
Підготувала Христина Ключківська
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (57), 2021 р.