23 липня, 2022
Можливості повідон-йоду в профілактиці поширення SARS-CoV‑2
У статті представлені докази віруліцидної активності повідон-йоду (PVP-I) щодо SARS-CoV‑2, а також детально описані механізми профілактичної дії полоскань і промивань ротової порожнини і горла його розчином.
Ключові слова: повідон-йод, COVID‑19, SARS-CoV‑2, антисептик, полоскання горла, промивання ротової порожнини.
Сьогодні значну частину зусиль у боротьбі з пандемією COVID‑19 направлено на впровадження загальної вакцинації для протидії цій інфекції, але перед суспільством і системами охорони здоров’я стоїть не менш важливе завдання – зменшити поширення SARS-CoV‑2. Що передбачає, у тому числі, і заходи соціального дистанціювання, і раціональне використання відповідних засобів індивідуального захисту (ЗІЗ), і дотримання гігієни в лікарнях, а також обережне поводження з біомедичними відходами.
На додаток до цих нефармацевтичних втручань вирішальним фактором, здатним уповільнити поширення вірусу, є ретельне дотримання гігієни порожнини рота з використанням віруліцидних засобів для промивання і полоскання ротової порожнини й горла. Лікарі деяких спеціальностей (стоматологи, отоларингологи тощо) зазнають підвищеного ризику зараження SARS-CoV‑2 через близькість до ротової порожнини, тому саме цій групі ризику рекомендується звернути особливу увагу на запобігання поширенню вірусу шляхом зниження вірусного навантаження SAR-CoV‑2 в ротовій порожнині.
Передопераційне промивання рота за допомогою відповідної віруліцидної рідини вважається основним профілактичним засобом для контролю вірусного навантаження в слині та аерозолі під час і після будь-якої стоматологічної процедури. На основі опублікованих у літературі даних PVP-I, йод із водорозчинним полімером полівінілпіролідоном, є ефективним профілактичним засобом проти коронавірусу (Kirk-Bayley J., 2020). Деконтамінація носової і ротової порожнини за допомогою PVP-I може зменшити кількість аерозольованих вірусних частинок до їх поширення (Pelletier J.S., 2020).
Було проведено ретельний аналіз результатів усіх досліджень, опублікованих у PubMed, ClinicalTrials.gov, EBSCO, Scopus, Web of Sciences, Cochranedatabase, ClinicalTrial.org, Google scholar njoj, щоб зібрати докази ефективності PVP-I проти SARS-CoV‑2 і в запобіганні поширенню інфікування.
Результати дослідження та їх обговорення
На основі досліджень in vitro тимчасові рекомендації Американської стоматологічної асоціації (ADA) щодо мінімізації ризику передачі COVID‑19 пропонують передпроцедурне полоскання ротової порожнини 1,5% перекисом водню або 0,2% PVP-I (Dexter F., 2020; Tessema B., 2020; Bidra A.S., 2020).
Центр із контролю та профілактики захворювань США (CDC) рекомендує перед процедурою промивати ротову порожнину розчинами антисептиків. Варто зазначити, що PVP-I безпечний для використання в ротовій і носовій порожнинах у концентраціях до 1,25% (Rahn R., 1997).
За відсутності доступних препаратів для звичайного стоматологічного використання під час пандемії COVID‑19 рекомендується розбавити 10% PVP-I у співвідношенні 1:20, потім 0,5 мл розведеного розчину PVP-I змішати з 9,5 мл стерильного фізіологічного розчину або інших розчинів, призначених для розведення (Frank S., 2020).
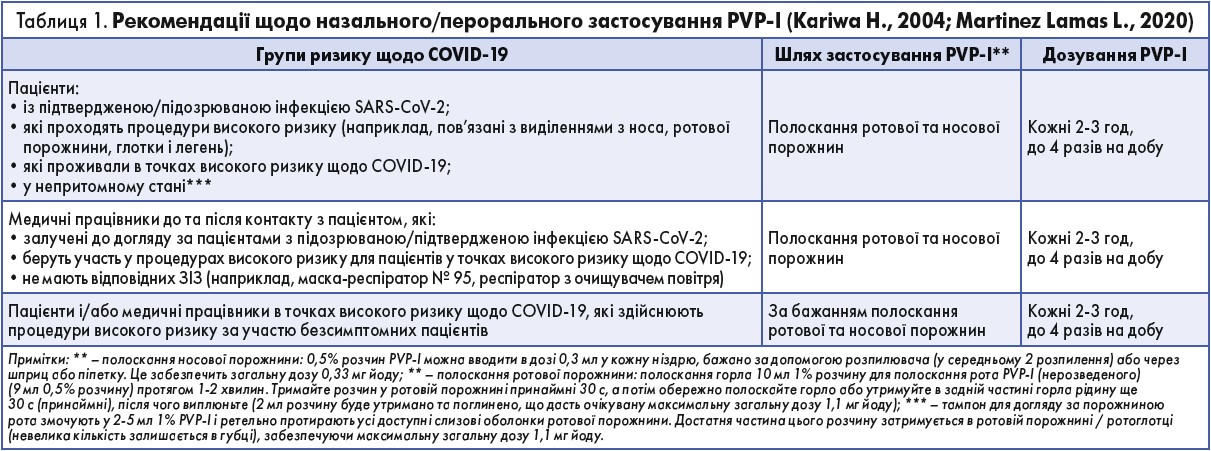
Bidra та співавт. (2020) рекомендують регулярно використовувати 0,5% PVP-I для полоскання ротової порожнини, щоб зменшити ризик внутрішньолікарняної передачі вірусу від безсимптомних носіїв. Також рекомендується часто використовувати оральні та назальні спреї PVP-I у лікарнях із неадекватним забезпеченням ЗІЗ (табл. 1). При цій концентрації поглинання йоду є мінімальним і нижчим за норму загального добового споживання йоду для здорової дорослої людини – 150 г (Frank S., 2020).
Наявні дані підтверджують віруліцидні властивості PVI-P проти SAR-CoV‑2. Передопераційне полоскання ротової порожнини і горла розчином PVP-I є важливою процедурою для запобігання поширенню інфекції під час пандемії COVID‑19.
Обґрунтування використання PVP-I під час інфекції SARS-CoV‑2
Дослідження показали, що різні ділянки ротової порожнини, такі як ясенні щілини, слизова оболонка щік, язик, мигдалини, піднебіння, мікротріщини на поверхні зубів, створюють ідеальну нішу для існування вірусних частинок у пацієнтів, які страждають на вірусні респіраторні інфекції (Pelletier J.S., 2020). Навіть запалення пародонту, спричинене біоплівкою, також пов’язане з розвитком інфекції нижніх дихальних шляхів, яка може спровокувати початок вентиляційної пневмонії (Frank S., 2020).
Багато систематичних оглядів і метааналізів підтвердили важливість ретельної гігієни порожнини рота і використання антисептичних засобів для запобігання респіраторним розладам і внутрішньолікарняним інфекціям (Peng X., 2020). Крім того, підтверджено, що обробка порожнини рота відіграє неабияку роль у регулюванні поширення SARS-CoV‑2, оскільки ротова порожнина «ідентифікована як місце високого ризику інфікування», при цьому слина є основним способом передачі вірусних частинок і потенційним джерелом поширення інфекції в громаді (To K.K. -W., 2019).
Вірусні частинки в інфікованих дихальних рідинах і краплях слини зумовлюють передачу на короткі відстані під час дихання, розмови, кашлю або чхання (Hoffmann M., 2020). Великі краплі слини, діаметр яких перевищує 60 мкм, зазвичай швидко осідають, обмежуючи передачу лише тим особам, які перебувають поблизу джерела інфекції (Tang J.W., 2006). Проте краплі меншого розміру (діаметр ≤60 мкм), які випаровуються і утворюють ядра аерозолю діаметром <10 мкм, мають здатність до передачі на великі відстані (Xu R., 2020).
За оцінками, при кожному чханні виділяється майже 40 тис крапель слини, тому надзвичайно важливо знизити вірусне навантаження цієї біологічної рідини (Edwards D.A., 2004). Дослідження підтвердили, що вірусне навантаження в слині пацієнта, інфікованого COVID‑19, на момент госпіталізації становить 1,2×108 інфекційних копій/мл. З огляду на рівень смертності від COVID‑19, який коливається від 0,39 до 4,05%, ризик передачі від інфікованих госпіталізованих осіб здоровим членам сім’ї, опікунам, медичним працівникам та іншим пацієнтам, які відвідують лікарню, є високим (Huang C., 2020). Ризик передачі інфекції також підвищується для госпіталізованих пацієнтів, які потребують таких процедур, як неінвазивна вентиляція, інтубація та аспірація, що сприяють утворенню біоаерозолю і призводять до внутрішньолікарняної передачі серед медичних працівників (Kirk-Bayley J., 2020).
Дослідження також показали, що SARS-COV‑2 ідентифікується в респіраторних, носових і оральних виділеннях пацієнтів із безсимптомним і слабосимптомним перебігом COVID‑19 (Chan J.F. - W., 2020).
Інфікована людина з вірусом SARS-CoV‑2 може поширити інфекцію майже на 406 осіб за 30 днів (Castagnoli R., 2020). І що важливо, невелика кількість рибонуклеїнової кислоти SARS-CoV‑2 виявляється в секреції слини ще довго після одужання (Rahn R., 1997).
Тому надзвичайно важливо знизити вірусне навантаження в слині та ротоглотці, щоб зупинити нозокоміальну передачу і зменшити внутрішньолікарняне поширення інфекції за допомогою розумного використання антисептичних засобів із віруліцидними властивостями, таких, зокрема, як PVP- I.
Полоскання рота PVP-I виявилося особливо корисним для медичних працівників, переважно стоматологів та отоларингологів. Лікарі зазначених спеціальностей зазнають підвищеного ризику інфікування, оскільки контактують зі слизовою оболонкою ротової порожнини і глотки безпосередньо під час діагностичних і лікувальних процедур, тоді як вірусні частинки залишаються в повітрі протягом 3-4 год, забруднюючи поверхні в навколишньому просторі.
Було показано, що полоскання PVP-I горла / ополіскування рота / використання спрея знижують частоту внутрішньолікарняної пневмонії та супутніх ускладнень і смертності від COVID‑19 майже на 40% (Castagnoli R., 2020). Професійний догляд за порожниною рота разом із ретельним використанням PVP-I може знизити рівень потенційних респіраторних патогенів і частоту аспіраційної пневмонії (van der Maarel-Wierink C.D., 2013). Тому повторне застосування PVP-I для полоскання порожнини рота показане пацієнтам із симптомами SARS-CoV‑2, особливо в перший і другий тиждень після появи ознак хвороби, оскільки вірусне навантаження в секретах ротової порожнини і ротоглотки є найвищим упродовж цього періоду (To K.K. -W., 2020). Також необхідно використовувати PVP-I у безсимптомних пацієнтів, оскільки вони можуть поширювати інфекцію як серед медичних працівників, так і серед оточуючих (Zou L., 2020).
Віруліцидний механізм дії PVP-I
PVP-I є мікробіцидом широкого спектра дії, який інактивує бактерії, гриби, найпростіші та декілька вірусів. Перша публікація про віруліцидні властивості PVP-I у 1975 р. показала, що з його допомогою титри герпесвірусу 2 типу були знижені на 92% (Amstey M.S., 1975). PVP-I може інактивувати віруси як з оболонкою, так і без неї (Wu Z., 2020). PVP-I-умісні засоби для полоскання і спрей для горла ефективні проти ротавірусів, аденовірусів, поліовірусів, вірусу паротиту, Коксакі, герпесу, краснухи, імунодефіциту людини та вірусу грипу (Eggers M., 2019). Найефективніше полоскання горла PVP-I може знизити частоту інфекцій, спричинених Staphylococcus aureus (у тому числі метицилін-резистентний золотистий стафілокок), Pseudomonas aeruginosa та Haemophilus influenzaе, майже на 50% в осіб із діагнозом хронічні інфекції легень / дихальних шляхів (Kanagalingam J., 2015). PVP-I має максимальну віруліцидну активність проти інших широко використовуваних антисептиків, як-от бензетонію хлорид, бензалконію хлорид, хлоргексидину глюконат і алкілдіаміноетілгліцин гідрохлорид (Kawana R., 1997). Якщо порівнювати з іншими антимікробними засобами, недостатньо ефективними проти коронавірусів, ефективність PVP-I щодо SARS-CoV‑2 є доволі вираженою.
Віруліцидна дія PVP-I пояснюється його вільним або незв’язаним йодом/I2, який виділяється в зовнішнє середовище з комплексу PVP-I. У водному розчині I2 та гіпойодиста кислота (HOI) є двома формами елементарного йоду, активними з точки зору антимікробної активності PVP-I (Schreier H. 1997). I2 дестабілізує мембранну оболонку і спричинює лізис вірусних білків (Rothe C., 2020). PVP-I спрямований на ліпідний шар SARS-CoV‑2, як і всіх коронавірусів (O’Donnell V.B., 2020), він також утворює різні комплекси з ненасиченими жирними кислотами та амінокислотами всередині клітини, індукує витікання цитозолю і погіршує синтез білка (Eggers M. 2019). Вільний йод навіть дегенерує нуклеопротеїни вірусних частинок, окисляє нуклеїнові кислоти, змінює метаболічні шляхи, що може спричинити незворотне ураження вірусу. Крім того, вільний йод поглинає вільні радикали, чинячи тим самим протизапальну дію під час вірусних інфекцій (Ito H., 2006).
Докази того, що PVP-I може інактивувати SARS-CoV‑2
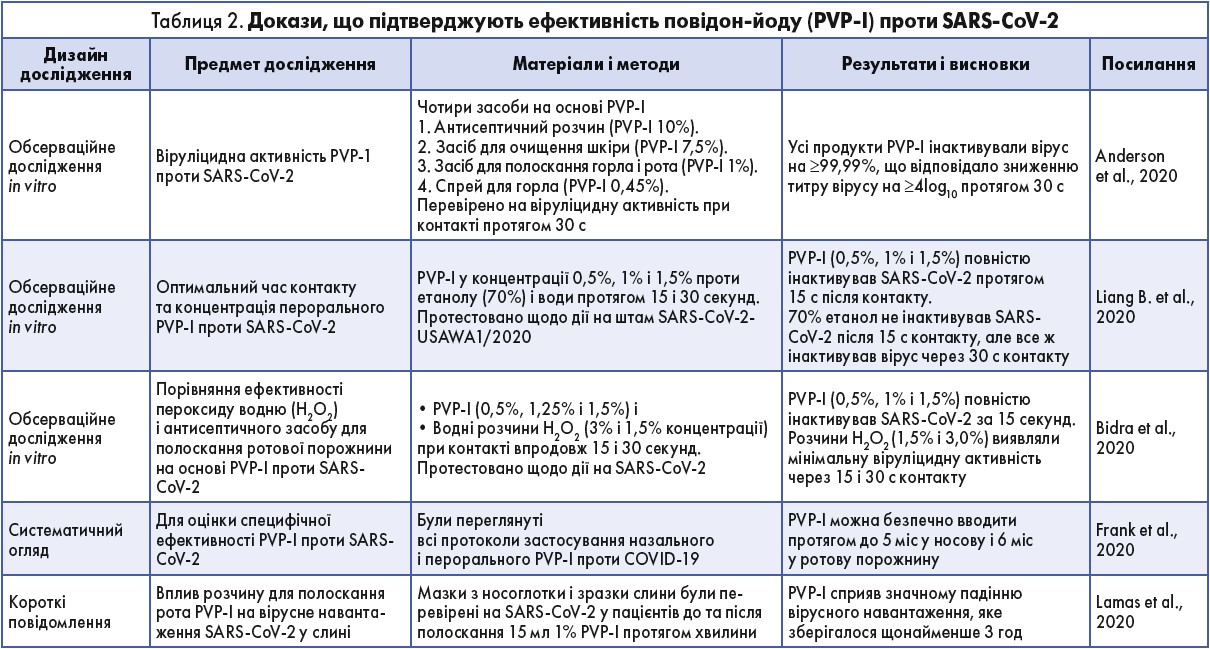
Тривале полоскання з відповідним розведенням PVP-I упродовж більш як 2 хв, до 4 разів на день, рекомендоване для зниження захворюваності на повітряно-крапельні респіраторні інфекції (Kohn W.G., 2003). Тому використання ополіскувача для ротової порожнини PVP-I було запропоноване як профілактична стратегія для ефективної інактивації вірусного навантаження в області рота і глотки, інфікованих SARS-CoV‑2 (Andersen K.G., 2020) (табл. 2). Респіраторне товариство Японії рекомендувало полоскання горла PVP-I для профілактики і лікування госпітальних і негоспітальних респіраторних інфекцій. Ці рекомендації засновані на попередніх дослідженнях, де полоскання горла PVP-I і спрей для горла виявили віруліцидні властивості проти низько- (H5N3, H7N7, H9N2) і високопатогенних штамів пташиного грипу А (H5N1) (Ito H., 2006). Полоскання горла 0,23% розчином PVP-I або використання спрея з PVP-I може значуще знизити вірусне навантаження вірусу пташиного грипу А протягом 10 с (Eggers M., 2018). Крім того, інше дослідження підтвердило ефективність полоскання горла PVP-I проти вірусів свинячого грипу (H3N2, H1N1 і H1N2) (Kariwa H., 2006).
У ході клінічних досліджень у лікарні препарат PVP-I на 58% зменшив кількість епізодів респіраторної інфекції (Nagatake T., 2002). На основі цих доказів міністерство охорони здоров’я, праці та соціального забезпечення Японії випустило рекомендацію щодо використання PVP-I як профілактичного заходу для запобігання інфекції дихальних шляхів після спалаху свинячого грипу H1N1 у 2009 році.
Так само полоскання 0,23-1% PVP-I ротової порожнини протягом 1-2 хв також може знизити вірусне навантаження SARS-CoV‑2 (Liang B., 2020). Liang та співавт. (2020) провели дослідження з оцінки токсичності in vivo та ефективності інактивації SARS-CoV‑2 за допомогою назального спрея PVP-I і офтальмологічних крапель і зробили висновок, що PVP-I може швидко інактивувати SARS-CoV‑2. В іншій статті, опублікованій Martínezet та співавт. (2020), 1% PVP-I знижував вірусне навантаження SARS-COV‑2 у назальних мазках і слині майже до непомітних меж, і ефект тривав 3-4 години. W.H. Chin та співавт. (2020) також виявили, що 7,5% PVP-I сприяв зниженню рівня вірусу SARS-CoV‑2 нижче можливих рівнів протягом 5 хвилин.
Різні країни розробили свої протоколи щодо застосування PVP-I для обробки ротової та носової порожнини під час COVID‑19. У Великій Британії пацієнтам, які перебувають у свідомості та інфіковані COVID‑19, або особам, недостатньо обстеженим на COVID‑19, вводять 0,5% розчин PVP-I 0,3 мл у ніс та 9 мл у ротову порожнину перед будь-якими процедурами (Martínez Lamas L., 2020). Так, пацієнтам без свідомості рекомендується нанесення на слизові оболонки ротової порожнини 2 мл розчину PVP-I. Інший протокол, у Піттсбурзі (штат Пенсильванія, США), рекомендував введення 240 мл 0,4% PVP-I в носову порожнину для промивання пазух і 10 мл 0,5% PVP-I для полоскання ротової порожнини кожні 2-3 год 4 рази на день у пацієнтів із COVID- 19 перед процедурами високого ризику (Mady L.J., 2020). Автор також рекомендував виконувати ці профілактичні заходи медичним працівникам перед оглядом або лікуванням пацієнтів із підозрою чи діагнозом COVID‑19, виконанням процедур високого ризику та в умовах недостатнього забезпечення ЗІЗ.
Більшість із цих протоколів стосуються як пацієнтів із симптомами, так і безсимптомних носіїв. Щоб запобігти перехресному зараженню серед стоматологів, ADA схвалила використання 0,2% PVP- I ополіскувача рота перед усіма стоматологічними процедурами під час пандемії COVID‑19. Оскільки комерційних препаратів PVP-I для звичайного стоматологічного лікування немає, рекомендується розводити 10% PVP-I (1:20), використовуючи 0,5 мл 10% PVP-I і 9,5 мл стерильних водних розчинів або фізіологічного розчину(Pelletier J.S., 2020).
Parhar та співавт. (2020) заявили, що «поки не будуть проведені підтверджувальні дослідження, найкраще розбавити PVP-I фізіологічним розчином (зазвичай 7,5%) у співвідношенні 1:3, щоб досягти концентрації менше 2%. Bidra та співавт. (2020) перевірили різну концентрацію PVP-I (0,5%, 1% і 1,5%) проти SARS-CoV‑2 і дійшли висновку, що всі розведені концентрації інактивували вірус SARS-CoV‑2 протягом 15 секунд. Дослідження також показало, що 70% етанол не інактивував повністю SARS-CoV‑2 навіть після 15 с контакту, але міг інактивувати вірус через 30 секунд. В іншому дослідженні Bidra (2020) in vitro порівнювали інактивацію SARS-CoV‑2 перекисом водню та PVP-I. Результати показали, що під час контакту впродовж 15 і 30 с розчин для полоскання PVP-I в усіх трьох концентраціях – 0,5%, 1,25% і 1,5% – повністю інактивував SARS-CoV‑2. Перекис водню в концентрації 1,5% і 3,0% виявляв мінімальну віруліцидну активність навіть через 30 с контакту.
Нещодавно опубліковане дослідження перевірило віруліцидну активність 8 комерційно доступних ополіскувачів для порожнини рота, що містять різні активні сполуки, проти 3 різних ізолятів SARS-CoV‑2 в умовах, які імітують виділення з носоглотки. Було виявлено, що 1% PVP-I ополіскувач для ротової порожнини значно знижував вірусну активність протягом короткого часу впливу (30 с) (Meister T.L., 2020).
Концентрацію та тривалість застосування розчину PVP-I можна визначити на основі швидкості потоку виділень слизової та слини людини. Оскільки швидкість потоку слини в пацієнта, який перебуває в стані свідомості, низька, а очищення PVP-I повільніше, ніж зазвичай, показана тривала експозиція PVP-I (de Toledo T. -A.,2020). Для повного знищення вірусу продукти PVP-I рекомендується використовувати щонайменше 2 тижні. Це втручання не має на меті вилікувати хворобу, але може значуще зменшити поширення вірусу. Таким чином, особам, які могли контактувати з інфікованими SARS-CoV‑2, або які подорожують чи прибули звідти, точками високого ризику щодо COVID-19, рекомендується часто використовувати ополіскувач PVP-I для зниження вірусного навантаження SARS- CoV‑2 в ділянці ротової порожнини й ротоглотки.
Безпека і переносимість PVP-I
PVP-I для полоскання і промивання рота добре переноситься порівняно з іншими антисептичними засобами, його можна безпечно застосовувати до 5 міс у носовій порожнині і до 6 міс – у ротовій (Challacombe S.J., 2020). У дослідженні in vitro з оцінки безпеки PVP-I на слизовій оболонці ротової порожнини апоптоз клітин відбувався при концентрації 1×102 мМ протягом доби (Mady L.J.,2020). Дослідження in vivo підтвердило, що тривале використання 1-1,25% PVP-I для полоскання горла не подразнює слизову оболонку і не призводить до будь-яких побічних ефектів (протягом 28 міс). Полоскання повідон-йодом не забарвлювало зуби і не змінювало смакові відчуття (Shankar S., 2020). Алергія на PVP-I також спостерігається вкрай рідко, із частотою поширення 0,4% (Eggers M., 2019).
Таким чином, проведені дослідження підтверджують, що застосування PVP-I для полоскання носової та ротової порожнин є простим безпечним недорогим та ефективним засобом профілактики поширення COVID‑19. Завдяки віруліцидній активності PVP-I проти SARS-CoV‑2 його використання у зазначений спосіб дає можливість зменшити ризик перехресної передачі вірусу.
Реферативний огляд Chopraa A., Sivaramanb K., Radhakrishnanc R., Balakrishnanb D., Narayanab A.
Can povidone iodine gargle/mouthrinse inactivate
SARS-CoV‑2 and decrease the risk of nosocomial and community transmission during the COVID‑19 pandemic? An evidence-based update.
Japanese Dental Science Review 57 (2021) 39-45.
Підготувала Анастасія Романова
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (57), 2021 р.