24 січня, 2023
Риногенний головний біль
Риногенний головний біль зазвичай асоціюється з гострим риносинуситом інфекційної етіології із залученням до патологічного процесу верхньощелепної (гайморової) пазухи. Біль розвивається в результаті складних нейрогуморальних рефлексів, локалізується переважно в середній третині обличчя, хоча можуть залучатися й інші ділянки голови [2, 3]. Риногенний головний біль часто помилково вважають іншим захворюванням, наприклад, мігренню, що призводить до неправильного вибору терапевтичної тактики та низької ефективності лікування [4]. Тому важливо правильно діагностувати та належно лікувати цей стан з урахуванням основних патофізіологічних змін, що супроводжують його розвиток.
Патофізіологія та клінічні особливості риногенного головного болю
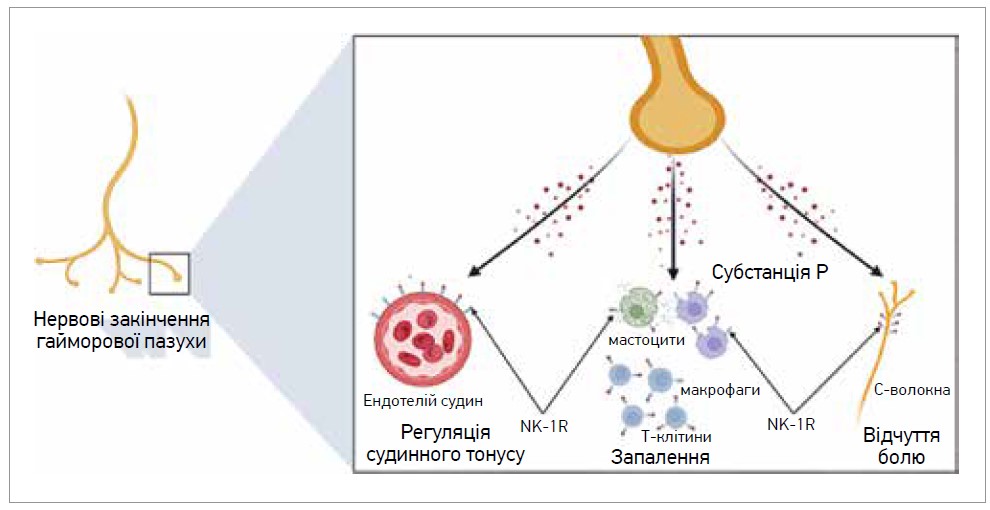
Загалом основною причиною риногенного головного болю є порушення функції приносової пазухи (пазух), яка в нормі забезпечує транспорт утвореного слизу до носової порожнини. Згодом виведений слиз стікає до ротоглотки. Гострий риносинусит спричиняє запалення пазухи, набряк її слизової оболонки, розвиток обструкції устя пазухи з подальшим накопиченням слизу та створенням негативного атмосферного тиску в її порожнині. Зміна тиску спричиняє подразнення аферентних C-волокон трійчастого нерва з подальшим вивільненням ними низки нейропептидів, головним чином субстанції P. Остання сприяє активації запалення, зумовлює підвищення проникності судин, екстравазацію плазми та набряк тканин, які додатково активують аферентні сенсорні волокна трійчастого нерва і підтримують тривале вивільнення вазоактивних й прозапальних молекул (рис. 1). Так відбувається формування хибного кола нейрогенного запалення, яке підтримує ринорею, закладеність носа, біль у носових пазухах і симптоми з боку верхніх дихальних шляхів [5-7]. Наразі відомо, що риногенний головний біль запускається як через класичні механізми больових подразників, які сходяться на рівні ядра трійчастого нерва (тригеміноцервікальний комплекс), так і через активацію парасимпатичної петлі, що сприяє розширенню судин, а також внутрішньочерепному поширенню нейрогенного запалення. Зокрема, больові стимули, що досягають ядра трійчастого нерва, активують пряму передачу сигналів до верхнього слиновидільного ядра, від якого прегангліонарні парасимпатичні волокна надходять до клинопіднебінного ганглія. Постгангліонарні волокна закривають рефлекторну дугу, спрямовуючи волокна, які разом із волокнами трійчастого нерва іннервують не лише слизову оболонку носа та пазух, а й мозкову оболонку і церебральні судини (рис. 2). Отже, парасимпатична активація, спричинена тривалим запаленням слизової оболонки носа, викликає периваскулярне вивільнення вазодилатувальних сполук у мозкових оболонках і церебральних судинах, що активує та сенсибілізує терміналі ноцицепторів трійчастого нерва з розвитком риногенного головного болю [8, 9].
Рис. 1. Хибне коло нейрогенного запалення
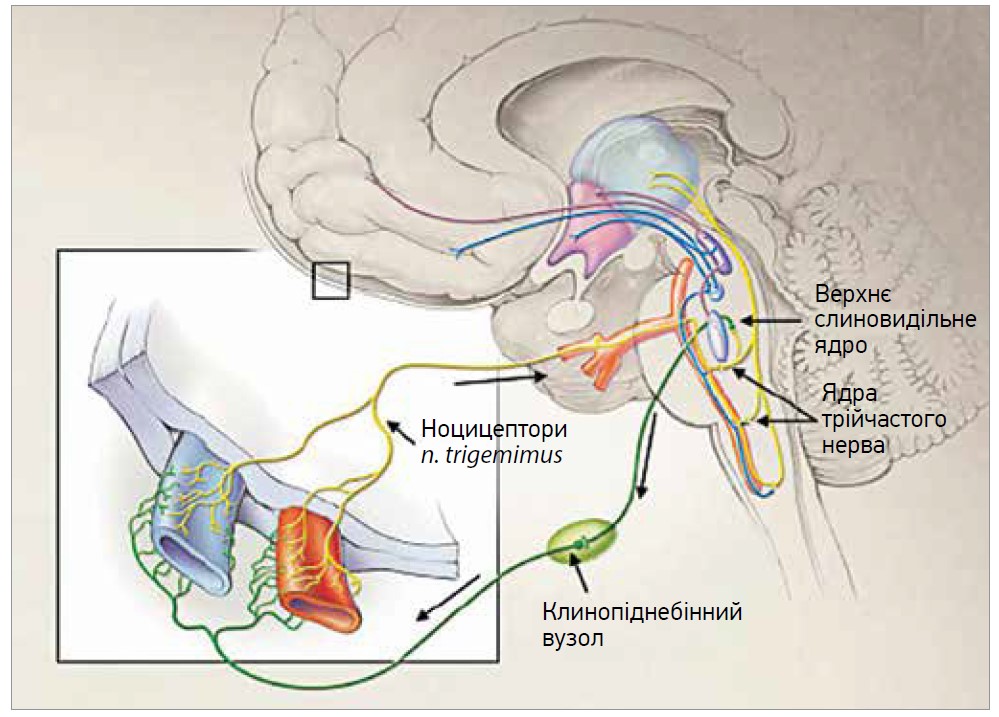 Рис. 2. Тригеміно-парасимпатичний рефлекс (адаптовано з Goadsby et al., 2022 )
Рис. 2. Тригеміно-парасимпатичний рефлекс (адаптовано з Goadsby et al., 2022 )
Описані рефлекси та місцеві процеси також мають місце у випадку головного болю при мігрені [10, 11]. Гілки трійчастого нерва, що іннервують менінгеальні кровоносні судини, вивільняють речовину Р і пептид, пов’язаний з геном кальцитоніну (сalcitonin gene-related peptide), які є факторами розвитку мігренозного болю [12, 13]. Сенсорні волокна трійчастого нерва передають стимули від обличчя, пазух, слизової оболонки носа, мозкових оболонок передньої середньої та задньої черепної ямки [14]. Це пояснює подібність мігренозного і риногенного головного болю та їхній складний зв’язок.
Діагностика риногенного головного болю
Діагноз риногенного головного болю підтверджується за наявності запальних змін у слизовій пазухи та в разі накопичення секрету в ній, що виявляється при виконанні назальної ендоскопії / комп’ютерної томографії. Сімейні лікарі, до яких звертається переважна більшість пацієнтів із попередньо риногенним головним болем, не мають можливості виконати ці дослідження, тому часто припускаються помилок у діагностиці та лікуванні. Слід нагадати, що термін «риногенний головний біль» стосується саме головного болю, пов’язаного з гострим або хронічним риносинуситом, тоді як біль лицьової локалізації, не пов’язаний з риносинуситом, називають нериногенним головним болем.
Згідно з результатами дослідження S.J. Novis і співавт., понад 90% діагнозів гострого і хронічного синуситу, встановлених у закладах первинної медичної допомоги, не відповідали загальноприйнятим критеріям цього захворювання [15]. Дослідження Е. Eross і співавт. продемонструвало, що зі 100 пацієнтів із діагностованим риногенним головним болем 86% мали ознаки мігрені або інших типів головного болю [16]. Отже, на рівні первинної медичної допомоги прослідковується чітка тенденція до надмірної діагностики риногенного головного болю, тоді як у дійсності в більшості випадків має місце мігрень (відповідно до її критеріїв, визначених Міжнародним товариством із вивчення головного болю, IHS), а також інші види головного болю [17].
До інших поширених станів, які можуть спричинити біль у ділянці обличчя або відчуття тиску, належать обструктивне апное сну, дисфункція скронево-нижньощелепного суглоба, стоматологічні інфекції, неврологічні захворювання.
Відрізнити нериногенний головний біль від риногенного дозволяють його певні ознаки. Важливою характеристикою нериногенного головного болю є комбінація назальних симптомів з іншими симптомами. Особливості вегетативної іннервації трійчастого нерва часто обумовлюють у пацієнтів нериногенним головним болем поєднання набряку і ринореї з такими вегетативними симптомами, як сльозотеча, періорбітальний набряк, пітливість.
Відповідно до даних C.P. Schreiber і співавт., серед пацієнтів із діагностованою мігренню 63% мали закладеність носа, 40% – ринорею [18]. У дослідженні A.M. Laury та співавт. близько 40% пацієнтів із лицьовим болем відзначили закладеність носа або ринорею [19].
Ретельний огляд літератури дозволив виявити низку супутніх симптомів, характерних для нериногенного головного болю. E. Eross і співавт. виявили, що в пацієнтів із нериногенним головним болем загальними тригерами були зміни погоди (83% випадків), сезонні коливання погоди (73% випадків) і вплив алергенів (62% випадків) [20].
 A.M. Agius і співавт. повідомили, що частота супутньої світлобоязні та нудоти при головному болю напруги в середній частині обличчя знаходилася на рівні 29 і 27% відповідно, за лицьової мігрені – 74 і 51% відповідно [21]. K.A. Schulz і співавт, дослідивши отоларингологічних пацієнтів із підтвердженим діагнозом мігрені, виявили значну частоту симптомів вестибулярного типу (48%), підвищеної чутливості до запахів (32,3%), а також симптомів, спричинених змінами погоди (47%) та стресом (69%) [22]. С.Р. Schreiber і співавт. у своєму дослідженні із залученням пацієнтів із лицьовою мігренню виявили високу частоту болю сильної інтенсивності (97%), болю пульсуючого характеру (89%), посилення болю під час активності (85%), світлобоязнь (79%), нудоту (73%) та фонофобію (67%) [23].
A.M. Agius і співавт. повідомили, що частота супутньої світлобоязні та нудоти при головному болю напруги в середній частині обличчя знаходилася на рівні 29 і 27% відповідно, за лицьової мігрені – 74 і 51% відповідно [21]. K.A. Schulz і співавт, дослідивши отоларингологічних пацієнтів із підтвердженим діагнозом мігрені, виявили значну частоту симптомів вестибулярного типу (48%), підвищеної чутливості до запахів (32,3%), а також симптомів, спричинених змінами погоди (47%) та стресом (69%) [22]. С.Р. Schreiber і співавт. у своєму дослідженні із залученням пацієнтів із лицьовою мігренню виявили високу частоту болю сильної інтенсивності (97%), болю пульсуючого характеру (89%), посилення болю під час активності (85%), світлобоязнь (79%), нудоту (73%) та фонофобію (67%) [23].
За даними авторів цього дослідження, нериногенний головний біль також має тенденцію реагувати на пероральні деконгестанти, як-от псевдоефедрин, що підтверджує роль вазоактивності в патофізіології мігрені. Знання цих особливостей дозволяє легко розрізнити риногенний головний біль від нериногенного та призначити відповідне лікування. У таблиці представлені основні ознаки нериногенного головного болю.
Оптимізація лікування риногенного головного болю
Риногенний головний біль розвивається одночасно з початком або загостренням риносинуситу і зазвичай зникає після ремісії або успішного лікування. Раптова поява двох або більше симптомів, включаючи виділення з носа/ринорею, закладеність носа, біль/тиск в обличчі, лобний головний біль і розлад нюху, тривалістю до 10 днів із великою імовірністю свідчить про гострий ринусиносит вірусної етіології [1]. Слід нагадати, що більшість випадків гострого риносинуситу спричинені вірусними інфекціями (до 98%), а лише 2% припадає на бактеріальні патогени. Отже, широке застосування антибіотиків при гострому риносинуситі вважається помилкою.
Про гострий бактеріальний риносинусит свідчить наявність щонайменше трьох із таких симптомів: слизові чи гнійні виділення з носової порожнини (їхня наявність під час риноскопії); значний (переважно однобічний) локальний біль, гарячка (>38 °C), підвищення ШОЕ (>20 мм/год) або С-реактивного білка (>60 мг/л), двофазність захворювання (погіршення після першої, більш легкої фази) [24].
З огляду на патофізіологію риногенного головного болю оптимальна терапія має бути спрямована на швидке усунення набряку / компресії слизової оболонки, пригнічення запалення, забезпечення ефективної аналгезії, відновлення нейровегетативного гомеостазу [1].
Сучасні підходи до лікування риногенного головного болю передбачають призначення таких груп лікарських засобів, як деконгестанти, кортикостероїди, засоби з аналгетичною та протизапальною дією, а за наявності показань – антибіотики.
Пероральні деконгестанти зазвичай призначають коротким курсом із метою забезпечення швидкого полегшення симптомів.
Важливу роль у лікуванні риногенного головного болю відіграють нестероїдні протизапальні препарати (НПЗП) [27]. Їх призначають у разі гострого риносинуситу з метою полегшення симптомів і купірування больового синдрому (згідно з оновленими рекомендаціями Американської академії оториноларингології, хірургії голови та шиї, AAO-HNS, 2015), а також зменшення проявів запалення слизової оболонки носа.
Механізм дії НПЗП полягає в інгібуванні синтезу простагландинів шляхом конкурентного зв’язування з циклооксигеназою (ЦОГ), ізоферменти якої каталізують перетворення арахідонової кислоти на простагландини. НПЗП здатні пригнічувати як ЦОГ‑1, так і ЦОГ‑2, при цьому ЦОГ‑2 переважно бере участь у синтезі прозапальних простагландинів, які відіграють важливу роль у патогенезі запалення і виникненні больового синдрому. Інгібування ЦОГ‑2 зумовлює зменшення вивільнення переважно простагландину Е2, що забезпечує реалізацію протизапального й знеболювального ефектів НПЗП.
Серед НПЗП у пацієнтів із риногенним головним болем особливе місце займає німесулід, який є переважно інгібітором ЦОГ-2. Німесулід має хорошу аналгетичну, протизапальну та жарознижувальну ефективність. Слід зазначити, що його знеболювальні та протизапальні властивості опосередковуються центральними (за рахунок інгібування ЦОГ-2 у ЦНС і взаємодії з ендоканабіноїдною системою) та багатьма іншими механізмами [28].
Німесулід інгібує фосфодіестеразу IV (ключовий фермент нейтрофілів і моноцитів, що відіграє важливу сигнальну роль у розвитку запалення), внаслідок чого відбувається пригнічення синтезу супероксидного радикала [32, 33]. Крім того, протизапальному ефекту німесуліду сприяє його здатність фосфорилювати й активувати глюкокортикоїдні рецептори [34].
Німесулід (як в експериментальних, так і клінічних дослідженнях) продемонстрував здатність зменшувати кількість мРНК претахікініну – попередника субстанції P, а також і самої субстанції P, яка бере важливу участь у розвитку та підтримці нейрогенного запалення[35, 36]. Це має важливе значення в розвитку периферичної нейронної сенсибілізації. У такому випадку призначення німесуліду надає можливість розірвати нейрогуморальне хибне коло, попередити розвиток хронізації больового синдрому та віддалених ускладнень.
У разі недостатньої ефективності німесуліду слід додатково призначити пероральний наркотичний аналгетик у низьких дозах, що надає змогу впливати на принципово інші шляхи розвитку та формування больових відчуттів. Найчастіше серед препаратів цього класу в лікуванні головного болю призначають кодеїн [37].
Аналгетичний ефект кодеїну (попередник морфіну) обумовлений спорідненістю до мю- і каппа-рецепторів у спинному мозку, а також вищих рівнів ЦНС. Зв’язування морфіну з його рецептором супроводжується інгібуванням внутрішньоклітинної аденілатциклази, що призводить до зниження рівня циклічного аденозинмонофосфату (цАМФ). Внаслідок цього блокується повторне вивільнення речовини P, дофаміну, ацетилхоліну та зменшуються больові відчуття [38].
Висновки
Риногенний головний біль часто зустрічається в клінічній практиці. З огляду на патофізіологічні особливості перебігу цього стану терапія має бути спрямована на зменшення набряку / стиснення слизової оболонки, запалення (включаючи нейрогенне запалення), а також сприяти відновленню нейровегетативного гомеостазу.
Завдяки особливостям механізму дії німесулід у поєднанні з деконгестантами здатен впливати на всі зазначені чинники, тому є адекватною терапевтичною стратегією лікування риногенного головного болю. В разі недостатнього знеболення аналгезію слід посилити пероральними наркотичними аналгетиками в низьких дозах.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 17 (534), 2022 р.