5 травня, 2023
Гіперурикемія та нирки: сучасний підхід до вирішення проблеми
Зростання захворюваності на подагру, метаболічний синдром, хронічну хворобу нирок (ХХН), а також кардіальні та нефрологічні патології, що спричиняють погіршення якості життя, ранню інвалідизацію пацієнтів і смертність, сьогодні зумовлюють особливу актуальність проблеми підвищення рівня сечової кислоти (СК) у крові (гіперурикемії). Істотний науковий і практичний інтерес є причиною розгляду питання впливу гіперурикемії на нирки. Ці та інші важливі нефрологічні теми були висвітлені в межах заходу Ukrainian Nephrology Week, що відбувався 10 березня на платформі Accemedin за підтримки Української асоціації нефрологів і фахівців із трансплантації нирки (м. Київ) та Української асоціації дитячих нефрологів (м. Київ). Було представлено безліч лекцій та кейсів від топових спікерів, під час проведення яких розглядалися питання профілактики, діагностики й лікування захворювань нирок із погляду фахівців різних спеціальностей. Увагу глядачів привернув семінар керівника навчального центру ТОВ «Інститут ревматології» (м. Київ), лікаря-ревматолога Клініки сучасної ревматології, члена Американської колегії ревматологів (ACR), доктора медичних наук, професора Єлизавети Давидівни Єгудіної щодо впливу гіперурикемії на функціонування і стан нирок, розвиток подагричного артриту й інших коморбідних патологій.
 Гіперурикемія – патологічний стан, що характеризується підвищеним рівнем СК у крові >360 мкмоль/л (>6 мг/дл) і з’являється внаслідок надмірного продукування уратів, абсолютного чи відносного порушення кліренсу СК у нирках, зниження кишкової секреції або комбінації цих механізмів. СК має 4-етапний механізм ниркової екскреції та наявна переважно в проксимальному звивистому канальці нефрона. За порушення будь-якого із цих етапів створюються умови для некорегованої гіперурикемії, кристалізації СК у кислій канальцевій рідині й ушкодження самих канальців, їхнього запалення, а також може спостерігатися інтерстиціальний фіброз, згодом – інтерстиціальний нефрит.
Гіперурикемія – патологічний стан, що характеризується підвищеним рівнем СК у крові >360 мкмоль/л (>6 мг/дл) і з’являється внаслідок надмірного продукування уратів, абсолютного чи відносного порушення кліренсу СК у нирках, зниження кишкової секреції або комбінації цих механізмів. СК має 4-етапний механізм ниркової екскреції та наявна переважно в проксимальному звивистому канальці нефрона. За порушення будь-якого із цих етапів створюються умови для некорегованої гіперурикемії, кристалізації СК у кислій канальцевій рідині й ушкодження самих канальців, їхнього запалення, а також може спостерігатися інтерстиціальний фіброз, згодом – інтерстиціальний нефрит.
Підвищення рівня СК у крові є патофізіологічним підґрунтям для появи такого метаболічного захворювання, як подагра, що характеризується прогресувальною виснажливою формою артриту на тлі підвищення рівня уратів у сироватці. Надлишок СК може накопичуватися в суглобах, нирках і зумовлювати хворобливе запалення, опосередковане інтерлейкіном-1 (IL-1). У клінічній практиці подагру розподіляють на первинну та вторинну. Первинна пов’язана із екскрецією або гіперпродукцією СК, неправильним дотриманням дієти чи надмірним вживанням алкоголю. Вторинна зумовлена лікарськими препаратами або станами, що спричиняють гіперурикемію: мієлопроліферативні патології або їхнє лікування, ниркова недостатність, захворювання ниркових канальців, отруєння свинцем, гіперпроліферативні шкірні захворювання, ферментативні дефекти (хвороби накопичення глікогену, дефіцит гіпоксантингуанінфосфорибозилтрансферази). Особливості клінічного перебігу подагри є досить відомими: нападоподібний і прогресувальний перебіг, максимальне запалення суглоба в 1-й день захворювання, відсутність симптомів у період між загостреннями, моноартрит у дебюті, наявність усіх ознак запалення, біль (частіше у першому) плеснофаланговому суглобі, асиметричний характер залучення, наявність вищезазначених провокувальних факторів.
Дослідження NHANES (2015-2016) свідчать про те, що поширеність подагри та гіперурикемії значно зростає у країнах, що розвиваються. В цей період розповсюдженість подагри становила 3,9% серед дорослого населення США (9,2 млн осіб): 5,2% (5,9 млн) у чоловіків і 2,7% (3,3 млн) у жінок. Поширеність гіперурикемії складала 20,2 та 20,0% відповідно. Відомо, що тенденція до зростання випадків виявлення хвороби збільшується з віком, особливо в чоловіків (3-4:1) віком >70 років (7-8%) (Kou C.F. et al., 2015). Епідемія ожиріння в усьому світі, зміна раціону харчування, неконтрольоване споживання фруктози, оброблених харчових продуктів, збагачених пурином, зловживання алкоголем і широке застосування діуретиків стали рушійними факторами для формування цієї статистики.
Підвищення СК і подагра – часті супутники ХХН, артеріальної гіпертензії, застійної серцевої недостатності, рідше – онкопатологій, анемій різного ґенезу тощо. Правильне визначення етіопатологічного механізму розвитку подагричного артриту за наявності гіперурикемії є ключовим для встановлення діагнозу.
Дані останніх років продемонстрували, що генетична схильність, чоловіча стать, деякі препарати (діуретики, циклоспорин, такролімус, β-блокатори, ритонавір) і продукти харчування є основними предикторами розвитку гіперурикемії, отже, й подагри. Люди, котрі регулярно споживають значну кількість червоного м’яса, морепродуктів, пива, алкоголю, цукровмісних напоїв, є схильнішими до прогресування подагри. Пиво – найнебезпечніший продукт, оскільки через його вживання до організму потрапляє значна кількість гуанозину, а також спостерігається естрогеноподібний вплив, а це зумовлює ожиріння в чоловіків. Психоемоційний стрес, інтенсивна м’язова робота на тлі поганого харчування, травми/опіки/інфекції та інші стани, що супроводжуються катаболізмом тканин, також пов’язані з ризиком розвитку подагри й гіперурикемії. Механізм їхньої дії зумовлений тим, що вони руйнують слизову оболонку шлунково-кишкового тракту та клітини імунної системи.
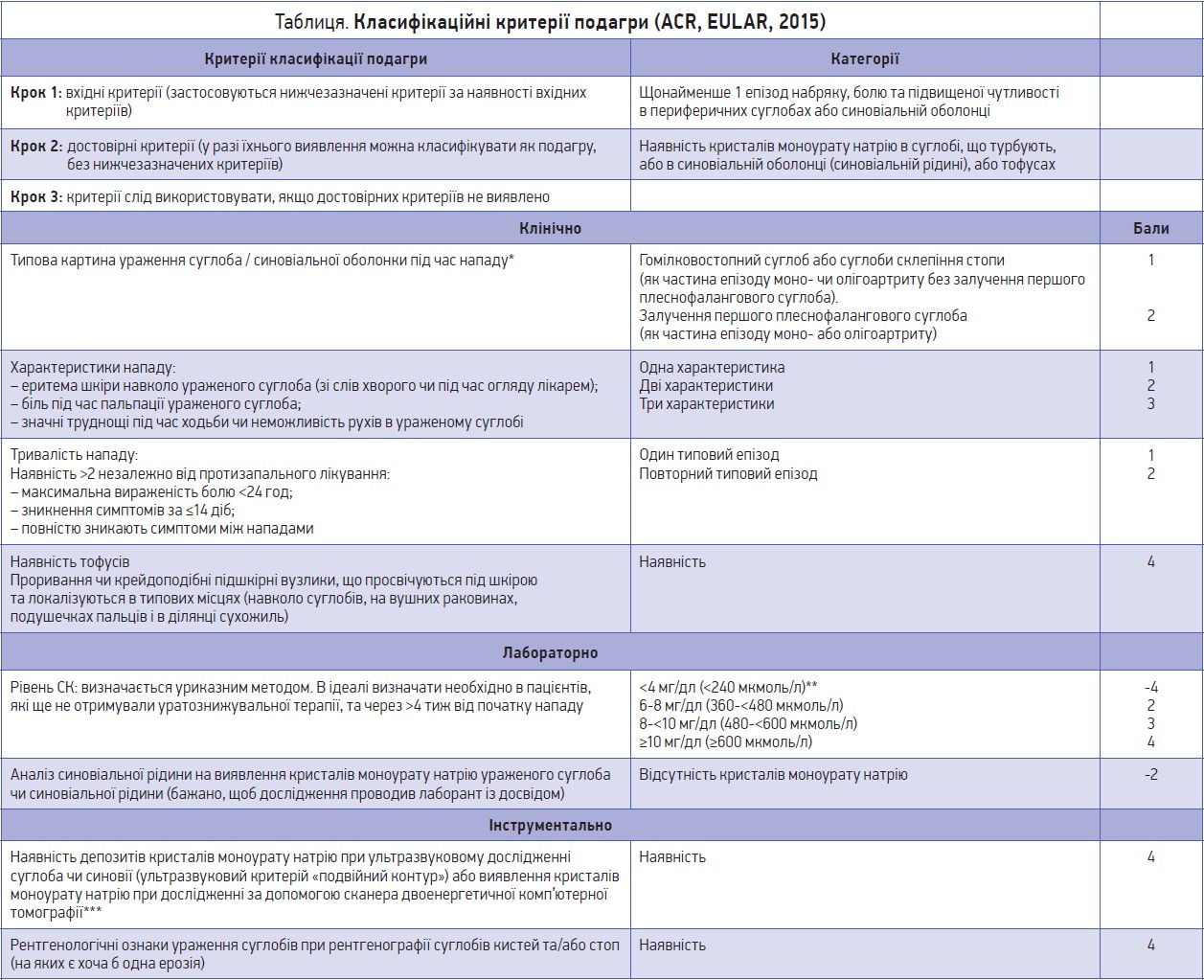
У 2015 році ACR спільно з Європейською антиревматичною лігою (EULAR) розроблено оновлені класифікаційні критерії діагностики подагри (табл.).
Примітки. * Напад, який включає симптоми набряку, болючості та/чи підвищеної чутливості в периферичних суглобах і сумках.
** Якщо рівень СК <4 мг/дл (<240 мкмоль/л), потрібно відняти 4 бали; якщо рівень СК ≥4-6 мг/дл (≥240 – <360 мкмоль/л), потрібно оцінити в 0 балів.
Якщо в синовіальній рідині кристалів моноурату натрію не виявлено, потрібно відняти 2 бали; якщо дослідження синовіальної рідини не проводили, потрібно оцінити в 0 балів.
Якщо інструментальних досліджень не проводили, потрібно оцінити в 0 балів.
Гіперехогенні гетерогенні пошкодження гіалінового хряща, що не залежать від кута ультразвукового променя (псевдопозитивний «подвійний контур» (артефакт); мають зникнути при зміні кута ультразвукового променя).
*** Зображення мають бути виявлені за допомогою сканера ДЕКТ при 80 та 140 кВт і бути проаналізованими спеціальною програмою для подагри з виявленням «колірних кодів» уратів. Сканування вважається позитивним, якщо виявлено «колірні коди» уратів у суглобах і навколосуглобових тканинах.
Ерозії характеризуються кортикальним розривом зі склеротичним обідком і нависаючими краями, за винятком дистальних міжфалангових суглобів.
Діагноз вважається достовірним, якщо за наведеними критеріями набрано ≥8 балів (максимум – 23).
Нововведення – в двох показниках із трьох категорій за відсутності певного показника віднімають бали від загальної суми балів:
- відсутність кристалів моноурату натрію (МУН) (2 бали) в ураженому суглобі чи синовіальній оболонці;
- якщо рівень СК у крові становить <4 мг/дл (<0,24 ммоль/л) (4 бали).
Якщо наявні такі показники, це значно знижує імовірність наявності подагри в пацієнта. Найнижчим балом у кожній групі є 0: рівень СК 4-6 мг/дл (0,24-0,36 ммоль/л) відповідає 0; якщо немає рентгенологічної картини, характерної для подагричного артриту, також рахуємо як 0 балів. Сума балів >8 дозволяє встановити достовірний діагноз подагри.
На жаль, концентрація СК не завжди відображає реальної тяжкості перебігу захворювання; для гострого нападу зазвичай характерним є нормальний її рівень. Рентгенологічні ознаки подагри, зокрема типовий симптом «пробійника», – пізні прояви захворювання; свідчать про те, що пацієнт хворіє уже >7 років. Що стосується визначення зон для рентгенологічного обстеження, то найчастіше це перший плеснофаланговий суглоб стопи чи кисті, рідше – гомілковостопний або середній відділ стопи. Для ранньої діагностики успішно використовують ультразвук, адже він надає змогу визначити типові доклінічні прояви, наприклад, «подвійний контур» у синовіальній рідині, а також обрати подальшу тактику лікування. Залежно від стадії перебігу подагри існує нефармакологічне лікування, показане за безсимптомної гіперурикемії, а також фармакологічне. Останнє доречне, коли атаки гострого нападу подагри стають тривалішими, а міжнападові періоди скорочуються.
Загальновідомо, що гіперурикемія – незалежний фактор виникнення не лише подагри, а й ХХН, ниркової дисфункції, уратного нефролітіазу (2-30/20-56% хворих), хронічного тубулоінтерстиціального нефриту (54-57%, 77-80% хворих), гострої сечокислої нефропатії (гостра подагрична нирка) як наслідок обструкції ниркових канальців кристалами уратів, а також кардіоваскулярних ускладнень (Gibson T., Hyperuricemia, dout and the kidney. Curr Opin Rheumatol, 2012). П’ятирічне проспективне дослідження за участю чоловіків без захворювання нирок показало, що підвищений рівень СК пов’язаний з мікроальбумінурією, розвитком ХХН (Eur J Clin Invest, 2014; BMC Nephrol, 2014). Інше 10-річне випробування за участю пацієнтів із ХХН ¾ стадії довело, що гіперурикемія – незалежний предиктор ризику смерті від усіх причин і прогресування термінальної стадії ХХН; зниження рівня уратів у сироватці до рівня <6,5 мг/дл знижує ризик ТТН (Am J Kidney Dis, 2009; PLoS ONE, 2015). У доклінічних дослідженнях установили, що гіперурикемія спричиняє ушкодження нирок шляхом множинних кристалонезалежних механізмів. Вони включають вазоконстрикцію ниркових артерій унаслідок ендотеліальної та мітохондріальної дисфункції. Крім депозиції кристалів, механізм прогресування ХХН спричинений гіперурикемією, запуском оксидативногго стресу, розвитком проліферації гладком’язових клітин, активацією ренін-ангіотензинової системи, що зумовлює як системну, так і клубочкову гіпертензію. Це спричиняє ішемію та інфільтрацію макрофагів, що зумовлює інтерстиціальні ушкодження, тубулоінтерстиціальний некроз, артеріолосклероз і гостре ушкодження нирок.
Нефролітіаз – ще одне поширене, асоційоване з гіперурикемією, захворювання нирок. Виокремлюють гостру уратну нефропатію і хронічну. В разі першої відбувається підвищена екскреція СК із сечею, що супроводжується осадженням кристалів СК у дистальних канальцях нирок та збірних протоках, а також спричиняє розвиток олігоануричної ниркової недостатності. Гостре ушкодження нирок за надмірного виведення СК зустрічається найчастіше в пацієнтів зі швидким злоякісним поділом клітин, як-от лімфома, лейкоз або мієлопроліферативна хвороба, після хіміотерапії або опромінення. Цьому сприяє швидкий лізис клітин, оскільки нуклеїнові кислоти, що утворюються, здатні до швидкої трансформації у СК. Хронічна уратна нефропатія – це форма хронічного захворювання нирок, зумовлена відкладенням кристалів уратів у медулярному інтерстиції нирок. Кристали індукують хронічну запальну реакцію, схожу на таку, що спостерігається за утворення тофусів в інших місцях тіла, та потенційно зумовлюють інтерстиціальний фіброз, ХХН. Клінічні особливості є неспецифічними: ниркова дисфункція, сечовий осад і протеїнурія.
Ниркова дисфункція внаслідок гіперурикемії визначається як сироватковий креатинін >1,4 мг/дл для чоловіків і 1,2 мг/дл для жінок. У результаті великого американського дослідження за участю 50 тис. пацієнтів виявлено, що початкова гіперурикемія (СК ≥8 мг/дл) асоціювалася із 2,9-кратним збільшенням ниркової дисфункції серед чоловіків і в 10,4 разу серед жінок порівняно з вихідною концентрацією СК у сироватці крові <5,0 мг/дл та після корекції за віком, курінням, вживанням алкоголю, фізичними вправами, глюкозою натще, вихідною протеїнурією, артеріальним тиском, ожирінням. Розрахункові показники захворюваності на термінальну хронічну ниркову недостатність (ХНН) на 1000 обстежених склали 1,22 для чоловіків без гіперурикемії та 4,64 для чоловіків із нею і 0,87 для жінок без гіперурикемії та 9,03 для жінок за її наявності.
Гіперурикемія також розглядається як маркер або незалежний фактор ризику розвитку серцево-судинних захворювань, а саме артеріальної гіпертензії. В American Journal of Medicine проведено масштабні дослідження з метою встановити фактори, які обумовлюють підвищення артеріального тиску в пацієнтів із гіперурикемією. Як відомо, ними виявилися дієта, збагачена пуринами чи фруктозою, генетичні фактори, чинники навколишнього середовища або навіть затримка внутрішньоутробного розвитку, низька кількість нефронів. Вплив на судини опосередкований підвищенням активних форм кисню, зниженням NO, що викликають васкулярне запалення та проліферацію гладком’язових клітин судин з інгібіцією ендотеліального фактора росту. Ці патофізіологічні зміни неодмінно спричинять формування ранньої стадії СК-індукованої вазоренальної гіпертензії, а згодом – пізню стадію сіль-чутливої нирковозалежної гіпертензії (N Engl J Med., 2008).
Лікування подагри за гіперурикемії та інших захворювань нирок має бути комплексним і базуватися на визначенні факторів ризику, вихідного рівня СК у крові. Лікарям слід намагатися розірвати хибне коло: гіперурикемія та ендотеліальна дисфункція – зниження ШКФ, системна й гломерулярна гіпертензія – зниження ниркової екскреції СК. Так, для пригнічення прогресування до термінальної стадії захворювання нирок СК сироватки має бути ≤6,0 мг/дл. На міждисциплінарному консенсусі (2020) було представлено основні кроки ведення пацієнтів із безсимптомною гіперурикемією (СК ≤6,8 мг/дл, або ≥400 мкмоль/л). Сьогодні більшість ревматологів схиляються до думки, що при безсимптомній гіперурикемії варто надати перевагу немедикаментозному лікуванню: дієта, помірна фізична активність, зниження маси тіла, відміна препаратів, що підвищують рівень СК у крові. Уратознижувальна терапія (УЗТ) не показана, якщо рівень СК становить 6,8-8,9 мг/дл (400-529 мкмоль/л) за нормальної ШКФ без супутньої хвороби нирок. Але в разі показників СК 6,8-8,9 мг/дл (400-529 мкмоль/л) або СК ≥9 мг/дл (≥530 мкмоль/л) та за наявності в пацієнта ХХН 3 чи 4 стадії УЗТ є обов’язковою (Management of asymptomatic Hyperuricemia: Integrated Diabetes & Endocrine Academy (IDEA) consensus statement, 2020).
На сьогодні протигіперурикемічні препарати, до яких належать інгібітори ксантиноксидази (ІКО) алопуринол і фебуксостат, урикозуричні засоби, беззаперечно рекомендуються пацієнтам із гіперурикемією, асоційованою із подагричним артритом або подагричною нефропатією. Багато даних свідчать про те, що фебуксостат (80 мг) знижує рівень СК значно краще, ніж алопуринол (300 мг), у пацієнтів із сечокам’яною хворобою (СКХ) і підвищеною екскрецією СК після 6 міс лікування. За допомогою великого дослідження (2019), у якому брали участь пацієнти віком ≈62 роки з вихідною ШКФ 42,1±8,8 та СК у сироватці 8,6±1,5 мг/дл, було виявлено, що протягом періоду спостереження (55,9±31,8 міс) група фебуксостату порівняно з алопуринолом і контрольною групою мала значно нижчий середній рівень СК (5,7±1,0 проти 7,1±1,2 та 8,0±0,8 мг/дл; р<0,001) й підтримувала значно вищі значення ШКФ постійно протягом 4 років. Група фебуксостату мала значно більший час виживання нирок без прогресування ХХН, ніж алопуринол і контрольна група (87,7 (95% довірчий інтервал (ДІ) 71,2-104,2) проти 77,6 (95% ДІ 60,2-94,9) проти 48,7 (95% ДІ 39,3-58,1) міс відповідно; р<0,001). Найважливішим є те, що фебуксостат значно знижував ризик прогресування ниркової хвороби на 74,3%, тоді як алопуринол продемонстрував незначний результат.
Ведення подагри (за рекомендаціями ACR/EULAR) містить такі групи препаратів, як нестероїдні протизапальні (НПЗП), колхіцин, ГК (за потреби), місцевий холод як ад’ювантна терапія за гострої атаки. Вибір препарату слід робити на основі індивідуальних чинників і переваг для хворого. Ціль – досягти рівня СК ≤6 мг/дл, а за наявності тяжкого захворювання з тофусами, нефролітіаз чи ерозії СК має складати ≤5 мг/дл. ІКО належать до засобів першої лінії, а урикозуричні – до другої. Супутня протизапальна терапія на початку УЗТ проводиться за допомогою НПЗП у половинній або повній дозі, колхіцину 0,5 чи 0,6 мг 1-2 р/день щодня або преднізолону ≤10 мг щодня протягом 3-6 міс. Згідно з ACR (2020), для пацієнтів із першим нападом подагри не слід розпочинати лікування з УЗТ (за винятком наявності таких факторів, як супутня ХХН ≥3 стадії, СК сироватки >9 мг/дл чи СКХ). Тривалість УЗТ визначається як умовно довічна, але це залежить від багатьох факторів. Наприклад, для хворих із клінічною ремісією, яким проводять УЗТ (без загострень протягом ≥1 року та тофусів), слід розглянути припинення або зниження дози УЗТ. Деякі джерела свідчать про те, що лише в 13% пацієнтів (27 зі 211) без лікування концентрація СК залишається на рівні <7 мг/дл. У людей із вищими концентраціями СК після відміни терапії спостерігалися частіші загострення, пов’язані з вищими рівнями СК. Якщо терапія добре переносилася та не провокувала ускладнень, група хворих продовжувала її (Hoboken, 2020). Є випадки, коли пацієнти приймають препарати ІКО, але при цьому в них постійно зберігаються високі концентрації СК (>6 мг/дл), незважаючи на максимальну дозу, що добре переноситься або зазначену Управлінням з контролю за якістю продуктів харчування та лікарських засобів (FDA) дозу ІКО, мають часті загострення подагри (>2 атак/рік) чи підшкірні тофуси. Таким хворим слід рекомендувати перейти на інший засіб ІКО, а не додавати як другий препарат урикозуричний агент. Це дозволяє досягти стійкої ремісії хвороби, зупинити стрімке прогресування подагри чи подагричного нефриту.
Отже, накопичені останніми роками дані свідчать, що гіперурикемія сприяє розвитку не лише таких захворювань, як подагра чи метаболічний синдром, а і є предиктором ХХН, інших патологій нирок. Установлення причинно-наслідкових зв’язків і механізму розвитку ниркової дисфункції або ХХН при гіперурикемії є важливою складовою для створення рекомендацій щодо її менеджменту. Скринінг на уратний дисметаболізм слід проводити в осіб, які мають родичів із клінічними проявами порушень обміну СК, із метаболічним синдромом, котрі постійно приймають препарати, що підвищують рівень СК, у молодих пацієнтів з резистентною до лікування артеріальною гіпертензією, осіб з уратною або змішаною уратно-оксалатною кристалурією, ХХН на тлі гломерулонефриту. Також на сьогодні зібрано безліч даних і клінічних протоколів, які демонструють доцільність застосування УЗТ для профілактики розвитку подагри чи прогресування ХХН на тлі гіперурикемії. Фебуксостат усе частіше є препаратом вибору з огляду на його високу ефективність, сприятливий профіль безпеки в пацієнтів із ХХН і наявність нефропротекторного ефекту.
Підготувала Христина Воськало