14 грудня, 2023
Гепарин-індукована тромбоцитопенія, або Коли гепарин спричиняє тромбоз
Нефракціоновані (НФГ) і низькомолекулярні гепарини (НМГ) є препаратами, що широко використовуються та запобігають артеріальним і венозним тромбозам. Однак їхнє застосування також пов’язано з парадоксальною реакцією, що зумовлює потенційно небезпечний для життя протромботичний стан, результатом чого є серйозні ускладнення (гангрена, ампутація кінцівок) або фатальні наслідки. Гепарин-індукована тромбоцитопенія (ГІТ) – це імуноопосередкована відповідь на введення гепарину, який спричиняє небезпечний для життя тромбоз і є клінічно значущим негеморагічним ускладненням. ГІТ вважається потенційно загрозливим для життя станом за терапії гепарином, що спричиняє утворення нових згустків крові, а не сприяє запобіганню утворення нових тромбів. Хоча при введенні гепарину імунна реакція зустрічається досить часто (від 8 до 50%), клінічні ускладнення у разі ГІТ виникають у ≈0,2-3% пацієнтів, які приймають гепарин протягом >4 дні; частіше спостерігаються в жінок [1-3]. У цьому стані тромбоцити різко знижуються до рівня ≥20×109/л. Смертність становить 10-20%.
Стисла історія вивчення ГІТ
Уперше гостра тромбоцитопенія, яка виникла протягом декількох хвилин після терапії гепарином, була описана в тварин у 1942 р. [4], а пізніше спостерігалася в людей як нетривале неімунне ускладнення за терапії гепарином [5]. Цей фармакологічний ефект гепарину (ГІТ, тип I) обумовлювався його аглютинувальною дією на тромбоцити [6, 7]. Про серйозніше імунне ускладнення (ГІТ, тип II) повідомили в 1958 р. хірурги R. Weismann і R. Tobin [8], котрі узагальнили серію випадків у 10 пацієнтів у їхній установі, в яких розвинувся парадоксальний тромбоз під час гепаринової терапії. Схожі результати отримано через декілька років B. Roberts і співавт. у 1964 р. [9], котрі описали ще одну серію випадків в 11 хворих і припустили, що цей клінічний синдром може бути «результатом механізму антиген – антитіло». В 1973 р. G. Rhodes і співавт. [10] представили характерні клінічні особливості цього захворювання шляхом систематичного обстеження 2 пацієнтів із ГІТ, відзначивши таке:
- супутні прояви тромбоцитопенії на додаток до тромбозу під час терапії гепарином;
- нормалізація рівня тромбоцитів після припинення терапії гепарином;
- наявність гепарин-залежних антитіл із використанням аналізу агрегації тромбоцитів у гострій фазі;
- рецидивна тромбоцитопенія за повторного застосування гепарину під час гострої фази захворювання.
Патогенез і патофізіологія ГІТ
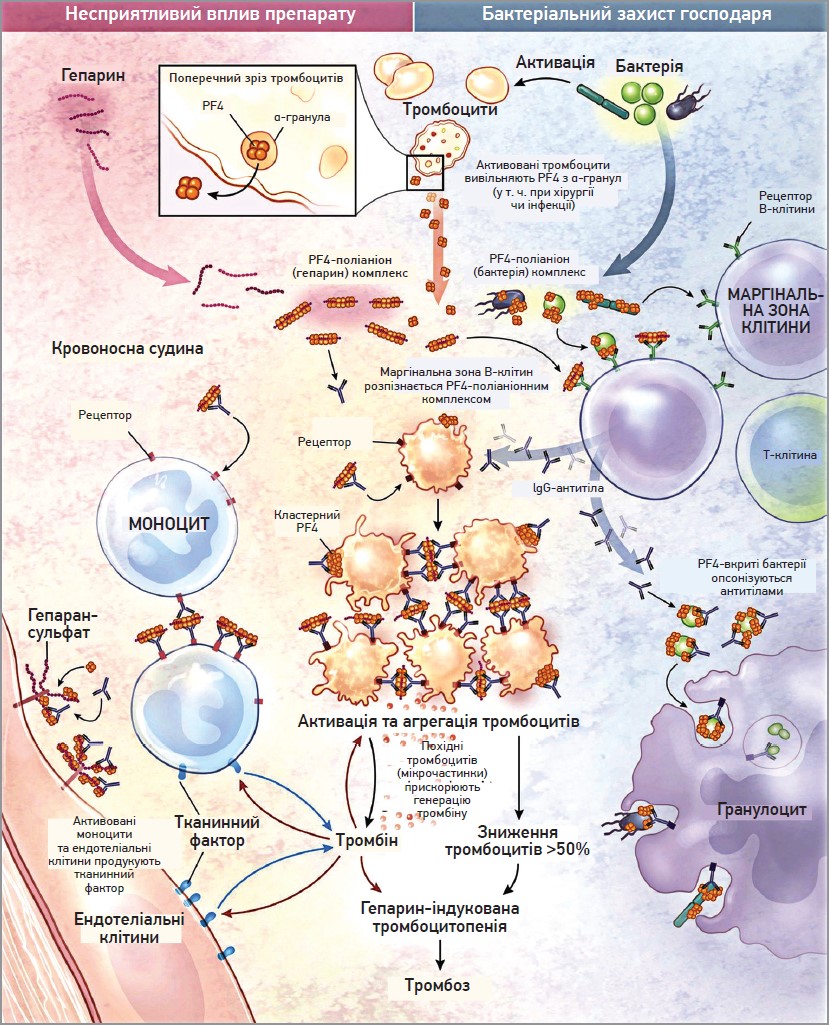
Побічний ефект, відомий як ГІТ, багато в чому схожий на механізм бактеріального захисту. Тромбоцитарний фактор 4 (PF4), що вивільняється з α-гранул тромбоцитів, зв’язується з поліаніонами, як-от гепарин, або поліаніонами на поверхні бактерій, зазнає конформаційних змін, що зумовлює утворення імунологічного комплексу PF4-поліаніон (гепарин) або PF4-поліаніон (бактерії). Після активації В-лімфоцити (ймовірно, B-клітини маргінальної зони) генерують анти-PF4-поліаніонні IgG. Ці антитіла можуть зв’язуватися з різними бактеріями, вкритими PF4, та опсонізувати їх. Однак ці антитіла також зв’язуються з комплексами PF4-гепарин, утворюючи імунокомплекси. Fc-ділянка IgG зв’язується з рецепторами Fcγ RIIa тромбоцитів, що спричиняє кластеризацію рецепторів Fcγ, отже, сильну активацію та агрегацію тромбоцитів. Це внутрішньосудинне споживання тромбоцитів зумовлює зменшення їхньої кількості та продукування мікрочастинок тромбоцитарного походження, які прискорюють утворення тромбіну. Крім того, антитіла ГІТ активують моноцити (за допомогою Fcγ RI) та (прямо чи опосередковано) ендотеліальні клітини.
В нормальних умовах PF4 зберігається в гранулах тромбоцитів і вивільняється після активації. Він заряджений позитивно і тому може зв’язуватися з негативно зарядженим гепаран-сульфатом (речовиною на поверхні ендотеліальних клітин). PF4 також може зв’язуватися з екзогенним гепарином із набагато вищою спорідненістю, ніж гепаран-сульфат, який може ініціювати імунну відповідь. ГІТ індукується антитілами типу IgG (IgA або IgM), що продукуються плазматичними клітинами, які розпізнають неоепітопи комплексу гепарин/PF4. Гепарин взаємодіє з PF4, утворюючи неоантиген в оптимальному стехіометричному співвідношенні (1:1). Результуючий комплекс зв’язується з Fc-рецепторами тромбоцитів і моноцитів, індукуючи їхню активацію та утворення прокоагулянтних мікрочастинок. Активовані тромбоцити виробляють протромботичні речовини (як-от тромбін) і PF4, створюючи стан тяжкої гіперкоагуляції та хибного кола, яке можна розірвати тільки шляхом відміни гепарину й початком відповідного лікування. Отже, імунні комплекси активують нейтрофіли, сприяючи утворенню позаклітинних нейтрофільних пасток, забезпечуючи ще один прокоагулянтний стимул. Кількість тромбоцитів знижується, оскільки покриті IgG тромбоцити видаляються макрофагами й одночасно активуються тромбоцити (вони витрачаються всередині судинного русла). В результаті утворюється значна кількість тромбіну, що спричиняє тромбоз (рис.).
Рис. Патогенез ГІТ
Розрізняють 2 типи ГІТ за механізмами розвитку, швидкістю зниження кількості тромбоцитів, принципами лікування (табл. 1).
|
Таблиця 1. Порівняльна характеристика ГІТ 1 та 2 типів |
||
|
Характеристика |
ГІТ‑1 |
ГІТ‑2 |
|
Механізм |
Неімунний |
Імунний |
|
Кількість тромбоцитів |
≥100×109/л/≥50% від початкового рівня |
≤100×109/л/≤50% від початкового рівня |
|
Маніфестація |
протягом перших 4 днів |
протягом 5-15 днів |
|
Тромбози |
рідко |
часто |
|
Лікування |
відміна гепарину |
скасування гепарину, призначення альтернативних антикоагулянтів |
Перший тип (ГІТ‑1) – це гепарин-асоційована неімунна тромбоцитопенія, що виникає після застосування гепарину в 10-30% хворих. Механізм ГІТ‑1 полягає у прямій активації тромбоцитів через специфічні рецептори P2Y12 та IIb/IIIa, що зумовлює їхню агрегацію. ГІТ‑1 не потребує додаткового лікування, крім відміни препарату. Тромбози за цього типу ГІТ розвиваються рідко.
Другий тип ГІТ (ГІТ‑2) являє собою імуноспецифічну реакцію, пов’язану з утворенням автоантитіл до комплексу гепарину та тромбоцитарного фактора [4]. Установлено, що застосування гепарину при ГІТ‑2 спричиняє формування гепарин-залежних антитіл, що розпізнають «власний» протеїн PF4 в тромбоцитарних гранулах [11]. Коли полімолекулярні комплекси гепарину, PF4 та антитіла класу IgG опиняються на поверхні тромбоцитів, Fc-«хвости» антитіл ГІТ взаємодіють із тромбоцитарними рецепторами Fc (FcIIa), що зумовлює активацію тромбоцитів [12, 13]. Крім активації тромбоцитів, антитіла ГІТ викликають гіперкоагуляцію (доведено in vivo підвищенням рівня тромбіну) [14]. У 5-10% хворих на ГІТ спостерігається зниження фібриногену. Зокрема, це свідчить про розвиток ДВЗ-синдрому [15]. Активація коагуляції при ГІТ‑2 відбувається також у результаті прокоагулянтних змін мембрани тромбоцитів [16]. Дослідження in vitro демонструють, що антитіла ГІТ спричиняють ушкодження ендотелію та вироблення тканинного фактора ендотеліоцитами [17] та моноцитами [18]. Якщо ці механізми вже запущені, ризик тромбозу зберігається від декількох днів до тижнів навіть після припинення застосування гепарину [19, 20]. ГІТ‑2 є серйозним ускладненням, що посилює перебіг основного захворювання в терапевтичних і хірургічних пацієнтів. Вона може перебігати приховано; клініцисти її клінічні прояви нерідко асоціюють з тяжкістю перебігу основного захворювання або післяопераційного періоду.
Діагностика ГІТ
ГІТ слід запідозрити, якщо кількість тромбоцитів знижується на >50%. Це може бути підтверджено наявністю тромбозу через 5-10 днів після введення гепарину та наявністю PF4/антитіл до гепарину. Кількість тромбоцитів зазвичай не менше 20×109/л, що пов’язано з їхньою сильною агрегацією, а не руйнуванням [21-24].
Діагностика ГІТ ґрунтується на 3 критеріях:
- пацієнт отримує чи зазнавав впливу НФГ або НМГ;
- наявний щонайменше один клінічний або лабораторний результат (значний), пов’язаний зі зниженням кількості тромбоцитів, а також венозний чи артеріальний тромбоз, що вперше виник;
- є лабораторні дані про наявність специфічних антитіл до ГІТ.
Клінічна діагностика
До ознак і симптомів ГІТ належать ті, які дозволяють припустити тромботичні ускладнення. Крім того, в разі підшкірного введення гепарину можуть виникнути еритема, біль або некроз шкіри. В пацієнтів, котрі отримують гепарин внутрішньовенно, можливий прояв лихоманки, гіпертонії, тахікардії, задишки та болю в грудях, а також висипу на шкірі.
За підозри ГІТ насамперед варто оцінити ймовірність виникнення з використанням шкали 4T на основі 4 параметрів:
- зниження кількості тромбоцитів (тромбоцитопенія);
- строки, коли сталося зниження;
- наявність чи відсутність тромбозу;
- інший можливий альтернативний діагноз (табл. 2).
|
Таблиця 2. Оцінка клінічної ймовірності ГІТ (4Т) |
|
|
Шкала 4Т |
Бали |
|
1. Тромбоцитопенія |
|
|
Зниження тромбоцитів >50% протягом останніх 3 днів, максимальне зниження ≥20×109/л |
2 |
|
Зниження кількості тромбоцитів 30-50%, максимальне зниження 10-19×109/л |
1 |
|
Зниження <30%, максимальне зниження <10×109/л |
0 |
|
|
|
|
2. Строки зниження кількості тромбоцитів |
|
|
Початок зниження тромбоцитів через 5-10 днів (або з 1-го дня після початку прийому гепарину протягом останніх 30 днів) |
2 |
|
Зниження з 1-го дня після початку та попередньої дії упродовж останніх 30-100 днів. Початок зниження тромбоцитів із 14-го дня |
1 |
|
Зниження тромбоцитів <4 днів без дії гепарину за останні 100 днів |
0 |
|
|
|
|
3. Тромбоз чи інші наслідки |
|
|
Новий тромбоз (підтверджений). Некроз шкіри в місці ін’єкції. Анафілактична реакція після болюсного введення гепарину. Крововилив у надниркові залози |
2 |
|
Прогресувальний або рецидивний тромбоз. Не некротичні ураження шкіри. Підозра на тромбоз (не підтверджено) |
1 |
|
Ні |
0 |
|
|
|
|
4. Інші причини тромбоцитопенії |
|
|
Немає іншої очевидної причини |
2 |
|
Можливі |
1 |
|
Напевно є |
0 |
Інтерпретація шкали 4T
1. Тромбоцитопенія. Зазвичай середня (≥20×109/л). Зниження тромбоцитів >30% через 5-10 днів після впливу НФГ або НМГ свідчить про ГІТ, хоча може бути й більш раннє зниження (24 год) у пацієнтів, які зазнали впливу гепарину в попередні 3 міс. Зазвичай це супроводжується кровотечею.
2. Терміни. Зазвичай симптоми з’являються протягом 5-10 днів у пацієнтів, які отримали НФГ або НМГ чи набагато швидше, якщо був попередній вплив (останні 30-100 днів).
3. Тромбоз. Це характерна клінічна ознака, що розвивається в 30-50% підтверджених ГІТ. Тромбоз може бути венозний (нижньої кінцівки, вісцеральний або венозний катетер) чи артеріальний (церебральний, гангрена нижніх кінцівок тощо). Це може бути початковим клінічним проявом, хоча зазвичай він виникає відразу після появи тромбоцитопенії.
4. Інші причини тромбоцитопенії. Багато захворювань, пов’язаних з ізольованою тромбоцитопенією (переважно на тлі прийому лікарських препаратів, імунної або інфекційної етіології, посттрансфузійна пурпура) чи із тромботичним феноменом.
Інтерпретація оцінки 4Т
Бали 0-3: дуже низька ймовірність ГІТ (<5%).
Бали 4-5: проміжна ймовірність (10-30%).
Бали 6-8: висока ймовірність (від 40 до >80%).
Вважається, що якщо розрахований бал ≥4, слід застосовувати лабораторні методи дослідження.
Лабораторна діагностика ГІТ
Для підтвердження діагнозу ГІТ використовують лабораторні методи дослідження (табл. 3).
|
Таблиця 3. Лабораторні методи дослідження для підтвердження ГІТ |
||||
|
Метод |
Механізм |
Чутливість |
Специфічність |
Коментарі |
|
SRA (Serotonine Release Assay). Аналіз вивільнення серотоніну |
Метод ґрунтується на взаємодії мічених 14С-серотоніном тромбоцитів донора, гепарину та сироватки пацієнта. При активації тромбоцитів відбувається вивільнення 14С-серотоніну, що інтерпретується як позитивна реакція |
90-98% |
>90% |
Золотий стандарт лабораторної діагностики ГІТ. Метод має обмеження, адже необхідно використовувати радіоактивні реагенти |
|
ELISA (Enzyme-Linked ImmunoSorbent Assay) |
Визначення антитіл проти PF4/гепарину незалежно від їхньої здатності активувати тромбоцити |
>95% |
>80% |
Висока частота хибно-позитивних результатів |
|
HIPA, Аналіз гепарин-індукованої активації тромбоцитів |
Візуальний підрахунок агрегації тромбоцитів донора за наявності сироватки пацієнта з додаванням гепарину |
90% |
30-50% |
Недорогий та швидкий метод. Результат – протягом 1-2 год |
|
PIFA (мембранний імунний тест) |
Антитіла в зразку плазми визначаються за їхньою реакцією з частинками, навантаженими комплексами гепарин-TF4 при проходженні через мембрану (PIFA) (фірма Akers Biosciences) |
95% |
80% |
Час виконання – декілька годин |
|
Поєднання аналізу HIPA та ELISA |
|
100 |
>95 |
|
Характеристика основних лабораторних тестів
1. Аналіз вивільнення 14C-серотоніну (SRA)
В методі SRA вимірюється вивільнення серотоніну зі щільних гранул тромбоцитів як маркера активації тромбоцитів, що найточніше імітує ГІТ шляхом вимірювання кількості тромбоцитів, які зазнали дегрануляції. Цей метод вважається золотим стандартом виявлення синдрому ГІТ. Оскільки при цьому використовуються екзогенні тромбоцити, можуть виникати хибнонегативні результати, коли частина Fc-антитіла має низьку спорідненість до Fc II-рецептора тромбоцитів. Хоча цей тест є високоспецифічним (89-100%), а також чутливішим за аналіз агрегації тромбоцитів і еталоном, за яким мають бути перевірені інші методи, він складний, дорогий, потребує радіоактивних сполук, надзвичайно трудомісткий і зазвичай вважається важкодоступним [25-29].
2. ELISA (фермент-пов’язаний імуносорбентний метод)
Лабораторна діагностика заснована на ідентифікації та/або кількісному визначенні PF4/антитіл до гепарину та має використовуватися винятково в пацієнтів із проміжною чи високою ймовірністю ГІТ.
Імуноаналіз (ELISA), який дозволяє виявити антитіла проти комплексу гепарин/PF4, має високу чутливість (90-95%), але низьку позитивну прогностичну цінність для виявлення клінічно значущих антитіл.
Джерелом PF4 при виконанні дослідження можуть бути рекомбінантний PF4, пов’язаний з гепарином, очищений PF4, пов’язаний з полівінілсульфонатом, лізати тромбоцитів, пов’язані з гепарином, іммобілізовані на поверхні лунки мікропланшета або частинки, що містять гепарин/PF4 як тверду фазу. В низці досліджень було показано обмеженість цього методу для діагностики ГІТ, оскільки захворювання підтвердили лише в 2-15% пацієнтів із позитивними антитілами. Обмеженням ELISA є те, що за використання цього методу виявляються як клінічно незначущі (непатогенні), так і клінічно значущі (патогенні) антитіла, які можуть реагувати з PF4 та гепарином, тому можна отримати позитивний результат за наявності непатогенних антитіл у хворих із ГІТ. Отже, виявлення антитіл до гепарину-PF4 методом ELISA не підтверджує ГІТ, проте негативний результат робить ГІТ украй малоймовірним. Нещодавно розроблені набори для аналізу ГІТ є більш селективними щодо патогенних антитіл і здатні виявляти лише патогенні антитіла IgG на відміну від антитіл IgA та IgM, що є непатогенними [30-33].
Із практичного погляду аналіз ELISA зазвичай клінічно доступний. Однак через своє обмеження, що полягає у неможливості розпізнавати клінічно значущі антитіла, що спричиняють ГІТ, його необхідно поєднувати із клінічними даними для встановлення діагнозу ГІТ.
3. Аналіз гепарин-індукованої активації тромбоцитів (HIPA)
Тест HIPA розроблено в 1991 р. і засновано на візуальній оцінці агрегації тромбоцитів у мікротитрувальній лунці з полістирольним U-подібним дном зі сталевими кульками, що обертаються та використовуються для перемішування тромбоцитів. Тромбоцити донора, сироватку пацієнта та гепарин перемішують за допомогою магнітного змішувача. Лунки оглядають візуально на тлі непрямого джерела світла з 5-хвилинними інтервалами. Зміна зовнішнього вигляду реакційної суміші від помутніння (неагрегованих тромбоцитів) до прозорості (агрегованих тромбоцитів) вважається позитивним результатом. Тест позитивний, якщо агрегація спостерігається протягом 30 хв [34-39].
Лікування ГІТ
Ключовим моментом у хворих із високим ступенем підозри чи підтвердженої гострої ГІТ є негайне припинення прийому гепарину (якщо він усе ще застосовується) та початок застосування альтернативних антикоагулянтів у терапевтичній дозі.
Для лікування ГІТ наразі схвалено 2 препарати – прямий інгібітор тромбіну аргатробан (США, Канада, Європейський Союз, Австралія) та інгібітор анти-Ха-фактора – данапароїд (Канада, Європейський Союз, Австралія).
Аргатробан часто застосовується в пацієнтів у критичному стані. Він має відносно нетривалий період напіврозпаду, що не залежить від функції нирок, але потребує внутрішньовенного введення. Оскільки аргатробан впливає на міжнародне нормалізоване відношення, перехід на варфарин має відбуватися за спеціальною схемою. У хворих із ГІТ для моніторингу терапії аргатробаном використовується такий лабораторний показник, як активований частковий тромбопластиновий час (АЧТЧ). На початку лікування необхідно визначити початковий рівень АЧТЧ, а надалі початкову дозу препарату слід скоригувати для досягнення стійкого значення АЧТВ у 1,5-3 рази вище від початкового рівня (не більше 100 с). АЧТЧ також слід визначати через 2 години після початку терапії та після будь-якої зміни дозування. Слід зазначити, що АЧТЧ може бути підвищеним у пацієнтів, котрі мають коагулопатію (наприклад, коагулопатію споживання або порушення функції печінки) чи в хворих, які попередньо отримували лікування варфарином. Така ситуація здатна зумовити недостатнє дозування аргатробану з ризиком прогресувального мікросудинного тромбозу та втратою кінцівок. Це обмеження можна обійти за допомогою аналізу зсідання крові на основі екарину (доступність якого обмежена) чи аналізу тромбінового часу із розведенням плазми (потрібний внутрішній стандарт аргатробану).
Данапароїд вводиться внутрішньовенно чи підшкірно. Цей препарат може надійно контролюватися за допомогою аналізу на анти-Xa-фактор. Цей препарат має тривалий період напіврозпаду, тому пацієнти з нирковою недостатністю потребують корекції дози. Підшкірна ін’єкція робить застосування цього препарату легшим, ніж аргатробану, оскільки дозволяє його використання поза відділенням інтенсивної терапії (табл. 4).
1-й вибір: данапароїд – за толерантності чи ниркової недостатності (CrCl <30 мл/хв) слід розглянути 2-й варіант.
2-й вибір: аргатробан – протипоказаний при тяжкій печінковій недостатності.
|
Таблиця 4. Лікування ГІТ |
|||
|
Доза |
Болюс в/в |
Інфузія в/в |
Моніторинг (цільова область) |
|
Данапароїд |
<55 кг: 1250 ОД 55-90 кг: 2500 ОД >90 кг: 3750 ОД |
400 Од/год протягом 2 год, потім 300 Од/год упродовж 2 год, згодом підтримувальна інфузія 200 Од/год протягом 5 днів |
Потрібна тільки при CrCl <30 мл/хв або за маси тіла >90 кг. Цільовий рівень анти-Ха складає 0,5-0,8 Од/мл |
|
Aргатробан (стандартна доза) |
Ні |
Почати з 2 мкг/кг/хв (розчин 1 мг/мл) |
Коефіцієнт АЧТЧ 1,5-3,0* (повторити протягом 2 год після зміни дози, щонайменше щодня) |
|
Aргатробан У критичному стані. Після операції на серці або за хвороби печінки |
Ні |
Почати |
Коефіцієнт АЧТЧ 1,5-3,0* (повторити протягом 4 год після зміни дози, щонайменше щодня) |
|
Примітка: * якщо коефіцієнт АЧТЧ перевищує 3,0, припинити інфузію аргатробану на 2 год доти, доки коефіцієнт АЧТЧ не знизиться до <3,0. Інфузію можна відновити з нижчою дозою. |
|||
Висновки
1. ГІТ є потенційно фатальним побічним ефектом гепарину, який частіше зустрічається при застосуванні НФГ, ніж НМГ.
2. ГІТ являє собою клініко-патологічний синдром: його діагноз ґрунтується на клінічних ознаках та наявності антитіл до ГІТ.
3. Антитіла проти PF4/гепарину зазвичай утворюються під час лікування гепарином. ГІТ виникає у пацієнтів з антитілами IgG, які активують тромбоцити.
4. Зв’язування ГІТ-антитіл із комплексами PF4/гепарин на поверхні тромбоцитів зумовлює активацію тромбоцитів, тромбоцитопенію та підвищення ризику артеріального тромбозу.
5. Активація тромбоцитів, моноцитів та ендотеліальних клітин спричиняє стан гіперкоагуляції та підвищений ризик венозного тромбозу.
6. Для діагностики ізольованої ГІТ важливим є моніторинг кількості тромбоцитів.
7. Моніторинг кількості тромбоцитів рекомендується більшості пацієнтів, які отримують НФГ і деяким хворим, котрі одержують НМГ.
8. Прийом гепарину слід негайно припинити в усіх ситуаціях, коли є серйозна підозра на ГІТ.
9. Через високий ризик тромбоутворення в пацієнтів із ГІТ антикоагулянтну терапію негепариновими антикоагулянтами слід розпочинати навіть за відсутності явного тромбозу.
10. Данапароїд забезпечує можливість антикоагулянтної терапії як у профілактичних, так і в терапевтичних дозах.
Список літератури знаходиться в редакції.