5 січня, 2024
Застосування гормону росту за різних форм низькорослості в дітей
 У листопаді 2023 р. в Чернівцях відбулося чергове засідання освітнього проєкту «Школа ендокринолога» з онлайн-трансляцією по всій Україні. У рамках заходу було розглянуто актуальні питання, які стосуються ендокринологічних захворювань та їхніх ускладнень, консервативного та хірургічного лікування таких станів, а також ведення хворих із супутньою патологією. Цього разу йшлося не лише про найпоширеніші ендокринологічні захворювання, з якими мало не щодня стикаються лікарі у своїй рутинній практиці, а й про більш рідкісні патології. Зокрема, про різні форми низькорослості в дітей і можливості терапії цих станів. На жаль, діагностика захворювання нерідко запізніла, а низькорослість тягне за собою цілу низку психологічних і соціальних проблем. Саме цій темі була присвячена доповідь доктора медичних наук, професора, завідувача відділення дитячої ендокринної патології ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» Наталі Андріївни Спринчук.
У листопаді 2023 р. в Чернівцях відбулося чергове засідання освітнього проєкту «Школа ендокринолога» з онлайн-трансляцією по всій Україні. У рамках заходу було розглянуто актуальні питання, які стосуються ендокринологічних захворювань та їхніх ускладнень, консервативного та хірургічного лікування таких станів, а також ведення хворих із супутньою патологією. Цього разу йшлося не лише про найпоширеніші ендокринологічні захворювання, з якими мало не щодня стикаються лікарі у своїй рутинній практиці, а й про більш рідкісні патології. Зокрема, про різні форми низькорослості в дітей і можливості терапії цих станів. На жаль, діагностика захворювання нерідко запізніла, а низькорослість тягне за собою цілу низку психологічних і соціальних проблем. Саме цій темі була присвячена доповідь доктора медичних наук, професора, завідувача відділення дитячої ендокринної патології ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» Наталі Андріївни Спринчук.
Проблема низькорослості
Протягом життя людина з низькорослістю стикається з певними психологічними та соціальними проблемами, зокрема:
- 56% помилково вважають, що вік молодший;
- 48% зазнають булінгу;
- 27% відчувають інше ставлення до них дорослих та інших дітей;
- 26% відчувають соціальний дискомфорт;
- 25% уникають участі у змаганнях та масових заходах.
Крім того, низькорослість має значний емоційний вплив:
- 63% турбує їх зріст;
- 38% непокояться з приводу їх відмінностей від однолітків;
- 33% мають низьку самооцінку;
- 21% переживають щодо свого подальшого розвитку;
- 21% перебувають у пригніченому стані і відчувають образу;
- 18% збентежені.
Отже, з огляду на значний травматичний вплив на якість життя пацієнтів із низькорослістю, вибір – лікувати чи не лікувати цей стан за наявності показань – не залишає сумнівів: лікувати!
Дефіцит ГР (ДГР) є клінічним синдромом, зумовленим зменшенням синтезу ГР або зниженням чутливості тканин до нього. ДГР може виникнути в будь-якому віці, є результатом як вроджених, так і набутих розладів, може бути як ізольованим, так і складовою множинної недостатності гіпофіза.
До вроджених причин ДГР належать: мутації генів, що кодують ГР, ГР-рецептор, рецептор рилізинг-гормону ГР (РГГР) і різні фактори транскрипції.
Іншою групою причин можуть бути структурні дефекти гіпоталамо-гіпофізарної ділянки: синдром «порожнього» турецького сідла, септо-оптична дисплазія, гіпоплазія гіпофіза, внутрішньочерепні пухлини, черепно-мозкові травми (ЧМТ), інфекція центральної нервової системи (ЦНС), інфаркт (синдром Шихана), інфільтративне/гранулематозне захворювання (саркоїдоз, гістіоцитоз, туберкульоз) та ін.
Лікування гіпоталамо-гіпофізарних уражень (променева терапія та хіміотерапія) також може спричиняти ДГР.
Критерії відбору для діагностики недостатності ГР у дітей
Якщо раніше показанням до призначення обстеження і подальшої терапії були явні генетичні порушення (наприклад, синдром Шерешевського–Тернера) і дефіцит соматотропного гормону, то сьогодні критерії відбору таких дітей значно розширилися, а саме:
- антропометричні показники: дефіцит росту – нижче -2,0 SD (SD – standard deviation, стандартне відхилення) від популяційної медіани для заданих хронологічного віку і статі;
- швидкість росту – важливий кумулятивний показник динаміки росту в часі – становить <1,0 SD. Виникає в дітей з органічними ураженнями і проявляється як зупинка раніше нормальної динаміки росту в будь-якому віці;
- кістковий вік – відставання більш ніж на 2 роки.
Визначення рівня інсуліноподібного фактора росту‑1 – перший крок у діагностиці ДГР
Визначення рівня інсуліноподібного фактора росту‑1 (IФР‑1) може використовуватись як скринінговий тест діагностики ДГР завдяки високій специфічності (72%) і тому, що рівень ІФР-1 практично не змінюється впродовж доби.
Рівень ІФР‑1 напряму залежить від віку, статі та стадії статевого дозрівання і може знижуватись у разі ДГР, неповноцінного харчування, некомпенсованої патології печінки, нирок та інших паренхіматозних органів тощо. Тому, коли ми бачимо, що є зниження рівня ІФР-1, – це ще не означає, що є зниження рівня ГР і потрібні подальші дослідження.
Діагностика недостатності ГР
Визначення базального рівня ГР сироватки та нічного піку мало інформативні, але можуть бути корисними. Більш інформативним є визначення спонтанних викидів ГР – протягом доби кожні 3-5 год до 20 нг/мл, час напіввиведення гормону становить 10-20 хвилин. Це дуже корисний метод дослідження за наявності протипоказань до проведення стимуляційних тестів або в разі відмови батьків від їх проведення. Катетер встановлюють на кілька годин і кожні 30 хв здійснюють забір крові. У разі спонтанного викиду ГР його вдається зафіксувати.
Стимуляційні тести – золотий стандарт діагностики. Для його проведення застосовують інсулін, аргінін, глюкагон, грелін (масиморелін), клонідин. У нормі рівень ГР піднімається до ≥10 нг/мл.
Треба зазначити, що на сьогодні поняття часткової недостатності ГР, яке застосовували раніше, відсутнє. Можливі індивідуальні коливання його рівня, тому точка відхилення становить 10 нг/мл. Варто пам’ятати, що ЧМТ, субарахноїдальний крововилив і променева терапія можуть мати транзиторні наслідки, тому стимуляційні тести проводять не раніше ніж через 12 міс після події.
Ще один показник, який можна використовувати для диференційної діагностики справжньої недостатності ГР з його дефіцитом за наявності соматичних причин, – це визначення рівня ІФР‑1-зв’язувального білка 3 (ІФР‑1-ЗБ‑3), який регулюється ГР, напряму корелює з рівнем ІФР‑1, але, на відміну ІФР‑1, менше залежить від індексу маси тіла (ІМТ).
Діагностика недостатності ГР у період пубертату
Діагностика недостатності ГР у період пубертату лишається дискутабельним питанням, але останнім часом все більше рекомендацій пропонують призначати статеві стероїди перед провокаційним тестом на ДГР у хлопчиків віком понад 11 років і дівчаток віком понад 10 років із прогнозованим ростом у межах -2 SD із метою запобігання некоректному лікуванню ГР дітей із конституціональною затримкою росту. Найліпші доступні докази існують для хлопчиків, але їх екстраполюють і на дівчат.
Розумним підходом для дівчаток буде призначення перорально 2 мг (1 мг для маси тіла <20 кг) β-естрадіолу (не етинілестрадіолу) два вечори поспіль перед тестом. У хлопчиків можна застосовувати тестостерон в/м у дозі 50-100 мг депо-препарату за тиждень перед тестом.
Ця рекомендація стосується пацієнтів, які раніше не отримували препарати ГР, а також тих пацієнтів, які мають біологічний статус, подібний до пубертатного – старше 10 років. Якщо біологічний статус менший (6-7 років), а хронологічний більший (10-11 років), то призначати ці препарати є недоцільним.
У процесі діагностики необхідно враховувати чинники, які здатні впливати на рівень ГР. Так, основними фізіологічними стимуляторами секреції та вивільнення ГР є глибокий сон, фізичне навантаження, голод і гіпоглікемія, стрес, статеві стероїди, амінокислоти (аргінін, лейцин).
До факторів, які пригнічують секрецію ГР, належать ожиріння, глюкокортикоїди, глюкоза, гіпотиреоз, ІФР‑1 (негативний зворотний зв’язок), β-адренергічні стимулятори та вільні жирні кислоти.
Редіагностика недостатності ГР
Редіагностику проводять не завжди і не всім пацієнтам. Потреба в ній може виникати:
- у постпубертатному періоді та в дорослих для уточнення або підтвердження діагнозу;
- за умови ізольованої недостатності ГР та після опромінення;
- через місяць після відміни лікування препаратами рекомбінантного ГР (рГР).
При діагностуванні ізольованої соматотропної недостатності ГР у дитинстві діагноз у дорослих підтверджується в 30-50% випадків. Важливість і необхідність терапії ізольованої соматотропної недостатності ГР в дорослих, яка в них була свого часу діагностована в дитинстві, уже доведені.
Діагностику не проводять пацієнтам:
- із множинною недостатністю аденогіпофіза (вроджена, генетична або післяопераційна) за умови рівня ІФР‑1 <-2 SDS (standard deviation score, коефіцієнт стандартного відхилення);
- зі вродженими вадами гіпоталамо-гіпофізарної ділянки за рівня IФР‑1 <-2 SDS;
- з ідіопатичним ізольованим ДГР за рівня ІФР‑1 <-2 SDS.
Тест на толерантність до інсуліну є золотим стандартом діагностики ДГР у дорослих і в перехідний період. Граничний рівень ГР 5,6 мкг/л мав найвищу діагностичну точність для прогнозування стійкого ДГР із чутливістю 77%, специфічністю 93%, правильністю діагнозу 87%.
Тест зі стимуляцією глюкагоном є перспективною альтернативою в дорослих, але не був схвалений під час перехідного періоду.
Лікування недостатності ГР у дітей
Основною метою лікування недостатності ГР у дітей є досягнення оптимального кінцевого зросту. Тому до закриття епіфізарних зон призначають рГР у дозі 0,025-0,033 мг/кг/добу. Як правило, ця доза є достатньою в переважній більшості випадків і не потребує подальшого титрування під час вибору ефективного препарату з доведеною ефективністю, до яких належить соматропін – Генотропін® (Pfizer, США).
З метою контролю ефективності лікування рекомендують визначати рівень ІФР‑1 і швидкість росту кожні 3-4 місяці.
Біологічно неактивний ГР
У разі біологічно неактивного ГР (БНГР) низькорослість поєднується з нормальним або навіть підвищеним рівнем соматотропного гормону (СТГ), але зменшенням чутливості периферичних тканин до дії ГР, тому призначення препаратів ГР буде неефективним, а час і кошти пацієнта будуть витрачені даремно. У цьому разі призначають препарати соматомедину, який, на жаль, поки не зареєстрований в Україні.
Лабораторними критеріями БНГР є: рівень СТГ нормальний або підвищений, рівень ІФР‑1 значно знижений, обов’язковий критерій – відсутність соматичної патології та нормальний IMT. Також діагноз підтверджує позитивний тест на чутливість до ГР (4-денна проба). Його проводять для диференційної діагностики синдрому БНГР з нечутливістю рецепторів до ГР. Вводять ГР у дозі 0,033 мг/кг/добу протягом 4 днів увечері, на 1-й і 5-й день уранці визначають рівень ІФР‑1. Пробу вважають позитивною в разі підвищення рівня ІФР‑1 у ≥2 рази.
Остаточний діагноз встановлюють у разі медико-генетичного підтвердження, оскільки нерідко спостерігають змішані форми БНГР та нечутливості рецепторів до нього, тому в разі позитивної 4-денної проби призначають препарати рГР у дозі 0,35-0,05 мг/кг/добу з індивідуальним титруванням.
Низькорослість і пубертат
Відсутність ростового «стрибка» у дітей під час статевого дозрівання потрібно розцінювати як прояв часткової соматотропної недостатності (необхідне проведення тестів на стимуляцію ГР), навіть якщо до цього періоду зріст відповідав нормальним показникам. У такому разі показано призначення препаратів ГР, починаючи з пубертату.
У США отримано схвалення на застосування вищих доз гормону в пацієнтів із ДГР під час статевого розвитку (індивідуальне титрування ГР) від 0,3 мг/кг/тиж (0,043 мг/кг/добу) до 0,7 мг/кг/тиж (0,1 мг/кг/добу). Це дуже висока доза, однак за умови регулярної оцінки показників і своєчасного титрування вона може бути виправдана, особливо в разі ідіопатичної низькорослості (ІН).
Ідіопатична низькорослість
Під ІН розуміють зріст нижче -2 SD відносно віку і статі. Існують форми ІН – сімейна і не сімейна із затримкою пубертату та без неї.
Критеріями ІН є нормальні довжина та маса тіла під час народження, відсутність диспропорцій у будові тіла, хронічних системних захворювань (з боку серця, легень, нирок та ін.), психоемоційних (стресових) чинників, аліментарних факторів і ферментопатій, інших ендокринопатій.
Для діагностики проводять дослідження функції СТГ (нормальна), рівня ІФР‑1 (нормальний або на нижній межі норми), пробу на продукування ІФР‑1 до ГР (слабо позитивна).
Під час диференційної діагностики треба звернути увагу на непропорційну низькорослість.
Наявність диспропорцій є показанням для проведення молекулярних досліджень найпоширеніших скелетних дисплазій (FGFR3, SHOX, NPR2, COMP, COL9A1, COL9A2, COL9A3, MATN3), оскільки такі пацієнти погано відповідають на терапію ГР через знижену чутливість рецепторів (переважно периферичних) до ГР.
Якщо низькорослість є пропорційною і має пренатальне походження, необхідно проаналізувати хромосомопатії та синдроми. Каріотипування показано для виключення хромосомопатій. Якщо є підозра на специфічний синдром із відомим молекулярним дефектом, треба провести молекулярне дослідження для його підтвердження. Якщо немає підозри на конкретний діагноз, можуть бути показані загально-геномні асоційовані дослідження або дослідження екзомів.
Скринінгові дослідження для уточнення IH:
- лабораторні: загальний аналіз крові, рівень креатиніну, електролітів, бікарбонатів, фосфату кальцію, альбуміну, тиреотропного гормону (ТТГ), Т4 вільного та IФР‑1;
- рекомендується скринінг на целіакію та ферментопатії. Рівень СТГ у таких пацієнтів у нормі, рівень IФР‑1 знижений, і, як правило, виявляють підвищення вмісту аланінамінотрансферази (AЛT). Правильна корекція ферментопатій у цьому випадку забезпечує дуже швидкий результат;
- каріотип треба визначати в усіх дівчат із незрозумілим низьким зростом, а також у низьких хлопчиків із супутніми аномаліями статевих органів;
- необхідно проводити рентгенологічне дослідження кистей та оцінювати рентген-вік. Це дає вказівки на потенціал росту дитини і звужує диференційну діагностику. Гормональна недостатність завжди супроводжується відставанням біологічного віку, тоді як для генетичних порушень це не характерно – відставання біологічного віку відсутнє або незначне;
- обстеження скелета потрібно проводити в пацієнтів із підозрою на хондродисплазію з аномальними пропорціями тіла або з SDS росту, значно нижчим за середній зріст батьків. Пацієнта має проконсультувати ортопед.
Лікування ІН
При лікуванні ІН рекомендовано призначати ГР кожній дитині зі зростом <-2,25 SD. Однак у клінічній практиці доводиться стикатися з тим, що ця точка відхилення вже запізніла і в такому разі не вдається досягти тих результатів, на які можна було б розраховувати, якщо почати терапію при затримці росту <-2 SD. У деяких країнах саме цей показник є точкою відхилення і показанням для початку терапії.
Дослідження показали, що застосування ГР збільшує середній зріст у когортах, але спостерігають помітну індивідуальну варіабельність, у тому числі є особи, які не реагують на лікування.
Подальшу оцінку користі застосування ГР пропонують проводити за SDS росту та психосоціальним станом протягом 12 міс після початку його застосування та оптимізації дози.
Розпочинати лікування ГР пропонують із дози 0,24 мг/кг/тиж (0,035 мг/кг/добу), деяким пацієнтам потрібна доза до 0,47 мг/кг/тиж (0,067 мг/кг/добу).
Золотим стандартом терапії низькорослості є препарат Генотропін® (Соматропін [походження рДНК] для ін’єкцій), нову інструкцію якого було перероблено і затверджено в жовтні 2023 року. Препарат показаний для лікування ІН, тобто низькорослості без ДГР, визначеної за SDS <-2,25 (темпи зростання, за яких досягнення нормального діапазону зросту в дорослому віці є малоймовірним), у дітей із незакритими епіфізарними зонами росту, в яких діагностична оцінка виключає інші причини низькорослості, що потребують спостереження або лікування за допомогою інших засобів.
Питання безпеки застосування ГР
При проведенні терапії ГР слід проводити скринінг можливих негативних проявів і безпеки лікування в усіх категоріях реципієнтів, а саме:
- визначення рівнів ІФР‑1 як моніторинг адекватності дози ГР;
- зниження дози ГР, якщо рівні ІФР‑1 перевищують референтний діапазон для віку та стадії статевого дозрівання;
- оцінка функції надниркових залоз і щитоподібної залози після початку терапії ГР і розгляд питання про призначення або підвищення доз гідрокортизону і/або левотироксину;
- оцінка та контроль метаболізму глюкози;
- консультації щодо ризику неоплазії;
- рекомендації щодо можливих несприятливих наслідків: внутрішньочерепної гіпертензії, епіфізеолізу головки стегнової кістки, прогресування наявного сколіозу (у пацієнтів із 3-4-ю стадією, необхідно порадитися з ортопедом на початку терапії, щоб уникнути прогресування захворювання).
Прийом ГР скасовують у таких випадках: злоякісні пухлини, швидкість росту менш ніж 2-2,5 см/рік (низька чутливість до ГР, наявність автоантитіл до ГР, закриті зони росту), кістковий вік у хлопчиків >16 років, у дівчат >15 років, досягнення бажаного зросту.
Зниження дози рГР необхідне в разі серйозних негативних проявів, маніфестації цукрового діабету, загострення внутрішньочерепної гіпертензії тощо.
Затримка внутрішньоутробного розвитку (ЗВУР)
Ще одна патологія, яка є причиною великої кількості питань і дискусій, – це ЗВУР, щодо якої було досягнуто консенсусу у 2023 р. (International Consensus Guidelines on Small for Gestational Age: Etiology and Management From Infancy to Early Adulthood, 2023). Цю міжнародну настанову розроблено експертами в галузі малого гестаційного віку (SGA) 10 педіатричних ендокринних товариств з усього світу. Усі експерти проголосували за сильні сторони рекомендацій, які дають нове та клінічно значуще уявлення про етіологію ЗВУР, у тому числі нові знання про епігенетичні причини. Наведено віддалені наслідки ЗВУР, нові варіанти лікування, у тому числі з використанням агоністів гонадотропін-рилізинг-гормону (аГРГ) на додаток до ГР. Для діагностики ЗВУР рекомендовано проводити точну антропометрію з використанням національних діаграм зросту.
Диференційна діагностика та лікування ЗВУР
Дітей віком 2 роки зі ЗВУР та стійким низьким зростом <-2,5 SDS або дітей віком 3-4 роки зі зростом <-2 SDS потрібно направляти на діагностичне обстеження (рівні СТГ, ІФР‑1). Якщо причина ЗВУР була пов’язана не з плодом, а з плацентарною недостатністю через патологію в матері, такі діти досить швидко відновлюються і наздоганяють у розвитку своїх однолітків. У разі дисморфічних ознак, серйозних вад розвитку, мікроцефалії, інтелектуальної недостатності та/або наявності ознак скелетної дисплазії треба розглянути можливість генетичного тестування.
Застосування ГР у дозі 0,033-0,067 мг/кг/добу рекомендовано в разі стійкого низького зросту в дітей віком 3-4 роки. Треба розглянути можливість додавання аГРГ до ГР на початку статевого дозрівання протягом 2 років, якщо очікуваний зріст дорослої людини буде нижче за -2,5 SDS. Усім дорослим особам молодого віку, народженим зі ЗВУР, потрібна консультація, щоб вести здоровий спосіб життя для запобігання кардіометаболічним ускладненням.
Застосування препаратів ГР в разі передчасного статевого розвитку
Проблема передчасного статевого дозрівання полягає в тому, що діти мають високорослість і є вищими за своїх однолітків, але якщо прорахувати кінцевий зріст, він буде низьким, тому що в таких дітей дуже швидко закриваються зони росту. Інша проблема в цій категорії пацієнтів – необхідність тривалого (декілька років) призначення аГРГ, що уповільнює процес статевого дозрівання, але знижує концентрацію ГР і такі діти згодом можуть відставати в рості.
Препарати ГР рекомендовано призначати пацієнтам, що застосовують аГРГ, за умови зниження швидкості росту в результаті зменшення концентрації ГР та IФР‑1. Рекомендовані дози – такі самі, як і в разі ДГР. Підсумовуючи, наводимо зручну схему ведення пацієнтів із порушеннями росту залежно від рівня ІФР-1 в процесі діагностики (див. рис.).
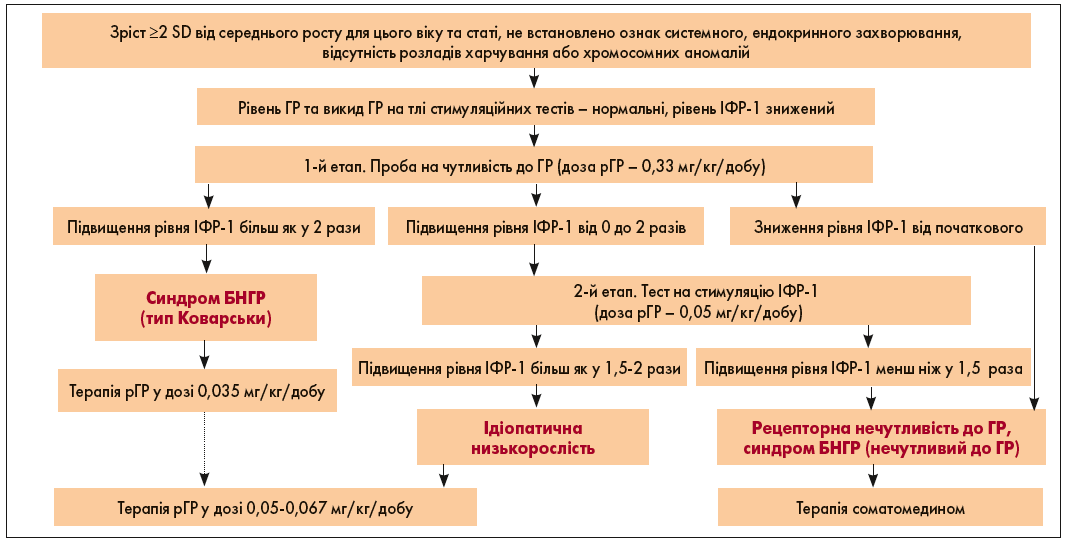 Рис. Проба на генерацію ІФР-1 до ГР
Рис. Проба на генерацію ІФР-1 до ГР
Новинки в лікуванні ДГР
Наразі в Україні проходить реєстрацію пролонгований препарат ГР для щотижневого введення – Енжела® (соматрогон) (Pfizer, США).
Дефіцит ГР є найпоширенішим дефіцитом гормону гіпофіза в дітей, його основними клінічними ознаками є низький зріст і низька швидкість росту. Точна своєчасна діагностика і лікування є критично важливими для поліпшення результатів у дітей із ДГР. Дотримання щоденної терапії ГР є неоптимальним, що впливає на результати лікування, тому застосування пацієнтами препаратів ГР тривалої дії має вищий комплаєнс і сприяє поліпшенню клінічних результатів.
Соматрогон (Енжела®) – нова молекулярна структура, що містить 3 копії СТР (carboxyl-terminal peptide) з бета-ланцюгом рГР, таким чином збільшуючи період напіврозпаду, що дає можливість застосовувати препарат 1 раз на тиждень. Дослідження фази 2 і 3 продемонстрували подібну річну швидкість росту, досягнуту за допомогою застосування соматрогону 1 раз на тиждень і соматропіну 1 раз на добу. Найпоширенішими побічними ефектами, пов’язаними з лікуванням, були реакції в місці ін’єкції. Щотижневе введення соматрогону загалом добре переносилося пацієнтами з ДГР. Технологія СТР дає можливість використовувати соматрогон (Енжела®) у пролонгованому дозуванні. Період напіввиведення соматрогону становить 28,2 год, тоді як період напіврозпаду рГР – 2-3 год. Механізм дії – подібний до такого рГР.
Висновки
- Життя з низькорослістю зумовлює значні психологічні проблеми.
- Дітям з IН та ЗВУР, поряд із ДГР, схвалено застосування препаратів ГР.
- В Україні тільки Генотропін® показаний для лікування ІН у дозі від 0,035 до 0,067 мг/кг/добу.
- Застосування препаратів ГР пролонгованої дії в дітей із низькорослістю демонструє клінічну ефективність завдяки більш високій прихильності педіатричної популяції до лікування.
Підготувала Ірина Чумак
Тематичний номер «Діабетологія. Тиреоїдологія. Метаболічні розлади» № 4 (64) 2023 р.



 Спринчук Н. А.
Спринчук Н. А.