29 лютого, 2024
Комбінована терапія розувастатином та езетимібом у пацієнтів із дисліпідемією та ризиком серцево-судинних і цереброваскулярних захворювань
Серцево-судинні захворювання (ССЗ) залишаються основною причиною смерті у світі. За оцінками Всесвітньої організації охорони здоров’я (ВООЗ), щорічні втрати від них сягають понад 17 млн осіб (близько 30% загальної смертності); серед причин смерті лідирують ішемічна хвороба серця (ІХС) та цереброваскулярна патологія (WHO, 2021). Одним із чинників ризику ССЗ є дисліпідемія, що потребує ретельного контролю параметрів ліпідного обміну, передусім рівня холестерину ліпопротеїдів низької щільності (ХС ЛПНЩ).
У країнах із низьким і середнім рівнями доходу тягар передчасної смертності є непропорційно високим порівняно з країнами з високим рівнем доходу (WHO, 2021). В Україні ССЗ є причиною майже 2/3 усіх випадків смерті, і цей показник лишається одним із найвищих серед країн Європи (близько 50 тис. випадків інфаркту міокарда [ІМ] і 111 тис. випадків інсульту на рік, причому останній є причиною до 50 тис. смертей, а майже у 20 тис. пацієнтів призводить до інвалідизації) (Chistik, 2022).
Небезпека полягає ще й у тому, що ІМ та інсульт, які раніше вважалися захворюваннями похилого віку, сьогодні значно «помолодшали». Так, за даними Міністерства охорони здоров’я України, у структурі захворюваності працездатного населення на хвороби системи кровообігу припадає 24% (здебільшого це ІМ та інсульт). У структурі смертності від цих захворювань частка осіб працездатного віку становить 9,3% (від гострого ІМ помирають 18,7%, інсульту – 17,4% (Chistik, 2022; Савустьяненко, 2015).
Головними причинами зростання захворюваності на ССЗ, зокрема серед представників молодшого покоління є: тютюнопаління, зловживання алкоголем, стрес, гіподинамія, надмірна маса тіла / ожиріння, цукровий діабет (ЦД), високий артеріальний тиск (АТ), дисліпідемія. Часто ці чинники поєднуються й діють синергічно, підвищуючи сукупний ризик виникнення гострих судинних патологій. Ефективна профілактика ССЗ ґрунтується на відповідних стратегіях контролю чинників ризику.
Дисліпідемія – вроджена чи набута патологія обміну жирів, яка супроводжується порушенням їх синтезу, транспорту та виведення з крові – є найактуальнішим модифікованим чинником атеросклеротичних ССЗ. Самостійно або у взаємодії з іншими ризиками дисліпідемія може спричиняти маніфестацію атеросклеротичного процесу, внаслідок чого відбувається звуження просвіту судин, нерідко з тромбуванням і розвитком серцево-судинних (СС) катастроф (Ferri et al., 2023; Mach et al., 2020).
Лікування дисліпідемії, зокрема зниження підвищеного рівня ХС ЛПНЩ, є невід’ємною складовою ведення пацієнтів із СС ризиком. У низці досліджень доведено ключову роль ХС ЛПНЩ у формуванні атеросклерозу, а також пряму залежність між вмістом ХС ЛПНЩ та ймовірністю розвитку ССЗ. Як зазначають дослідники, на кожен 1 ммоль/л зменшення концентрації ХС ЛПНЩ у крові можна очікувати зниження відносного ризику розвитку ССЗ майже на 20% (Silverman et al., 2016).
За настановою Європейського товариства кардіологів і Європейського товариства атеросклерозу (ESC/EAC, 2019), для осіб із дуже високим СС ризиком рекомендований цільовий рівень ХС ЛПНЩ <1,4 ммоль/л (або зниження рівня ХС ЛПНЩ щонайменше на 50% проти вихідного рівня). У разі високого СС-ризику терапевтична тактика має забезпечувати зниження на ≥50% ХС ЛПНЩ проти початкового показника та досягнення цільового рівня ХС ЛПНЩ <1,8 ммоль/л. За помірного СС-ризику прагнути цільового рівня ХС ЛПНЩ <2,6 ммоль/л, а якщо ризик низький – <3,0 ммоль/л (Mach et al., 2020). Ефективними шляхами зменшення концентрації ХС ЛПНЩ є інгібування біосинтезу ХС (терапія статинами) та блокування адсорбції ХС у кишечнику (зокрема, завдяки прийманню езетимібу).
Вибір належної гіпохолестеринемічної терапії має основоположне значення, оскільки відносне зниження ризику великих судинних подій не залежить від початкових рівнів ХС ЛПНЩ або наявності ЦД чи хронічної хвороби нирок (ХХН), але є пропорційним рівню зниження вмісту ХС ЛПНЩ. При цьому поєднання інтенсивності лікування та дотримання належної прихильності ефективнішому сприяє зниженню рівня ХС ЛПНЩ та, відповідно, СС наслідків у пацієнтів із високим ризиком (Khunti et al., 2018). Комбіновану терапію широко використовують для лікування таких захворювань, як артеріальна гіпертензія (АГ) та ЦД. Щодо лікування дисліпідемії, то цей фармакологічний підхід почали застосовувати відносно нещодавно.
Ефективність ліпідознижувальної терапії статинами
Статини – це група препаратів, які контролюють синтез ХС у печінці завдяки інгібуванню ферменту 3-гідрокси‑3-метилглутарил-кофермент А редуктази. Згідно з рекомендаціями ESC/EAC (2019) та Американської кардіологічної асоціації й Американської колегії кардіологів (AHA/ACC, 2018), статини є засобами першої лінії терапії за гіперхолестеринемії та комбінованих гіперліпідемій, яку призначають для профілактики ССЗ (Mach et al., 2020; Grundy et al., 2018). Результати масштабного метааналізу даних 26 рандомізованих клінічних досліджень (РКД) за участю 170 тис. пацієнтів продемонстрували, що зниження рівня ХС ЛПНЩ на кожен 1 ммоль/л із використанням лише статинів супроводжується зменшенням смертності: із будь-яких причин – на 10%, через основні СС-ускладнення – на 23%, через інсульт – на 17% (Baigent et al., 2010).
Розувастатин – потужний статин із доведеною ефективністю
Одним із найпотужніших і широкодоступних представників статинів є розувастатин – гідрофільний статин із високою гепатоселективністю, низькою системною біодоступністю (дуже обмеженим проникненням до позапечінкових тканин і, отже, низьким ризиком міотоксичності), із мінімальним залученням до метаболізму системи цитохрому Р450, що зумовлює його хорошу переносимість. Даних про клінічно значущу взаємодію розувастатину та ліків, що інгібують систему CYP, нині бракує (Semenova and Sergienko, 2018).
Ефективність і безпеку розувастатину для пацієнтів різних груп оцінювали в багатьох клінічних дослідженнях завдяки програмі GALAXY, яка охоплює дані 23 багатоцентрових клінічних РКД, названі за іменами космічних об’єктів. Зокрема, дослідження COMETS, DISCOVERY, LUNAR, MERCURY-I, MERCURY-II, ORBITAL тощо були присвячені вивченню впливу на ліпідний профіль і маркери запалення; ASTEROID, METEOR, ORION, COSMOS, SATURN – оцінюванню прогресування атеросклерозу в коронарних і сонних артеріях; AURORA, CORONA та JUPITER – впливу на прогноз захворювання (Schuster, 2007).
Лікування розувастатином (5‑40 мг на добу) допомагає знижувати рівень ХС ЛПНЩ на 39‑55% (за даними метааналізів – до 52‑63%) (Barter et al., 2010). Це потужний статин за здатністю знижувати рівень загального ХС і ХС ЛПНЩ із доведеною можливістю знижувати також рівень тригліцеридів (ТГ) та підвищувати рівень холестерину ліпопротеїдів високої щільності (ХС ЛПВЩ) (Toth and Dayspring, 2011). За призначення пацієнтам із гіперхолестеринемією розувастатин (10‑40 мг/добу) підвищує рівень ХС ЛПВЩ до 14% і знижує рівень ТГ до 28%. При цьому 90% максимально можливого гіполіпідемічного ефекту розувастатину вдається досягти через 2 тижні від початку лікування. Виразність гіполіпідемічної дії робить розувастатин препаратом вибору для пацієнтів із сімейною гіперхолестеринемією (Wiegman et al., 2015). Хоча терапія статинами не завжди є ефективною щодо досягнення цільових рівнів ХС ЛПНЩ, особливо для осіб високого та дуже високого ризику. Зокрема, у дослідженні за участю 165 тис. пацієнтів без ССЗ в анамнезі, але з ризиком їх розвитку, яким було призначено гіполіпідемічну терапію статинами, понад 50% не досягли цільового рівня ХС ЛПНЩ (Akyea et al., 2019). Це значно підвищило ризик ССЗ, зокрема ІХС, інсультів та захворювань периферичних артерій. Ще гірша ситуація спостерігається серед осіб із дуже високим СС-ризиком. Метою епідеміологічних досліджень DYSIS І та ІІ було оцінити ефективність контролю гіперліпідемії у пацієнтів, які отримували статини. За результатами дослідження, в умовах реальної клінічної практики цільового рівня ХС ЛПНЩ досягла лише незначна частка осіб із дуже високим СС ризиком. Так, у дослідженні DYSIS ІІ за участю понад 10 тис. осіб із дуже високим СС ризиком, цільового рівня ХС ЛПНЩ (<1,8 ммоль/л) вдалося досягти лише 29,4% пацієнтів із ІХС та 18,9% – із гострим коронарним синдромом (Gitt et al., 2017). Попри безумовну ефективність статинів, лікування препаратами цього класу може бути недостатньо для досягнення рекомендованих цільових показників ХС ЛПНЩ у пацієнтів із високим і дуже високим СС ризиком і для контролю рівня ТГ за змішаної гіперліпідемії (Ferri et al., 2023).
Дані досліджень DA VINCI і SANTORINI свідчать, що серед європейських пацієнтів із високим і дуже високим ризиком атеросклеротичних ССЗ лише 20‑33% досягають цільових показників рівня ХС ЛПНЩ. Тому перспективною стратегією є комбінування статинів із препаратами інших класів, зокрема езетимібом (Ray et al., 2021; Ray et al., 2023).
Механізм дії езетимібу
Езетиміб – це представник нового класу ліпідознижувальних речовин, які селективно пригнічують інтестинальну абсорбцію холестерину. Йому притаманний відмінний від інших класів гіполіпідемічних засобів (зокрема, статинів) механізм дії. Він гальмує всмоктування ХС без впливу на абсорбцію ТГ, жирних кислот, жовчних кислот, прогестерону, етинілестрадіолу та жиророзчинних вітамінів А і D. Інгібуючи всмоктування ХС на рівні ворсинок слизової оболонки тонкого кишківника завдяки взаємодії з білком Niemann-Pick C1-Like 1 (NPC1L1), езетиміб знижує рівень ХС, що надходить до печінки (Ouchi et al., 2019). Це сприяє активації рецепторів ЛПНЩ, що супроводжується посиленням кліренсу ХС ЛПНЩ із крові. За терапії езетимібом інгібування NPC1L1 зумовлює зниження всмоктування ХС на 54% порівняно з прийманням плацебо, що сприяє зниженню рівня ХС ЛПНЩ на 20,4% та збільшенню рівня ХС ЛПВЩ майже на 3% (Sudhop et al., 2002).
Ефективність комбінованої терапії розувастатином та езетимібом
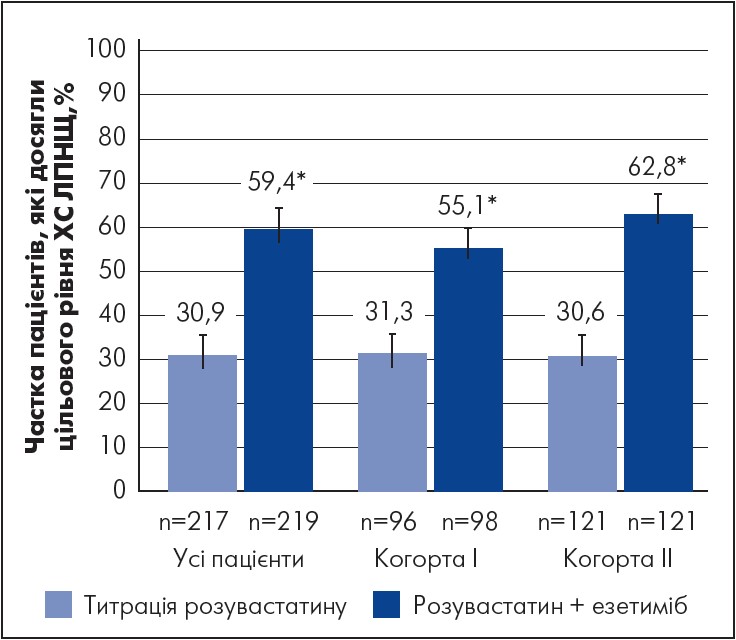
У багатоцентровому (57 центрів у 10 країнах) 6-тижневому рандомізованому подвійному сліпому клінічному дослідженні з паралельними групами (ACTE) порівнювали ефективність і безпеку двох стратегій лікування пацієнтів (440 чоловіків і жінок віком 18‑79 років) із гіперхолестеринемією та високим СС-ризиком: додавання езетимібу до розувастатину та підвищення дози розувастатину (Bays et al., 2011). Первинною метою дослідників було порівняти ефективність додавання езетимібу до схеми лікування розувастатином (5 або 10 мг) та подвоєння дози розувастатину (із 5 до 10 мг/добу або з 10 до 20 мг/добу) щодо зниження рівня ХС ЛПНЩ. До спостереження було залучено пацієнти з гіперхолестеринемією та високим / дуже високим ризиком розвитку ішемічної хвороби серця (ІХС), які не досягали рівня ХС ЛПНЩ, рекомендованого для лікування дорослих Національною освітньою програмою США з питань холестерину (NCEP ATP III), а саме <2,6 ммоль/л для осіб із високим / дуже високим ризиком без атеросклерозу та <1,8 ммоль/л для пацієнтів із дуже високим ризиком, які страждають на атеросклероз судин. Додатково порівнювали ефективності терапевтичних підходів щодо зниження рівня ХС ЛПНЩ залежно від стартової дози розувастатину; досягнення рекомендованого згідно з NCEP ATP III вмісту ХС ЛПНЩ (<1,8 або <2,6 ммоль/л); зміни відносно з вихідним значенням рівня інших ліпідів; а також оцінювання безпеки терапії. За дизайном дослідження, 197 (44,8%) пацієнтів отримували розувастатин у відкритому режимі в дозі 5 мг/добу, 243 (55,2%) пацієнти – у дозі 10 мг/добу протягом 4‑5 тижнів вступного періоду. Надалі осіб, які приймали розувастатин (5 мг) упродовж вступного періоду (когорта І), рандомізували на дві групи: учасники першої продовжували приймати по 5 мг розувастатину і додатково – по 10 мг езетимібу; другої – проводили титрацію стартової дози розувастатину до 10 мг. Пацієнтів, які приймали розувастатин (10 мг) упродовж вступного періоду (когорта ІІ), теж рандомізували на дві групи: учасники першої продовжували приймати по 10 мг розувастатину і додатково – по 10 мг езетимібу; другої – проводили титрацію стартової дози розувастатину до 20 мг. Додавання езетимібу (по 10 мг) до стартової дози розувастатину допомогло досягти суттєвішого зниження рівня ХС ЛПНЩ, ніж підвищення дози розувастатину як серед усіх пацієнтів (первинна кінцева точка), так і окремо в когортах (вторинна кінцева точка). Значно більшій частці пацієнтів із високим / дуже високим ризиком ІХС без атеросклерозу судин вдалося досягти рівня ХС ЛПНЩ <2,6 ммоль/л та значно більшій частці пацієнтів із дуже високим ризиком ІХС та з атеросклерозом судин – досягти рівня ХС ЛПНЩ <1,8 ммоль/л у разі додавання до стартової дози розувастатину езетимібу (по 10 мг), ніж за титрації дози розувастатину в бік збільшення (рис. 1).
Примітки: всі пацієнти (об’єднані дані): додавання 10 мг езетимібу до 5 або 10 мг розувастатину порівняно з титрацією розувастатину до 10 чи 20 мг; когорта І – додавання 10 мг езетимібу до 5 мг розувастатину порівняно з титрацією розувастатину до 10 мг; когорта II – додавання 10 мг езетимібу до 10 мг розувастатину порівняно з титрацією розувастатину до 20 мг; * p<0,001.
Рис. 1. Досягнення цільового рівня ХС ЛПНЩ після 6 тижнів терапії в межах дослідження ACTE
Адаптовано за H. E. Bays et al. Safety and efficacy of ezetimibe added on to rosuvastatin 5 or 10 mg versus up-titration of rosuvastatin in patients with hypercholesterolemia (the ACTE Study). Am J Cardiol. 2011 Aug 15. Vol. 108, № 4. Р. 523‑30.
Результати аналізу об’єднаних даних засвідчили, що додавання 10 мг езетимібу до стартової дози розувастатину сприяло суттєвішому зниженню рівня ХС ЛПНЩ порівняно з титруванням доз розувастатину в пацієнтів обох когорт (-21% проти -5,7% відповідно). Учасники обох когорт досягли значнішого зменшення рівня ТГ у групах комбінованої терапії (розувастатин+езетиміб), ніж у групах титрування доз розувастатину (-6,3 проти -3,2% відповідно). Рівні загального ХС, ХС не-ЛПВЩ та аполіпопротеїну В суттєвіше знизилися в учасників груп комбінованої терапії (розувастатин + езетиміб) порівняно з тими, хто отримував подвоєні дози розувастатину (табл. 1).
|
Таблиця 1. Зміни показників вмісту ліпідів та високочутливого С-реактивного білка на 6-му тижні від початку лікування учасників дослідження ACTE |
||||||
|
Показники |
Зміни від початку лікування*,% |
|||||
|
|
Когорта I |
Когорта II |
Об’єднаний аналіз |
|||
|
|
Розувастатин 5 мг + езетиміб 10 мг (n=98) |
Розувастатин 10 мг (n=96) |
Розувастатин 10 мг + езетиміб 10 мг (n=121) |
Розувастатин 20 мг (n=121) |
Усі пацієнти (розувастатин 5, 10 мг) + езетиміб 10 мг (n=219) |
Усі пацієнти (розувастатин 10, 20 мг) (n=217) |
|
ХС ЛПНЩ |
-17,9 |
-5,6 |
-23,7 |
-6,3 |
-21,0 |
-5,7 |
|
Загальний ХС |
-10,7 |
-3,9 |
-14,3 |
-4,1 |
-12,6 |
-3,9 |
|
ХС не-ЛПВЩ |
-13,6 |
-5,2 |
-20,5 |
-5,7 |
-17,1 |
-5,2 |
|
Тригліцериди |
-1,6 |
-3,6 |
-9,8 |
-2,9 |
-6,3 |
-3,2 |
|
Аполіпопротеїн В |
-11,8 |
-5,2 |
-15,7 |
-4,0 |
-13,8 |
-4,4 |
|
ХС ЛПВЩ |
-2,7 |
1,8 |
1,6 |
1,9 |
-0,5 |
1,7 |
|
Аполіпопротеїн AI |
2,5 |
0,3 |
0,0 |
1,0 |
-1,2 |
0,6 |
|
ЛПНЩ / ЛПВЩ |
-13,8 |
-5,8 |
-24,1 |
-6,3 |
-19,4 |
-6,2 |
|
Загальний ХС / ХС ЛПВЩ |
-5,5 |
-4,1 |
-14,9 |
-4,3 |
-10,7 |
-4,2 |
|
ХС не-ЛПВЩ / ХС ЛПВЩ |
-7,1 |
-5,1 |
-20,8 |
-5,1 |
-14,6 |
-5,1 |
|
Аполіпопротеїн В / аполіпопротеїн AI |
-8,3 |
-4,8 |
-14,6 |
-3,7 |
-11,8 |
-4,2 |
|
Високочутливий С-реактивний білок |
-13,1 |
-13,4 |
-13,2 |
-14,1 |
-14,1 |
-13,0 |
|
Примітка. * Середні значення, визначені за методом найменших квадратів. |
||||||
Адаптовано за H. E. Bays et al. Safety and efficacy of ezetimibe added on to rosuvastatin 5 or 10 mg versus up-titration of rosuvastatin in patients with hypercholesterolemia (the ACTE Study). Am J Cardiol. 2011 Aug 15. Vol. 108, № 4. Р. 523‑30
Терапевтичний ефект езетимібу при його додаванні до стабільної дози (5 або 10 мг) розувастатину порівняно зі збільшенням дози розувастатину зберігався незалежно від віку, статі, раси, ризиків пацієнтів, вихідних рівнів ХС ЛПНЩ і ТГ, наявності в них метаболічного синдрому / ЦД. За результатами дослідження АСТЕ, зниження показників вмісту ХС ЛПНЩ та досягнення цільового рівня цих показників було суттєвішим за комбінованої терапії розувастатином та езетимібом (додаванні 10 мг езетимібу до стартової дози розувастатину), ніж при збільшенні дози розувастатину вдвічі. Додавання езетимібу до розувастатину допомогло знизити рівень ХС ЛПНЩ на 21%, тоді як подвоєння стартової дози розувастатину – лише на 6%. Зниження рівня ХС ЛПНЩ спостерігалося незалежно від віку пацієнтів, статі, расової належності, ризиків, вихідних показників ХС ЛПНЩ і ТГ, наявності метаболічного синдрому / ЦД. Профілі безпеки та переносимості в АСТЕ були зіставними для всіх варіантів лікування та відповідали описаним раніше для аналогічних за тривалістю курсів езетимібу та розувастатину. Серйозних побічних ефектів, пов’язаних із прийманням препаратів, не виявлено, а частота реакцій із боку печінки, м’язів, шлунково-кишкового тракту та шкіри була низькою та не відрізнялася від такої в інших дослідженнях комбінації езетимібу зі статинами (Bays et al., 2011).
Доведено, що комбінація езетимібу зі статинами значно знижує рівень ХС ЛПНЩ у пацієнтів із гострим коронарним синдромом (Murphy et al., 2016). Комбінування езетимібу та статинів допомагає значно зменшити розмір коронарної бляшки порівняно з монотерапією статинами (Ueda et al., 2017).
Результати метааналізу даних 20 досліджень ефективності езетимібу щодо зниження рівня ХС ЛПНЩ у пацієнтів з атеросклеротичними ССЗ засвідчили, що комбінована терапія езетимібом зі статинами сприяла істотнішому зниженню рівня ХС ЛПНЩ порівняно з монотерапією статинами (середня різниця -0,364 ммоль/л; 95% довірчий інтервал [ДІ] від -0,465 до -0,259; p=0,0001) після 6‑12 міс. лікування (або на момент часу, найближчий до 6‑12 міс.).
За даними аналізу підгруп, комбіноване втручання порівняно з контрольною групою було ефективнішим щодо зменшення розміру фіброзно-жирових бляшок (зважена середня різниця [ЗСР]=-1,01; 95% ДІ від -3,6 до 1,6; p=0,003), об’єму некротичного ядра (ЗСР=-5,41; 95% ДІ від -13,3 до 2,5; p=0,35), а також зміни об’єму щільної кальцифікації (ЗСР=-1,14; 95% ДІ від -1,4 до -0,8; p=0,62). Отже, додавання езетимібу до терапії статинами сприяє значущому поліпшенню зниження рівня ХС ЛПНЩ порівняно з монотерапією статинами (Omidi et al., 2023).
Метою багатоцентрового рандомізованого відкритого дослідження з паралельними групами ROSETTA-Stroke (ROSuvastatin plus Ezetimibe Treatment for Target LDL‑C Achievement), проведеного в 13 центрах Південної Кореї за участю 530 пацієнтів, було порівняння ефективності комбінації розувастатину (10 мг) / езетимібу (10 мг) і розувастатину (20 мг) для досягнення цільового показника рівня ХС ЛПНЩ у пацієнтів із нещодавнім ішемічним інсультом атеросклеротичного походження (або супутніми атеросклеротичними СС захворюваннями) (Hong et al., 2023). Основні результати дослідження представлено в таблиці 2.
|
Таблиця 2. Основні результати дослідження ROSETTA-Stroke |
||||
|
Основні результати |
Розувастатин (10 мг) / езетиміб (10 мг) (n=273) |
Розувастатин (20 мг) (n=257) |
Відношення шансів |
Значення p |
|
Первинний |
||||
|
Зниження ХС ЛПНЩ ≥50% |
198 (72,5%) |
148 (57,6%) |
1,944 (1,352‑2,795) |
0,0003 |
|
Вторинні |
||||
|
ХС ЛПНЩ <1,81 ммоль/л |
219 (80,2%) |
168 (65,4%) |
2,148 (1,450‑3,184) |
0,0001 |
|
Зниження ХС ЛПНЩ ≥50% або ХС ЛПНЩ <1,81 мг/дл |
230 (84,2%) |
188 (73,2%) |
1,963 (1,281‑3,008) |
0,0018 |
|
Абсолютне зниження ХС ЛПНЩ (ммоль/л) |
1,88±0,957 |
1,673±0,908 |
|
0,0111 |
|
Відносне зниження ХС ЛПНЩ (%) |
53,9±21,1 |
47,9±20,5 |
|
0,0010 |
|
Основні судинні події |
1 (0,4%) |
9 (3,5%) |
0,101 (0,013‑0,805) |
0,0091 |
Адаптовано за K. S. Hong et al. Moderate-intensity rosuvastatin plus ezetimibe versus high-intensity rosuvastatin for target low-density lipoprotein cholesterol goal achievement in patients with recent ischemic stroke: a randomized controlled trial. J Stroke. 2023 May. Vol. 25, № 2. Р. 242‑250.
За даними оцінювання безпеки, не виявлено суттєвих відмінностей між групами комбінованої терапії розувастатином (10 мг) / езетимібом (10 мг) і монотерапії розувастатином (20 мг) за частотою будь-яких побічних ефектів (36,9 проти 36,9%; p=0,9969) та серйозних побічних ефектів (7,5 проти 7,7%; p=0,9244) (Hong et al., 2023). Результати дослідження ROSETTA-Stroke підтвердили, що комбінована терапія розувастатином та езетимібом є ефективнішою, ніж монотерапія розувастатином для інтенсивного зниження рівня ХС ЛПНЩ у пацієнтів, які нещодавно перенесли ішемічний інсульт і розпочали гіполіпідемічну терапію. На кожні 100 пацієнтів, які отримували розувастатин (10 мг) плюс езетиміб (10 мг) раз на добу, майже 73 досягли зниження рівня холестерину ЛПНЩ на ≥50%, а близько 80 мали рівень ХС ЛПНЩ <1,81 ммоль/л через 90 днів (Hong et al., 2023).
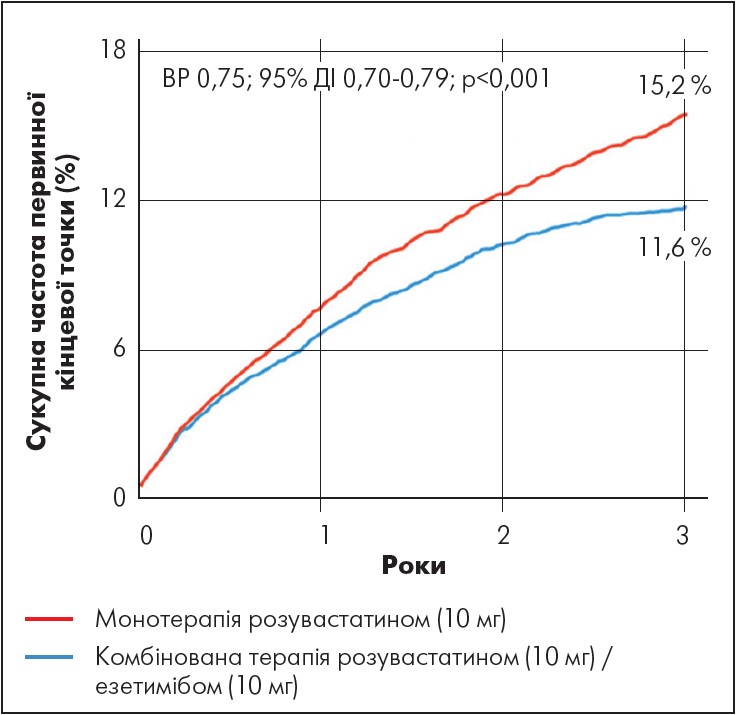
Метою рандомізованого обсерваційного дослідження RACING було порівняння ефективності та безпеки високоінтенсивної монотерапії розувастатином та комбінованої терапії (розувастатин / езетиміб) для пацієнтів з атеросклеротичними ССЗ, яким був імплантований стент із медикаметозним покриттям (n=72 050). Зокрема, 10 794 пацієнти отримували комбіновану терапію (розувастатин 10 мг плюс езетимібом 10 мг), 61 256 пацієнтів – монотерапію розувастатином (20 мг). Первинною кінцевою точкою була комбінована частота СС смерті, ІМ, реваскуляризації коронарної артерії, госпіталізації для лікування серцевої недостатності та нефатального інсульту впродовж 3-річного періоду спостереження. Комбінована гіполіпідемічна терапія була пов’язана з меншою частотою первинної кінцевої точки (11,6 проти 15,2% для групи монотерапії; відношення ризиків [ВР] 0,75; 95% ДІ 0,70‑0,79; p<0,001) (рис. 2).
Рис. 2. Сукупна частота первинної кінцевої точки (СС смерть, ІМ, реваскуляризації коронарної артерії, серцевої недостатності або нефатального інсульту) протягом 3-річного періоду спостереження в межах дослідження RACING
Адаптовано за S.-J. Lee et al. Combination lipid-lowering therapy in patients undergoing percutaneous coronary intervention. J Am Coll Cardiol. 2023 Aug. Vol. 2, № 5. Р. 401‑410.
Порівняно з монотерапією статинами високої інтенсивності, комбінована гіполіпідемічна терапія була пов’язана з меншою кількістю припинень лікування (6,5 проти 7,6%; ВР 0,85; 95% ДІ 0,78‑0,94; p<0,001) і меншою частотою нових випадків ЦД (7,7 проти 9,6%; ВР 0,80; 95% ДІ 0,72‑0,88; p<0,001). Комбінована ліпідознижувальна терапія розувастатином та езетимібом асоціювалася зі сприятливими клінічними результатами та дотриманням режиму лікування пацієнтів з імплантованим стентом із медикаментозним покриттям (Lee et al., 2023).
Терапевтичний підхід до застосування комбінованих препаратів
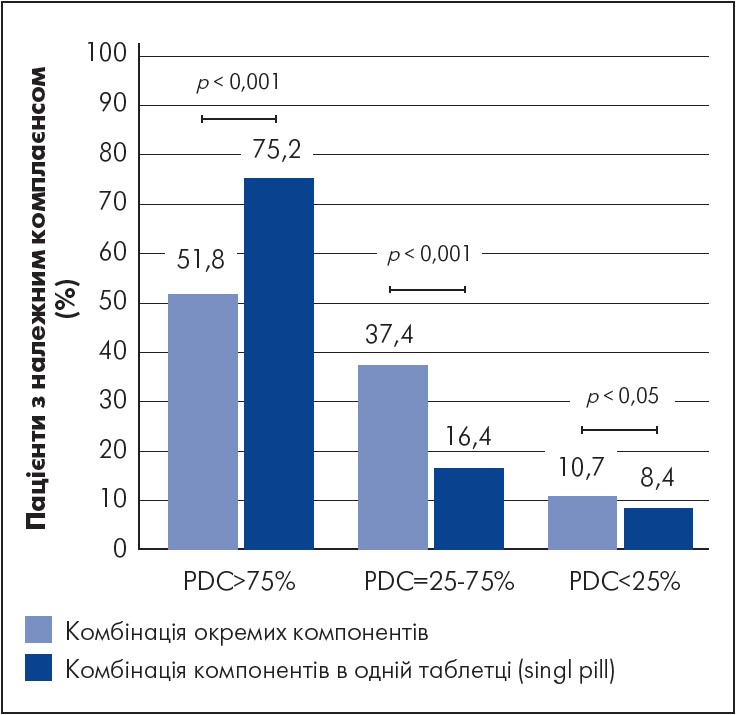
Застосування препаратів, що являють собою комбінацію діючих речовин, часто є лікуванням першої лінії для ефективного та безпечного фармакологічного контролю ризику ССЗ та церебровасулярних захворювань. Поєднуючи в одній лікарській формі дві діючі речовини з різними механізмами дії, можна досягати цільових рівнів ХС ЛПНЩ, уникаючи максимальних доз кожного з компонентів окремо. Це допомагає зменшити частоту дозозалежних побічних ефектів. Стратегія зниження рівня ХС ЛПНЩ комбінацією статинів та езетимібу сприяє поліпшенню клінічних результатів пацієнтів із високим ризиком атеросклерозу та підвищує прихильність до медикаментозної терапії. Спрощення схеми лікування завдяки зменшенню кількості препаратів підвищує прихильність до лікування. Метою дослідження, виконаного в умовах реальної клінічної практики в Італії, було вивчити зміни комплаєнсу пацієнтів, які отримували комбіновану терапію розувастатином та езетимібом як двома окремими препаратами, а згодом перейшли на приймання їх комбінації. Прихильність оцінювали як частку днів, у які пацієнти приймали медикаментозну терапію, протягом 12 міс. до і після переведення з окремих препаратів на їх комбінацію. Аналіз налічував дані 1219 пацієнтів (61,1% чоловіків, середній вік 66,2±10,4 року). Серед них 83,3% мали ССЗ; 26,4% – ЦД; 16,2% – ССЗ і ЦД. За даними дослідження, значно вища частка пацієнтів повністю дотримувалася приймання комбінованого препарату порівняно із застосуванням окремих препаратів (75,2 проти 51,8%; p<0,001) (рис. 3) (Zambon et al., 2023). Частки пацієнтів, які не повністю дотримувалися лікування, і тих, хто його не дотримувався, були нижчими за приймання комбінованого препарату, ніж за поєднання окремих препаратів (16,4 проти 37,4% [p<0,001] і 8,4 проти 10,7% [p<0,05] відповідно). Дослідники дійшли висновку, що перехід від терапії кількома таблетками до приймання лікарської форми у вигляді комбінованого препарату може мати позитивний вплив на рівень прихильності до гіполіпідемічних препаратів (Zambon et al., 2023). Тому перспективним є застосування препаратів, що містять дві діючі речовини, наприклад статин (розувастатин) та езетиміб, і виготовлені за новітньою технологією «дуопіл».
Примітка. PDC – частка днів, у які пацієнти приймали медикаментозну терапію.
Рис. 3. Показники прихильності пацієнтів до терапії комбінацією розувастатин / езетиміб в одній таблетці та у вигляді двох окремих препаратів
Адаптовано за A. Zambon et al. Adherence to free and single-pill combination of rosuvastatin/ezetimibe: findings from a real-world analysis in Italy. European Journal of Preventive Cardiology. 2023. Vol. 30, № l: i8333.4.1.
Застосування комбінованої терапії з фіксованою дозою за допомогою твердих капсул
Нині у фармації широко застосовують технології, які дають змогу створювати удосконалені форми лікарських препаратів. Такою є технологія «дуопіл»: застосування двох окремих таблеток, кожна з яких створена за своєю технологією, в одній капсулі. У тверді капсули можна вміщувати порошки, гранули, міні- / мікротаблетки або менші капсули – у більшу. Ці комбінації можуть містити кілька активних фармацевтичних інградієнтів (АФІ), щоб уникнути проблем несумісності, пов’язаних із певними препаратами. Меншу капсулу можна інкапсулювати в більшу, що дасть можливість ефективно розділити дві речовини та зберегти їх синергетичний ефект. У такий спосіб вдається вирішити не тільки питання несумісності, але й утворення домішок через взаємодію АФІ, оскільки між препаратами немає контакту. Залежно від вимог до рецептури, дві або більше активні речовини можна комбінувати у формі пелет, мікротаблеток або порошків. Ця комбінація надає пацієнтам можливість приймати препарат раз на добу, що сприяє поліпшенню прихильності до лікування. Ще одна перевага полягає в тому, що можна досягти комбінації різних параметрів профілю вивільнення (один препарат може бути у формі з негайним вивільненням, а інший – із модифікованим або кожен у складі комбінації може бути розроблений для вивільнення в різних ділянках шлунково-кишкового тракту). Це може бути досягнуто завдяки використанню декількох таблеток із різними покриттями для забезпечення кількох профілів вивільнення препарату. Використання міні- або мікротаблеток забезпечує вищу точність щодо варіації маси діючої речовини, а також можливостей досягнення різних профілів її вивільнення (Diez et al., 2019; Bhat and Solanki, 2021). У межах дослідження J. L. Katzmann et al. (2022) за участю 311 242 пацієнтів із дуже високим СС ризиком застосування комбінованих препаратів (статин+езетиміб) сприяло зниженню рівня ХС ЛПНЩ на 28,4% (1,03±1,01 ммоль/л), тоді як за приймання статинів та езетимібу у формах окремих таблеток ці показники становили лише 19,4% (0,71±0,87 ммоль/л); p <0,0001.
Настанови щодо комбінованої терапії розувастатином / езетимібом
Лікування пацієнтів із дисліпідемією є актуальною проблемою для лікарів різних спеціальностей. Провідні світові експерти профільних установ шукають шляхи її розв’язання та розробляють відповідні клінічні настанови і рекомендації. Дослідники зауважують на необхідності створення універсальної настанови щодо лікування дисліпідемії, керівні принципи якої полегшать цей процес. За наявними натепер настановами, статини, зокрема розувастатин, є засобом медикаментозної терапії першої лінії для первинної профілактики ССЗ. Щодо комбінованої терапії розувастатином / езетимібом, то вона рекомендована як помірно інтенсивна (розувастатин 5‑10 мг / езетиміб 10 мг; розувастатин 20 мг / езетиміб 10 мг) та високоінтенсивна терапія (розувастатин 10 мг / езетиміб 10 мг; розувастатин 20‑40 мг / езетиміб 10 мг) у настанові Польської асоціації з вивчення ліпідів / Колегії сімейних лікарів Польщі / Польського товариства сімейної медицини (PoLA/CFPiP/PCS, 2016) (Banach et al., 2016). Відповідно до настанов ACC/AHA (2018), для вторинної профілактики рекомендовано максимально переносиму терапію статинами. Також слід розглянути додаткове застосування езетимібу, якщо рівень ХС ЛПНЩ не знижується до цільового рівня – 1,81 ммоль/л. Пацієнти з тяжкою первинною гіперхолестеринемією, у яких рівень ХС ЛПНЩ >4,91 ммоль/л, потребують максимально переносимої терапії статинами. Якщо рівень ХС ЛПНЩ не знижується щонайменше на 50% і лишається >2,59 ммоль/л, рекомендовано додатково призначити езетиміб (Grundy et al., 2018). У настанові ESC/EAS (2019) зазначено, що інтенсифікація терапії статинами завдяки додаванню езетимібу може допомогти досягненню цільових рівнів ХС ЛПНЩ у 67% пацієнтів (Mach et al., 2020).
Висновки
Отже, на відміну від поєднання двох діючих речовин в одній таблетці, форма застосування комбінованої терапії з фіксованою дозою за допомогою твердих капсул допомагає відокремити діючі речовини та запобігти їх взаємодії. До того ж кожна з таблеток містить оптимально підібрані додаткові речовини. Застосування цієї форми дає змогу зберегти фармакокінетику та біодоступність, притаманні кожній із діючих речовин.
Приймання комбінованої терапії розувастатином (10 мг) / езетимібом (10 мг) допомагає досягти ефективного зниження рівня ХС ЛПНЩ у пацієнтів із дисліпідемією. Відносно низькі дози двох компонентів зумовлюють сприятливий профіль безпеки при застосуванні такої комбінації. Стратегія поєднання двох діючих речовин (розувастатину та езетимібу) в одній капсулі забезпечує належне дотримання схеми лікування.
Сьогодні на фармринку України доступний комбінований препарат Розуліп® Плюс, кожна капсула якого містить 10 або 20 мг розувастатину і 10 мг езетимібу. Це робить можливим індивідуально підбирати відповідну дозу та ефективно контролювати рівень ХС ЛПНЩ у пацієнтів із різним ризиком ССЗ та цереброваскулярними захворюваннями.
Підготувала Наталія Купко
Тематичний номер «Інсульт» №1 2023 р.