23 серпня, 2024
Інфекції сечовивідних шляхів: сучасні підходи до профілактики та лікування
 Інфекції сечовивідних шляхів (ІСШ) являють собою надзвичайно актуальну проблему для практичної медицини, оскільки дана нозологія характеризується значною поширеністю. З нею стикаються у своїй клінічній практиці лікарі різних спеціальностей, зокрема урологи, гінекологи, терапевти, сімейні лікарі та анестезіологи. ІСШ можуть виступати як самостійне захворювання або бути коморбідними станами, ускладнюючи перебіг основної патології (наприклад, при цукровому діабеті, вагініті, аднекситі, аденомі передміхурової залози тощо). Для лікування та профілактики рецидивуючих ІСШ (рІСШ) рекомендовано проведення антимікробної терапії, однак протягом останніх десятиліть спостерігається швидке зростання резистентності збудників ІСШ до антибактеріальних препаратів. Це вимагає перегляду існуючих протоколів лікування та імплементації дієвих протимікробних стратегій для профілактики ІСШ. Клінічно доведена ефективність, високий профіль безпеки, а також відсутність ризику формування мікробної резистентності при застосуванні пробіотичних штамів Lactobacillus, D-манози та екстракту журавлини стали підґрунтям для внесення їх до переліку дієвих антимікробних засобів, рекомендованих Європейською асоціацією урології (EAU) для профілактики ІСШ.
Інфекції сечовивідних шляхів (ІСШ) являють собою надзвичайно актуальну проблему для практичної медицини, оскільки дана нозологія характеризується значною поширеністю. З нею стикаються у своїй клінічній практиці лікарі різних спеціальностей, зокрема урологи, гінекологи, терапевти, сімейні лікарі та анестезіологи. ІСШ можуть виступати як самостійне захворювання або бути коморбідними станами, ускладнюючи перебіг основної патології (наприклад, при цукровому діабеті, вагініті, аднекситі, аденомі передміхурової залози тощо). Для лікування та профілактики рецидивуючих ІСШ (рІСШ) рекомендовано проведення антимікробної терапії, однак протягом останніх десятиліть спостерігається швидке зростання резистентності збудників ІСШ до антибактеріальних препаратів. Це вимагає перегляду існуючих протоколів лікування та імплементації дієвих протимікробних стратегій для профілактики ІСШ. Клінічно доведена ефективність, високий профіль безпеки, а також відсутність ризику формування мікробної резистентності при застосуванні пробіотичних штамів Lactobacillus, D-манози та екстракту журавлини стали підґрунтям для внесення їх до переліку дієвих антимікробних засобів, рекомендованих Європейською асоціацією урології (EAU) для профілактики ІСШ.
Ключові слова: інфекції сечовивідних шляхів, урогенітальна мікробіота, уропатогенна E. coli, антибіотикорезистентність, пробіотики, Lactobacillus, D-маноза, екстракт журавлини, Мальвосан.
Провідна роль внутрішньоклітинної персистенції E. coli в патогенезі рІСШ
ІСШ уражають понад 150 млн людей на рік у всьому світі й залишаються найпоширенішим урологічним захворюванням у країнах Європи та США [1]. Неускладнені ІСШ частіше зустрічаються у жінок. Повідомляється, що майже 50% жінок мали в анамнезі хоча б один епізод ІСШ, натомість близько 20-30% страждають на рІСШ протягом життя [2-4].
Розвиток ІСШ у жінок ініціюється контамінацією вагінальної та періуретральної зон уропатогенними мікроорганізмами. Підтвердженням цього слугують результати мікробіологічного дослідження вагінальних виділень 140 жінок, які виявили значно вищий рівень колонізації Escherichia coli у піхві жінок із рІСШ порівняно із жінками без ІСШ (35% проти 11%; p<0,01) [5]. Було доведено, що вагінальні ізоляти E. coli жінок із рІСШ мають ті самі фактори вірулентності, що й уропатогенна E. coli (UPEC), виділена із сечовивідних шляхів (наприклад, наявність поверхнево-адгезивних органел – P-пілі) [6]. Після колонізації бактерії здатні швидко розмножуватися в уротеліальних клітинах, утворюючи спільноти, які здатні уникати захисних механізмів господаря, формуючи тим самим внутрішньоклітинні резервуари (рисунок) [7]. Ці бактерії можуть перебувати в стані спокою в уротеліальних клітинах сечового міхура протягом багатьох місяців, не будучи виявленими, до дії тригерного фактора (наприклад, переохолодження, стрес та ін.) [7-10].
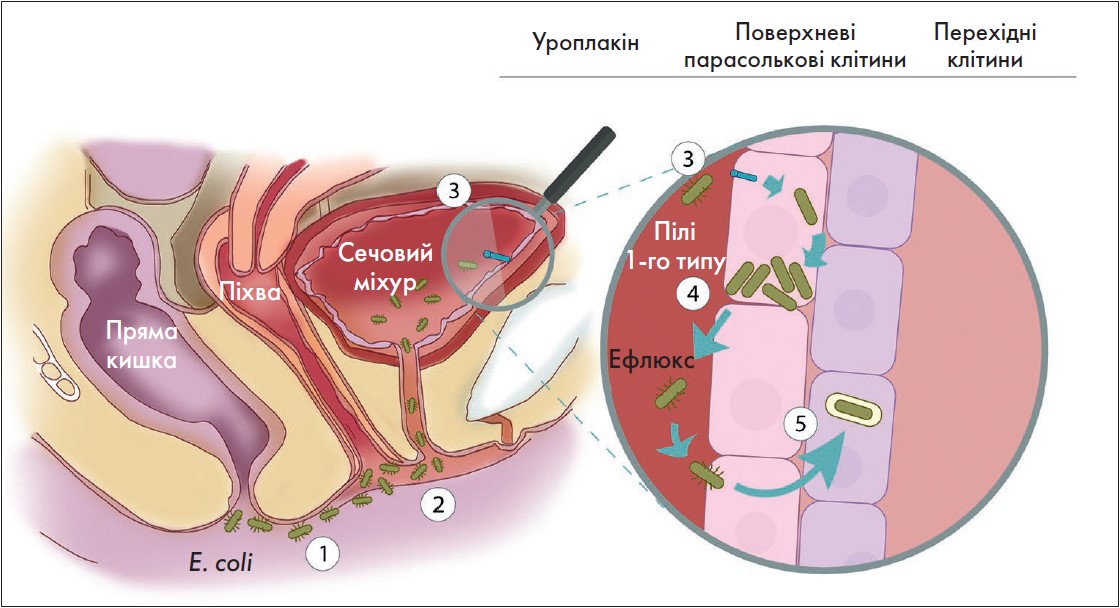
Рис. Патогенез ІСШ (адаптовано Sihra N. et al., 2018)
Антибіотикорезистентність як нагальна проблема при виборі лікування ІСШ
ІСШ є одним із найчастіших показань до призначення антибіотиків у всьому світі [11, 12]. Однак жінки із рІСШ часто потребують кількох схем лікування антибіотиками протягом короткого періоду часу, і лікарі нерідко застосовують протимікробні засоби як профілактику виникнення рІСШ, що суттєво підвищує ризик антибіотикорезистентності [13-16].
Окрім розвитку мультирезистентних штамів, використання антибіотиків при ІСШ має й інші недоліки. Так, встановлено, що у 25-35% випадків рІСШ виникали протягом 6 міс після першого курсу протимікробної терапії [17, 18] і в 44% випадків – протягом 12 міс [19, 20]. Наведені дані свідчать, що більшість наявних інструментів боротьби з мультирезистентними грамнегативними бактеріями втрачають ефективність. Тому антимікробні засоби є перспективною стратегією профілактики ІСШ, яка здатна підвищувати захисні властивості слизових оболонок урогенітального тракту та стійкість до збудників інфекцій, знижуючи при цьому ризик антибіотикорезистентності.
Відповідно до оновленої клінічної настанови EAU (2024) щодо профілактики й лікування ІСШ, яка була представлена на щорічному конгресі у Парижі, пробіотики (Lactobacillus rhamnosus GR-1 та Lactobacillus reuteri RC-14), D-маноза та екстракт журавлини (Vaccinium macrocarpon) рекомендовані до призначення для запобігання розвитку ІСШ [21].
Роль Lactobacillus reuteri й Lactobacillus rhamnosuss у підтриманні балансу урогенітальної мікробіоти та зниженні ризику ІСШ
У сучасній клінічній практиці спостерігається тенденція до розширення сфер застосування пробіотичних засобів. Зростаюча кількість досліджень зосереджується на вивченні їх позитивного впливу на нормалізацію стану мікробіомів різних локусів організму, а також на формування та перебіг різноманітних патологічних станів. Особливу увагу науковців привертає потенціал пробіотиків у контексті урологічних захворювань, зокрема їх роль у профілактиці та лікуванні ІСШ.
Результати низки клінічних досліджень демонструють перспективність застосування конкретних штамів Lactobacillus, зокрема що найвищу ефективність демонструють саме штами Lactobacillus rhamnosus GR‑1, Lactobacillus reuteri B‑54 та Lactobacillus reuteri RC‑14 [22-24]. Згідно з даними метааналізу Grin et al. (2013), у пацієнток, які отримували Lactobacillus, зареєстровано статистично значуще зниження частоти рІСШ [25]. Ghane et al. (2020) зазначали, що пробіотичні штами L. rhamnosus і L. reuteri є безпечними та ефективними засобами профілактики рІСШ у жінок [26].
Метааналіз Ng et al. (2018) на підставі оцінки сумарного показника відношення ризиків (ВР) у шести рандомізованих контрольованих дослідженнях за участю 620 пацієнтів підтвердив сприятливий ефект Lactobacillus щодо профілактики ІСШ (ВР 0,684, 95% ДІ 0,438-0,929, p<0,001) [27]. Позитивний клінічний вплив пробіотиків був доведений також у шести систематичних оглядах [28-33]. За висновками Falagas et al. (2006), штами L. rhamnosus GR‑1 та L. reuteri RC‑14 виявилися найефективнішими серед усіх досліджуваних лактобацил у запобіганні виникненню рІСШ [28].
У великому рандомізованому клінічному дослідженні Beerepoot et al. (2012) було проведено порівняння ефективності 12-місячного щоденного застосування триметоприму-сульфаметоксазолу (TMP-SMX) із пероральним прийомом L. rhamnosus GR-1 та L. reuteri RC-14 у 252 жінок із рІСШ. Результати показали, що обидві групи препаратів сприяли зменшенню загальної кількості епізодів ІСШ (від 7,0 до 2,9 і від 6,8 до 3,3 епізоду на рік у групах антибіотиків і пробіотиків відповідно). Однак слід зазначити, що вже протягом місяця лікування TMP-SMX резистентність E. coli до антибіотиків зросла з 20-40 до 80-95% [34].
У дослідженні T. Akgьl та T. Karakan (2018), опублікованому в Turkish Journal of Urology, розглядається роль пробіотиків у лікуванні жінок із рІСШ. Автори описують механізми дії цих пробіотиків, включаючи конкурентне витіснення патогенів, продукцію антимікробних речовин та модуляцію імунної відповіді. Дані клінічних досліджень вказують на потенціал L. rhamnosus GR-1 та L. reuteri RC-14 у зниженні частоти рецидивів ІСШ [30].
D-маноза в лікуванні ІСШ
D-маноза – моносахарид, який міститься в різних рослинах, фруктах і ягодах, зокрема в журавлині, а також виробляється в організмі людини з глюкози або утворюється в результаті розпаду ендогенних глікокон’югатів для синтезу глікопротеїнів [35]. Дослідження демонструють, що вільна D-маноза в сечі може насичувати специфічний для манози фімбріальний адгезин E. coli, відомий як FimH, і блокувати адгезію цього збудника до епітеліальних клітин сечовивідних шляхів. Це так зване конкурентне гальмування розглядається як один із потенційних механізмів запобігання розвитку ІСШ [36, 37]. Вільна D-маноза в сечі навіть у низьких концентраціях (<20 мкг/мл) може пригнічувати адгезію бактерій, опосередковану пілі 1‑го типу, до слизової оболонки сечовивідних шляхів [38]. Cusumano et al. (2011) повідомили, що пероральне введення активних антагоністів FimH зменшувало колонізацію UPEC в уретрі через 6 год порівняно з контрольною групою. Крім того, концентрація E. coli в мишей, яким був уведений антибіотик, імовірно, була вищою порівняно з тими тваринами, які отримували антагоніст FimH (манозу) [39].
У відкритому клінічному дослідженні Kranjčec et al. (2014) D-маноза не поступалася за ефективністю нітрофурантоїну у профілактиці повторних епізодів ІСШ протягом 6 міс після активного лікування антибіотиками, що свідчить про те, що D-маноза може використовуватися як дієва альтернативна для запобігання рІСШ без ризику розвитку антибіотикорезистентності [40]. Перехресне дослідження Porru et al. (2014) продемонструвало, що прийом добавок D-манози значно затримує початок рІСШ порівняно з антибіотиками [41].
Пілотне дослідження Domenici et al. (2016) підтвердило ефективність D-манози як при лікуванні гострих ІСШ (13‑денний курс), так і з профілактичною метою (6‑місячний курс) у жінок із симптомною (дизурія, часте сечовипускання, невідкладні позиви, біль унизу живота, нікт- і гематурія) або безсимптомною (діагностується як ≥103 КУО/мл сечі) ІСШ [42].
Ala-Jaakkola et al. (2021) оцінили пул клінічних досліджень щодо ролі D-манози у профілактиці й лікуванні ІСШ, доступних у базах PubMed, Scopus і Web of Science до січня 2021 року. За даними метааналізу, маноза ефективно запобігала утворенню бактеріальних біоплівок на поверхні уроепітелію, що підтверджує її потенціал у запобіганні ІСШ [43].
Захисні властивості екстрактів журавлини та гібіскусу
Сучасні дані також повідомляють, що екстракт журавлини здатний суттєво зменшувати частоту рецидивів ІСШ, сприяючи підтриманню балансу корисних мікроорганізмів у сечостатевому тракті та запобігаючи мікробній колонізації [21]. Результати нещодавніх досліджень демонструють, що фітотерапія на основі екстракту журавлини посилює захисні властивості, запобігаючи адгезії уропатогенів. Vasileiou et al. (2013) провели огляд клінічного статусу профілактичних ефектів вживання журавлини проти ІСШ. Результати аналізу показали, що журавлина може бути ефективною у профілактиці ІСШ у певних груп пацієнтів, особливо у жінок із рІСШ [44].
Wang et al. (2012) здійснили систематичний огляд та метааналіз рандомізованих контрольованих досліджень щодо ефективності продуктів, які містять журавлину, для профілактики ІСШ. Їхні результати продемонстрували, що продукти із журавлиною значно знижують ризик ІСШ у певних підгрупах, зокрема у жінок із рІСШ [45].
Канадське агентство з лікарських засобів та технологій у галузі охорони здоров’я (Canadian Agency for Drugs and Technologies in Health) у 2016 році провело огляд клінічної ефективності та настанов щодо використання продуктів журавлини або місцевої естроген-базованої терапії для профілактики ІСШ [46].
Ще одним ефективним компонентом фітотерапії для купірування та профілактики ІСШ є гібіскус (Hibiscus). Екстракт гібіскусу проявляє бактеріостатичний ефект проти більшості збудників ІСШ (Staphylococcus spp., Streptococcus spp., Enterococcus faecalis, E. coli, Enterobacter spp., Candida spp. та ін.). Завдяки антисептичним, спазмолітичним і сечогінним властивостям гібіскус пригнічує запальні процеси у сечовивідних шляхах, зменшуючи прояви дискомфорту та симптомів дизурії [47].
Chou et al. (2016) повідомили про результати першого звіту із застосуванням транскриптомічного аналізу, який ґрунтувався на даних клінічних спостережень, щодо механізму дії Hibiscus sabdariffa. За висновками авторів, екстракт гібіскусу ефективно пригнічував індуковану ліпополісахаридами активацію ядерного фактора kB у клітинах і продукцію інтерлейкіну 1b, зменшуючи таким чином запальний процес у нирках, що свідчить про потенційну користь добавок з екстрактом гібіскусу для лікування захворювань сечовивідних шляхів [47].
Рекомендації EAU 2024 [21] визначають пробіотичні штами Lactobacillus, D-манозу та екстракт журавлини як ключові складові протимікробного підходу в менеджменті неускладнених ІСШ.
Дані сучасних досліджень демонструють, що комбінація D-манози, пробіотиків і рослинних екстрактів, зокрема журавлини, має потенційні переваги у профілактиці повторних епізодів ІСШ у жінок [48-50]. Повідомлялося, що 14‑денна терапія комбінованим засобом D-манози, екстракту гібіскусу (Hibiscus sabdariffa) і пробіотика Lactobacillus здатна зменшувати ризик бактеріурії та ІСШ у пацієнток після інвазивного уродинамічного дослідження [48]. Panchev et al. (2012) повідомили, що триденний пероральний прийом комбінованого засобу з D-манозою та екстрактом журавлини пацієнтами з гострою ІСШ сприяв більш швидкому клінічному покращенню порівняно з триденним прийомом антибіотика. Так, полегшення симптомів ІСШ через 48 год спостерігалося у 97% пацієнтів із групи D-манози + екстракт журавлини, тоді як у групі антибіотика цей показник склав лише 65,3% [51].
Таким чином, з огляду на проблему прогресування антибіотикорезистентності все актуальнішими в медичній практиці стають дієтичні добавки з комплексною дією на розвиток, перебіг і профілактику ІСШ. Мальвосан (компанія Eubion Corporation, Польща) розроблений відповідно підходу останніх рекомендацій EAU щодо ведення ІСШ. Мальвосан повністю відповідає вимогам щодо ефективної профілактики неускладнених ІСШ, визначеним EAU (2024) [21].
Саше Мальвосан містить у своєму складі штами Lactobacillus (L. reuteri – 2,5Ч109 КУО та L. rhamnosus – 2,5Ч109 КУО), які зарекомендували свою високу ефективність щодо UPEC-штамів, D-манозу (600 мг), яка протидіє адгезії патогенів до слизової сечовивідних шляхів і формуванню бактеріальних біоплівок, а також екстракти ягід журавлини (Vaccinium macrocarpon 300 мг) та гібіскусу (Hibiscus sabdariffa 100 мг), які володіють протизапальними, антибактеріальними, антиадгезивними та імуностимулюючими властивостями, що підтверджують клінічні дослідження.
Отже комбіноване застосування даних речовин надає потенційні переваги у профілактиці й лікуванні ІСШ, може розглядатися як альтернатива застосуванню антимікробних засобів при рІСШ, як сучасний клінічний підхід щодо зменшення рецидивів захворювання та запобігання розвитку резистентності збудників ІСШ.
Список літератури знаходиться в редакції.
Тематичний номер «Акушерство. Гінекологія. Репродуктологія» № 3 (59) 2024 р.



 Шуляк О.В.
Шуляк О.В.