26 вересня, 2021
Канадські рекомендації щодо ведення осіб з ожирінням та пов’язаними з ним ускладненнями
Ожиріння – поширене хронічне захворювання, що має прогресуючий і рецидивуючий перебіг. Воно чинить суттєвий негативний вплив на якість життя пацієнтів, підвищує ризик довгострокових клінічних ускладнень, зокрема серцево-судинних (СС). Особи, які страждають на ожиріння, нерідко стикаються зі стигматизацією, що призводить до збільшення захворюваності та смертності незалежно від ваги та індексу маси тіла (ІМТ). Торік було розроблено канадські рекомендації на основі сучасних досягнень в епідеміології, патофізіології, діагностиці, профілактиці та лікуванні осіб з ожирінням, а також експертних суджень та досвіду хворих. При цьому акцент було зроблено на важливості поліпшення здоров’я та якості життя пацієнта, а не лише зниження ваги, а також зазначено важливість зниження ризиків, асоційованих з ожирінням. Пропонуємо до вашої уваги ключові положення даних рекомендацій.
За останні три десятиліття поширеність ожиріння неухильно зростала у всьому світі. Дане захворювання стало серйозною проблемою охорони здоров’я у багатьох країнах, при цьому воно пов’язане з чималими витратами, а також негативно впливає на фізичне та психічне здоров’я.
У межах епідеміологічних досліджень ожиріння визначають шляхом обчислення індексу маси тіла (вага/зріст у квадраті), за допомогою якого можна стратифікувати пов’язані з ним ризики для здоров’я на популяційному рівні. Наявність ожиріння встановлюють як ІМТ >30 кг/м2 та класифікують як ступені 1 (30‑34,9), 2 (35‑39,9) і 3 (≥40). Ожиріння спричинене складною взаємодією численних генетичних, метаболічних, поведінкових та факторів навколишнього середовища, причому останні вважаються безпосередньою причиною значного зростання поширеності цього захворювання.
Мозок відіграє центральну роль в енергетичному гомеостазі за рахунок регулювання споживання їжі та витрати енергії. В умовах енергетичного дисбалансу, коли споживання їжі перевищує витрати енергії, її надлишок перетворюється на жир і зберігається у жировій тканині. Терапія, спрямована на зміни цих нейрогормональних механізмів, здатна стати ефективним інструментом у довгостроковій перспективі.
Потенційні соматичні ускладнення, пов’язані з ожирінням:
- ЦД 2-го типу;
- захворювання жовчного міхура;
- неалкогольна жирова хвороба печінки;
- подагра.
Надлишкові, ектопічні жирові відкладення є джерелами адипоцитокінів та медіаторів запалення, які здатні впливати на метаболізм глюкози й жирів. Це призводить до зростання кардіометаболічного та онкологічного ризиків, а отже, зменшення тривалості життя на 6‑14 років.
Терапевтичні кроки у межах надання медичної допомоги особам з ожирінням
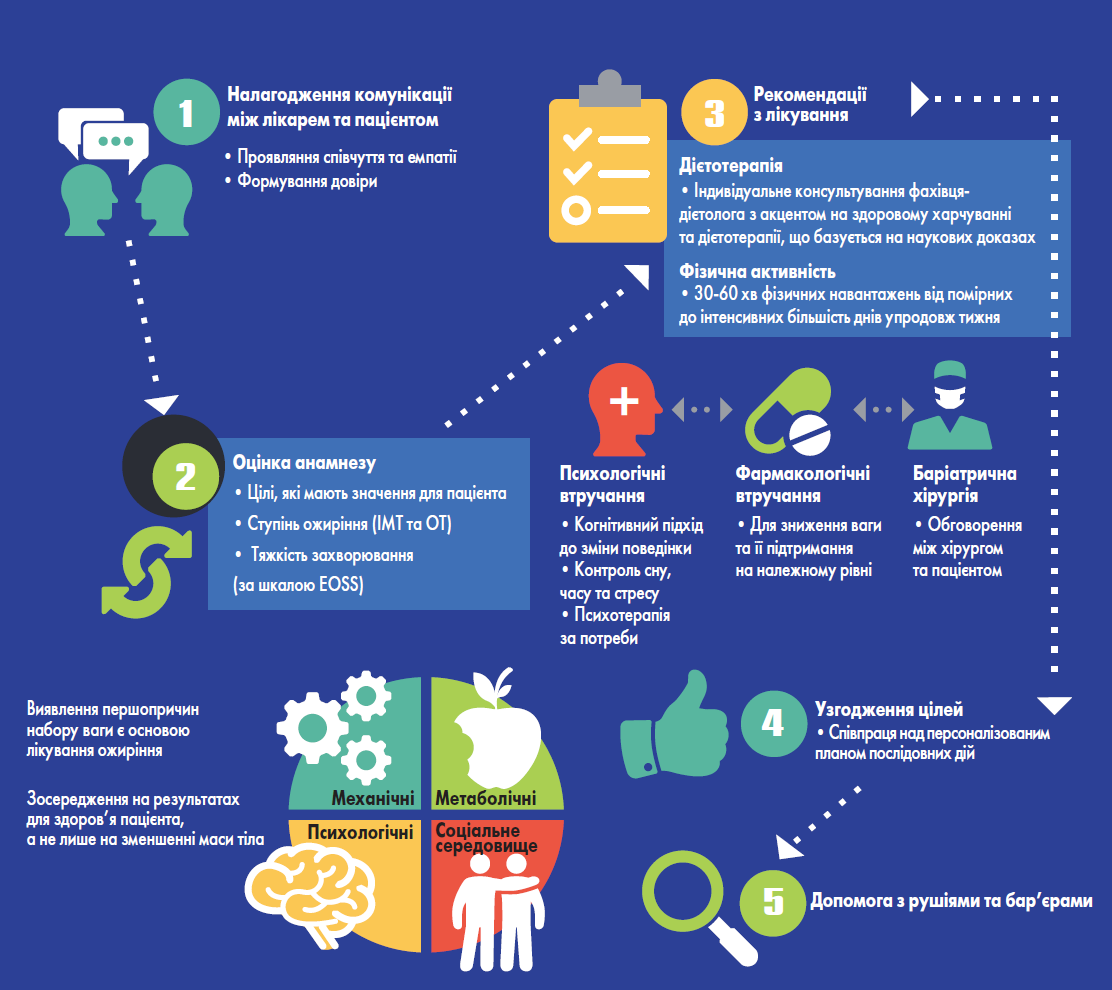
На рисунку 1 наведені ключові положення ведення пацієнтів з ожирінням.
Рис. 1. Ключові положення ведення пацієнтів з ожирінням
Крок 1: визнання ожиріння хронічним захворюванням та налагодження комунікації з пацієнтом
Фахівці у галузі охорони здоров’я мають розглядати ожиріння як хронічну хворобу, спричинену аномальним чи надмірним накопиченням жиру в організмі, що погіршує здоров’я, корелює з підвищеним ризиком передчасної захворюваності та смертності. Необхідно підвищувати обізнаність працівників медичних закладів про ожиріння, фактори ризику та пов’язані з ним проблеми для зменшення стигматизації, дискримінації та, відповідно, поліпшення догляду за хворими.
Не слід вважати, що всі пацієнти прагнуть лікуватися із приводу ожиріння. Спершу варто поговорити із хворим про його ставлення до ожиріння і на основі отриманої інформації вживати відповідних заходів, зокрема терапевтичних.
Крок 2: обстеження
Клініцисти мають пропагувати комплексний (холістичний) підхід до здоров’я з акцентом на нормалізації способу життя та встановленні основних причин підвищення ваги. Необхідно обстежити хворого на ожиріння за допомогою відповідних скринінгових та діагностичних методів для виявлення основних причин, ускладнень та бар’єрів на шляху терапії.
У клінічній практиці було запропоновано нові підходи до діагностики ожиріння. ІМТ не є точним показником для виявлення ускладнень, пов’язаних з ожирінням, хоча широко використовується для його оцінки та класифікації. Окружність талії (ОТ) незалежно асоційована зі зростанням серцево-судинного (СС) ризику, але все ж не є надійним предиктором вісцеральної жирової тканини на індивідуальній основі. Тож сукупне визначення ІМТ та ОТ у межах клінічної оцінки допомагає краще встановити фенотип ожиріння підвищеного ризику, особливо в осіб із нижчим ІМТ. У разі ІМТ поза межами норми (25‑34,9 мг/м2) слід регулярно вимірювати ОТ для виявлення суб’єктів із підвищеною імовірністю вісцерального ожиріння та ризиків для здоров’я загалом.
Основні причини розвитку ожиріння включають біологічні фактори, такі як генетика, епігенетика, нейрогормональні механізми, супутні хронічні захворювання, застосування ліків, що спричиняють ожиріння, соціальне середовище, індивідуальний життєвий досвід та психологічні фактори (тривожність, компульсивне переїдання, синдром дефіциту уваги й гіперактивності тощо). Спілкування, психотерапевтична робота з пацієнтами важливі для розуміння та виявлення/усунення ключових причин ожиріння, а також розробки персоналізованої терапії з довгостроковою перспективою взаємодії лікаря та хворого.
На додаток, детальний анамнез для виявлення основних причин ожиріння, відповідне фізичне обстеження та лабораторні дослідження необхідні для визначення когорти пацієнтів, яка отримає найбільшу користь від лікування. Едмонтську систему класифікації ожиріння (EOSS), яка враховує метаболічні, фізичні та психологічні параметри хворих, було розроблено для полегшення вибору оптимального лікування. У популяційних дослідженнях показано, що EOSS є кращим предиктором смертності від будь-яких причин порівняно з обчисленням лише ІМТ або ОТ.
Окрім того, рекомендовано вимірювати артеріальний тиск (АТ) на обох руках, рівень глюкози натще або глікованого гемоглобіну (HbA1С) та виконувати ліпідограму для визначення кардіометаболічного ризику. За потреби слід також визначити вміст аланінамінотрансферази для скринінгу на наявність неалкогольної жирової хвороби печінки.
Крок 3: обговорення варіантів лікування
Для дорослих осіб, які страждають на ожиріння, потрібно застосовувати індивідуальний план лікування з урахуванням основних причин ожиріння та запровадженням змін у поведінці (наприклад, харчуванні, фізичній активності). Аеробні вправи (30‑60 хв) упродовж тижня можуть сприяти незначному зменшенню маси тіла, поліпшенню кардіометаболічних параметрів та підтриманню належної ваги після схуднення. Довгострокове дотримання режиму належного харчування з огляду на індивідуальні вподобання, потреби та цілі лікування є важливим елементом контролю здоров’я та ваги.
Лікувальне харчування є основою терапії всіх хронічних захворювань, включно з ожирінням. Дієтотерапію слід застосовувати у поєднанні з іншими втручаннями (психологічними, фармакологічними, хірургічними) відповідно до стану здоров’я чи маси тіла окремого пацієнта. Зниження ваги за рахунок модифікації способу життя, що лежить в основі всіх терапевтичних стратегій, може сприяти значному зменшенню супутніх патологій, асоційованих з ожирінням. Психологічні та поведінкові методики допомагають клініцисту переконати пацієнта ініціювати зміни способу життя, яких можна дотримуватися із плином часу. Якщо цього недостатньо для належної втрати маси тіла та поліпшення самопочуття пацієнтів, доцільно розглянути інтенсивніші стратегії, як-то фармакологічні та хірургічні втручання.
Крок 4: узгодження цілей терапії
Оскільки ожиріння є хронічним захворюванням, лікування у довгостроковій перспективі передбачає тісну співпрацю пацієнта та клініциста. Необхідно узгодити із хворим реалістичні очікування, оптимальну терапію та стійкі цілі щодо зміни поведінки й результатів для здоров’я загалом. Через хронічний перебіг хвороби лікування має бути довготривалим та включати індивідуальний план дій для кожного окремого пацієнта.
Крок 5: налагодження взаємодії між лікарем та пацієнтом
Слід вдосконалити навчання та інформування медичних працівників для підвищення їхньої освіченості з метою надання ефективної допомоги особам з ожирінням. Також необхідно виділяти більше ресурсів охорони здоров’я для покращення доступу хворих до дієвих поведінкових, фармакологічних та хірургічних варіантів терапії.
Рекомендації
Зменшення упередженості щодо ваги при лікуванні осіб з ожирінням
Медичні працівники мають оцінити власне ставлення до ожиріння, зокрема те, як це може вплинути на надання медичної допомоги (1а, А). Також потрібно враховувати, що внутрішня упередженість щодо ваги в осіб з ожирінням може впливати на їхню поведінку, здоров’я та результати терапії (2а, В). Слід уникати використання осудливих слів (1a, A), зображень (2b, B) та заходів (2a, B) під час роботи із хворими.
Епідеміологія ожиріння у дорослих
Клініцисти повинні розглядати ожиріння як хронічне захворювання, спричинене аномальним або надмірним накопиченням жиру в організмі, що погіршує здоров’я, з урахуванням підвищеного ризику передчасної захворюваності та смертності (2b, В). Розробка науково обґрунтованих стратегій на рівні системи охорони здоров’я та політики має бути спрямована на боротьбу з ожирінням у дорослих (2b, В). Доцільно проводити регулярний контроль осіб з ожирінням на національному та регіональному рівнях, включно зі самозвітуванням (2b, В).
Скринінг
Фахівці у галузі охорони здоров’я, які беруть участь у скринінгу, обстеженні та лікуванні осіб, що страждають на ожиріння, мають обговорити із хворими їхню готовність розпочати лікування (4, D). На початковому етапі варто виміряти зріст, вагу та ІМТ у всіх дорослих пацієнтів (2a, B), а також ОТ в осіб з ІМТ 25‑35 кг/м2 (2b, B). При обстеженні хворих доцільно ретельно вивчити анамнез для виявлення першопричин збільшення маси тіла, а також ускладнень ожиріння та потенційних перешкод для лікування (4, D).
Рекомендовано вимірювати АТ на обох руках, рівень глюкози натще або глікований гемоглобін та ліпідний профіль для визначення кардіометаболічного ризику та, за потреби, вміст аланінтрансферази для виявлення неалкогольної жирової хвороби печінки в осіб з ожирінням (3, D). На додачу, варто розглянути можливість використання EOSS для визначення ступеня ожиріння та прийняття клінічних рішень (4, D).
Важливість залучення у щоденне життя пацієнтів та роль психічного здоров’я в лікуванні ожиріння
Лікарям рекомендовано регулярно запитувати осіб з ожирінням, чи мають вони труднощі з самообслуговуванням, наприклад купанням, одяганням, контролем кишечнику та сечового міхура, доглядом за шкірою, ногами тощо (3, С). Також у пацієнтів слід оцінювати ризик падінь, оскільки це може впливати на їхню здатність та інтерес до фізичних навантажень (3, С).
Рекомендований регулярний контроль ваги, рівня глюкози та ліпідів у пацієнтів із психічними розладами та тих, хто приймає ліки, які можуть призвести до підвищення ваги (3, С). При виборі психотропних препаратів потрібно враховувати як їх ефективність, так і вплив на масу тіла (2а, В). Метформін та психотерапію, як-то когнітивно-поведінкова, слід розглядати для запобігання набору маси тіла в осіб із тяжкими психічними захворюваннями, які отримують антипсихотичні засоби із потенційним несприятливим явищем у вигляді підвищення ваги (1а, А). Лездексамфетамін та топірамат можна застосовувати додатково до психотерапії для зменшення патології харчової поведінки та маси тіла в осіб із зайвою вагою або ожирінням та розладом із приступами переїдання (1а, А).
Дієтотерапія
Рекомендації щодо харчування для дорослих мають були персоналізовані з урахуванням цінностей, уподобань пацієнта та цілей лікування для запровадження безпечного, ефективного, адекватного дієтичного підходу з можливістю його тривалого дотримання (4, D). Індивідуальну дієтотерапію повинен призначати фахівець-дієтолог для нормалізації ваги, ОТ, контролю глікемії, досягнення цільового рівня ліпідів та АТ (1а, А). Дорослі з ожирінням, що мають предіабет або цукровий діабет (ЦД) 2-го типу, мають отримувати дієтотерапію для зменшення маси тіла й ОТ, а також поліпшення глікемічного контролю та АТ (2а, В).
У дорослих з ожирінням та предіабетом можна розглянути інтенсивні поведінкові заходи, спрямовані на зниження ваги на 5‑7%, для поліпшення глікемічного контролю, нормалізації АТ та ліпідних показників крові, зменшення імовірності ЦД 2-го типу (1а, А), мікросудинних ускладнень (як-то ретинопатія, нефропатія, невропатія), а також смерті через СС-патології та з будь-яких причин (1а, В). Для дорослих з ожирінням та ЦД 2-го типу доцільно розглянути інтенсивні втручання у життя, направлені на зменшення маси тіла на 7‑15%, з метою досягнення ремісії ЦД 2-го типу, зниження частоти нефропатії, обструктивного апное сну та депресії (1а, А). На додаток, рекомендоване застосування бездієтного підходу для поліпшення якості життя хворих, психологічних результатів (загальне самопочуття, сприйняття образу тіла), зменшення СС-наслідків і когнітивних обмежень, нормалізації маси тіла та харчової поведінки, підвищення фізичної активності тощо (3, С).
Фізична активність
Аеробні вправи (30‑60 хв на день від помірних до інтенсивних упродовж тижня) можна розглядати для дорослих, які прагнуть:
- незначно скинути вагу та схуднути (2а, В);
- зменшити абдомінальну та вісцеральну жирову тканину (1a, A), навіть без втрати ваги;
- підтримувати нормальну вагу після схуднення (2а, В);
- підвищити кардіореспіраторну витривалість та рухливість (2а, В).
Для дорослих із зайвою вагою або ожирінням тренування з обтяженням можуть сприяти підтриманню нормальної ваги або помірному збільшенню м’язової маси та рухливості (2а, В). При підвищенні інтенсивності вправ є нагода збільшити кардіореспіраторну витривалість та скоротити час, необхідний для досягнення переваг, що спостерігаються при аеробних тренуваннях середньої інтенсивності (2а, В).
Оптимальна фізична активність із/без втрати ваги може вплинути на низку кардіометаболічних факторів ризику в дорослих із надмірною вагою або ожирінням, включно з гіперглікемією та чутливістю до інсуліну (2b, B), високим АТ (1a, B) і дисліпідемією (2a, B). Окрім того, регулярні фізичні навантаження можуть покращити якість життя, пов’язану зі здоров’ям, настрій (зменшити депресію, тривогу) та ставлення до образу тіла у цій популяції пацієнтів (2b, B).
Психологічні та поведінкові втручання
Існують багатокомпонентні психологічні втручання, що поєднують модифікацію поведінки (встановлення цілей, самоконтроль, розв’язання проблем), когнітивну терапію та стратегії, основані на нормалізації режиму харчування й фізичної активності. Вони повинні бути включені у плани з контролю схуднення, поліпшення здоров’я та якості життя (1a, A) для забезпечення прихильності до терапії, впевненості та внутрішньої мотивації пацієнта (1b, A).
Фахівці у галузі охорони здоров’я мають надавати довгострокову допомогу з постійним інформуванням осіб з ожирінням для підтримання впевненості у подоланні перешкод (самоефективність), внутрішньої мотивації (особисті глибокі причини для змін) та встановлення послідовних цілей. Вони повинні бути реалістичними й досяжними, допомагати самостійно контролювати поведінку та аналізувати невдачі шляхом адаптивного мислення (1а, А). Пацієнтам з ожирінням слід донести те, що успіх лікування пов’язаний із поліпшенням здоров’я, функціонування та якості життя завдяки встановленню досяжних поведінкових цілей, а не якомога більшою втратою ваги (1а, А).
Фармакотерапія
Ключові факти для медичних працівників
- У Канаді разом зі здоровим способом життя для тривалої терапії ожиріння застосовують три лікарські засоби, як-то ліраглутид, комбінований препарат налтрексон/бупропіон* та орлістат. Встановлено, що всі ці медикаменти ефективніше за плацебо зменшують масу тіла впродовж щонайменше одного року.
- Лікарські засоби, що не схвалено для фармакотерапії ожиріння, не мають для цього використовуватися.
- Індивідуальна відповідь на медикаментозне лікування ожиріння є гетерогенною і відрізняється у різних пацієнтів. Щоб обрати найвідповідніший препарат, треба розглянути його механізм дії, безпеку, потенційні побічні ефекти / толерантність до нього, протипоказання, взаємодію з іншими засобами, спосіб застосування та вартість.
Рекомендації
Фармакотерапію для втрати маси тіла можна використовувати в осіб з ІМТ ≥30 кг/м2 або ІМТ ≥27 кг/м2 та ускладненнями, пов’язаними з надлишком жиру в організмі. Медикаментозне лікування має поєднуватися з лікувальною дієтотерапією, фізичною активністю та психологічними методами (ліраглутид 3,0 мг [2а, В], комбінація налтрексону/бупропіону [2а, В], орлістат [2а, В]).
Фармакотерапію можна використовувати, аби підтримувати втрату маси тіла (що досягають завдяки здоровому способу життя) та попереджати її набір (ліраглутид 3,0 мг або орлістат) [2а, В]. Для осіб, в яких є цукровий діабет (ЦД) 2-го типу та ІМТ ≥27 кг/м2, медикаментозне лікування можна використовувати у поєднанні зі здоровим способом життя для втрати маси тіла та поліпшення глікемічного контролю (ліраглутид 3,0 мг [1а, А], комбінація налтрексону/бупропіону [2а, В], орлістат [2а, В]).
Медикаментозне лікування разом зі здоровим способом життя рекомендоване особам із предіабетом та надлишковою масою тіла чи ожирінням (ІМТ ≥27 кг/м2), щоб загальмувати розвиток або попередити ЦД 2-го типу (ліраглутид 3,0 мг [2а, В], орлістат [2а, В]).
Не слід використовувати безрецептурні препарати, якщо їх не ухвалено для контролю маси тіла (4, D, консенсус). Для осіб, які мають надлишкову масу тіла або ожиріння та потребують фармакотерапії у зв’язку з іншими патологічними станами, запропоновано обирати лікарські засоби, що не асоційовані з набором ваги (4, D, консенсус).
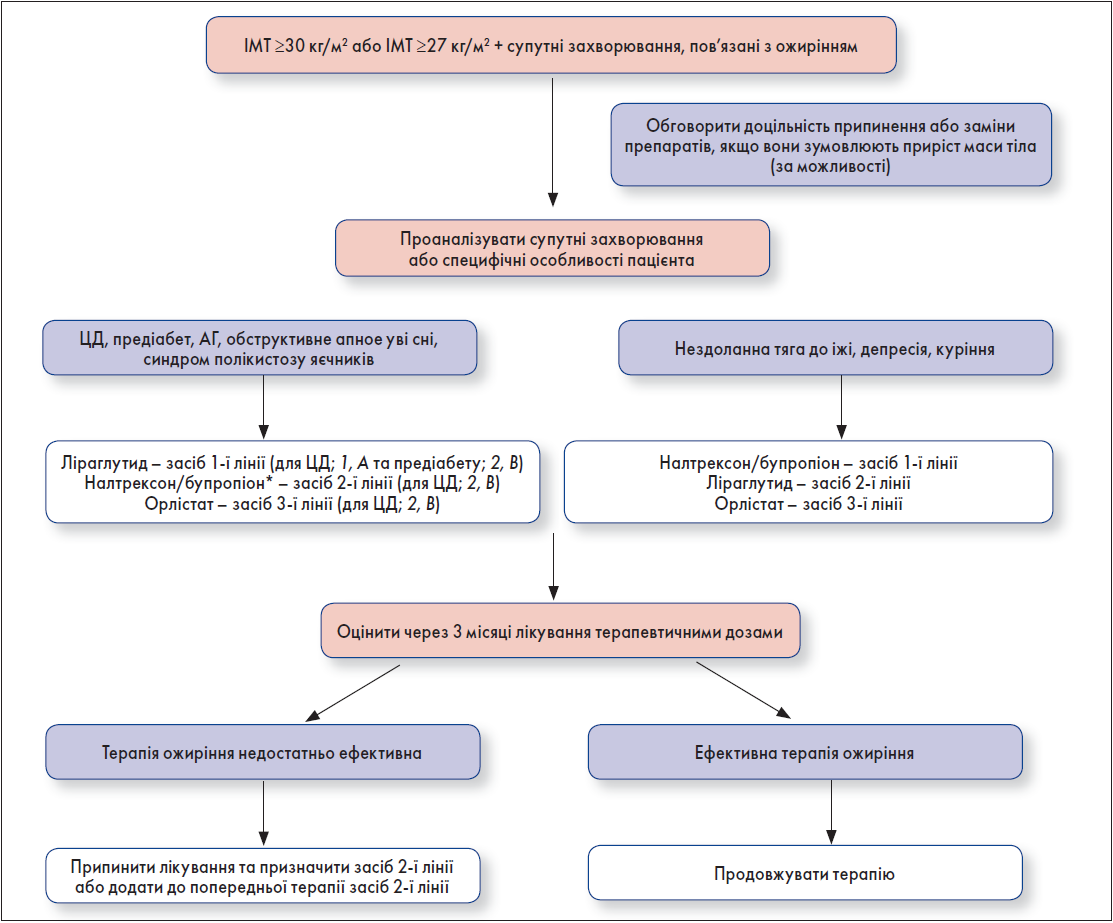
Алгоритм вибору фармакотерапії в осіб з ожирінням наведено на рисунку 2.
Рис. 2. Алгоритм вибору фармакотерапії в осіб з ожирінням
Примітка: * В Україні даний препарат відсутній.
Аналіз використання фармакотерапії при ожирінні
Існує кілька чинників, які треба розглянути для вибору належної фармакотерапії для пацієнтів із надлишковою масою тіла або ожирінням. Етіологія ожиріння є складною та гетерогенною. Необхідно розпізнавати та, за можливості, корегувати такі складові чинники, як психосоціальні, емоційні та гедоністичні. Механізм дії, побічні ефекти, безпеку й толерантність до кожного препарату треба розглядати в контексті супутніх хвороб і тих засобів, які вже приймає кожний окремий пацієнт. Із хворими слід обговорювати вартість медикаментів, шлях їх введення (пероральний або підшкірний) і кратність приймання, оскільки все це – бар’єри у прихильності до лікування. Важливо оцінити засоби, які пацієнт вже застосовує, адже вони можуть спричиняти набір ваги. У деяких випадках доцільно обговорити приймання інших медикаментів.
Якщо клінічно значущої втрати маси тіла досягти за допомогою фармакотерапії не вдалося, необхідно розглянути інші чинники, котрі можуть бути причиною неефективності лікування. До них належать неадекватні дози, низька прихильність до терапії, бар’єри на шляху до змін у способі життя, а також психосоціальні й медичні фактори. Також треба усвідомлювати, що відповідь на лікування будь-яким медикаментом характеризується значною гетерогенністю. Якщо клінічно значущої ефективності терапії (впродовж трьох місяців використання повних доз / тих, до яких пацієнт максимально толерантний) досягти не вдалося, і при цьому немає явних причин неефективності лікування, необхідно розглянути інший засіб або підхід для корекції ожиріння.
На сьогодні неможливо передбачити, який саме засіб буде найефективнішим у конкретного пацієнта. Проте наразі відбувається еволюція точної медицини, складовими якої є гормональне та генетичне профілювання. Тому в майбутньому, ймовірно, стане можливим робити такий прогноз.
Регуляторні органи рекомендують припинити медикаментозне лікування ожиріння, якщо впродовж трьох місяців приймання терапевтичної дози не вдалося втратити ≥5% маси тіла. Однак фармакотерапію також призначають, щоб підтримати втрату ваги, якої було досягнуто завдяки попереднім змінам у способі життя або перебуванню на дуже малокалорійній дієті.
Лікарські засоби проти ожиріння є частиною довготривалої терапії. Клінічні випробування цих медикаментів однозначно демонструють, що після припинення терапії маса тіла збільшується.
Не рекомендовано починати фармакотерапію ожиріння у вагітних, жінок, які годують грудьми, та тих, хто намагається завагітніти. Немає даних, що дозволяють інформувати стосовно часу, коли треба припинити медикаментозне лікування ожиріння перед зачаттям.
Градація доказовості та сила рекомендацій
Рівні доказовості
- Рівень 1а: дані метааналізу РКД
- Рівень 1b: дані принаймні 1 РКД
- Рівень 2а: дані принаймні 1 контрольованого дослідження без рандомізації
- Рівень 3: дані неекспериментальних описових досліджень, таких як порівняльні, кореляційні та дослідження випадок/контроль
- Рівень 4: дані зі звітів / висновки експертних комітетів, клінічний досвід фахівців
Сила рекомендацій
- Клас A: безпосередньо на основі даних рівня 1
- Клас B: безпосередньо на основі даних рівня 2 або екстрапольованої рекомендації на основі даних рівня 1
- Клас C: безпосередньо на основі даних рівня 3 або екстрапольованої рекомендації з доказів рівня 1 чи 2
- Клас D: безпосередньо на основі доказів рівня 4 або екстрапольованої рекомендації на основі даних рівня 1, 2 чи 3
Примітки: РКД – рандомізоване контрольоване дослідження.
Адаптовано за P.G. Shekelle et al., 1999
Механізми дії та ефективність препаратів
Орлістат. Препарат є напівсинтетичним похідним ліпстатину та потужним селективним інгібітором панкреатичної ліпази. Отже, він пригнічує перехід харчових тригліцеридів (ТГ) до вільних жирних кислот, які здатні всмоктуватися. Як наслідок, близько 30% вживаних ТГ екскретується, переважно з калом, що спричиняє дефіцит калорій. Наразі орлістат – єдиний засіб для терапії ожиріння, який не має спрямованого специфічного впливу на апетит або механізми насичення. Препарат був ухвалений для терапії ожиріння в Канаді 1999 р. (таблиця).
Міністерство охорони здоров’я Канади ухвалило орлістат як засіб для зменшення маси тіла або зниження ризику її набору після попередньої втрати у пацієнтів з ІМТ ≥30 кг/м2 або ≥27 кг/м2 за наявності супутніх захворювань (наприклад, АГ, ЦД 2-го типу, дисліпідемії, надмірної кількості вісцерального жиру). Ухвалена доза становить 120 мг тричі на добу з їжею або впродовж 1 год після неї.
Згідно з результатами систематичного огляду і метааналізу рандомізованих контрольованих випробувань ефективності орлістату (120 мг три рази на добу), середня втрата маси тіла (за вирахуванням ефекту плацебо) складала 2,9% через один рік терапії. Окрім того, 54 і 26% пацієнтів на орлістаті досягли втрати маси тіла ≥5 та ≥10% відповідно порівняно з 33 і 14% осіб у групі плацебо. Показано, що орлістат ефективно підтримує масу тіла після її втрати на дуже низькокалорійній дієті впродовж восьми тижнів. У групі орлістату набір ваги був нижчим, ніж на тлі плацебо через три роки спостереження (4,6 кг vs 7,0 кг).
Лікування орлістатом асоційоване зі значними побічними ефектами з боку шлунково-кишкового тракту, зокрема жировими плямами на спідній білизні, жирними випорожненнями, флатуленцією з виділенням калу, збільшеною дефекацією та імперативними позивами до неї. Ці несприятливі явища можуть спокунати пацієнтів, які не бажають обмежувати харчові жири, до припинення терапії. Довготривалий аналіз терапії ожиріння в Канаді показав, що впродовж 6 місяців, 1 та 2 років орлістат приймали 18, 6 і 2% осіб відповідно.
Також орлістат впливає на всмоктування жиророзчинних вітамінів (A, D, E, K). Пацієнтів треба інформувати про це й рекомендувати приймати мультивітаміни щонайменше за 2 год до або після приймання орлістату.
Орлістат протипоказаний хворим із хронічним синдромом мальабсорбції або холестазом. У деяких пацієнтів на тлі препарату підвищується рівень оксалатів у сечі. Зафіксовано випадки оксалатної нефропатії з нирковою недостатністю. Також були рідкісні повідомлення про тяжке ураження печінки або гостру печінкову недостатність.
Орлістат впливає на абсорбцію вітаміну К. Тож якщо пацієнт приймає пероральні антикоагулянти, необхідно ретельно моніторувати міжнародне нормалізоване відношення. Орлістат порушує всмоктування левотироксину та/або солі йоду. У хворих, які застосовують левотироксин, слід моніторувати функцію щитоподібної залози. На додаток, спостерігалося зниження плазмового рівня циклоспорину в разі одночасної терапії орлістатом. Отже, у таких пацієнтів необхідно частіше перевіряти вміст циклоспорину. Орлістат змінює абсорбцію антиконвульсантів. Це пояснює, чому хворим, які приймають такі препарати, слід бути під наглядом, аби встановити, чи змінюється у них частота та/або тяжкість судом.
Зафіксовано вкрай невеликий ефект орлістату на втрату маси порівняно із плацебо. Також шлунково-кишкові побічні дії обмежують його призначення при ожирінні.
Ліраглутид. Це препарат для щоденного підшкірного введення, що є аналогом глюкагоноподібного пептиду 1 (ГПП‑1) людини й діє на центральні проопіомеланокортинові (POMC)/CART нейрони. Засіб прискорює відчуття насичення, робить його тривалішим і пригнічує голод. Окрім того, ліраглутид транзиторно гальмує спорожнення шлунка.
Ліраглутид стимулює вивільнення інсуліну та пригнічує глюкагон, коли підвищується глюкоза. Препарат було ухвалено в Канаді для терапії ЦД 2-го типу в добовій дозі 1,2 або 1,8 мг. Майже максимальний терапевтичний ефект (зниження HbA1С) досягається за дози 1,8 мг. У 2015 р. ліраглутид ухвалено в Канаді для тривалого лікування ожиріння незалежно від наявності супутнього ЦД 2-го типу в добовій дозі 3,0 мг. Рекомендованою початковою дозою ліраглутиду є 0,6 мг/добу із наступним титруванням по 0,6 мг щотижнево до досягнення цільової дози 3,0 мг/добу.
Згідно з результатами досліджень, в осіб із нормоглікемією або предіабетом застосування ліраглутиду в дозі 3,0 мг впродовж одного року на тлі змін у способі життя зумовлювало втрату маси тіла на 8%. У групі плацебо (лише зміни способу життя) зниження ваги становило 2,6%. Якщо навести ці результати у вигляді категорійних даних, через один рік терапії 63,2% осіб, що приймали ліраглутид, втратили ≥5% маси тіла, тоді як у групі плацебо таких пацієнтів виявилося 27,1%. Зменшення маси тіла на ≥10% було зареєстроване в 33,1 та 10,6% осіб відповідно. Пацієнтів із предіабетом оцінювали через три роки. Стійка втрата ваги у групах ліраглутиду та плацебо складала 6,1 і 1,9% відповідно.
Якщо на низькокалорійній дієті втрата маси тіла становила 6%, призначення ліраглутиду в дозі 3,0 мг (із консультаціями щодо здорового способу життя) забезпечило додаткове зниження ваги на 6,2% наприкінці першого року лікування (порівняно з 0,2% у групі плацебо, де застосовували лише постійну консультацію зі здорової харчової поведінки). Пацієнтів, здатних підтримувати початкову втрату ≥5% маси тіла, у групі ліраглутиду було більше (81,4%), ніж серед тих, хто отримував лише плацебо (48,9%). Осіб, в яких набір ваги становив ≥5% маси тіла, на ліраглутиді виявилося менше (1,9%), ніж при застосуванні плацебо (17,5%).
Найпоширенішим побічним ефектом ліраглутиду є нудота внаслідок транзиторного гальмування шлункового спорожнення. Пацієнтів також турбують закреп, діарея, серцебиття й блювання. Повільніше титрування дози допомагає зменшити несприятливі реакції з боку шлунково-кишкового тракту. Ліраглутид порівняно із плацебо підвищує ризик розвитку жовчних конкрементів на 1,4%.
Також ліраглутид при зіставленні з плацебо незначно підвищує ймовірність панкреатиту. Більшість таких випадків асоційована з жовчнокам’яною хворобою. Ліраглутид протипоказаний пацієнтам із власним або родинним анамнезом медулярного раку щитоподібної залози або особистим анамнезом множинних ендокринних неоплазій 2-го типу. Це пояснюється тим, що на гризунах був продемонстрований підвищений ризик медулярного раку щитоподібної залози на тлі застосування даної молекули. У дослідженнях за участю людей ліраглутид не спричиняв розвитку даної патології. Ліраглутид гальмує спорожнення шлунка, що порушує всмоктування пероральних медикаментів, які приймає пацієнт.
Вплив фармакотерапії на стан здоров’я
Профілактика ЦД 2-го типу. ЦД 2-го типу є частим ускладненням ожиріння, а профілактика ЦД – важлива мета тривалої терапії ожиріння. Особа із предіабетом має високий ризик розвитку ЦД 2-го типу. Впродовж 3‑5 років він виникає приблизно в 25% пацієнтів із підвищеною глікемією натщесерце або порушеною толерантністю до глюкози. За наявності предіабету втрата 1 кг маси тіла асоційована зі зниженням відносного ризику ЦД 2-го типу на 16%.
Фармакотерапія ожиріння здатна попереджати або гальмувати розвиток ЦД 2-го типу. Вплив орлістату на профілактику ЦД вивчали у клінічному випробуванні, де взяли участь 3305 осіб з ожирінням та нормальною (79%) або порушеною (21%) толерантністю до глюкози. Пацієнтів рандомізували на дві групи. В обох учасники змінювали спосіб життя, а далі в одній із них додавали орлістат, тоді як в іншій – плацебо. Через чотири роки лікування кумулятивна частота ЦД становила 6,2% у групі орлістату та 9% – плацебо, тобто ризик прогресування до ЦД зменшувався на 37,3%. Порівняно із нормоглікемією, за порушеної толерантності до глюкози пацієнти отримували від орлістату більше користі з точки зору його здатності знижувати частоту прогресування до ЦД. Вторинний аналіз показав, що первинна причина ефективнішої профілактиці ЦД полягає у більшій втраті маси тіла.
Ліраглутид у дозі 3,0 мг виявився ефективним для попереджання та гальмування розвитку ЦД 2-го типу в осіб із предіабетом. До клінічного випробування SCALE Obesity and Prediabetes було залучено 2254 пацієнтів, які приймали ліраглутид (n=1505) або плацебо (n=749) додатково до змін у способі життя. Впродовж 3-річного лікування 3,0 мг ліраглутиду порівняно із плацебо час до розвитку ЦД 2-го типу був у 2,7 раза довшим, а ризик знижувався на 79%. Такий позитивний вплив, найімовірніше, був зумовлений поєднанням антигіперглікемічного ефекту ліраглутиду з опосередкованою ним втратою маси тіла.
ЦД 2-го типу. При ожирінні порівняно з його відсутністю за ЦД 2-го типу контроль глікемії, АТ і ліпідного профілю є гіршим, а застосування ліпідознижувальних та антигіпертензивних засобів – частішим.
Розглядати вплив протидіабетичної терапії на масу тіла слід в контексті вибору препарату, який забезпечує найліпший контроль глікемії. Агоністи рецепторів ГПП‑1 та інгібітори котранспортера натрію/глюкози, крім поліпшення глікемічного контролю, також зумовлюють втрату ваги. Метформін, інгібітори дипептидилпептидази‑4 та акарбоза на масу тіла зазвичай не впливають. Інсулін, стимулятори його вивільнення та тіазолідиндіони спричиняють набір ваги. Фармакотерапія ожиріння поліпшує контроль ЦД і може бути корисною для зменшення маси тіла.
Встановлено, що орлістат покращує глікемічний контроль за ЦД 2-го типу. До метааналізу було включено дані 2550 осіб із ЦД 2-го типу та ожирінням. Пацієнтів рандомізували на групи орлістату (120 мг тричі на добу) та плацебо. Було показано, що орлістат у середньому статистично значніше зменшував глікемію натщесерце та HbA1С, ніж плацебо (1,39 vs 0,47 ммоль/л та 0,74 vs 0,31% відповідно). На тлі застосування орлістату втрата маси тіла становила 3,8 кг порівняно із 1,4 кг у групі плацебо. Первинною причиною поліпшення глікемічного контролю на тлі використання орлістату було зниження ваги, хоча препарат також мав позитивні метаболічні ефекти, що не залежали від впливу на масу тіла. Серед пацієнтів із мінімальною втратою ваги (1% від вихідного показника) орлістат статистично більш значущо знижував глікемію натщесерце (0,83 vs 0,02% ммоль/л) та HbA1С (0,29 vs 0,14%).
У клінічному випробуванні SCALE ліраглутид у дозі 3,0 мг порівнювали з ліраглутидом по 1,8 мг та плацебо як доповнення до зміни способу життя в осіб з ожирінням та ЦД 2-го типу. Через один рік на тлі застосування 3,0 мг ліраглутиду маса тіла зменшувалася на 6% (n=423) порівняно із 4,7% на ліраглутиді в дозі 1,8 мг (n=211) та 2% – плацебо (n=212). Клінічно значущої втрати ваги на ≥5% досягли 54,3% пацієнтів на ліраглутиді в дозі 3,0 мг, 40,4% на ліраглутиді по 1,8 мг та 21,4% – плацебо. Зменшення маси тіла на ≥10% відбулося у 25,2% осіб при використанні 3,0 мг ліраглутиду, 15,9% – 1,8 мг ліраглутиду та 6,7% – плацебо (лише модифікація способу життя). Ліраглутид у дозі 3,0 мг знижував рівень HbA1С на 1,3% порівняно з 1,1 та 0,3% на ліраглутиді по 1,8 мг і плацебо відповідно. Крім того, ліраглутид у дозах 3,0 та 1,8 мг зменшував сумарне використання пероральних антигіперглікемічних засобів при зіставленні з плацебо.
Інші чинники СС-ризику. Втрата маси тіла, якої досягають завдяки фармакотерапії, може сприяти не лише контролю глікемії, але й корекції чинників СС-ризику. У метааналізі продемонстровано, що орлістат помірно поліпшував ліпідний профіль та злегка знижував АТ (таблиця).Ліраглутид порівняно із плацебо знижував систолічний АТ на 2,8 мм рт. ст., а також помірно корегував ліпідні показники. Серед осіб з ожирінням і предіабетом (період спостереження – три роки) частота серцевого ритму зростала на 2 уд./хв щорічно. Налтрексон/бупропіон помірно поліпшував параметри ліпідного профілю. Цей препарат зменшував позитивний ефект втрати маси тіла на АТ, імовірно, внаслідок того, що інгібує зворотне захоплення норадреналіну. Налтрексон/бупропіон протипоказаний пацієнтам із неконтрольованою АГ, а в осіб з контрольованою АГ має призначатися з обережністю.
Не існує регуляторних вимог, щоб оцінювати СС-безпеку засобів для фармакотерапії ожиріння у клінічних випробуваннях із реєстрацією кардіоваскулярних кінцевих точок. Однак такі дослідження можуть бути затребувані регуляторними органами, особливо за виникнення будь-якого сумніву щодо несприятливого впливу на той чи інший чинник СС-ризику.
Встановлено, що у пацієнтів із ЦД 2-го типу ліраглутид у дозах 1,2‑1,8 мг знижує частоту СС-подій і летальних випадків. Ці дані були прийняті Управлінням із контролю за якістю продуктів харчування та медикаментів США (FDA) як достатній доказ СС-безпеки ліраглутиду в дозі 3,0 мг в осіб з ожирінням без ЦД 2-го типу.
Отже, дотепер немає рандомізованих клінічних випробувань лікарських засобів для терапії ожиріння, в яких було б продемонстроване зниження частоти СС-подій або летальних випадків в осіб без ЦД.
Інші супутні хвороби, пов’язані з ожирінням. Втрата маси тіла поліпшує перебіг супутніх хвороб, асоційованих з ожирінням, зокрема стеатозу печінки, синдрому полікистозу яєчників (СПКЯ), обструктивного апное сну та остеоартриту.
У невеликому дослідженні 41 особу з ІМТ >27 кг/м2, в яких неалкогольний стеатогепатоз (НАСГ) верифікувався за допомогою біопсії, розподілили на дві групи. В обох пацієнти отримували дієту з калорійністю 1400 ккал/добу та вітамін Е (800 МО/добу). Проте в одній групі впродовж 36 тижнів призначали орлістат, а в іншій – плацебо. На тлі терапії групи не відрізнялися за позитивною динамікою печінкових ферментів та індексом активності хвороби. Також не спостерігалося значущих відмінностей за зменшенням маси тіла (на 8,3% при застосуванні орлістату та 6% – плацебо). Орлістат не збільшував втрату ваги, не поліпшував печінкових ферментів і гістопатологічних змін, не знижував інсулінорезистентності. Особи зі значнішою втратою маси тіла характеризувалися кращою динамікою індексу активності НАСГ як у групі орлістату, так і плацебо.
У невеликому випробуванні (n=52) терапія ліраглутидом у дозі 1,8 мг/добу сприяла повному зворотному розвитку НАСГ у 39% хворих порівняно із 9% у групі плацебо. Ці висновки базувалися на результатах біопсії печінки, яку виконували через 48 тижнів лікування. Отриманий позитивний результат можна пояснити комбінованою дією втрати маси тіла з безпосереднім позитивним впливом на печінку.
У невеликому дослідженні, що включало жінок із СПКЯ, терапія ліраглутидом у дозі 1,8 мг упродовж 26 тижнів сприяла «чистій» втраті маси тіла на 5,2 кг, зменшенню вмісту печінкового та вісцерального жиру та зворотному розвитку СПКЯ. У пацієток не оцінювали частоту менструацій, фертильність або прояви гірсутизму.
Немає досліджень належної якості, в яких би вивчали орлістат або налтрексон/бупропіон при СПКЯ.
Ліраглутид – єдиний засіб для фармакологічної терапії ожиріння, вплив якого на перебіг обструктивного апное сну оцінено у спеціальному дослідженні. У пацієнтів із помірним або тяжким обструктивним апное уві сні, що були не здатні чи не бажали користуватися СРАР-пристроєм, ліраглутид у дозі 3,0 мг на тлі змін способу життя значуще зменшував кількість подій апное/гіпопное (-12,2 події/год vs -6,1 події/год на тлі здорового способу життя без призначення засобу).
Вплив фармакотерапії ожиріння на перебіг остеоартриту належним чином ще не вивчено.
Психічне здоров’я та якість життя пацієнтів
При виборі фармакотерапії психічних розладів (наприклад, депресії або психозу) необхідно враховувати вплив засобу на масу тіла. Це стосується також тих препаратів, які призначають при розладах харчової поведінки або синдромі гіперактивності й дефіциту уваги.
Зв’язок між психічним здоров’ям та ожирінням є складним. Проте у більшості досліджень встановлено, що успіх терапії ожиріння асоційований із покращанням показників психічного здоров’я. У деяких, але не всіх клінічних випробуваннях показано, що втрата маси корелює з поліпшенням якості життя пацієнтів. Оскільки більшість засобів для терапії ожиріння діє на мозок, важливо дослідити їх вплив на психічне здоров’я та впевнитися у безпеці.
Було продемонстровано, що ліраглутид у дозі 3,0 мг покращує пов’язану зі здоров’ям якість життя в осіб з ожирінням і предіабетом, а також асоційовану з масою тіла якість життя у пацієнтів із ЦД 2-го типу. Також встановлено нейропсихіатричну безпеку цього засобу.
Баріатрична хірургія
У кандидатів для проведення баріатрії слід провести комплексне клінічне обстеження та оцінку харчування з коригуванням дефіциту поживних речовин (4, D). Відмова від куріння до процедури може мінімізувати пери- та післяопераційні ускладнення (2a, B). Баріатричну хірургію варто розглядати для осіб з ІМТ ≥40 кг/м2 або з ІМТ ≥35 кг/м2 та наявністю принаймні одного захворювання, пов’язаного з ожирінням (4, D; консенсусний висновок), з метою:
- зменшення загальної смертності (2b, B);
- ефективнішого довгострокового зниження ваги порівняно з лише медикаментозним лікуванням (1а, А);
- контролю та ремісії ЦД 2-го типу в поєднанні з оптимальною фармакотерапією (2а, В);
- значного поліпшення якості життя (3, С);
- тривалої ремісії більшості захворювань, пов’язаних з ожирінням, зокрема дисліпідемії, гіпертонії, стеатозу печінки та неалкогольного стеатогепатиту (3, С).
Проведення баріатрії слід розглядати у пацієнтів із погано контрольованим ЦД 2-го типу та ожирінням I ступеня (ІМТ 30‑35 кг/м2) незважаючи на оптимальну фармакотерапію. Крім того, така процедура може бути корисною для зниження ваги та/або для контролю захворювань, асоційованих з ожирінням, в осіб із ожирінням I ступеня, у котрих оптимальне медикаментозне лікування та контроль поведінки виявилися недостатньо ефективними.
Висновки
Таким чином, ожиріння – складне й гетерогенне хронічне захворювання, асоційоване з підвищеним ризиком передчасної захворюваності та смертності серед хворих. Воно має різні прояви, потребує індивідуального лікування та тривалої підтримки. Ведення пацієнтів з ожирінням має базуватися на науково-обґрунтованих принципах лікування хронічних захворювань, життєвому досвіді хворих та виходити за межі спрощених підходів «менше їсти, більше рухатися» тощо.
Для осіб з ожирінням необхідно забезпечити доступ до інформації та відповідних заходів, як-от лікувальне харчування, фізична активність, психологічні методики, фармакотерапія та хірургічне втручання, з метою поліпшення клінічних результатів та якості життя пацієнтів.
Довідка «ЗУ»
САКСЕНДА® (ліраглутид) – єдиний в Україні аналог глюкагоноподібного пептиду 1 (ГПП‑1), схвалений для застосування з метою зниження ваги як доповнення до дієти і фізичних навантажень у дорослих пацієнтів із початковим ІМТ більш як 30 кг/м2 (ожиріння) або 27‑30 кг/м2 (надмірна вага) за наявності хоча б одного супутнього захворювання, пов’язаного з масою тіла, як-от предіабет або ЦД 2-го типу, артеріальна гіпертензія, дисліпідемія або обструктивне апное сну (відповідно до інструкції для медичного застосування лікарського засобу САКСЕНДА® (ліраглутид), розчин для ін’єкцій, 6 мг/мл; р/п UA/18651/01/01, Наказ МОЗ України від 23.03.2021 № 548). Препарат рекомендований для лікування ожиріння згідно з канадськими практичними клінічними рекомендаціями 2020 р.
Підготувала Олена Коробка
Оригінальний текст документа, включно зі списком літератури, читайте на сайті www.obesitycanada.ca