4 лютого, 2021
Проблеми та можливості покращення контролю кардіометаболічних ризиків під час пандемії COVID‑19
 Пандемія коронавірусної хвороби COVID‑19 кидає виклик системам охорони здоров’я у всьому світі, потребує безпрецедентних зусиль медичної спільноти та мобілізації усіх ресурсів для щоденного порятунку життів. Тим часом тягар хронічних неінфекційних захворювань, зокрема серцево-судинних (ССЗ), стає ще важчим для суспільства через двосторонні зв’язки з коронавірусною інфекцією [1]. Кардіометаболічна хвороба та її клінічні форми, зокрема ішемічна хвороба серця та цукровий діабет (ЦД) 2 типу, і до пандемії були провідними причинами втрати працездатності та передчасної смерті, а під час пандемії вони також сприяють більш тяжкому перебігу захворювання та смерті від COVID‑19.
Пандемія коронавірусної хвороби COVID‑19 кидає виклик системам охорони здоров’я у всьому світі, потребує безпрецедентних зусиль медичної спільноти та мобілізації усіх ресурсів для щоденного порятунку життів. Тим часом тягар хронічних неінфекційних захворювань, зокрема серцево-судинних (ССЗ), стає ще важчим для суспільства через двосторонні зв’язки з коронавірусною інфекцією [1]. Кардіометаболічна хвороба та її клінічні форми, зокрема ішемічна хвороба серця та цукровий діабет (ЦД) 2 типу, і до пандемії були провідними причинами втрати працездатності та передчасної смерті, а під час пандемії вони також сприяють більш тяжкому перебігу захворювання та смерті від COVID‑19.
Наразі умови для своєчасної діагностики, профілактики й лікування артеріальної гіпертензії, ожиріння, дисліпідемії та дисглікемії суттєво погіршилися через перепрофілювання медичних закладів, вимушену самоізоляцію, а також обмежений доступ населення до фахівців. Наявні докази свідчать про несприятливий перебіг COVID‑19 у пацієнтів із зазначеними факторами ризику. З іншого боку, описані механізми негативного впливу вірусу SARS-CoV‑2 на ренін-ангіотензинову систему (РАС) та інші ланки ендокринної регуляції [1, 2].
Коронавірус і кардіометаболічний синдром
Нещодавно у журналі Американської колегії кардіологів було опубліковано матеріали спеціального семінару, присвяченого епідеміологічним і патофізіологічним зв’язкам коронавірусу з компонентами кардіометаболічного синдрому [2].
Ожиріння. За даними низки досліджень, хворі з COVID‑19 та ожирінням частіше потрапляли до відділення інтенсивної терапії (ВІТ) та мали вищі показники смертності, ніж пацієнти без ожиріння. В одному з досліджень за участю 3615 хворих з COVID‑19 госпіталізація та частота переведень до ВІТ пацієнтів з ожирінням були вищими у віковій групі <60 років порівняно з віком >60 років [3]. Отже, навіть у молодшій віковій групі надмірна маса тіла є значимим фактором ризику тяжкого перебігу COVID‑19. Можливі механізми цього факту включають порушення регуляції імунної відповіді з високими співвідношеннями лептин/адипонектин, малорухливість, підвищену експресію ангіотензинперетворювального ферменту 2 (АПФ‑2) в жировій тканині епікарда, супутні серцево-легеневі захворювання та ліпотоксичність.
Дисглікемія. Хвороба COVID‑19 асоційована з гіршими клінічними наслідками в пацієнтів із ЦД 2 типу. Потенційні механізми зв’язку коронавірусу із глікемічним контролем включають цитокін-опосередковане посилення інсулінорезистентності периферійних тканин і стан гіперкоагуляції; підвищену експресію АПФ‑2 під дією інгібіторів РАС; пряму дію вірусу на панкреатичний АПФ‑2, що спричиняє зниження резерву β-клітин; глікозиляцію вірусного шипового білка й АПФ‑2, що полегшує прикріплення та проникнення вірусу до клітин.
Дисліпідемія. Частота COVID-асоційованих уражень серця й смертність є вищими серед пацієнтів старшого віку із супутніми захворюваннями та факторами ризику, як-от гіпертензія, ЦД, хронічні захворювання нирок, атеросклеротичні ССЗ і хронічна серцева недостатність (СН). Вірусні захворювання супроводжуються системною запальною відповіддю, що спричиняє ушкодження власних тканин і дисфункцію органів. У пацієнтів з COVID‑19 ураження серця асоціюється з лейкоцитозом, підвищеним рівнем прокальцитоніну та С-реактивного білка. Статини мають, крім холестерин-знижувального ефекту, протизапальні властивості, що разом зменшують серцево-судинний ризик. Більшість пацієнтів із ССЗ належать до категорії дуже високого ризику розвитку серцево-судинних подій; їм показана профілактична терапія статинами. Хоча багато пацієнтів з COVID‑19 приймають статини, їх використання спеціально для лікування вірусних захворювань залишається невивченим [2].
Гіпертензія. Поширеність гіпертензії серед дорослого населення США в 2015-2016 роках становила 44,1% за критеріями Американської колегії кардіологів та Американської асоціації серця. Серед осіб з підвищеним кров’яним тиском 49,5% мали ожиріння, 63,2% – гіперхолестеринемію, 27,2% – ЦД. Однією із центральних ланок РАС є АПФ‑2 – фермент, що перетворює ангіотензин І та ангіотензин ІІ на ангіотензин(1-9) й ангіотензин(1-7) відповідно, з яких останній має кардіопротекторні властивості. Пригнічення АПФ‑2, що відбувається після прикріплення вірусу SARS-CoV‑2, порушує кардіопротекцію через контррегуляцію РАС. У популяції пацієнтів з COVID‑19 гіпертензія асоціювалася із супутніми ССЗ (24,3%), діабетом (15,2%) і вищою смертністю [4]. За даними іншого дослідження, гіпертензія в 2,5 разу підвищувала ризик тяжкого перебігу COVID‑19 та летального наслідку (переважно серед пацієнтів віком >60 років) [5]. Саме тому під час пандемії COVID‑19 профілактика та своєчасне виявлення кардіометаболічних порушень є дуже актуальними.
Кардіометаболічна профілактика на рівні первинної ланки. Ефективна стратегія – цілеспрямоване виявлення пацієнтів високого ризику
Близько 80% кардіометаболічних захворювань (КМЗ) пов’язані з факторами ризику, які піддаються корекції, зокрема гіперхолестеринемія, підвищений кров’яний тиск, куріння, ожиріння, малорухливість, нездорове харчування та зловживання алкоголем. Втручання в спосіб життя продемонструвало можливість контролю зазначених чинників і зменшення ризику КМЗ у пацієнтів з початковим високим ризиком. Отже, первинною метою системи охорони здоров’я має бути виявлення та корекція несприятливих факторів у пацієнтів з високим ризиком для попередження клінічної маніфестації КМЗ. Слід орієнтуватися на те, що більша частина популяції високого ризику й досі не знає про свій ризикований статус. Саме тому заслуговує на увагу стратегія систематичного оцінювання ризиків для ідентифікації осіб з підвищеним ризиком КМЗ у щоденній практиці первинної ланки медичної служби. Як демонструють нові дослідження, саме такий систематичний підхід дає змогу суттєво підвищити виявлення окремих значимих факторів ризику й охоплення населення первинною профілактикою.
Так, у рандомізованому контрольованому дослідженні INTEGRATE, яке проводилося в Нідерландах із квітня 2014 по квітень 2017 року [6], вивчали ефективність покрокової стратегії профілактики КМЗ на первинній ланці (загалом 37 амбулаторій загальної практики). Для участі у випробуванні відбирали пацієнтів віком 45-70 років, які не мали КМЗ або факторів ризику КМЗ за даними медичних записів. Першим кроком у досліджуваній стратегії первинної профілактики було визначення індивідуального ризику КМЗ за допомогою опитувальника (онлайн або в паперовій формі), який містив усього 7 запитань щодо статі, віку, статусу куріння, індексу маси тіла (маса та зріст), обхвату талії та сімейної історії передчасних ССЗ (у віці <65 років) або ЦД 2 типу. Подальшим кроком для пацієнтів з підвищеним ризиком КМЗ було запрошення відвідати лікаря для додаткового профілювання ризиків, що включало вимірювання артеріального тиску та лабораторні тести на холестерин, ліпопротеїни і рівень глюкози натще. На третьому кроці пацієнтам надавали поради щодо модифікації способу життя та за наявності показань призначали відповідне лікування для корекції виявлених факторів ризику згідно з національним клінічним протоколом. У контрольній групі пацієнти заповнювали стандартний опитувальник здоров’я; в них не обчислювали персональний ризик КМЗ і не надавали їм індивідуальних порад з модифікації способу життя. Впродовж року спостереження пацієнти отримували рутинне лікування.
Загалом дослідження налічувало 30 934 учасників. Імплементація структурованої покрокової програми профілактики КМЗ забезпечила виявлення в 2-3 рази більше пацієнтів з високим ризиком і суттєве зниження розрахункового 10-річного ризику смерті від ССЗ упродовж року після проведення відповідних профілактичних втручань. Утричі більше антигіпертензивних і ліпідознижувальних препаратів було призначено в дослідній групі, що зумовило суттєве зниження систолічного артеріального тиску (в середньому – 2,26 мм рт. ст.) та ліпопротеїнів низької щільності (ЛПНЩ) (-0,16 ммоль/л) за рік порівняно з контрольною групою.
Отже, ці результати підтверджують доцільність упровадження програм цілеспрямованого виявлення пацієнтів високого ризику й індивідуалізованого підходу до корекції способу життя для профілактики КМЗ [6].
Нова модель кардіометаболічно зумовленого хронічного захворювання як основа для розробки стратегії ефективної профілактики
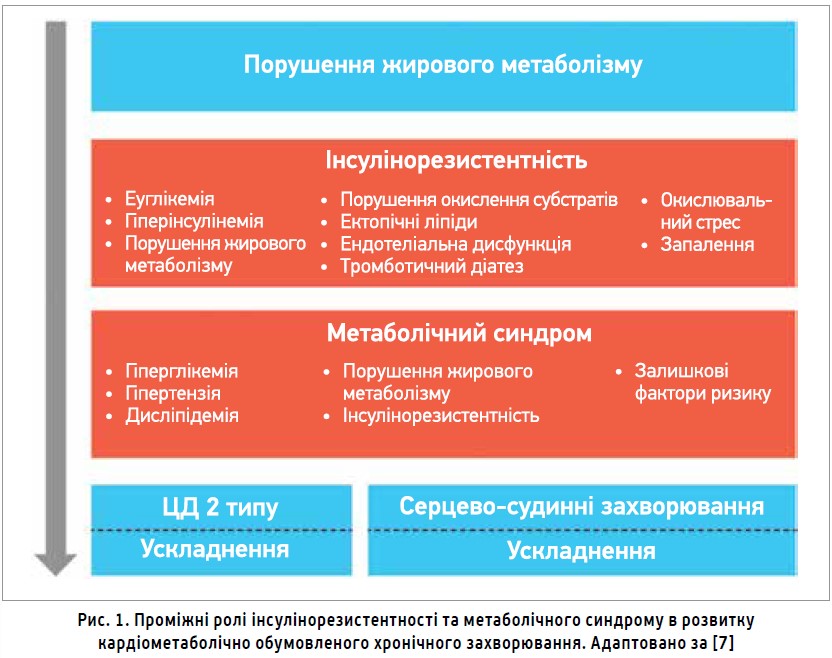
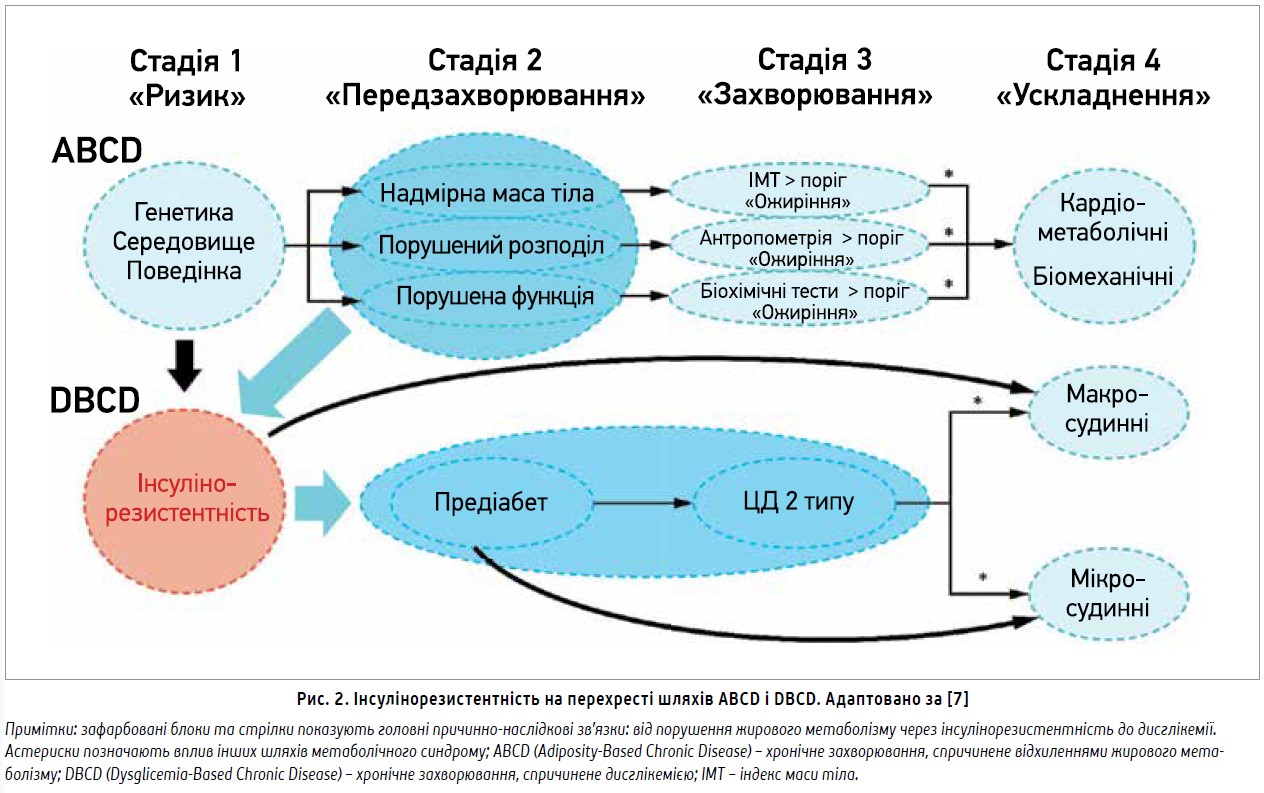
В більшості випадків лікування ССЗ розпочинається після гострої клінічної маніфестації у вигляді стенокардії, гострого коронарного синдрому, інсульту, застійної СН. Водночас відомо, що ССЗ являє собою тривалий процес, який розпочинається в ранні періоди життя з успадкованих і набутих факторів ризику. Важливо, що деякі з них, зокрема надмірна маса тіла та дисглікемія, піддаються корекції. ЦД 2 типу й ожиріння водночас можуть бути як проявами, так і рушіями (драйверами) цього хронічного процесу. З урахуванням цих двосторонніх зв’язків сформульовано нову концепцію кардіометаболічно обумовленого хронічного захворювання (КМОХЗ), у прогресуванні якого центральну роль має інсулінорезистентність (рис. 1, 2). Саме з резистентністю тканин до дії інсуліну пов’язують залишковий ризик після терапії статинами [7].
В моделі КМОХЗ виокремлюють 3 первинних (генетика, середовище, поведінка) та 2 метаболічних рушії (ожиріння і дисглікемія), що сприяють настанню трьох серцево-судинних подій – розвитку ішемічної хвороби серця, СН і фібриляції передсердь. Описані специфічні механізми, які пов’язують ранні первинні рушії з подальшим розвитком ожиріння, інсулінорезистентності, дисфункції β-клітин і метаболічного синдрому, що, своєю чергою, зумовлюють розвиток ССЗ. Практичним призначенням моделі КМОХЗ є пошук дієвих терапевтичних мішеней для профілактики ССЗ. У першому огляді, присвяченому цій проблемі, автори фокусують увагу на таких чинниках розвитку ССЗ, як відхилення жирового метаболізму та дисглікемія [7]. На думку авторів, «хронічне захворювання, спричинене відхиленнями жирового метаболізму» (adiposity-based chronic disease, ABCD) є більш науково точним, дієвим і менш стигматизуючим діагностичним терміном, ніж «ожиріння» [7]. ABCD – складне хронічне прогресуюче захворювання, що включає відхилення в кількості, розподілі та функції жирової тканини, характеризується кардіометаболічними, біомеханічними чи психологічними ускладненнями, які спричиняють захворюваність й смертність. Термін ABCD ухвалено Американською асоціацією клінічних ендокринологів і Європейською асоціацією з вивчення ожиріння [8, 9]. Водночас запропоновано термін «хронічне захворювання, спричинене дисглікемією» (dysglicemia-based chronic disease, DBCD), який може бути коректнішим за термін «діабет» для позначення спектра патофізіологічних подій на шляху від інсулінорезистентності та предіабету до ЦД 2 типу і ССЗ. Дисглікемія є загальним терміном, що об’єднує всі форми діабету та предіабету, включно зі станами підвищеного ризику розвитку ЦД 2 типу, як-от інсулінорезистентність. Основні прояви інсулінорезистентності – нормоглікемія або гіперглікемія з гіперінсулінемією. Термін DBCD ухвалено Американською асоціацією клінічних ендокринологів [10].
Інсулінорезистентність та ССЗ
Вплив інсулінорезистентності на судинну систему включає:
1) дефекти глюкозного гомеостазу, окислення субстратів, мітохондріальної функції;
2) підвищений рівень запалення та окислювальний стрес;
3) аномалії ліпідів і ліпопротеїнів;
4) порушення накопичення ліпідів в адипоцитах через дефекти ліполізу та синтезу тригліцеридів;
5) порушення регуляції судинного тонусу через зниження активності ендотеліальної синтази оксиду азоту (eNOS) і продукції NO [7].
Дисліпідемія, пов’язана з інсулінорезистентністю, характеризується:
1) надмірною постпрандіальною хіломікронемією;
2) підвищеним умістом тригліцеридів у плазмі;
3) низьким рівнем ліпопротеїнів високої щільності;
4) підвищеною концентрацією ЛПНЩ.
У стані інсулінорезистентності ті самі процеси, що порушують дію інсуліну в скелетних м’язах, відбуваються і в міокарді. В кардіоміоцитах накопичуються ектопічні ліпіди, що спричиняє міокардіальну ліпотоксичність. Порушення утилізації субстратів у поєднанні з аномальною активацією ренін-ангіотензин-альдостеронової системи, ендотеліальною дисфункцією, активацією симпатичної нервової системи, оксидативним стресом і запаленням спричиняють структурні зміни в серці. Втрата кардіоміоцитів і порушення роботи скоротливих білків зумовлюють розвиток фіброзу. Підвищена жорсткість міокарда порушує діастолічну релаксацію і наповнення шлуночка перед систолою. В результаті розвивається СН зі збереженою фракцією викиду, що супроводжується розширенням лівого передсердя, збільшенням маси лівого шлуночка та розвитком діастолічної дисфункції. Із часом діастолічна дисфункція може прогресувати до систолічної дисфункції, тобто розвивається СН зі зниженою фракцією викиду [7].
Інсулінорезистентність (навіть на тлі нормоглікемії) може спричиняти прискорений розвиток атеросклерозу, міокардіальну дисфункцію, а також підвищує ризик серцево-судинних подій. Сукупність відхилень, включаючи запалення, збільшення передсердь, діастолічну та систолічну дисфункцію шлуночків, пов’язана з підвищеним ризиком розвитку миготливої аритмії. Дослідження IRAS (Insulin Resistance Atherosclerosis Study) та BIP (Bezafibrate Infarction Prevention Trial) чітко продемонстрували, що інсулінорезистентність асоціюється з розвитком серцево-судинних подій [11, 12].
Отже, запропонована концепція КМОХЗ фокусує увагу на двох основних факторах ризику – порушенні жирового метаболізму та дисглікемії, які є рушіями розвитку серцево-судинних проблем і мають стати важливими мішенями профілактичної терапії [7].
Сучасні можливості медикаментозної корекції ожиріння і дисглікемії
У рамках концепції раннього виявлення і профілактики КМЗ набуває популярності інноваційний терапевтичний підхід до лікування ЦД 2 типу – інкретинова терапія, що включає призначення агоністів рецепторів глюкагоноподібного пептиду 1 (арГПП-1). Цей клас протидіабетичних засобів покращує глюкозний гомеостаз шляхом стимуляції секреції інсуліну, інгібування секреції глюкагону, прямої та непрямої супресії ендогенної продукції глюкози, пригнічення апетиту за рахунок регуляції вивільнення греліну, підвищення чутливості тканин до інсуліну через зниження маси тіла, а також зменшення запального ушкодження бета-клітин. Важливою перевагою арГПП-1 є низький ризик розвитку гіпоглікемії [13].
Дані, отримані в клінічних дослідженнях і на практиці, вказують на наявність у арГПП-1 сприятливих серцево-судинних ефектів поза регуляцією обміну глюкози. Так, екзенатид і ліраглутид виявили здатність знижувати рівень артеріального тиску, масу тіла й концентрацію атерогенних фракцій ліпідів. Ліраглутид у дослідженнях in vitro й in vivo покращував циркуляцію крові, підвищуючи рівень оксиду азоту та пригнічуючи адгезію прокоагулянтних факторів. Водночас ліраглутид продемонстрував сприятливий вплив на ремоделювання серця після інфаркту міокарда [13, 14].
В масштабних клінічних дослідженнях зазначені ефекти реалізувалися в суттєве зменшення частоти серцево-судинних подій та смертності. Зокрема, в дослідженні LEADER (Liraglutide Effect and Action in Diabetes: Evaluation of CV Outcome Results) за участю 9340 пацієнтів зі встановленим атеросклеротичним ССЗ або з факторами його ризику оцінювали ефекти ліраглутиду за трикомпонентною кінцевою точкою – серцево-судинна смерть, нефатальний інфаркт міокарда та нефатальний інсульт. У результаті лікування частота настання подій кінцевої точки була меншою на 13% у групі ліраглутиду (відносний ризик (ВР) 0,87; 95% довірчий інтервал (ДІ) від 0,78 до 0,97) порівняно із групою плацебо. Смертність від усіх причин зменшилася на 15% (ВР 0,85; 95% ДІ від 0,74 до 0,97) переважно за рахунок серцево-судинної смертності [15].
Впровадження арГПП-1 вже стало поворотним моментом в лікуванні ЦД. Цей клас препаратів дає змогу індивідуально адаптувати лікування до потреб конкретного пацієнта для досягнення кращого метаболічного контролю і зниження ризику ССЗ [13]. Наразі арГПП-1 рекомендовані профільними діабетичними товариствами для лікування пацієнтів із ЦД 2 типу як перша лінія терапії, а також й на більш пізних стадіях його прогресування в поєднанні з інсуліном. В експертному консенсусі Американської колегії кардіологів 2020 року рекомендовано застосування двох нових класів цукрознижувальних засобів – інгібіторів натрійзалежного котранспортера глюкози 2 типу та арГПП-1 всім хворим із ЦД 2 типу й атеросклеротичним ССЗ задля зниження серцево-судинних ризиків [16]. За ключовими словами cardiovascular disease and GLP‑1 RAs у базі даних клінічних випробувань ClinicalTrials.gov знайдено 46 досліджень, 22 з яких завершені, а 2 мають опубліковані попередні результати; це свідчить про підвищений інтерес до серцево-судинних ефектів арГПП-1 та їх практичного застосування.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 2 (495), 2021 р.