27 лютого, 2025
Невідкладна допомога при періопераційній анафілаксії: алгоритм Ради з реанімації Великої Британії для лікарів-анестезіологів
Періопераційна анафілаксія є життєвозагрозливим станом, спричиненим реакцією гіперчутливості негайного типу. Хронологічний зв’язок між введеними препаратами згідно анестезіологічної карти та розвитком анафілактичної реакції є важливим первинним етапом ведення пацієнтів з алергічними реакціями під час загальної анестезії. Лікування анафілаксії включає як негайну стабілізацію стану пацієнта, так й ідентифікацію тригера. Тісна співпраця між провідними науковими та медичними установами має важливе значення для належного ведення пацієнтів із періопераційною анафілаксією як під час розвитку ускладнення, так і при підготовці до наступних хірургічних втручань.
Ключові слова: періопераційна анафілаксія, адреналін, алергічні реакції, реанімація, інфузійна терапія.
Періопераційна анафілаксія є рідкісним, але потенційно небезпечним ускладненням, яке необхідно враховувати під час проведення загальної анестезії, коли виникає різке погіршення показників серцево-легеневої та дихальної систем пацієнта. Настанова Ради з реанімації Великої Британії щодо періопераційної анафілаксії наголошує на важливості раннього внутрішньовенного введення адреналіну та проведення інфузійної терапії, а також окреслює рекомендації щодо лікування рефрактерної анафілаксії та подальшого спостереження за пацієнтом. Розроблений алгоритм схвалений Королівським коледжем анестезіологів, Асоціацією анестезіологів Великої Британії, Британським товариством алергології й клінічної імунології та Професійною спілкою клінічної імунології Британського товариства імунології. Автором ключових рекомендацій оновленого алгоритму є керівний комітет Спілки з питань періопераційної алергії у співпраці з Радою з реанімації Великої Британії.
Основні положення
- У випадку різкого погіршення показників серцево-судинної та дихальної систем слід розглянути ймовірність розвитку анафілаксії.
- Першою лінією лікування періопераційної анафілаксії є внутрішньовенне (в/в) введення адреналіну (епінефрину). Початкова доза адреналіну 50 мкг рекомендована у дорослих і дітей віком >12 років (0,5 мл із розведення 1 мг препарату на 10 мл‑1 фізіологічного розчину [титр* 1:10 000]). Деякі пацієнти можуть відповідати на менші дози адреналіну (10-50 мкг), які титрують до відповідного клінічного ефекту.
* 1 мл розчину адреналіну 0,18% розводять у 9 мл розчину NaCl 0,9%; отримують 1 мг адреналіну в 10 мл або 0,01 мг (10 мкг) в 0,1 мл.
- Введення адреналіну має супроводжуватися в/в введенням кристалоїдних розчинів. Рекомендовано вводити швидкі болюси розчинів у великих об’ємах: дорослим і дітям віком >12 років – 500-1000 мл; дітям віком <12 років – до 20 мл/кг). Залежно від клінічного стану може призначатися багаторазове введення рідини.
- Якщо ознаки анафілаксії зберігаються, незважаючи на болюсне введення адреналіну, розпочніть інфузію адреналіну. Інфузія адреналіну в низьких дозах через периферичний венозний доступ є ефективною альтернативою, якщо центральний венозний доступ відсутній.
- Розпочніть серцево-легеневу реанімацію (СЛР), якщо систолічний артеріальний тиск (АТ) <50 мм рт. ст., незважаючи на початкове введення адреналіну та в/в інфузійну терапію.
- Антигістамінні препарати та кортикостероїди не є препаратами вибору для невідкладного лікування анафілаксії. Не слід надавати перевагу даним групам препаратів порівняно з уведенням адреналіну та проведенням інфузійної терапії.
Актуальність проблеми
Періопераційна анафілаксія під час проведення анестезії є потенційно життєзагрозливим ускладненням із частотою виникнення від 1:353 до 1:18 600 та ризиком смерті в межах 1-4% від всієї кількості випадків проведення загального знеболення. Показники смертності внаслідок розвитку анафілаксії під час анестезії є значно вищими, ніж смертність від анафілаксії з інших причин.
Періопераційна анафілаксія – це клінічний діагноз, встановити який у періопераційному періоді може бути досить складно, оскільки типові ознаки алергічної реакції, такі як кропив’янка та інші шкірні прояви, відсутні приблизно у третині випадків. Диференціальна діагностика періопераційної анафілаксії включає широкий спектр діагнозів, у тому числі надмірні фізіологічні реакції на використання препаратів для індукції загальної анестезії, маніпуляції на дихальних шляхах та хірургічні втручання. Найчастіше періопераційна анафілаксія виникає після індукції анестезії, причому симптоми зазвичай проявляються протягом декількох хвилин після введення препарату, який викликає алергічну реакцію негайного типу. Час до зупинки серця після в/в введення є швидшим, ніж при інших шляхах впливу тригерного препарату, і зазвичай складає 5-10 хвилин. Модифікована шкала Рінга – Мессмера включає фенотипи періопераційних алергічних реакцій та градацію їх тяжкості (таблиця).
|
Таблиця. Оцінка передбачуваних періопераційних алергічних реакцій за модифікованою шкалою Рінга – Мессмера |
|
|
Ступінь тяжкості |
Клінічні ознаки |
|
1 |
Зміни шкірних покривів та/або слизових оболонок: генералізована еритема та/або кропив’янка |
|
2 |
Ознаки помірного поліорганного ураження: симптоми з боку шкірних покривів та/або слизових оболонок із помірною гіпотензією або без неї; тахікардія; помірний бронхоспазм або шлунково-кишкові симптоми |
|
3 |
Життєзагрозливе моно- або поліорганне ураження: гіпотензія, що загрожує життю; тахікардія або брадикардія з/без серцевої аритмії; тяжкий бронхоспазм; симптоми з боку шкірних покривів та/або слизових оболонок; шлунково-кишкові симптоми |
|
4 |
Зупинка серця або дихання |
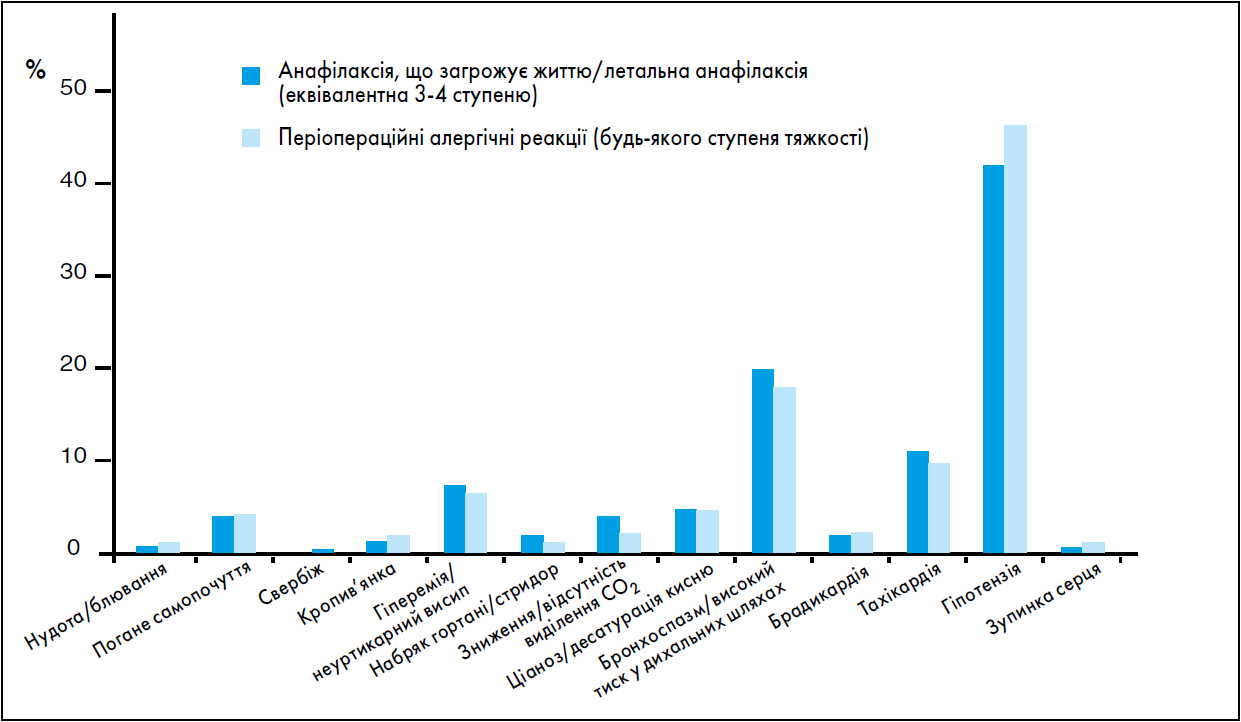
За даними 6-го Національного проекту Королівського коледжу анестезіологів (NAP6), гіпоксія була рідкісним симптомом анафілаксії, хоча часто відзначалася впродовж першої години після реанімації. Ангіоневротичний набряк дихальних шляхів був вкрай рідкісним при тяжкій періопераційній анафілаксії. Натомість зміни шкірних покривів, такі як генералізована еритема або кропив’янка, трапляються частіше і є основним симптомом у 10-40% випадків періопераційних реакцій (рис. 1). Іноді зміни шкірних покривів можна побачити лише після відновлення адекватної перфузії та/або зняття хірургічної пов’язки.
Рис. 1. Частота симптомів періопераційної анафілаксії
Лікування періопераційної анафілаксії
Рання діагностика та лікування потенційної анафілаксії має вирішальне значення. «Якщо сумніваєшся – лікуй» – корисна настанова в контексті будь-якої значної, неочікуваної серцево-судинної або респіраторної події. Перегляд настанов щодо лікування анафілаксії нещодавно був проведений Робочою групою з анафілаксії Великої Британії (RCUK) із метою оновлення рекомендацій 2021 року з невідкладного лікування періопераційної алергічної реакції негайного типу. Консенсусні рекомендації Міжнародної групи з підозри на періопераційні алергічні реакції (ISPAR) щодо лікування анафілаксії також описують лікування даної патології.
Спірними питаннями лікування анафілаксії є:
- раннє введення адреналіну паралельно з підтримкою дихальних шляхів;
- проведення вентиляції легень;
- положення пацієнта лежачи на спині;
- збільшення об’єму циркулюючої крові (ОЦК) шляхом в/в введення ізотонічного кристалоїду.
Лікування будь-якого порушення прохідності дихальних шляхів має включати перевірку правильності розміщення ендотрахеальної трубки для виключення нерозпізнаної інтубації стравоходу та оцінку прохідності анестезіологічного контуру й трахеальної трубки.
Міжнародний консенсус визначає, що адреналін є препаратом першої лінії для лікування анафілаксії. Настанова RCUK 2021 року рекомендує внутрішньом’язове (в/м) введення адреналіну, що є найбільш оптимальним способом для більшості медичних працівників завдяки простоті введення та сприятливому профілю безпеки. Однак у періопераційному періоді, коли пацієнти перебувають під ретельним наглядом анестезіолога, широко поширеною є думка, що в/в введення адреналіну є більш доцільним. Введення адреналіну в/в сприяє більш швидкому покращенню стану пацієнта, ніж в/м введення, і дає змогу більш точно титрувати дозу препарату залежно від клінічного ефекту. У дорослих пацієнтів початкова доза адреналіну для в/в введення складає 50 мкг (0,5 мл від розчину 1 мг адреналіну на 10 мл фізіологічного розчину або розчину для інфузій, розведення 1:10 000) і рекомендована алгоритмом RCUK, хоча деякі пацієнти можуть демонструвати покращення гемодинаміки у відповідь на введення менших доз (10-50 мкг), які титрують для досягнення необхідного ефекту.
Рефрактерна анафілаксія встановлюється у випадку, коли ознаки та симптоми ускладнення не зникають після введення адреналіну. У проведених дослідженнях в/в інфузії низьких доз адреналіну продемонстрували вищу ефективність порівняно з болюсним введення й асоціювалися з меншою загальною дозою препарату, частотою двофазних реакцій і сприятливим профілем безпеки. З огляду на це й відповідно до міжнародних рекомендацій, періопераційний алгоритм RCUK рекомендує розпочинати в/в інфузію адреналіну в низьких дозах, якщо початкова відповідь на в/в болюсне введення є неоптимальною. Адреналін слід вводити через периферичну венозну канюлю, якщо відсутній центральний венозний доступ. Дозволено використовувати місцеві протоколи для інфузії адреналіну. У якості альтернативи представлений алгоритм дій, які передбачені протоколом, складеним на основі оновлених опублікованих рекомендацій (рис. 2).
Рис. 2. Алгоритм лікування періопераційної анафілаксії Ради з реанімації Великої Британії
Швидкі болюсні введення великих об’ємів інфузійних розчинів рекомендовано призначати у випадку невідкладного лікування анафілаксії для відновлення та підтримання адекватного об’єму ОЦК. Початкові болюси інфузій складають 500-1000 мл (або 20 мл/кг у дітей віком <12 років). Подальші болюси рідини слід титрувати відповідно до реакції організму. Деякі випадки періопераційної анафілаксії можуть вимагати призначення більших об’ємів інфузій: до 3-5 л у дорослих і 60-100 мл/кг у дітей.
Не встановлено чіткої переваги використання колоїдів у якості інфузійної терапії перед кристалоїдами у випадку анафілаксії. Натомість колоїди (особливо на основі желатину) самостійно можуть викликати алергічні реакції. Покращити венозне повернення до серця можна, нахиливши донизу головний край стола або піднявши ноги пацієнта. Якщо клінічна відповідь є неоптимальною незважаючи на інфузію адреналіну та відповідну рідинну реанімацію, слід розпочати застосування вазопресорів другої лінії (на додаток до адреналіну).
Немає чітких доказів, які б надавали перевагу одному вазопресору над іншим. У пацієнтів, які приймають β-блокатори, можна розглянути можливість застосування глюкагону, хоча докази його ефективності обмежені. Сугамадекс не є препаратом вибору у випадку проведення реанімаційних дій при підозрі на анафілаксію. СЛР має бути розпочата у дорослих із систолічним АТ <50 мм рт. ст., особливо на фоні брадикардії. У цьому випадку дози адреналіну слід титрувати на основі реакції серцево-судинної системи на компресії грудної клітки. У разі зупинки серця адреналін слід вводити в/в згідно із протоколами розширеної реанімації. Тривалу СЛР (включаючи екстракорпоральну підтримку, якщо це можливо) слід розглянути при зупинці серця, яка спричинена анафілаксією, оскільки цей стан є потенційно зворотним.
У пацієнтів із тяжким персистуючим бронхоспазмом можна розглянути можливість застосування сальбутамолу та іпратропію у формі небулайзера або парентеральних бронходилататорів. Їх слід використовувати як додаткову терапію, а не як альтернативу інфузії адреналіну. Відсутні докази переваг та/або недоліків в/в застосування β2-агоністів або сульфату магнію для лікування анафілаксії. Кетамін та леткі анестетики (наприклад, севофлуран) також мають бронхолітичну дію, проте відсутні докази ефективності їх застосування при анафілаксії. Дані настанови визначені ISPAR.
Основним ефектом кортикостероїдів є зниження пізньої (а не ранньої) запальної відповіді. Однак метааналізи підтвердили відсутність будь-яких доказів того, що кортикостероїди можуть зменшувати ступінь тяжкості анафілактичної реакції або запобігають двофазним реакціям. Дані свідчать про те, що в багатьох медичних закладах кортикостероїди відтерміновують належне лікування адреналіном. З цієї причини рутинне призначення кортикостероїдів більше не рекомендовано для початкового лікування анафілаксії. Немає доказів, які б підтверджували або спростовували їхню ефективність при рефрактерній анафілаксії, тому доцільно розглядати кортикостероїди як додаткову терапію до адреналіну для лікування рефрактерного шоку або бронхоспазму.
Антигістамінні препарати не рекомендовано застосовувати для початкового невідкладного лікування анафілаксії: вони не ефективні проти серцево-судинних і респіраторних проявів і не покращують виживаність. Блокатори Н1-рецепторів, введені у вигляді швидкого в/в болюсу, також можуть посилювати гіпотензію. Існують докази того, що введення антигістамінних препаратів затримує у клінічній практиці застосування адреналіну та інших методів лікування в умовах невідкладної допомоги. Антигістамінні препарати можуть бути корисними для лікування ангіоневротичного набряку, кропив’янки та свербежу після стабілізації стану пацієнта.
Клінічне спостереження за пацієнтом після розвитку періопераційної анафілаксії
При анафілаксії дегрануляція тучних клітин призводить до вивільнення ферменту триптази, внаслідок чого її концентрація в сироватці крові може суттєво не збільшуватися впродовж ≥30 хв після появи симптомів і досягати піку лише через 1-2 год після прояву ознак анафілаксії. Період напіввиведення триптази короткий (близько 2 год), і концентрація ферменту може нормалізуватися протягом 6-8 год, тому дуже важливо правильно обрати час для забору зразків крові. В ідеалі мають бути взяті три зразки:
- перший – як тільки стан пацієнта стабілізується (забір крові не має затримувати початкове лікування та реанімаційні заходи);
- другий – протягом 1-4 год після появи симптомів (але бажано – через 1-2 год після появи симптомів);
- третій – щонайменше через 24 год після прояву ознак анафілаксії (базовий зразок).
Міжнародними настановами прийняте консенсусне рівняння щодо оцінки значного підвищення рівня триптази: 1,2 Ч базовий рівень триптази + 2 мг/л. Це називається динамічним підвищенням рівня триптази, яке може спостерігатися, навіть якщо піковий рівень знаходиться в межах норми. Слід зазначити, що відсутність підвищення рівня триптази не виключає анафілаксії. Усіх пацієнтів із підозрою на періопераційні реакції гіперчутливості слід скеровувати до спеціалізованої алергологічної служби для проведення стандартного алергологічного тестування, незалежно від результатів визначення рівня триптази тучних клітин.
Реферативний огляд підготувала Катерина Пашинська
За матеріалами: Dodd A., Turner P.J., Soar J., Savic L.; representing the UK Perioperative Allergy Network. Emergency treatment of peri-operative anaphylaxis: Resuscitation Council UK algorithm for anaesthetists 11 January 2024 https://doi.org/10.1111/аnae.16206.