3 листопада, 2021
Сучасна роль антисептиків у лікуванні хронічних ран
До вашої уваги представлено основні результати дослідження міжнародної групи експертів стосовно ефективності, безпечності та переносимості місцевих антисептиків при лікуванні критично колонізованих, інфільтрованих біоплівками хронічних ран. Розглянуто особливості застосування повідон-йоду для догляду за ранами. Представлено новий алгоритм лікування хронічних ран, що довго не загоюються, із критичною колонізацією або інфільтрацією біоплівками.
Ключові слова: хронічна рана, біоплівка, критична колонізація, повідон-йод.
Загоєння рани – складний та високоорганізований процес, необхідний для відновлення фізіологічної бар’єрної функції шкіри, який запобігає подальшим ушкодженням або інфекційним ускладненням [1, 2]. Звичайний процес загоєння рани включає три послідовні фази: запалення, проліферацію та ремоделювання [1], що опосередковуються різними типами клітин, включаючи фібробласти, кератиноцити, ендотеліальні клітини та макрофаги, активність яких ретельно координується рядом факторів росту, цитокінів та хемокінів [3]. Однак порушення фізіологічного перебігу фаз загоєння може призвести до розвитку хронічної рани [1, 4]. Хронічні рани, що включають трофічні виразки нижніх кінцівок (внаслідок хронічної венозної або артеріальної недостатності), синдром діабетичної стопи та пролежні, є значним тягарем як для окремого пацієнта, так і для системи охорони здоров’я у цілому [5, 6].
Існує багато факторів, які можуть бути причиною затримки та/або неспроможності загоєння хронічної рани, а саме: вік пацієнта, нутритивний статус (наприклад, ожиріння), насиченість рани киснем, а також наявність хронічного захворювання (наприклад, цукрового діабету) або імунодефіцитного стану [7, 8]. Деякі види лікування також можуть перешкоджати загоєнню ран, наприклад хіміотерапевтичні засоби, променева терапія, тривале застосування кортикостероїдів та нестероїдних протизапальних препаратів [9, 10].
Утім чи не найбільш вагомим фактором, який може вплинути на загоєння хронічної рани, а згодом збільшити ймовірність її інфікування, є інфільтрація біоплівками [11‑14]. Останні являють собою структуровані угруповання бактерій, обмежені загальною захисною полімерною мембраною й здатні прикріплюватися до будь-якої поверхні [11, 15, 16]. Біоплівки перешкоджають нормальному перебігу процесу загоєння рани, утримуючи її у фазі запалення [17, 18]. Нещодавній систематичний огляд та метааналіз показали, що поширеність біоплівок у хронічних ранах становить 78,2% [13, 20]. Їх важко візуалізувати макроскопічно, і незалежно від того, розташовані біоплівки на поверхні чи глибоко у рані, їх ідентифікація та діагностика можуть бути складними [21].
Нещодавно було розроблено керівні настанови, покликані допомогти клініцистам у розпізнаванні ознак і симптомів біоплівок при хронічних ранах, а отже, оптимізувати догляд за пацієнтами [21]. Проте на даний час не існує золотого стандарту діагностичних тестів, які б дозволили лікарям підтверджувати наявність біоплівок у хронічних ранах [11, 18, 21, 26].
До теперішнього часу терапія, спрямована на знищення біоплівок у хронічних ранах, ґрунтувалася переважно на використанні звичайних антибіотиків та антисептиків [16]. Однак біоплівки можуть бути дуже стійкими до антимікробних засобів, що призводить до неефективності лікування [31‑35]. Останні настанови рекомендують використання місцевих антисептиків як терапії першої лінії при лікуванні хронічних ран [21].
Автори провели огляд літератури з метою порівняння антисептиків для лікування хронічних ран – повідон-йоду та срібла й на основі отриманих результатів запропонували новий алгоритм лікування хронічних, важко колонізованих, інфільтрованих біоплівками ран.
Антимікробний спектр дії
Відмінності в антимікробному спектрі активності повідон-йоду та срібла зумовлені різними механізмами дії кожного з антисептиків.
Повідон-йод
Спектр активності повідон-йоду включає грампозитивні й грамнегативні бактерії (у т.ч. штами, стійкі до антисептиків та антибіотиків), гриби, найпростіші, віруси, спорові бактерії та амеби [37‑43]. Результати досліджень показують, що повідон-йод демонструє швидкий початок дії та виражену антимікробну активність після часу експозиції 1 хв [71, 72]. Дослідження продемонстрували потужну антимікробну ефективність повідон-йоду проти деяких вірусів (вірус Ебола, коронавірус MERS-CoV та коронавірус SARS-CoV) усього через 15 с після контакту [73‑75]. Крім того, нещодавнє дослідження in vitro показало, що повідон-йод також проявляє швидку й потужну активність проти вірусу SARS-CoV‑2. Результати продемонстрували, що розчини повідон-йоду проявляли ≥99,99% віруліцидну активність проти SARS-CoV‑2 після 30-секундної експозиції, а отже, повідон-йод може стати важливою складовою майбутніх стратегій боротьби з інфекцією COVID‑19 [76]. Незважаючи на більш ніж 150-річне використання цього антисептика, немає свідчень щодо стійкості бактерій до йоду, що пов’язано з його численними механізми дії [44, 45, 48, 77]. Крім того, немає доказів перехресної резистентності до антибіотиків або інших антисептиків при застосуванні повідон-йоду у широкому діапазоні грампозитивних і грамнегативних бактерій [40, 46, 47].
Препарати на основі срібла
Лікарські засоби для догляду за ранами, що містять срібло (солі срібла, колоїдне срібло, наночастинки срібла), потребують вивільнення його позитивно заряджених іонів для прояву антимікробної активності [68, 78, 79]. Деякі композиції з більш високим вивільненням срібла продемонстрували антимікробну активність через 30 хв після контакту з клінічно значущими бактеріями [81]. Засоби на основі срібла проявляють бактерицидну активність щодо грамнегативних і грампозитивних бактерій, деяких грибів та вірусів [56‑62]. Проте було задокументовано стійкість бактерій до іонів срібла [63‑66], яка, згідно з отриманими даними, кодується на плазмідах [82]. Це викликає особливе занепокоєння, оскільки перенесення плазмід між бактеріями у хронічних ранах може викликати стійкість до іонів срібла у багатьох видів бактерій [83].
Ефективність проти біоплівок
Всесвітня організація світових лікувальних товариств (The World Union of Wound Healing Societies) визнала йод ефективним антимікробним засобом проти біоплівок [18], що було підтверджено у численних дослідженнях. Субінгібіторні концентрації повідон-йоду (0,17, 0,35 та 0,7%) пригнічували розвиток біоплівок Staphylococcus epidermidis та S. aureus – двох найпоширеніших видів бактерій, що присутні у хронічних ранах [17, 85]. Hill та співавт. (2010), використовуючи in vitro модель біоплівок хронічної рани, продемонстрували, що змішані біоплівки Pseudomonas та Staphylococcus руйнувалися під впливом 1% розчину повідон-йоду. Притому що ані ципрофлоксацин, ані флуклоксацилін не мали такого ефекту [86]. Крім того, у цьому ж дослідженні зрілі 7-денні змішані біоплівки були повністю зруйновані після застосування розчину повідон-йоду [86].
Повідон-йод у знижених концентраціях (0,25%) був ефективний in vitro стосовно біоплівок, сформованих стійкими до багатьох препаратів S. aureus, Klebsiella pneumoniae, Pseudomonas aeruginosa та C. albicans [87]. У дослідженнях доведено, що 10% розчин повідон-йоду здатний руйнувати як ранні (90 хв), так і зрілі (48 год) біоплівки, утворені Candida auris – стійкими до антимікробних засобів дріжджами [88, 89].
Ефективність повідон-йоду проти біоплівок зумовлена швидким початком дії (in vitro), при цьому повне знищення зрілих 3-денних біоплівок S. aureus та P. aeruginosa досягається вже після 15-хвилинної експозиції. Крім того, 10% розчин повідон-йоду продемонстрував більшу ефективність проти біоплівок, що складалися з P. aeruginosa, Streptococcus pyogenes, MRSA та Bacteroides fragilis порівняно з 0,05% розчином ацетату срібла. За результатами дослідження використання повідон-йоду виявилося найбільш ефективним у зменшенні кількості бактерій із плином часу (57%) порівняно з ацетатом срібла (27%) [91]. У подальшому дослідженні пов’язки з йодом продемонстрували більшу антимікробну ефективність проти зрілих біоплівок P. aeruginosa та S. aureus протягом 24 год порівняно із пов’язками на основі срібла [92].
Цитотоксичність та переносимість
Основними функціями будь-якої пов’язки є механічний та антимікробний захист рани. Щільний контакт елементів пов’язки із клітинами, які є ключовими учасниками процесу загоєння рани, неминучий, тому дуже важливо, щоб вони були сумісними між собою [109]. Цитотоксичні ефекти речовин, з якими накладають пов’язки, можуть зменшувати життєздатність, проліферацію та міграцію клітин, що беруть участь у процесі загоєння рани, і, таким чином, сповільнювати його [109].
Лабораторний аналіз, проведений на культурі клітин мишачих фібробластів, показав, що повідон-йод має найнижчу цитотоксичність порівняно з нітратом срібла та сульфадіазином срібла [132]. Крім того, з-поміж протестованих антисептиків повідон-йод продемонстрував унікальну властивість стимулювати фібробласти, що може бути ключовим чинником поліпшення загоєння ран [133]. У дослідженні in vitro цитотоксичної дії широко використовуваних антисептиків на людські фібробласти та мезенхімальні стромальні клітини повідон-йод був єдиним засобом, після дії якого клітини залишалися життєздатними за мінімальної бактерицидної концентрації (МБК; 1,32 г/л).
Bigliardi та співавт. (2017) зазначили, що у дослідженнях in vivo повідон-йод добре переноситься при використанні у відповідних концентраціях, натомість як цитотоксичність повідон-йоду спостерігалася лише в деяких дослідженнях in vitro [134]. Дійсно, щільність дендроцитів та мікросудин у хронічних виразках нижніх кінцівок була вищою після 6 тижнів лікування повідон-йодом порівняно із сульфадіазином срібла та хлоргексидином. Загалом, повідон-йод демонструє хороший профіль переносимості [49].
Лікування ран
При лікуванні ран важливо враховувати не лише антимікробну ефективність та потенційну цитотоксичність антисептиків, а й те, як вони можуть впливати на складні клітинні та позаклітинні механізми, що беруть участь у процесі загоєння ран. Ідеальний антисептик має володіти здатністю полегшувати загоєння ран [49].
Повідон-йод посилює загоєння ран за рахунок збільшення експресії трансформуючого фактора росту β, неоваскуляризації та повторної епітелізації [143]. Дослідження in vitro свідчать, що повідон-йод може полегшити загоєння ран, посилити протизапальну дію, поглинаючи супероксидні аніони та інгібуючи вироблення активних форм кисню поліморфно-ядерними лейкоцитами людини [144]. Так, застосування повідон-йоду у поєднанні з гідроколоїдною пов’язкою при лікуванні виразок на фоні хронічної венозної недостатності нижніх кінцівок супроводжувалося вираженим зменшенням запалення, васкуліту та фагоцитарної інфільтрації рани порівняно із застосуванням лише гідроколоїдної пов’язки, що призвело до пришвидшення її загоєння [145]. У подальшому дослідженні швидкість загоєння хронічних виразок нижніх кінцівок була значно збільшена за допомогою повідон-йоду порівняно з контролем, що скоротило час загоєння на 2‑9 тижнів [135].
Нещодавнє проспективне дослідження IV фази, проведене за участі 106 дорослих пацієнтів, показало, що використання пов’язок із повідон-йодом сприяло зменшенню часу епітелізації порівняно з гідроцелюлярною пов’язкою та вазеліновою марлею [146]. Порівняно з пінними пов’язками на основі срібла або зі звичайною марлею пінна пов’язка з 3% розчином повідон-йоду була найефективнішою для загоєння ран, сприяла неоваскуляризації, повторній епітелізації та відкладенню колагену [149]. Крім того, 10% розчин повідон-йоду ефективніше сприяв неоваскуляризації, ніж розчин нітрату срібла [150].
Алгоритм лікування хронічних ран
Із розглянутих антисептиків повідон-йод має особливі характеристики, які забезпечують оптимальне лікування хронічних, незагойних ран із критичною колонізацією та/або інфільтрацією біоплівками, а саме:
- високу швидкість дії;
- потужну ефективність проти біоплівок;
- широкий спектр протимікробної активності;
- ранозагоювальні властивості.
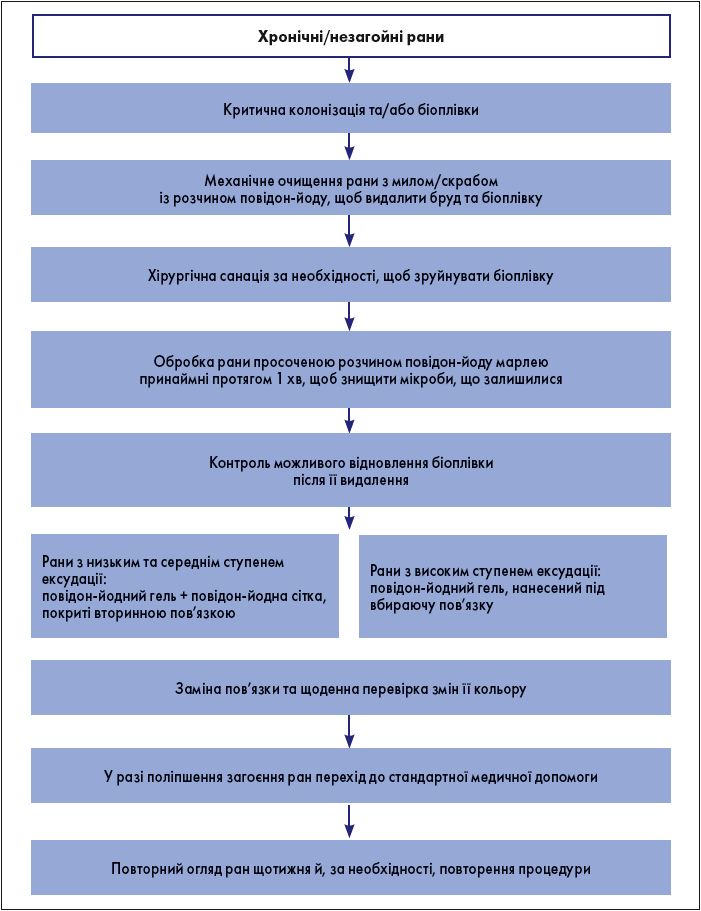
На рис. 1 представлено практичний алгоритм видалення біоплівки та лікування критично колонізованих ран із використанням розчину повідон-йоду.
Правильний менеджмент рани має вирішальне значення для її успішного загоєння. Лише дотримання усіх складових комплексу TIMERS (рис. 2) дозволяє максимально ефективно вирішити проблему хронічних/незагойних ран [23, 163].
Рис. 1. Менеджмент хронічних, незагойних ран TIMERS
Рис. 2. Алгоритм лікування хронічних, незагойних ран із критичною колонізацією та/або наявністю біоплівок
Висновки
Останні дані свідчать про те, що більшість хронічних ран мають біоплівки, які можуть перешкоджати загоєнню ран і призводити до неефективного лікування, обтяжуючи як пацієнта, так і систему охорони здоров’я. Повідон-йод демонструє потужну ефективність проти біоплівок, утворених різноманітними мікробами, включаючи S. aureus, S. epidermidis та P. aeruginosa. З огляду на те, наскільки різноманітна мікробна спільнота може бути присутня у хронічних ранах, ширший спектр протимікробної активності повідон-йоду робить його найбільш вигідним антисептиком порівняно з препаратами срібла. Повідон-йод відповідає всім вимогами щодо ідеального антисептика для догляду за хронічними ранами, а саме не викликає набутої бактеріальної стійкості або перехресної резистентності, має низьку цитотоксичність, добру переносимість і здатність прискорювати загоєння ран.
Список літератури знаходиться в редакції.
Реферативний огляд підготувала Марія Грицуля
За матеріалами: Alves P. J. et al. Update on the role of antiseptics in the management of chronic wounds with critical colonisation and/or biofilm / International wound journal / 13 December 2020.