5 травня, 2022
Порівняння ефективності цефтазидиму/авібактаму та поліміксину В у пацієнтів з інфекціями, викликаними карбапенем-резистентною Klebsiella pneumoniae
Ретроспективне дослідження
Серйозною проблемою для системи охорони здоров’я у всьому світі є різке підвищення частоти інфекцій, викликаних карбапенем-резистентною Klebsiella pneumoniae (CRKP). Найактуальніші завдання, спрямовані на обмеження цих інфекцій: подолання високих показників смертності від них та пошук ефективних методів лікування. Однак досліджень, що оцінюють ефективність наявних антибіотиків для лікування CRKP-інфекції, на сьогодні недостатньо. Метою цього дослідження було порівняння ефективності поліміксину В та цефтазидиму/авібактаму у пацієнтів із CRKP-інфекцією та визначення факторів ризику, що впливають на показники 7-денної бактеріальної ерадикації і 28-денної смертності від будь-якої причини.
Ключові слова: карбапенем-резистентна Klebsiella pneumoniae, цефтазидим/авібактам, поліміксин В, мікробіологічний кліренс, 28-денна смертність.
У 1982 році Карл Фрідландер вперше описав Klebsiella pneumoniae, що відноситься до родини Enterobacteriaceae і повсюдно поширена у навколишньому середовищі, на поверхні рослин і слизових оболонок тварин. У людському організмі цю бактерію виявляють у шлунково-кишковому тракті та носоглотці. Вона може бути збудником багатьох внутрішньолікарняних інфекцій, зокрема пневмонії, інфекцій сечовивідних шляхів (ІСШ), а також інфекцій кровотоку в осіб зі зниженим імунітетом та у пацієнтів після певних медичних втручань (Zhang et al., 2014; Martin et Bachman, 2018). Гіпервірулентна K. pneumoniae (hvKP), окремий підтип бактерії, яку зазвичай виділяють у країнах Азіатсько-Тихоокеанського регіону, іноді викликає позагоспітальні та метастатичні інфекції у пацієнтів із нормальною функцією імунної системи і молодих, здорових осіб (Thomas et Russo, 2019). Наявність у пацієнтів зазначених інфекцій підвищує у них ризик виникнення абсцесів печінки, сепсису, пневмонії, некротизуючого фасціїту й менінгіту.
Окрім hvKP, протягом останніх 20 років у всьому світі стрімко підвищилась частота виділення CRKP. Загальносвітова кількість CRKP-інфекцій становить 60-90% від усіх CRE-інфекцій (інфекцій, викликаних карбапенем-резистентними ентеробактеріями), зареєстрованих у США, Європі та Китаї. Частота виділення CRKP особливо висока у Китаї: вона різко зросла із 2,9% у 2005 році до 25% у 2021 році (за даними Мережі епідеміологічного антимікробного нагляду Китаю). За результатами багатоцентрового дослідження, до якого було залучено 25 лікарень третинного рівня у 14 провінціях Китаю, встановлено, що K. pneumoniae спричинила захворювання у 73,9% із 664 випадків CRE-інфекцій (Zhang et al., 2018). Через обмеженість існуючих терапевтичних опцій показники смертності пацієнтів із CRKP-інфекціями також підвищились до 40-50%.
На CRKP діють лише деякі антибіотики. Традиційно найбільш ефективними терапевтичними схемами є комбінації поліміксинів із меропенемом, іміпенемом, цефтазидимом або тайгецикліном. Однак у зв’язку із тяжкими побічними ефектами, властивими поліміксинам, зокрема токсичним впливом на нирки та нервову систему, ці антибіотики показані лише як терапія останньої лінії.
У 2015 та 2016 роках Управління із санітарного нагляду за якістю харчових продуктів і медикаментів США (FDA) схвалило застосування цефтазидиму/авібактаму (CAZ/AVI) для лікування ускладнених інтраабдомінальних інфекцій (уІАІ), ускладнених інфекцій сечовивідних шляхів (уІСШ), госпітальних та вентилятор-асоційованих пневмоній (ГП/ВАП).
Комбінований препарат для внутрішньовенного введення CAZ/AVI містить цефалоспорин ІІІ покоління цефтазидим та синтетичний не-β-лактамний інгібітор β-лактамаз авібактам у сталому співвідношенні 4:1. Антибактеріальна дія цефтазидиму полягає здебільшого в інгібуванні перехресного зшивання пептидоглікану при синтезі клітинної стінки бактерій, що викликає клітинний лізис і загибель патогенів. Авібактам пригнічує ферменти бактерій класу A, C і β-лактамази деяких бактерій класу D (за Амблером), зокрема карбапенемазу K. pneumoniae, проте не інгібує ензими із групи метало-β-лактамаз (Zhanel et al., 2013).
Зростання частоти CRKP-інфекцій, високий рівень смертності від них і відсутність ефективних методів лікування є однією з найбільших сучасних проблем системи охорони здоров’я. Метою цього ретроспективного дослідження було оцінити ефективність терапевтичних схем, у яких основним препаратом був поліміксин B або CAZ/AVI, у пацієнтів із CRKP-інфекціями та визначити фактори ризику, що впливають на 7-денний мікробіологічний кліренс і 28-денну смертність.
Матеріали та методи дослідження
Автори провели багатоцентрове ретроспективне обсерваційне дослідження в лікарні Жуйцзінь (м. Шанхай, Китай), та Шанхайському дев’ятому народному госпіталі (м. Шанхай, Китай) із 8 січня 2018 року по 6 липня 2020 року. Критерії включення були такими: наявність у пацієнта культурально підтвердженої CRKP-інфекції та призначення йому поліміксину B або CAZ/AVI у формі монотерапії або комбінованої терапії. Критеріями виключення були: вік пацієнта <16 років та тривалість застосування антибіотика <24 год.
Пацієнтів із CRKP-інфекцією, що відповідали критеріям включення, розподілили у групу поліміксину В та групу CAZ/AVI відповідно до основного, призначеного їм антибіотика. CAZ/AVI вводили в дозі 2,5 г внутрішньовенно кожні 8 год, коригуючи дозу у пацієнтів зі зниженою функцією нирок. Поліміксин В вводили в дозі 1,25-1,5 мг/кг кожні 12 год після навантажувальної дози 2,0-2,5 мг/кг, відповідно до Настанов Міжнародного консенсусу щодо оптимального призначення поліміксинів.
Первинними результатами були показники смертності на 28-й день від початку досліджуваної інфекції, бактеріальної ерадикації та клінічного видужання. Крім того, дослідники проаналізували фактори ризику, що впливали на 7-денний мікробіологічний кліренс та 28-денну смертність пацієнтів із CRKP-інфекцією.
Результати
Порівняння ефективності поліміксину B і CAZ/AVI у пацієнтів із CRKP-інфекціями
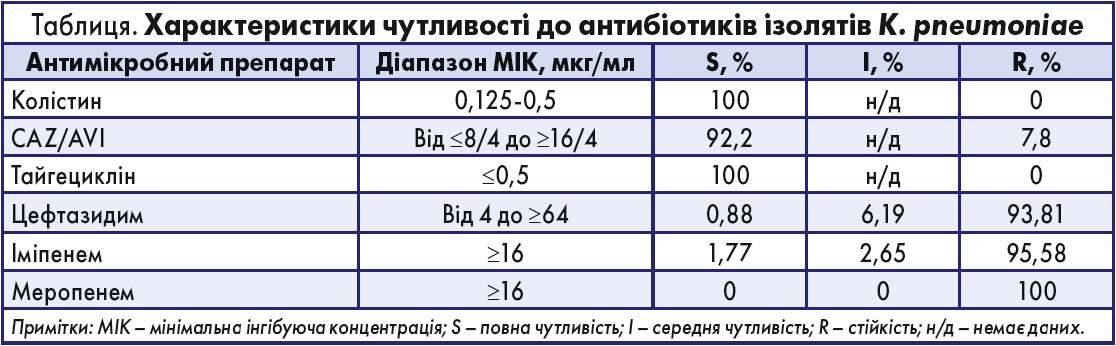
Протягом періоду дослідження вчені проаналізували дані 115 пацієнтів із CRKP-інфекціями, які відповідали критеріям включення й отримували поліміксин В (n=78, 67,8%) або CAZ/AVI (n=37, 32,2%). Характеристики чутливості до антибіотиків ізолятів K. pneumoniae представлені у таблиці. Майже всі ізоляти K. pneumoniae були стійкими до меропенему, іміпенему, цефтазидиму, проте чутливими до колістину, тайгецикліну і CAZ/ AVI. Вік пацієнтів становив від 51 до 72 років.
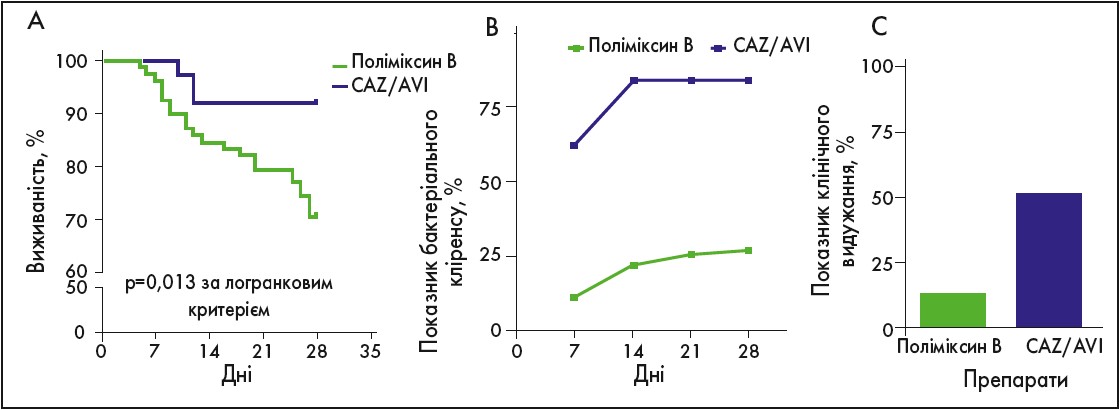
Рис. Порівняння ефективності поліміксину В та CAZ/AVI у пацієнтів із CRKP-інфекціями.
Порівняння кривих виживаності Каплана – Меєра (А), показників 28-денного бактеріального кліренсу (В) та показників клінічного видужання (С) у пацієнтів із CRKP-інфекціями, які отримували поліміксин В та CAZ/AVI
Показники 28-денної смертності у групах CAZ/AVI та поліміксину B становили 8,1 і 29,5% відповідно. За даними аналізу виживаності встановлено, що терапія поліміксином В була асоційована із вищим рівнем 28-денної смертності, ніж лікування CAZ/AVI (χ2=6,190, p=0,013) (рис. А).
При цьому 7-денний мікробіологічний кліренс зареєстровано у 62,2% пацієнтів із групи CAZ/AVI та у 11,5% пацієнтів із групи поліміксину В (р<0,001), тоді як 28-денний мікробіологічний кліренс відбувся у 83,8% осіб із групи CAZ/AVI та у 26,9% пацієнтів із групи поліміксину B (p<0,001) (рис. В). Показник клінічного видужання на 28-й день зареєстровано у 51,4 та 11,5% осіб із групи CAZ/AVI та поліміксину B відповідно (рис. С).
Фактори ризику, що впливають на 7-денний мікробіологічний кліренс у пацієнтів із CRKP-інфекцією
Показники мікробіологічного кліренсу на 7-й день становили 62,2% у групі CAZ/AVI і 11,5% у групі поліміксину В відповідно. Для визначення факторів ризику, що впливають на швидкість бактеріальної ерадикації, автори виконали однофакторний та багатофакторний аналізи, використавши дані всіх учасників дослідження. Усіх пацієнтів із CRKP-інфекціями розподілили на групу неналежного кліренсу та групу достатнього кліренсу, залежно від показників бактеріального кліренсу на 7-й день дослідження. Статистично значущі відмінності між групами були зумовлені вищим індексом коморбідності Чарльсона (≥3), попереднім застосуванням антибіотиків (впродовж 90 днів до початку дослідження) і схемою терапії, де основним антибіотиком був CAZ/AVI.
Фактори ризику, що впливають на 28-денну смертність від будь-якої причини у пацієнтів із CRKP-інфекцією
Для аналізу наведених показників автори використали дані 115 пацієнтів із CRKP-інфекцією. Цих пацієнтів класифікували на групу осіб, які вижили, і групу осіб, які не вижили, залежно від результатів лікування на 28-й день дослідження. Загальний показник 28-денної смертності у пацієнтів із CRKP-інфекціями становив 22,6% (26/115).
За результатами аналізу виявлено, що наступні фактори незалежно знижували 28-денну смертність від CRKP-інфекції: схеми терапії, де основним антибіотиком був CAZ/AVI, довша тривалість стаціонарного лікування після встановлення діагнозу CRKP-інфекції та вищий кліренс креатиніну (відношення шансів 0,989, p=0,23).
Обговорення
Факторами ризику, які сприяють виникненню CRKP-інфекції, є подовжена тривалість стаціонарного лікування, перебування у відділенні інтенсивної терапії (ВІТ), попереднє застосування антибіотиків, прийом карбапенемів (Liu et al., 2018).
На сьогодні кількість клінічних даних щодо порівняння ефективності поліміксинів та CAZ/AVI в осіб із CRKP-інфекціями недостатня.
Van Duin et al. проаналізували дані 137 пацієнтів із інфекціями, викликаними карбапенем-резистентними ентеробактеріями (CRE-інфекціями). Метою дослідження було порівняти показники ефективності терапевтичних схем, де основними препаратами були колістин і CAZ/AVI. Автори встановили, що показники 30-денної госпітальної смертності при застосуванні схем, де основними препаратами були CAZ/AVI і колістин, становили 9 і 32% відповідно (van Duin et al., 2018).
Результатами даного ретроспективного дослідження доведено, що застосування у пацієнтів із CRKP-інфекцією CAZ/AVI значно знижувало рівень 28-денної смертності, підвищувало показники 7-денного мікробіологічного кліренсу та 28-денного клінічного видужання порівняно з призначенням поліміксину В. Приблизно 74% пацієнтів, залучених до дослідження, отримували лікування в умовах ВІТ.
За даними цього дослідження встановлено, що CAZ/AVI був ефективнішим в осіб із CRKP-інфекціями, ніж інші рекомендовані до застосування препарати, зокрема схема «карбапенем плюс аміноглікозид», «карбапенем плюс колістин»; результати цього дослідження зіставні з результатами інших багатоцентрових ретроспективних когортних досліджень (Knaus et al., 1985; Krapp et al., 2017; Hu et al., 2018; Li et al., 2021; Lin et al., 2021).
Tsolaki et al. провели ретроспективне обсерваційне дослідження за участю 77 пацієнтів із CRE-інфекціями, які перебували на штучній вентиляції легень у ВІТ, щоб оцінити результати лікування, мікробіологічні показники та профілі безпеки призначених препаратів. Автори довели, що схема, яка містила CAZ/AVI, була ефективнішою, ніж інші антибіотики, рекомендовані при CRE-інфекції, оскільки її застосування підвищувало показники виживаності, бактеріальної ерадикації та клінічного видужання (Tsolaki et al., 2020).
Висновки
За результатами дослідження встановлено, що при лікуванні CRKP-інфекцій більш ефективним було застосування CAZ/AVI, ніж призначення поліміксину B, особливо в осіб у дуже тяжкому стані. Індекс коморбідності Чарльсона (≥3) і попереднє застосування антибіотиків (впродовж 90 днів до початку дослідження) були незалежними факторами ризику, що сприяли неналежній бактеріальній ерадикації. У пацієнтів, які отримували терапевтичні схеми, де основним препаратом був CAZ/AVI, бактеріальний кліренс реєстрували швидше. До того ж більшість із них мали вищу виживаність, ніж пацієнти із групи поліміксину В. Факторами, що знижували 28-денну смертність, були довша тривалість стаціонарного лікування із приводу CRKP-інфекції й вищий вихідний кліренс креатиніну. Для визначення найбільш ефективних схем терапії CRE-інфекцій із застосуванням CAZ/AVI потрібні подальші масштабні клінічні випробування.
Підготувала Анна Сакалош
За матеріалами: Fang J. еt al. Efficacy of Ceftazidime-Avibactam Versus Polymyxin B and Risk Factors Affecting Clinical Outcomes in Patients With Carbapenem-Resistant Klebsiella pneumoniae Infections a Retrospective Study. Front Pharmacol. 2021 Dec 10;12:780940. doi: 10.3389/fphar.2021.780940. PMID: 34955849; PMCID: PMC8703033.
Надруковано за підтримки Представництва
«Пфайзер Експорт Бі. Ві.».
PP-ZVA-UKR-0054