5 травня, 2022
Первинна профілактика та лікування венозних тромбоемболічних ускладнень в умовах сьогодення
За матеріалами конференції
У статті представлено сучасні принципи лікування й профілактики венозних тромбоемболічних ускладнень (ВТЕУ), а також особливості терапії пацієнтів із ВТЕУ та коронавірусною хворобою. Розглянуто проблему ведення хворих із ВТЕУ у разі судинних втручань, зокрема критерії підбору оптимальної тромбопрофілактики.
Ключові слова: венозні тромбоемболічні ускладнення, венозна тромбоемболія, низькомолекулярний гепарин, тромбоз глибоких вен, тромбоемболія легеневої артерії, еноксапарин.
На конференції «Сухаревські читання: судинна хірургія, флебологія та ангіологія в епоху COVID‑19», яка відбулась 9-10 вересня минулого року, тему венозних тромбоемболічних ускладнень представили декілька доповідачів. Відкрила секцію і модерувала її віце-президент Асоціації судинних хірургів, флебологів та ангіологів України, головний науковий співробітник відділу магістральних судин ДУ «Національний інститут хірургії та трансплантології ім. О.О. Шалімова НАМН України» (м. Київ), доктор медичних наук, професор Лариса Михайлівна Чернуха.
Професор Л.М. Чернуха навела численні міжнародні настанови, згідно з якими препарати для лікування венозної тромбоемболії (ВТЕ) обирають на підставі віку пацієнта, наявності в нього факторів ризику та протипоказань. Доповідач наголосила на важливості первинної тромбопрофілактики ВТЕ у пацієнтів, госпіталізованих із гострим COVID‑19 або будь-яким іншим гострим захворюванням та супутніми факторами ризику виникнення ВТЕ (Bikdeli B. et al., 2020). За сучасних умов для тромбопрофілактики ВТЕ найчастіше застосовують низькомолекулярний гепарин (НМГ). В осіб, госпіталізованих із гострим перебігом COVID‑19, НМГ або фондапаринукс мають перевагу над нефракціонованим гепарином (CHEST Guideline and Expert Panel Report, 2020).
Продовжив висвітлення теми завідувач кафедри загальної хірургії Івано-Франківського національного медичного університету, доктор медичних наук, професор Іван Михайлович Ґудз. Він наголосив на недооціненості проблеми ВТЕ у хірургічній практиці. Так, за даними дослідження ENDORSE, більшість (64,4%) хірургічних пацієнтів мають підвищений ризик ВТЕ, однак лише 58,8% таких хворих отримують належну профілактику. Доповідач навів парадоксальний факт: судинні хірургічні втручання посідають друге місце за ризиком виникнення ВТЕ серед усіх операційних втручань (Smilowitz N.R. et al., 2017), притому що саме судинна хірургія спрямована на лікування тромбозів та емболій. За результатами дослідження TREVO, у якому оцінювали частоту післяопераційних ВТЕ, загальна летальність від них становила 21,1%.
Він наголосив на недооціненості проблеми ВТЕ у хірургічній практиці. Так, за даними дослідження ENDORSE, більшість (64,4%) хірургічних пацієнтів мають підвищений ризик ВТЕ, однак лише 58,8% таких хворих отримують належну профілактику. Доповідач навів парадоксальний факт: судинні хірургічні втручання посідають друге місце за ризиком виникнення ВТЕ серед усіх операційних втручань (Smilowitz N.R. et al., 2017), притому що саме судинна хірургія спрямована на лікування тромбозів та емболій. За результатами дослідження TREVO, у якому оцінювали частоту післяопераційних ВТЕ, загальна летальність від них становила 21,1%.
До факторів ризику ВТЕ, що пов’язані з хірургічним втручанням, відносяться:
- обсяг і тривалість хірургічного втручання;
- інатраопераційне положення на операційному столі;
- тип анестезії;
- післяопераційна іммобілізація.
Встановлено, що подовження тривалості операційного втручання у 2 рази підвищує ризик виникнення ВТЕ також удвічі (Kim J.Y.S. et al., 2015). Крім того, ймовірність ВТЕ підвищує застосування спінальної анестезії (Nakamura M. et al., 2017).
Слід враховувати й фактори ризику ВТЕ, пов’язані з особливостями пацієнта:
- вік >60 років;
- ожиріння;
- ВТЕ в анамнезі;
- злоякісні новоутворення;
- вагітність;
- замісна терапія естрогенами;
- запальні захворювання кишечника;
- спадкові тромбофілічні стани.
Вік є першочерговим фактором, що впливає на виникнення ВТЕ. Доповідач представив діаграму, відповідно до якої у госпіталізованих осіб віком 60-89 років частота тромбоемболії легеневої артерії (ТЕЛА) була приблизно вдвічі вищою, ніж у молодших пацієнтів (Stein P.D. et al., 1999; Vaitkus P. L. et al., 2005).
Іншим вагомим чинником, що сприяє виникненню ВТЕ, є наявність у пацієнта ожиріння. Відносний ризик виникнення неспровокованої ТЕЛА, не пов’язаний із попереднім хірургічним втручанням, травмою або раком, збільшувався приблизно на 8% із підвищенням ІМТ на 1 кг/м2. В осіб із ІМТ ≥35 кг/м2 цей ризик був майже шестикратним (Al Otaib N. et al., 2017).
ВТЕ виникає під впливом багатьох чинників. Зокрема, було порівняно відносний ризик ВТЕ в осіб із факторами ризику й у представників загальної популяції (Scheres L.J.J. et al., 2018). Відповідно до отриманих результатів, ризик ВТЕ був суттєво вищим в осіб, які перенесли хірургічне втручання, мали активне злоякісне чи хронічне запальне захворювання, наприклад хронічну хворобу нирок, ВІЛ-інфекцію, хворобу, що супроводжувалася гіпертиреозом, запальне захворювання кишечника, системний червоний вовчак.
У госпіталізованих пацієнтів щонайменше кожні 48 год оцінюють ризик виникнення ВТЕ. Для цього переважно використовують перший варіант шкали Caprini. Професор І.М. Ґудз зауважив, що краще застосовувати модифіковану версію шкали (2013), адже в ній враховані додаткові фактори ризику, який визначають за загальною сумою балів:
- 0 балів – дуже низький,
- 1-2 бали – низький,
- 3-4 бали – помірний,
- 5 балів – високий.
Одночасно із ймовірністю появи ВТЕ обов’язково визначають ризик кровотечі за шкалою HAS-BLED.
На думку доповідача, сьогодні лікарі недооцінюють важливість тромбопрофілактики, зокрема у післяопераційному періоді. Між тим рутинна тромбопрофілактика знижує частоту захворюваності й смертності та витрати на медичне обслуговування у госпіталізованих осіб із ризиком виникнення тромбозу глибоких вен (ТГВ) і ТЕЛА.
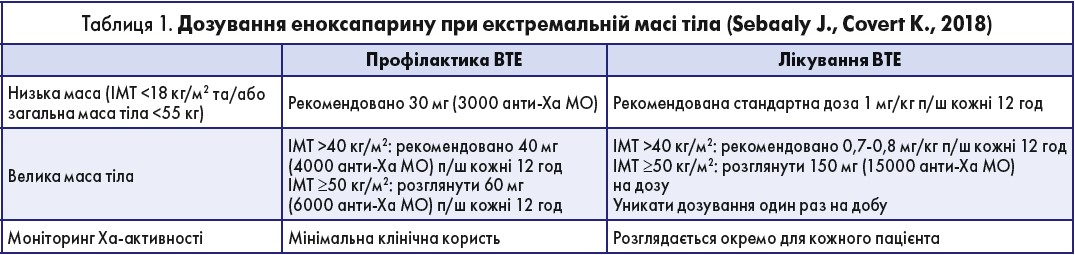
Доза еноксапарину, який застосовують для тромбопрофілактики, залежить від маси тіла пацієнта. Дозування пацієнтам із стандартною масою тіла призначають відповідно до інструкції для медичного застосування препарату. Дози в осіб із екстремально високою або низькою масою розраховуються виходячи з додаткових рекомендацій (табл. 1).
Доза низькомолекулярного гепарину має бути подвоєна, якщо оцінка стану пацієнта за шкалою Caprini становить >8 балів (комбінація віку та ІМТ >35 кг/м2, серцева недостатність, підвищений рівень D-димеру, ВТЕ в особистому або сімейному анамнезі) (Marston W. et al., 2020).
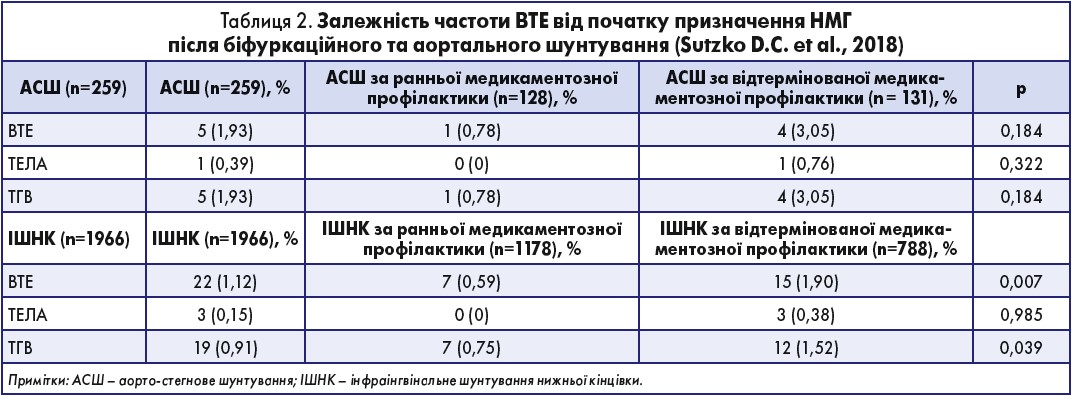
Доповідач зауважив, що дуже важливим є час початку тромбопрофілактики, оскільки відтермінований початок застосування НМГ пов’язаний із високим ризиком виникнення у пацієнта емболій (табл. 2).
Як вказано у таблиці, в осіб, які підлягали аорто-стегновому шунтуванню й пізно отримали НМГ, ризик ВТЕ та ТГВ зростав у чотири рази, на відміну від пацієнтів, яким НМГ було призначено вчасно. В осіб, які перенесли інфраінгвінальне шунтування нижньої кінцівки й отримали відтерміновану профілактику НМГ, частота ВТЕ була вдвічі вищою, ніж у пацієнтів, що отримали її вчасно. Також в умовах відтермінованої профілактики зареєстровано вищу частоту ТГВ (приблизно у 1,5 раза) і три випадки ТЕЛА (в осіб, яким вчасно ввели НМГ, не було виявлено легеневих емболій).
Тромбопрофілактику призначають на час стаціонарного лікування, а можливість її наступного продовження визначають індивідуально. Важливо, що ризик виникнення у пацієнта ВТЕ оцінюють на двох етапах:
- на стаціонарному етапі (хірургічне втручання + фактори ризику пацієнта);
- після виписки зі стаціонару (фактори ризику пацієнта).
Якщо на момент виписки у пацієнта відзначаються >8 балів за шкалою Caprini (ІМТ >35 кг/м2, підвищений рівень D-димеру, ВТЕ в особистому або сімейному анамнезі, обмежена рухливість), йому показана подальша тромбопрофілактика (Marston W. et al., 2020).
Клінічний випадок
Пацієнт, 56 років, підлягав біфуркаційному аорто-стегновому шунтуванню із приводу сухого некрозу другого пальця правої нижньої кінцівки та хронічної артеріальної недостатності (IIb) лівої нижньої кінцівки. У пацієнта був виявлений безсимптомний COVID‑19 (експрес-тест, підтверджений методом імуноферментного аналізу).
Доповідач наголосив на важливості проведення у цій ситуації тромбопрофілактики, оскільки втручання на аорті й клубових артеріях призводять до ТГВ практично в кожного п’ятого пацієнта (у випадку периферичної реконструкції – у кожного сьомого пацієнта). До того ж наявність у даного пацієнта коронавірусного захворювання, навіть без клінічних ознак, змушувала враховувати додатковий ризик тромбозу.
З урахуванням усіх факторів ризику, зокрема наявності у пацієнта ожиріння й тривалого тютюнопаління в анамнезі, його оцінка за модифікованою шкалою Caprini склала 6 балів. Додавши 2 бали за наявність асимптомної коронавірусної хвороби, лікарі отримали 8 балів, що означало дуже високий ризик виникнення тромбоемболії. Оскільки пацієнт мав обмежену функціональну активність і приймав ацетилсаліцилову кислоту, він також мав високий ризик виникнення кровотечі за шкалою HAS-BLED.
Доза препарату для тромбопрофілактики була розрахована на підставі інструкції для медичного застосування та наявного у хворого ожиріння (ІМТ – 40 кг/ м2). Пацієнту було призначено еноксапарин у дозі 0,4 мл двічі на добу. На момент лікування у нього було виявлено втричі вищий за норму рівень D-димеру, який залишався високим на етапі виписки, тому пацієнту було продовжено тромбопрофілактику амбулаторно.
У наступній сесії доповідав доцент кафедри хірургії з курсом невідкладної та судинної хірургії Національного медичного університету ім. О.О. Богомольця (м. Київ), кандидат медичних наук Денис Сергійович Миргородський. Він присвятив свою доповідь особливостям лікування тромбозу глибоких вен в умовах пандемії COVID‑19.
Тромболітична терапія є дієвим методом лікування не лише ішемічного інсульту, гострого коронарного синдрому, ТЕЛА, а й ТГВ (Maekawa K. et al., 2019). Так, отримано багато даних про ефективність тромболітичної терапії, призначеної на ранніх стадіях тромбозу (Goldhaber S.Z. et al., 2017). Натомість доцільність застосування фібринолітиків на пізніх стадіях гострих венозних тромбозів є дискутабельною (Sillesen H.H. et al., 2015).
Доповідач представив результати дослідження, проведеного на кафедрі хірургії з курсом невідкладної та судинної хірургії НМУ у 2021 році. Метою випробування була оцінка ефективності терапії ТГВ на фоні пандемії COVID‑19. У дослідженні взяли участь 87 пацієнтів, яких було розподілено на дві групи: основну і контрольну. До основної групи увійшли 35 осіб із COVID‑19, госпіталізованих до загальнопрофільних відділень і відділення інтенсивної терапії; до групи контролю – 52 пацієнти із тромбозами, які не мали коронавірусної інфекції та онкологічних захворювань.
Період дослідження становив 14 діб. Протягом 1-7-ї доби були вивчені показники 23 пацієнтів з основної групи та 28 – із групи контролю. Впродовж 8-14-ї доби спостереження велося за 12 учасниками основної групи і 24 пацієнтами із контрольної групи.
Пацієнтам основної групи призначали тромболітик і Клексан® або тільки Клексан® (діюча речовина – еноксапарин), натомість учасники групи контролю спершу отримували тромболітичну терапію, а потім – Клексан®.
Таким чином, основна група отримувала:
- терапію від COVID‑19 за відповідним протоколом;
- тромболітичну терапію тканинним активатором плазміногена (tPA) внутрішньовенно болюсно в дозі 10 мг та крапельно в дозі 1 мг/кг, але загалом не більше 100 мг, за наявності проксимального тромбозу;
- пацієнти з дистальними формами ураження й після тромболізису отримували прямі антикоагулянти – Клексан® 300 підшкірно у дозі 100 анти-Ха МО/кг 2 рази на добу кожні 12 год із контролем активованого часткового тромбопластинового часу (АЧТЧ) протягом 14 діб;
- компресійну терапію;
- лімфовенотоніки;
- знеболювальні та протизапальні препарати.
Група контролю отримувала:
- тромболітичну терапію tPA внутрішньовенно болюсно в дозі 10 мг та крапельно в дозі 1 мг/кг, але загалом не більше 100 мг.
- Після тромболітичної терапії учасникам групи було призначено:
- прямі антикоагулянти – Клексан® 300 підшкірно у дозі 100 анти-Ха МО/кг 2 рази на добу кожні 12 год із контролем АЧТЧ із подальшим призначенням непрямих антикоагулянтів за схемою протягом 14 діб;
- компресійну терапію;
- лімфовенотоніки;
- знеболювальні та протизапальні препарати.
Ефективність лікування визначалася за такими критеріями:
- динаміка клінічних симптомів (больового синдрому);
- реканалізація тромбозу за даними УЗД або флебографії (повна, часткова, відсутня).
Вихідні характеристики пацієнтів відрізнялися за віком, і ця різниця була статистично значущою (p=0,003). В основній групі середній вік пацієнтів становив 64 роки, а учасники групи контролю були приблизно на 10 років молодші. У групах не було виявлено статистично значущих відмінностей за статтю, однак слід відзначити, що в основній групі переважали чоловіки.
В обох групах були представлені всі стадії хронічної венозної недостатності за класифікацією CEAP без статистично достовірних відмінностей. При цьому в основній групі переважали особи зі стадіями С0 і С1 (34% проти 18% у групі контролю). До того ж в основній групі переважали пацієнти з дистальною формою ураження, тобто тромбозами гомілково-підколінного сегмента (48,6%), натомість як у контрольній групі реєстрували зазвичай проксимальні тромбози, локалізовані у підколінно-стегновому (40,4%) і стегново-здухвинному (36,5%) сегментах. У більшості досліджуваних на момент госпіталізації біль (визначений за шкалою Numerical Rating Scale) був помірним або сильним. Виражений нестерпний біль реєстрували лише у 17-20% пацієнтів.
Після тромболітичної терапії було відзначено поступове зменшення інтенсивності болю (приблизно на 4 бали за 5 діб). Темпи полегшення болю були найвищими протягом перших двох діб. У групі контролю біль зменшувався повільніше, ніж у групі пацієнтів із COVID‑19. Якщо зіставити показники зменшення болю під впливом тромболітиків і препарату Клексан®, то протягом перших 3 діб у хворих після тромболітичної терапії больовий синдром усувався ефективніше. Згодом у хворих обох груп інтенсивність болю дієво зменшувалась.
За показником реканалізації між групами не виявлено статистично значущої різниці. Однак в основній групі відзначалося менше осіб із повною реканалізацією, ніж у групі контролю. Порівнюючи ступінь реканалізації при застосуванні тромболітика, дослідники не виявили статистично значущої різниці між результатами груп. Повну реканалізацію було виявлено у 37,5% пацієнтів з основної групи й у 32,7% – із контрольної. Часткову реканалізацію було зареєстровано у 25% пацієнтів з основної групи й у 51,9% – із контрольної. Варто зазначити, що в основній групі виявлено більшу кількість осіб, у яких не відбулося реканалізації (37,5% проти 16,4% пацієнтів із групи контролю).
У підсумку спікер зауважив, що важливе значення для лікування й профілактики ВТЕУ в умовах стаціонару має еластична компресія нижніх кінцівок. Зокрема, застосування спеціальних гольфів і панчіх із градуйованою компресією є ефективнішим, ніж бинтування кінцівок еластичним бинтом.
Таким чином, своєчасна тромбопрофілактика дозволяє значно зменшити ризик тромбоемболічних ускладнень і покращити прогноз для пацієнтів, зокрема у разі судинних втручань.
Підготувала Анна Сакалош