14 грудня, 2021
Інгібіція протеолізу як напрям профілактики та терапії гострої респіраторної вірусної інфекції
 Респіраторні вірусні інфекції є наймасовішими захворюваннями, що посідають провідне місце в структурі інфекційних хвороб. Так, вірус грипу А – один з найпоширеніших інфекційних збудників, пов’язаний зі значною захворюваністю та смертністю [18]. Широке розповсюдження і високу інтенсивність епідемічного процесу при вірусних інфекціях зумовлює надзвичайна активність механізму передачі.
Респіраторні вірусні інфекції є наймасовішими захворюваннями, що посідають провідне місце в структурі інфекційних хвороб. Так, вірус грипу А – один з найпоширеніших інфекційних збудників, пов’язаний зі значною захворюваністю та смертністю [18]. Широке розповсюдження і високу інтенсивність епідемічного процесу при вірусних інфекціях зумовлює надзвичайна активність механізму передачі.
Останнім часом значна увага приділяється ролі протеолізу як особливої форми біологічного контролю [2]. Відомо, що обмежений протеоліз є пусковим та/або ключовим патогенетичним механізмом багатьох фізіологічних і патологічних процесів (згортання крові, апоптозу, активації низки гормонів, попередження агрегації білкових молекул тощо) й забезпечує швидку відповідь організму на мінливі умови чи сигнали [7].
Доведено, що протеолітичні реакції мають важливу роль у взаємодії між вірусом і клітиною-хазяїном [24]. Протеази мають вирішальне значення для реплікації вірусу, оскільки вони розщеплюють вірусні поліпептиди-попередники (як структурні, так і функціональні білки), сприяючи розвитку вірусу в інфікованій клітині-хазяїні [16]. Саме протеолітична активація зумовлює інфекційну активність вірусу та здатність його до генералізації інфекції, тому властивості вірусу уражати певні тканини організму визначаються наявністю в органах і тканинах ферментів, необхідних для протеолітичної активації вірусного потомства.
Встановлено, що протеолітична активація поширена серед вірусів і при вірусній інфекції є високоспецифічним процесом, який здійснюється певними протеазами клітинного чи вірусного походження, при цьому в деяких вірусів розщеплення білка-попередника є основним механізмом, що зумовлює утворення функціональних білків, а в більшості інших це стосується переважно вірусних глікопротеїнів, котрі здійснюють функції адсорбції та злиття.
Поверхневий глікопротеїн вірусу грипу гемаглютинін (ГA) опосередковує перший важливий етап у життєвому циклі вірусу – його проникнення до клітин-мішеней. Зараження вірусом грипу ініціюється ГА через зв’язування з рецепторами, а також злиттям вірусної та ендосомальної мембран [18].
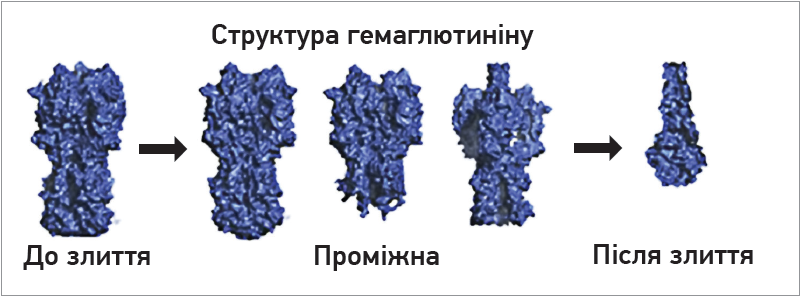
ГА синтезується як білок-попередник та потребує розщеплення протеазами клітини-хазяїна для переходу в активну форму, щоб отримати здатність до злиття (рис. 1). Інфекційність вірус грипу здобуває після протеолітичного розрізання ГА (молекулярна маса 75 кДа) на 2 фрагменти ГА1 (55 кДа) і ГА2 (20 кДа), які зберігають сульфідний зв’язок. В субодиниці ГА2 вивільняється N‑кінцевий пептид (пептид злиття). Цей пептид робить пори в клітинних ліпідних мембранах для проникнення вірусу до клітини-мішені, обумовлюючи вивільнення вірусної РНК та ініціацію інфекційного процесу [12].
Рис. 1. Зміни структури гемаглютиніну при підготовці до злиття [12]
Протягом тривалого часу було мало відомо про протеази в дихальних шляхах людини [8], які мають вирішальне значення щодо інфекційності вірусу грипу. Доведено, що протеолітичну активацію вірусів грипу та параміксовірусів здійснюють трипсиноподібні протеази клітини, котрі гідролізують пептидний зв’язок між аргініном і лізином. Хімотрипсин і гемолізин розщеплюють білок-попередник зі зсувом на 3 та 1 амінокислоту відповідно.
Цікаво, що деякі бактерії підтримують активацію ГА шляхом секреції протеаз, які розщеплюють ГА, або завдяки активації клітинних протеаз, отже, вони можуть сприяти поширенню вірусу та посиленню його патогенності [13].
Загалом ГА забезпечує одразу декілька процесів, що дозволяють вірусу потрапити до клітини-господаря: приєднання до молекули сіалової кислоти мембрани епітеліоциту; злиття мембран; ендоцитоз вірусу; злиття оболонки вірусу з оболонкою ендосоми. Ці процеси відбуваються завдяки дії трансмембранних серинових протеаз II типу (TMPRSS2, TMPRSS4, HAT), локалізованих в епітелії верхніх дихальних шляхів. Отже, протеолітичне розщеплення ГА має важливе значення для інфекційності вірусу грипу, а протеази, що здійснюють це розщеплення, є привабливими мішенями для терапевтичного втручання [11].
Також велике значення має підготовка поверхні епітеліоциту для того, аби вірус міг приєднатися [9]. Цей процес продовжується протеазами і всередині клітини, які створюють необхідні умови для реплікації, збірки та вивільнення вірусу із клітини. В умовах активації протеолізу деградувати можуть й інші білки, що виконують функцію захисту (інтерферони тощо), порушуючи так процес противірусного захисту.
Ще під час епідемії коронавірусу тяжкого гострого респіраторного синдрому (SARS-CoV) було продемонстровано, що проникнення вірусу потребує ендосомальної протеази катепсину L; також виявлено, що інфікування SARS-CoV може бути суттєво індуковано при застосуванні трипсину [10].
Встановлено, що у вірусів грипу та COVID‑19 схожі механізми протеолітичної активації на етапі проникнення вірусу до клітини-господаря. Глікопротеїн гемаглютиніну вірусу грипу зазнає протеолізу під час упаковки вірусу; спайковий білок коронавірусу (S) також зазнає протеолізу після зв’язування з рецепторами клітини-господаря [25].
Вірус SARS-CoV‑2 проникає до клітини-хазяїна шляхом прямого злиття оболонки вірусу з мембраною клітини-хазяїна чи злиття мембрани всередині ендосоми після ендоцитозу [10].
Білок S коронавірусу має ключову роль на ранніх етапах вірусної інфекції, при цьому домен S1 відповідає за зв’язування з рецептором, а домен S2 опосередковує злиття мембрани [10].
Проходження вірусу ініціюється зв’язуванням рецептор-зв’язувального домену білка S із рецепторами клітини-хазяїна людини на поверхні клітини. Одним з основних рецепторів для SARS-CoV‑2 є ангіотензинперетворювальний фермент‑2 (ACE2), який широко експресується в клітинах легень, кишечнику, печінки, серця, ендотелію судин, яєчок і нирок (рис. 2).
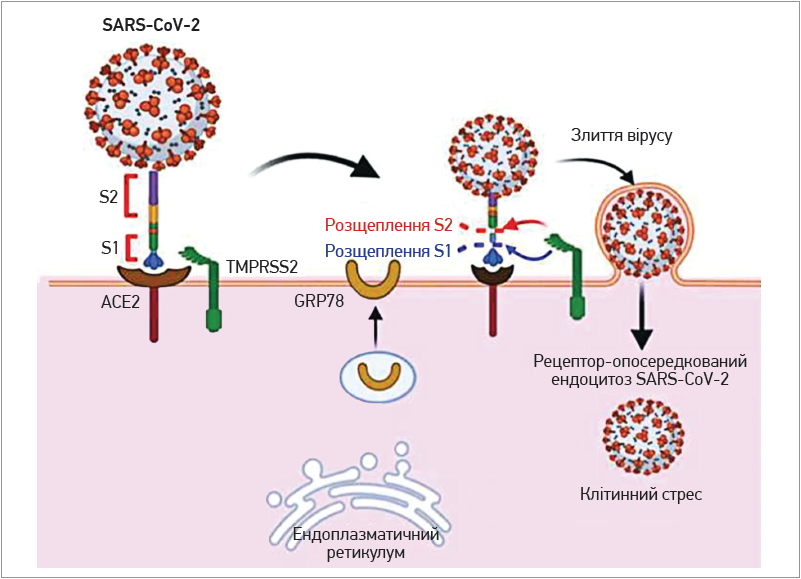
Рис. 2. Протеоліз і проникнення вірусу SARS-CoV-2 до клітини [15]
S‑глікопротеїн SARS-CoV‑2 зв’язується з рецепторами клітини-хазяїна (ACE2, TMPRSS2 і GRP78), знайденими в епітеліальних клітинах легень людини, щоб полегшити механізм проникнення вірусу. Ці рецептори клітини-господаря експресуються в різних тканинах, включаючи клітини легень людини, нирки та шлунково-кишковий тракт. Взаємодія зв’язування ACE2 з ділянкою рецептор-зв’язувального домену білка S є визначальним фактором для проникнення вірусу до клітини-хазяїна. Розщеплення білка S протеазами клітини-хазяїна також необхідне для подальшого злиття вірусної та клітинної мембрани. Після проникнення вірусу до клітини-хазяїна через ендоцитоз, опосередкований рецептором, стан клітинного стресу спричиняє експорт GRP78 для подальшої активації та взаємодії вірусу із клітиною-хазяїном. Вірусна інфекція не обмежується епітеліальними клітинами легень людини, оскільки ACE2 експресується в різних тканинах, включаючи нирки, серце, печінку, сітківку й ентероцити кишечнику та інших тканин всього тіла. Це свідчить про можливу тропність вірусу до різних тканин.
Після взаємодії рецептор-зв’язувального домену білок S зазнає протеолітичного розщеплення, яке каталізується декількома протеазами хазяїна, як-от фурин, TMPRSS2 і катепсин B/L. Білок S протеолітично розщеплюється на кордоні S1-S2 [10]. Аналіз послідовності геному SARS-CoV‑2 виявив наявність вставки на кордоні S1/S2 із 12 нуклеотидів або 4 амінокислот, пролін-аргінін-аргінін-аланін (PRRA), який є консенсусним сайтом розщеплення фурину (рис. 3). Фурин – одна з основних протеаз, що використовуються SARS-CoV‑2 для праймування білка S [23]. Фурин як трансмембранний білок I типу належить до сімейства міжклітинних Ca2+-залежних серинових ендопептидаз; він також відомий як пропротеїнова конвертаза. Фурин експресується в різних органах і тканинах людини, включаючи легені, шлунково-кишковий тракт, центральну нервову систему та репродуктивні тканини.
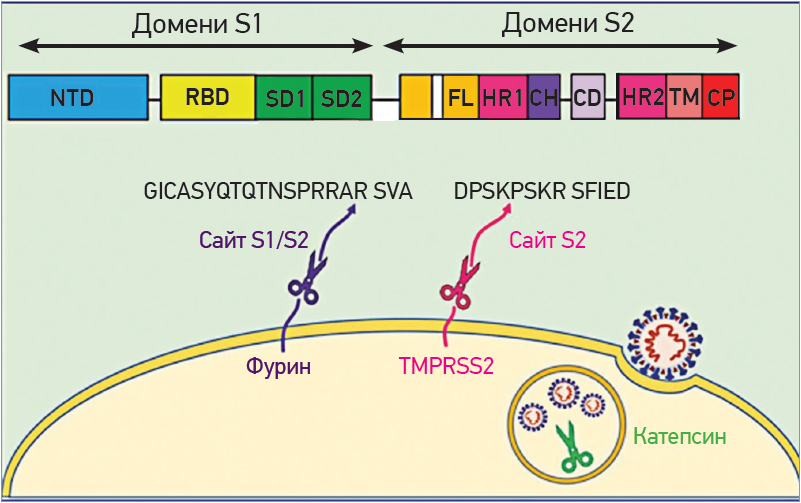
Рис. 3. Протеази забезпечують злиття та проникнення SARS-CoV-2 до клітини
Примітки: різні домени білка SARS-CoV-2 S (зліва направо): N-кінцевий домен NTD; домен, що зв’язує рецептор RBD;
субдомени SD1 і SD2; петля злиття FL; повтор 1 гептади HR1; центральна спіраль CH; домен з’єднувача CD;
повтор 2 гептади HR2; трансмембранна ділянка TM; цитоплазматичний хвостовий домен CP.
Важливо, що злитий пептид білка S коронавірусу розташований нижче за N‑кінець домену стебла S2. Отже, після зв’язування з рецепторами хазяїна білок S SARS-CoV‑2 має зазнати конформаційного переходу, щоб відкрити внутрішній злитий пептид. Після цього відкритий злитий пептид сприяє злиттю цитоплазматичної або ендосомальної мембрани, що зумовлює кінцеве досягнення проникнення вірусу та вивільнення вірусної РНК у цитоплазму клітин-господарів. У цитоплазмі вірусна РНК використовує клітину-господаря та власний механізм для реплікації свого генетичного матеріалу й збирання нових вірусних частинок [25].
Пропротеїноконвертази (наприклад, фурин), протеази клітинної поверхні (як-от TMPRSS2), а також лізосомальні протеази (наприклад, катепсин) беруть участь у протеолізі білка S SARS-CoV‑2. Фурин розщеплює багатоосновний сайт (PRRA) на кордоні S1/S2, щоб відокремити S1 від домену S2. Згодом TMPRSS2 розщеплює сайт S2’ для подальшого експонування внутрішнього злиття пептиду для злиття мембрани. Катепсини, переважно локалізовані в лізосомі, індукують протеоліз після ендоцитозу віріонів для злиття вірусної оболонки з ендосомальними мембранами.
Отже, при інфекції COVID‑19 протеолітична обробка активує білок S і забезпечує злиття мембрани вірусу з мембраною клітини-господаря з подальшим вивільненням вірусної РНК до цитоплазми господаря. Лізосомальні протеази (катепсин) після ендоцитозу вірусних частинок (у разі проникнення вірусу до клітини за ендоцитозним типом) сприяють формуванню автофагосоми; пропротеїнові конвертази (фурин) дозволяють знову складати вірус (тобто утворюються нові віріони), позаклітинні протеази (еластаза) сприяють виходу вірусу із клітини.
Пандемічна ситуація з новою коронавірусною інфекцією COVID‑19 (COronaVIrus Disease 2019) потребує не лише вакцинації для запобігання поширенню захворювання, а й розробки нових ліків, спрямованих на зниження вірусного навантаження, пригнічення надлишкової імунної відповіді, запобігання розвитку тяжких ускладнень, як-от гострий респіраторний дистрес-синдром [6].
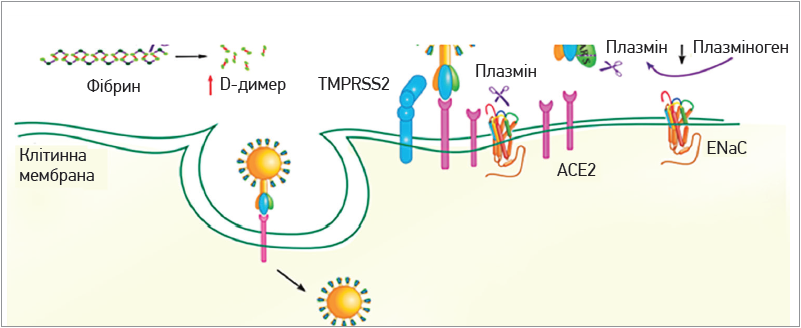
Система активаторів плазміногена є однією з перспективних мішеней для вивчення механізмів розвитку пневмонії, системного запалення та синдрому дисемінованого внутрішньосудинного згортання при COVID‑19 [6]. Один з основних активаторів плазміногена – серинова протеаза урокіназа. Протеолітично активний плазмін розщеплює надлишок фібрину з утворенням високих концентрацій D‑димеру, що спричиняє зміну фібринолітичних властивостей крові. Крім того, плазмін також протеолізує субодиницю епітеліального натрієвого каналу (ENaC), розташовану на апікальній поверхні мембран епітеліальних клітин легень та нирок. Це збільшує здатність іонів Na проникати до епітеліальних клітин і зумовлює порушення водно-сольового обміну в тканинах [6] (рис. 4).
Рис. 4. Протеоліз і активація гемостазу при COVID-19 [6]
Останні дослідження дозволили визначати значення протеолітичної активації в інфекційному процесі, що стало передумовами використання її як мішені з метою лікування вірусної інфекції. Оскільки за допомогою протеолітичного розщеплення модулюється активність білка та підвищується ефективність реплікації вірусу, вплив на протеази є важливою складовою терапевтичної стратегії [20]. При порушенні протеолітичної активації відбуватиметься складання вірусних частинок, однак віріони, що утворюються, будуть неінфекційними, оскільки в їхньому складі будуть відсутні активні білки злиття, котрі забезпечують проникнення вірусу до здорових клітин.
Установлено, що застосування при SARS комбінації лопінавіру з ритонавіром разом із рибавірином асоціювалося зі значним зниженням несприятливих результатів (гострий респіраторний дистрес-синдром і летальність) порівняно лише з монотерапією рибавірином (2,4 проти 28,8%) [14].
Вважається, що вплив на ACE2, GRP78 і TMPRSS2 має потенційно високе терапевтичне значення. Важливо пригнічувати механізм проникнення, унеможливлюючи процес злиття, ніж блокувати подальшу протеолітичну активацію вірусу [15]. Продемонстровано роль пригнічення активності 3CL- протеази [17].
Нещодавно розпочато клінічне випробування I фази з оцінкою засобу, що пригнічує протеази SARSCoV‑2 і порушує здатність вірусу до самовідтворення; його призначено як фармакологічний засіб для запобігання розвитку COVID‑19 у людей, які зазнали впливу збудника. Препарат зворотно реагує із залишком цистеїну, розташованим у місці зв’язування [21, 22].
Активація глікопротеїну гемаглютиніну вірусу грипу шляхом розщеплення протеазами клітини-господаря має важливе значення для вірусної інфекційності, що свідчить про протеоліз гемаглютиніну як мішень до лікування грипу. Цим можна пояснити те, що інгібітори протеолізу озельтамівір, занамівір, апротинін, амінокапронова кислота використовуються при грипі.
Ще у 80-х роках минулого століття при лікуванні респіраторних вірусних інфекцій та для їхньої профілактики активно почали застосовувати амінокапронову кислоту, яка є добре відомим інгібітором фібринолізу. За результатами експериментальних і клінічних досліджень продемонстровано активність щодо вірусних інфекцій, але її механізм впливу на той час не був достатньо зрозумілим. Пізніше було встановлено, що амінокапронова кислота блокує проникнення вірусу до клітин носоглотки та бронхолегеневої системи на ранніх етапах взаємодії вірусу із чутливими клітинами. Це дозволило дійти висновку, що в період епідемічного підйому захворюваності на ГРВІ для екстреної профілактики доцільним є одночасне призначення амінокапронової кислоти в інтраназальній та пероральній формах [4, 5, 19].
Здатність амінокапронової кислоти інгібувати протеолітичну активність чинить гальмувальний вплив на ранні етапи взаємодії вірусу із чутливими клітинами, а також пригнічує протеолітичний процесинг гемаглютиніну. Внаслідок цього не створюється функціонально активний білок вірусу грипу, який забезпечує його інфекційну активність, а також пригнічується утворення дочірніх вібріонів.
Клінічні спостереження продемонстрували ефективність амінокапронової кислоти при лікуванні дітей різного віку, хворих на грип й інші ГРВІ. Зокрема, було встановлено, що вона особливо ефективна на ранніх термінах хвороби через зниження частоти токсичних синдромів і вторинних бактеріальних ускладнень (у ≥2 рази).
Аналіз епідеміологічної ефективності використання довів, що діти, які отримали препарат, хворіли достеменно рідше, ніж ті, котрі його не отримували. Ця тенденція збереглася і в подальші 4 міс. Кількість дітей, які хворіли до 6 р/рік, зменшилася на 60%. Курс профілактики скоротив тривалість одного захворювання в середньому на 2,7 дня (Гридіна Т. Л. і співавт., 2010).
З огляду на доказову базу Державний фармакологічний центр Міністерства охорони здоров’я України своїм листом за № 6780/212-8 від 16 листопада 2009 року ухвалив рішення рекомендувати внести до інструкції для медичного застосування лікарський засіб амінокапронова кислота до розділу «Показання»: лікування і профілактика грипу та ГРВІ у дітей та дорослих».
Коронавірус SARS-CоV‑2 (2019-nCoV) має схожі механізми проникнення до клітини; репродукція вірусного потомства майже ідентична такому вірусу грипу, тому цілком імовірно, що амінокапронова кислота може виявитися ефективним засобом як лікування COVID‑19, так і стримування подальшого поширення пандемії COVID‑19.
На сьогодні амінокапронову кислоту рекомендовано застосовувати з метою лікування і профілактики грипу / ГРВІ в дітей та дорослих [3]. Обґрунтованим є використання амінокапронової кислоти місцево. Рекомендовано кожні 2-3 год закладати в носові ходи на 5-10 хв ватні турунди, рясно зволожені 5% розчином АКК чи виготовленим із порошку на непідсолодженій воді, або в зазначені строки інстилювати його по ≥3-5 крапель в кожний носовий хід. Розчин також можна використовувати для інгаляцій.
При тяжких гіпертоксичних формах грипу чи ГРВІ дози препарату можуть бути підвищені на 30-40%, при цьому половину добової дози може бути доцільним ввести внутрішньовенно краплями. При внутрішньовенному введенні необхідний контроль коагулограми.
За потреби препарат можна застосовувати в комбінації з іншими відомими противірусними препаратами (озельтамівір) або інтерфероном чи його індукторами, що підвищує ефективність лікування.
Інтраназальні інстиляції АКК (3-4 р/день) доцільно проводити дітям і дорослим протягом епідемічного періоду з метою профілактики. В осередках інфекції тим, хто контактує із хворим, рекомендовано доповнювати інтраназальні інстиляції пероральним використанням препарату (як при лікуванні).
Тривалість перорального застосування амінокапронової кислоти в разі грипу та ГРВІ зазвичай становить 3-7 днів, однак цей термін може бути подовжений за необхідності.
На вітчизняному фармацевтичному ринку амінокапронова кислота представлена препаратом АКК® у вигляді готового розчину (50 мг/мл) у пластикових контейнерах по 2 мл.
Вищевикладена інформація обґрунтовує доцільність застосування АКК з метою зменшення ризику інфікування SARS-CoV‑2, профілактики тяжкого перебігу COVID‑19 та стримування подальшого поширення пандемії. Ці завдання є особливо актуальними з огляду на появу нових небезпечних штамів коронавірусу, малочутливих до існуючих вакцин.
Список літератури знаходиться в редакції.