1 квітня, 2026
Стратегії подолання резистентності при лікуванні хронічного болю: роль дулоксетину після недостатньої відповіді на терапію габапентиноїдами
Хронічний біль є однією із провідних причин втрати працездатності та зниження якості життя у світі, спричиняючи вагомі соціально-економічні наслідки. За сучасними епідеміологічними оцінками, його поширеність серед дорослого населення становить 20‑30%, а в окремих країнах сягає понад 30% [1, 2]. Дані останніх років свідчать про тенденцію до зростання частоти хронічного болю, що суттєво обмежує повсякденну активність та соціальне функціонування (high-impact chronic pain) [3]. У глобальному контексті хронічний біль призводить до суттєвої інвалідизації дорослого населення та входить до переліку ключових чинників втрати років життя з урахуванням непрацездатності [4].
Особливу клінічну значущість має висока коморбідність хронічного болю із тривожно-депресивними розладами. За даними систематичних оглядів та метааналізів останніх років, клінічно значущі симптоми депресії виявляються приблизно у 35‑45% пацієнтів із хронічним болем, тоді як симптоми тривоги реєструються у 30‑50% випадків [5‑7]. Наявність афективної коморбідності пов’язана із вищою виразністю больового синдрому, перебільшенням інтенсивності та наслідків симптомів (катастрофізація), гіршою відповіддю на лікування та вищим ризиком хроніфікації [8]. Патофізіологічною основою взаємозв’язку хронічного болю та тривожно-депресивних розладів є дисфункція низхідних серотонін- і норадренергічних антиноцицептивних систем, а також підвищена чутливість центральної нервової системи до больових сигналів (центральна сенситизація) [9].
Попри широке застосування габапентиноїдів у лікуванні нейропатичного та змішаного больового синдрому, сучасні дослідження демонструють, що до 40‑50% пацієнтів не досягають клінічно значущої редукції болю або припиняють терапію через побічні ефекти (ПЕ) [10]. Одним із провідних чинників недостатньої ефективності габапентиноїдів може бути переважання механізмів центральної сенситизації. Відомо, що анальгетичний ефект габапентину та прегабаліну реалізується через модуляцію функції α2δ-субодиниці кальцієвих каналів, зменшуючи вивільнення збуджувальних нейромедіаторів, зокрема глутамату і субстанції P. У пацієнтів із хронічним болем, що супроводжується порушенням функціонування низхідних серотонін-норадренергічних механізмів контролю болю, терапевтичний потенціал габапентиноїдів може бути обмеженим [10].
Важливу роль також відіграє мультимодальний характер больового синдрому. Поєднання нейропатичного, ноцицептивного та афективного компонентів болю формує складний клінічний фенотип, який потребує впливу на декілька нейробіологічних ланок одночасно. У таких випадках терапія, спрямована лише на модуляцію кальцієвих каналів, може не забезпечувати достатнього клінічного ефекту [11].
Водночас коморбідні тривожно-депресивні розлади здатні посилювати сприйняття болю. Відомо, що дефіцит серотоніну та норадреналіну пов’язаний із підвищеною больовою чутливістю, що додатково обмежує ефективність габапентиноїдів у частки пацієнтів. Не виключається також формування фармакорезистентності або толерантності при тривалому застосуванні габапентину чи прегабаліну, що може знижувати клінічну відповідь із часом [12].
У цьому контексті інгібітори зворотного захоплення серотоніну та норадреналіну, зокрема дулоксетин, набувають особливої клінічної значущості. Дулоксетин демонструє доведену ефективність при діабетичній нейропатії, фіброміалгії, остеоартриті та хронічному болю в попереку, що підтверджено сучасними рандомізованими дослідженнями, а також є препаратом вибору згідно з оновленими міжнародніми рекомендаціями [13, 14]. Його механізм дії спрямований на відновлення балансу серотонін- і норадренергічної нейротрансмісії, що дозволяє одночасно впливати на больовий та афективний компоненти патологічного процесу [15].
Отже, з огляду на високу поширеність хронічного болю, значну частоту терапевтичної резистентності до габапентиноїдів та тісний патогенетичний зв’язок болю із тривожно-депресивними розладами, а також наукову обґрунтованість і суттєву клінічну актуальність, було виконане дослідження ефективності й переносимості дулоксетину.
Матеріали й методи дослідження
Метою дослідження було оцінити клінічну ефективність та переносимість дулоксетину (використовувався препарат Симода) у 87 пацієнтів із хронічним больовим синдромом різного генезу, які не досягли адекватного анальгетичного ефекту або мали клінічно значущі ПЕ на тлі терапії габапентином чи прегабаліном. Наукову роботу проводили у форматі проспективного відкритого спостережного клінічного проєкту тривалістю вісім тижнів на базі лікувальних закладів України.
Протокол дослідження передбачав три планових візити: перший (базовий, 0-й тиждень), другий (візит 2, 4-й тиждень) та третий (візит 3, 8-й тиждень). На момент включення у дослідження всі пацієнти отримували терапію габапентиноїдами, зокрема прегабалін або габапентин у стандартних терапевтичних дозах. Перехід із габапентину чи прегабаліну на дулоксетин здійснювався за принципом поетапної крос-титрації з метою мінімізації ризику синдрому відміни, запобігання транзиторному посиленню больового синдрому та забезпечення оптимальної переносимості терапії (табл. 1 і 2). У пацієнтів із виразним больовим синдромом або недостатньою клінічною відповіддю через 2‑4 тижні лікування доза дулоксетину могла бути підвищена до 90‑120 мг/добу. При застосуванні максимальної дози 120 мг препарат призначали у два приймання (60 мг вранці та 60 мг увечері) для поліпшення переносимості.
|
Таблиця 1. Схема перехресної крос-титрації для пацієнтів, які приймали прегабалін |
|||||
|
День |
Прегабалін (мг/добу) |
Кратність |
Дулоксетин (мг/добу) |
Кратність |
Коментар |
|
1‑3 |
Якщо добова доза 450‑600 мг – знизити до 300 мг (150 мг Ч 2 р/день) |
2 р/день |
– |
– |
Початок зниження дози прегабаліну |
|
4‑6 |
150 мг Ч 2 р/день |
2 р/день |
30 мг |
1 р/день (ранок) |
Початок приймання дулоксетину, зниження дози прегабаліну |
|
7-9 |
75 мг Ч 2 р/день або 75 мг на ніч |
2 р/день |
60 мг |
1 р/день |
Зменшення дози прегабаліну, збільшення дози дулоксетину |
|
10‑12 |
75 мг на ніч або відміна |
1 р/день |
60 мг |
1 р/день |
Завершення приймання прегабаліну |
|
13‑14 |
0 мг |
– |
60‑120 мг |
1 р/день (60‑90 мг) 2 р/день (120 мг) |
Повна відміна прегабаліну |
|
Таблиця 2. Схема перехресної крос-титрації для пацієнтів, які приймали габапентин |
|||||
|
День |
Габапентин (мг/добу) |
Кратність |
Дулоксетин (мг/добу) |
Кратність |
Коментар |
|
1‑3 |
Якщо добова доза 1200‑2400 мг – знизити до 900 мг/добу |
3 р/день |
– |
– |
Старт зниження дози габапентину (звичайна доза) |
|
4‑6 |
300 мг Ч 3 р/день |
3 р/день |
30 мг |
1 р/день (ранок) |
Початок приймання дулоксетину |
|
7‑9 |
300 мг Ч 2/день |
2 р/день |
60 мг |
1 р/день |
Зменшення дози габапентину, збільшення дози дулоксетину |
|
10‑12 |
300 мг Ч 1 раз (на ніч) |
1 р/день |
60 мг |
1 р/день |
Завершення приймання габапентину |
|
13‑14 |
0 мг |
— |
60‑120 мг |
1 р/день (60‑90 мг) |
Повна відміна габапентину |
Критерії включення:
- вік ≥18 років;
- хронічний біль тривалістю ≥3 місяців;
- інтенсивність болю ≥4 балів за візуальною аналоговою шкалою (ВАШ);
- недостатній ефект або ПЕ під час приймання габапентину чи прегабаліну;
- здатність надати письмову інформовану згоду та виконувати процедури дослідження.
Критерії виключення:
- наявність суїцидальних думок за опитувальником про стан здоров’я (PHQ‑9), пунктом 9 (≥2 балів);
- наявність серйозних психічних розладів;
- клінічно значущі соматичні захворювання;
- тяжка печінкова або ниркова недостатність;
- вагітність чи лактація;
- приймання інгібіторів моноаміноксидази, трициклічних антидепресантів, карбамазепіну, топірамату;
- застосування опіоїдних анальгетиків.
Кінцевою точкою оцінювання єфективності дослідження була зміна інтенсивності болю за ВАШ між 1-м та 3-м візитами. Мінімально клінічно значущим вважалося зниження болю на ≥2 бали або ≥50% від вихідного рівня за шкалою ВАШ.
Оцінювальні інструменти:
- Зміна показників за підшкалою впливу болю на функціонування короткого опитувальника болю (BPI‑I).
- Поліпшення функціонування ≥30% за BPI‑I.
- Редукція депресивної симптоматики за PHQ‑9 ≥5 балів.
- Редукція тривоги за опитувальником із генералізованої тривоги (GAD‑7) ≥4 бали.
- Визначення переносимості терапії за анкетою для оцінювання частоти, інтенсивності та тягаря побічних ефектів (FIBSER).
Оцінювання пацієнтів за інструментами ВАШ, BPI‑I, GAD‑7 та PHQ‑9 проводилося на всіх трьох візитах. Аналіз переносимості за FIBSER здійснювався на 4-му та 8-му тижнях лікування.
Перед включенням у дослідження всі пацієнти підписували письмову інформовану згоду на участь. Дані фіксувалися в їхніх індивідуальних медичних картах. Дослідження здійснювалося відповідно до принципів належної клінічної практики та етичних стандартів.
Математично-статистичний метод оцінювання проводився за допомогою програмного забезпечення Microsoft Excel 2019. Кількісні математичні зміни наведені як середне значення (М) та стандартне відхилення (SD). Порівняння кількісних показників між двома незалежними групами виконували із застосуванням непараметричного критерію Манна–Уїтні. Рівень статистичної значущості вважали досягнутим при p<0,05.
Результати дослідження та обговорення
Відповідно до аналізу соціально-демографічних та клініко-анамнестичних характеристик обстежених, у дослідження було включено репрезентативну за віком та статтю когорту осіб із наявним хронічним больовим синдромом (табл. 3).
|
Таблиця 3. Соціально-демографічні та клініко-анамнестичні характеристики пацієнтів |
|
|
Показник |
Значення |
|
Вік, роки (M±SD) Мin/max, рік |
51,7±14,0 24‑79 |
|
Стать, n (%) Чоловіки Жінки |
34 (39,1%) 53 (60,9%) |
|
Сімейний стан, n (%) Одружені Неодружені |
62 (71,3%) 25 (28,7%) |
|
Освіта, n (%) Вища Середня спеціальна |
47 (54%) 40 (46%) |
|
Зайнятість, n (%) Працюють Не працюють |
50 (57,5%) 37 (42,5%) |
|
Місце проживання, n (%) Міська місцевість Сільська місцевість |
70 (80,5%) 17 (19,5%) |
|
Зв’язок хронічного болю із психотравмою в анамнезі Ні Так |
60 (69%) 27 (31%) |
|
Тривалість хронічного болю, n (%), місяці Від 3 до 5 місяців Від 6 до 9 місяців Від 10 до 12 місяців Понад 12 місяців |
7 (8%) 20 (23%) 29 (33,1%) 31 (35,6%) |
|
Причина хронічного болю, n (%) Центральний нейропатичний біль (травма, інсульт) Головний біль Постгерпетична нейропатія Біль у спині Міофасціальний біль Фіброміалгія Діабетична нейропатія Остеоартрит |
5 (5,7%) 7 (8%) 7 (8%) 9 (10,4%) 9 (10,4%) 11 (12,6%) 17 (19,5%) 22 (25,3%) |
|
Фармакотерапія габапентиноїдами, n (%) Прегабалін Габапентин |
69 (79,3%) 18 (20,7%) |
|
Середня доза прегабаліну на добу, мг (M±SD) Мin/max, мг |
262,9±115,4 75‑600 |
|
Середня доза габапентину на добу, мг (M±SD) Мin/max, мг |
842,9±394,8 600‑1800 |
Середній вік пацієнтів становив 51,7±14,0 року, що відображало переважання осіб середнього та старшого віку, для яких характерні як більша поширеність хронічного болю, так і вищий ризик коморбідних порушень настрою. У гендерній структурі вибірки домінували жінки (60,9%). Більшість учасників перебували у шлюбі (71,3%), мали вищу освіту (54%) та понад половина з них (57,5%) були працевлаштовані. Водночас 42,5% пацієнтів не працювали, що могло відображати функціональні обмеження, пов’язані з больовим синдромом та тривогою і депресією. Переважання мешканців міської місцевості (80,5%), ймовірно, було пов’язане із кращою доступністю спеціалізованої медичної допомоги.
У третини учасників (31%) простежувався зв’язок виникнення або хроніфікації болю із психотравмувальними подіями в анамнезі, що підкреслювало значення психоемоційних чинників у формуванні хронічного больового синдрому. За тривалістю болю більшість пацієнтів (68,7%) мали симптоматику понад 10 місяців, а у 35,6% тривалість перевищувала 12 місяців, що відповідало критеріям хронічного больового розладу. Це свідчило про стійкий характер больового синдрому та високу ймовірність формування центральної сенситизації.
Структура причини хронічного болю у досліджуваній когорті була гетерогенною та демонструвала поєднання ноцицептивних, нейропатичних і змішаних механізмів. Найпоширенішими були остеоартрит (25,3%) та діабетична нейропатія (19,5%). У пацієнтів з остеоартритом біль мав переважно ноцицептивний характер із поступовим переходом у центральну сенситизацію, тоді як при діабетичній нейропатії домінував нейропатичний компонент із дизестезіями, парестезіями та пекучим характером болю.
Окрему групу становили пацієнти із фіброміалгією (12,6%) та міофасціальним больовим синдромом (10,4%), де провідну роль відіграють механізми центральної сенситизації та дисфункція низхідних антиноцицептивних систем. У цих випадках біль часто поєднувався із виразною астенією, порушеннями сну, когнітивною дисфункцією та високим рівнем тривожно-депресивної симптоматики. Біль у спині (10,4%) здебільшого мав змішаний механізм із поєднанням дегенеративних змін хребта, м’язово-тонічного компонента та вторинної центральної сенситизації.
Постгерпетична нейропатія (8%) характеризувалася стійким нейропатичним болем зі значною алодинією (біль від подразників, які зазвичай не викликають болю) та гіпералгезією, що суттєво знижувало якість життя пацієнтів. Головний біль (8%), зокрема хронічні цефалгії напруження або мігренозного спектра, також супроводжувався емоційною нестабільністю та підвищеною тенденцією до соматизації. Центральний нейропатичний біль після травми або інсульту (5,7%) відзначався особливою резистентністю до стандартної терапії та високим рівнем афективної коморбідності.
На момент включення у дослідження всі пацієнти отримували терапію габапентиноїдами, переважно прегабалін (79,3%), рідше – габапентин (20,7%). Середня добова доза прегабаліну становила 262,9±115,4 мг (діапазон – 75‑600 мг/добу), габапентину – 842,9±394,8 мг (діапазон – 600‑1800 мг/добу).
Середній показник за суб’єктивною шкалою оцінки ефективності попереднього лікування габапентиноїдами становив 3,40±1,29 бала, що відповідає низькому рівню терапевтичної відповіді. Зазначені дані узгоджуються з результатами сучасних досліджень, відповідно до яких 40‑50% пацієнтів із хронічним больовим синдромом не досягають клінічно значущого зменшення інтенсивності болю при застосуванні габапентину або прегабаліну, що підкреслює актуальність пошуку альтернативних фармакотерапевтичних стратегій.
Аналіз динаміки інтенсивності болю
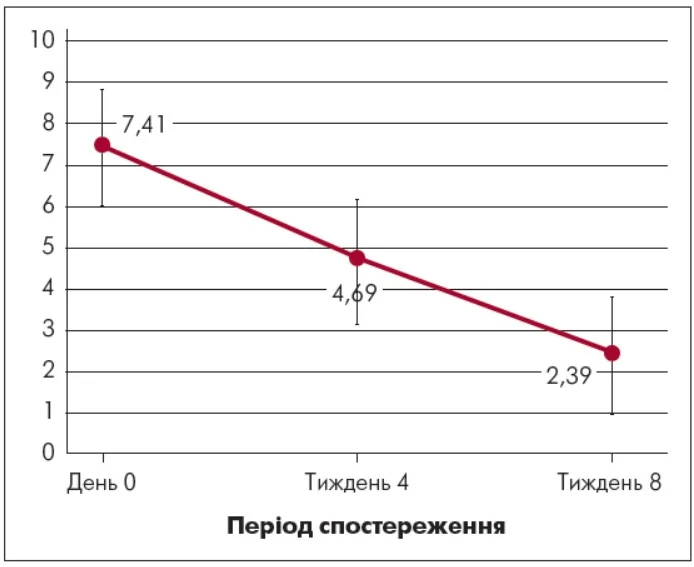
Оцінювання динаміки інтенсивності болю за шкалою ВАШ продемонструвало потужне та послідовне зниження больового синдрому впродовж восьми тижнів лікування дулоксетином (рис. 1). На момент включення у дослідження пацієнти мали виразний і тривалий больовий синдром. Середній показник інтенсивності болю за ВАШ становив 7,41±1,30 бала, що відповідало високому рівню больового навантаження та суттєвому функціональному обмеженню.
Примітки: 0 балів – немає болю; 1‑3 балів – слабкій біль; 4‑5 балів – середній біль; 6‑7 балів – сильний біль; 8‑9 балів – дуже сильний біль; 10 балів – нестерпний біль.
Рис. 1. Редукція хронічного болю впродовж лікування за ВАШ
Больовий синдром мав хронічний перебіг (≥3 місяців) із тенденцією до прогресування, попри попередню терапію габапентиноїдами. Клінічно значущим є те, що інтенсивність болю залишалася високою навіть на тлі приймання нестероїдних протизапальних препаратів, що свідчило про обмежену роль периферичного запального компонента у частини обстежуваних та домінування центральних механізмів болю. Пацієнти повідомляли про зниження рівня життєвої активності, підвищену втомлюваність, емоційну лабільність та формування поведінки уникнення активності через страх посилення болю.
На 4-му тижні лікування дулоксетином було зафіксоване суттєве зменшення інтенсивності больового синдрому порівняно із вихідним рівнем. Середній показник за ВАШ знизився до 4,69±1,31 бала (Δ=-2,72; p<0,001) що відповідало переходу від виразного до помірного ступеня болю. Клінічно це проявлялося помітним послабленням постійного фонового болю, зменшенням інтенсивності больових відчуттів у стані спокою та при фізичному навантаженні. Пацієнти повідомляли про зниження частоти нічних пробуджень, поліпшення якості сну та зменшення ранкової скутості. Зменшення болю сприяло підвищенню толерантності до повсякденної активності та зростанню рівня фізичної витривалості.
На 8-му тижні лікування дулоксетином відзначалося подальше та виразніше зменшення інтенсивності больового синдрому. Середній показник за ВАШ знизився до 2,39±1,15 бала, що відповідало легкому або мінімальному ступеню болі. Середня редукція інтенсивності болю порівняно із вихідним рівнем становила -5,02 бала (p<0,001), що свідчило про потужний клінічний ефект терапії. У більшості пацієнтів (91%) спостерігалося зниження болю більш ніж на 50% від початкового рівня, що відповідало високій клінічній відповіді на лікування дулоксетином.
Загальна ефективність лікування дулоксетином у пацієнтів із хронічним болем становила 68%, що відображало значну редукцію інтенсивності больового синдрому за ВАШ упродовж восьми тижнів терапії. Отриманий показник свідчив про виразний клінічний ефект лікування та підтвердив доцільність застосування дулоксетину в осіб із недостатньою відповіддю на попередню терапію габапентиноїдами.
Оцінювання динаміки тривожної симптоматики
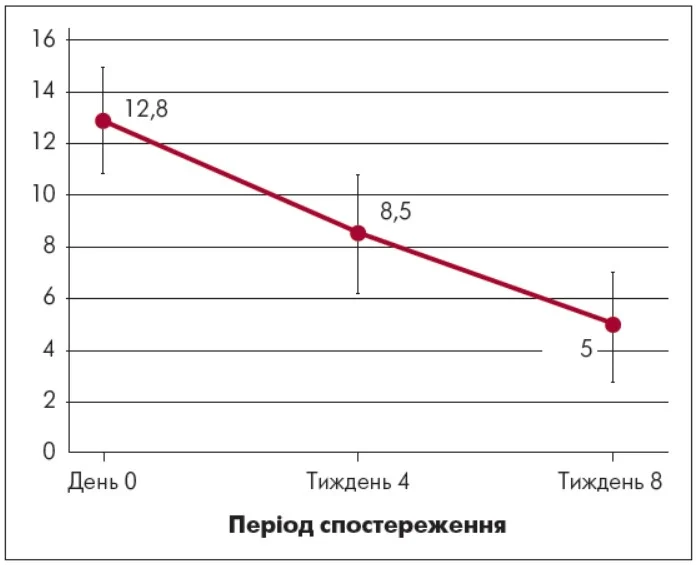
Аналіз динаміки тривожної симптоматики за опитувальником GAD‑7 продемонстрував статистично та клінічно значущу редукцію симптомів впродовж лікування дулоксетином (рис. 2). На момент включення у дослідження у більшості пацієнтів (68,9%) були виявлені клінічно значущі прояви тривоги за GAD‑7 (≥10 балів), тоді як у 31,1% спостерігалася субклінічна тривога (≤10 балів). Середній показник тривоги на початку лікування становив 12,8±2,4 бала, що відповідало помірному рівню генералізованої тривоги. Учасники із виразнішим больовим синдромом частіше повідомляли про постійне внутрішнє напруження, неконтрольоване занепокоєння та катастрофізацію симптомів.
Примітки: 0‑4 балів – відсутність тривоги; 5‑9 балів – легка тривога; 10‑14 балів – помірна тривога; 15‑21 балів – високий рівень тривоги.
Рис. 2. Редукція тривожної симптоматики за GAD‑7
На 4-му тижні лікування показник тривоги знизився до 8,5±2,1 бала (Δ=-3,0; p<0,05), що супроводжувалося паралельним зменшенням інтенсивності болю. Клінічно це проявлялося редукцією психоемоційного напруження, зменшенням проявів тривоги, відчуття внутрішньої скутості, м’язової напруженості й порушень сну, а також поліпшенням переносимості больових відчуттів.
На 8-му тижні лікування дулоксетином середній бал тривоги за GAD‑7 знизився до 5,0±1,8 бала (Δ=-6,5; p<0,001), що відповідало мінімальному або субклінічному рівню тривоги. Зниження інтенсивності болю супроводжувалося пропорційним зниженням тривожної симптоматики, що клінічно відображало ослаблення катастрофізації болю, зменшення страху руху та відновлення емоційної стабільності.
Загальна ефективність лікування тривоги становила 54% редукції симптоматики від вихідного рівня, що свідчило про виразну клінічну відповідь на терапію дулоксетином. До завершення 8-го тижня більшість пацієнтів досягли рівня мінімальної або субклінічної тривоги, що відображало не лише статистично достовірне поліпшення, але й функціонально значуще відновлення психоемоційної регуляції та соціальної адаптації.
Аналіз показників депресивної симптоматики
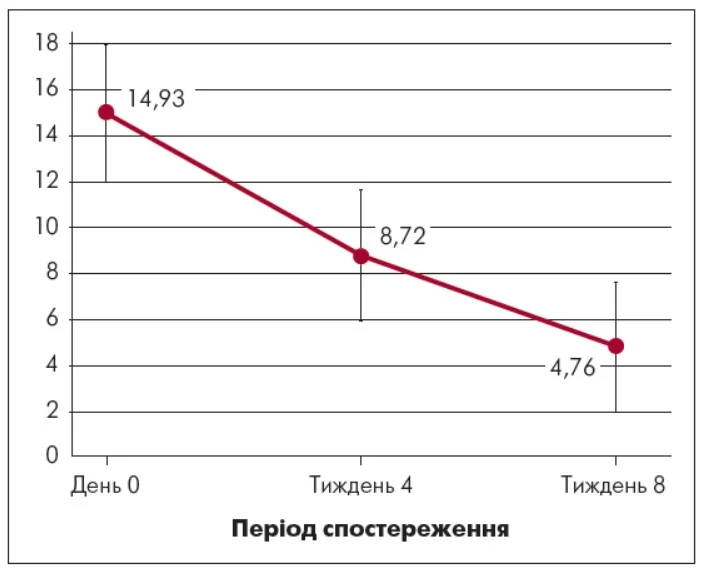
Оцінювання показників депресивної симптоматики за опитувальником PHQ‑9 показало виразну позитивну клінічну динаміку впродовж лікування дулоксетином (рис. 3). На момент включення у дослідження у більшості пацієнтів (75,9%) реєструвався клінічно значущий рівень депресивної симптоматики за PHQ‑9 (≥10 балів), тоді як лише у 24,1% – субклінічна депресія (≤10 балів). Середній показник рівня депресії на початку лікування становив 14,93±5,54 бала, що відповідало помірно вираженому депресивному епізоду.
Примітки: 0‑4 балів – відсутність депресії; 5‑9 балів – легкий рівень депресії; 10‑14 балів – помірна рівень депресії; 15‑19 балів – помірно тяжкий рівень депресії; 20‑27 балів – тяжка депресія.
Рис. 3. Редукція депресивної симптоматики за PHQ‑9
Пацієнти з інтенсивнішим больовим синдромом частіше демонстрували стійке зниження настрою, втрату інтересу та задоволення від повсякденної діяльності, зменшення мотивації та ініціативності, а також виразну астенію, когнітивну сповільненість та труднощі з концентрацією уваги.
На 4-му тижні лікування середній показник депресії за PHQ‑9 знизився до 8,72±3,63 бала, що відповідало переходу від помірного до легкого рівня депресивної симптоматики (Δ=-6,21; p<0,001) і свідчило про клінічно значущий ефект уже на ранньому етапі терапії. Відзначалися поліпшення емоційного фону, зменшення виразності ангедонії, часткове відновлення активності, нормалізація сну та редукція астенічного компоненту.
На 8-му тижні лікування дулоксетином середній показник знизився до 4,76±2,29 бала, що відповідало мінімальному чи субклінічному рівню депресії (Δ=-10,17; p<0,001).
Загальна ефективність лікування депресивної симптоматики становила 68%, що свідчило про виразну клінічну відповідь на терапію дулоксетином. Це дозволило розцінювати отриманий результат як наближення до стану функціональної ремісії.
Варто зазначити, що отримані результати підтверджують тісний клініко-патогенетичний взаємозв’язок депресії та хронічного больового синдрому. Розлади настрою підсилюють суб’єктивне сприйняття болю через когнітивні механізми, тоді як хронічний біль підтримує та поглиблює депресивну симптоматику, формуючи замкнене патогенетичне коло. Синхронна редукція проявів депресії та зниження інтенсивності болю впродовж лікування свідчить про вплив терапії на спільні патофізіологічні ланки і, відповідно, доцільність інтегрованого підходу до лікування пацієнтів із коморбідними больовими й афективними розладами.
Оцінювання впливу болю на соціальне функціонування
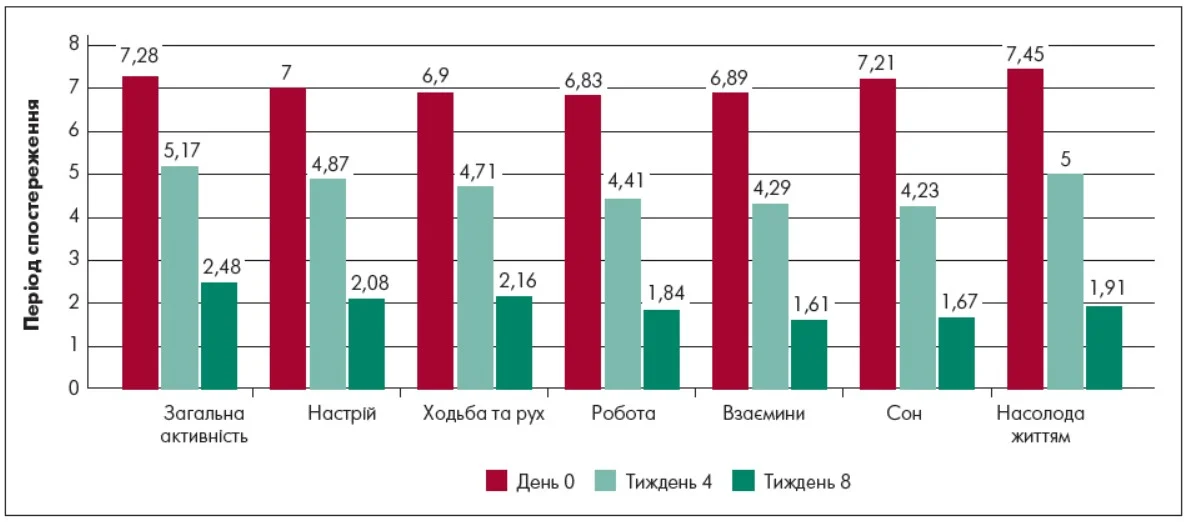
Аналіз впливу болю на соціальне функціонування за опитувальником BPI‑I продемонстрував виразну позитивну динаміку впродовж восьми тижнів лікування дулоксетином (рис. 4). Вихідний клінічний профіль пацієнтів відзначався суттєвим впливом болю на всі ключові компоненти соціального та психоемоційного функціонування, що відображало комплексну функціональну дезадаптацію, пов’язану із больовим синдромом. Найвищі показники впливу болю спостерігалися у сферах насолоди життям (7,46±2,24 бала), загальної активності (7,28±1,87 бала), задоволеність сном (7,21±2,06 бала) та настроєм (7,00±2,03 бала), що свідчило про глибоке порушення базових сфер життєдіяльності та суб’єктивного благополуччя. Пацієнти повідомляли про труднощі засинання через біль, часті нічні пробудження та відсутність відчуття відновлення після нічного відпочинку.
Примітки: 0‑3 бали – мінімальний вплив болю; 4‑6 балів – помірний вплив болю; 7‑10 балів – виразний вплив болю.
Рис. 4. Динамика впливу болю на соціальне функціонування за BPI‑I
Рухливість/ходьба (6,90±1,90 бала) була суттєво обмеженою; зокрема пацієнти повідомляли про труднощі при тривалому пересуванні, зменшення витривалості та зниження рівня фізичної активності. Показник впливу болю на роботу (6,83±1,92 бала) свідчив про зниження професійної та побутової продуктивності. Пацієнти відзначали труднощі з концентрацією уваги, зменшення темпу виконання завдань і потребу в зниженні навантаження. У сфері міжособистісних взаємин (6,89±1,98 бала) фіксувалося виразне порушення соціального функціонування. Біль був пов’язаний зі зниженням соціальної активності, обмеженням спілкування, підвищеною дратівливістю та тенденцією до соціальної ізоляції. Слід зауважити, що больовий синдром суттєво впливав на загальну активність пацієнтів. Високі показники (7,46±2,24 бала) вказували на значне зниження здатності відчувати насолоду, втрату інтересу та задоволення від повсякденної діяльності, а також істотне зниження суб’єктивної якості життя.
На 4-му тижні лікування дулоксетином було зафіксоване статистично та клінічно значуще зниження функціональної недостатності, пов’язаної з хронічним болем за всіма доменами BPI‑I порівняно із вихідним рівнем. У сфері загальної активності середній показник знизився до 5,17±1,66 бала (Δ=-2,19; p<0,05), що відображало зменшення обмежень у виконанні повсякденних побутових завдань та зниження поведінки уникання фізичного навантаження. Вплив болю на настрій також суттєво зменшився до 4,87±1,61 бала (Δ=-2,13; p<0,05). Це свідчило про редукцію афективної насиченості болю, зниження рівня емоційної напруженості та поступове відновлення психологічної стабільності.
У сфері рухливості чи ходьби показник зменшився приблизно на третину (4,71±1,64 бала, Δ=-2,19; p<0,05), що вказувало на поліпшення фізичної активності, зменшення обмежень під час пересування та зниження страху руху, пов’язаного з очікуванням посилення болю. Сфера оцінки звичної роботи продемонструвала дуже виразну позитивну динаміку, зокрема показник знизився до 4,41±1,74 бала (Δ=-2,49; p<0,001). Це відображало підвищення працездатності, поліпшення концентрації уваги і зменшення негативного впливу болю на професійну та побутову продуктивність.
Вплив болю на міжособистісні взаємини зменшився до 4,29±1,90 бала (Δ=-2,54; p<0,001). Пацієнти рідше повідомляли про соціальну ізоляцію, підвищену дратівливість та обмеження контактів з оточенням. Суттєві зміни спостерігалися і у сфері задовленості сном (4,29±1,98 бала, Δ=-2,60; p<0,001). Зменшення нічного болю супроводжувалося поліпшенням безперервності сну, зменшенням кількості пробуджень та підвищенням суб’єктивного відчуття відновлення після нічного відпочинку.
Значуща позитивна динаміка спостерігалася у сфері насолоди життям, де загальний показник суб’єктивного благополуччя знизився до 4,15±1,85 бала (Δ=-3,06; p<0,001). Пацієнти відзначали поліпшення загального самопочуття, підвищення життєвої активності та зменшення емоційної напруженості. Водночас було встановлене зростання впевненості у можливості контролю симптомів, що є важливим компонентом психологічної адаптації при хронічному больовому синдромі.
На 8-му тижні терапії спостерігалося подальше достовірне зниження показників функціональної обмеженості, пов’язаної з хронічним болем за всіма доменами BPI‑I, що вказувало на потужний анальгетичний терапевтичний ефект. Отримані значення наближалися до рівня мінімального впливу болю, що відображало виразне відновлення повсякденного та психосоціального функціонування.
Редукція болю наприкінці лікування супроводжувалася відновленням повсякденної активності та підвищенням фізичної витривалості. Пацієнти повідомляли про зменшення болю у спокої та при фізичній активності, що дозволяло виконувати побутові обов’язки без виразного дискомфорту. Середній ступінь обмеження загальної активності знизився до 2,48±1,35 бала (Δ=-4,80; p<0,001). Третина пацієнтів (37%) відновила повноцінну участь у трудовій діяльності або збільшила її обсяг. Середній показник задоволення звичною роботою продемонстрував суттєве поліпшення до 1,84±1,40 бала (Δ=-5,06; p<0,001).
Наприкінці лікування пацієнти відзначали підвищення рівня життєвої активності, зменшення втомлюваності та емоційної напруженості, пов’язаної з постійним очікуванням болю. Формування відчуття контролю над симптомами мало важливе значення для психологічної стабілізації та зменшення тривожності. Середній показник обмеження рухливості знизився до 2,16±1,52 бала (Δ=-4,74; p<0,001). Пацієнти демонстрували відновлення переносимості фізичного навантаження та зменшення обмежень у пересуванні.
Зменшення інтенсивності болю також сприяло відновленню соціальних контактів, зниженню ізоляції та підвищенню якості взаємодії з оточенням. Середній показник виразності болю знизився до 1,61±1,25 бала (Δ=-5,22; p<0,001). Зменшення больового навантаження зумовлювало нормалізацію сну, зниження частоти пробуджень та поліпшення суб’єктивного відчуття відновлення, що покращувало загальне самопочуття. Середне значення впливу болю на задоволеність сном знизилося до 1,67±1,57 бала (Δ=-5,22; p<0,001).
Наприкінці лікування відзначалося потужне зниження тривожно-депресивної симптоматики. Також спостерігалося зменшення соматизованих проявів тривоги (як-от вегетативна напруга, порушення концентрації уваги, відчуття внутрішнього неспокою). Середній показник впливу болю на настрій знизився до 2,08±1,50 бала (Δ=-4,92; p<0,001).
Пацієнти повідомляли про зростання відчуття контролю над симптомами, відновлення життєвої перспективи та підвищення впевненості у здатності підтримувати досягнуте поліпшення. Середній показник насолоди життям знизився до 1,91±1,43 (Δ=-5,30; p<0,001).
Отже, отримані результати свідчать, що терапія дулоксетином була пов’язана із поступовим відновленням функціонального та психосоціального статусу пацієнтів.
Аналіз динаміки побічних ефектів
Аналіз динаміки ПЕ за опитувальником FIBSER продемонстрував статистично достовірне та клінічно значуще зниження частоти, тяжкості й функціональної обтяжливості ПЕ впродовж лікування (табл. 3). На момент включення у дослідження всі пацієнти отримували терапію габапентиноїдами, що було пов’язано із наявністю клінічно значущих ПЕ. Середня частота ПЕ становила 46,0±24,0%, що відповідало межі «рідко/іноді» за FIBSER. Середній показник їх тяжкості становив 3,41±1,05 бала, що характеризувало помірний ступінь виразності, тоді як функціональна обтяжливість досягала 3,24±1,11 бала, що свідчило про помітний негативний вплив на повсякденне функціонування.
|
Таблиця 4. Динаміка побічних ефектів під час лікування дулоксетином за FIBSER |
||||
|
Час спостереження |
Частота ПЕ, % (M±SD) |
Тяжкість ПЕ (M±SD) |
Функціональна обтяжливість (M±SD) |
р |
|
День 0 |
46,0±24,0 |
3,41±1,05 |
3,24±1,11 |
|
|
Тиждень 4 |
24,2±20,0 |
1,63±0,98 |
1,56±0,96 |
p<0,001 |
|
Тиждень 8 |
13,2±7,65 |
0,93±0,63 |
0,67±0,40 |
p<0,001 |
|
Примітки: Частота ПЕ: не було (0%); дуже рідко (10‑24%); рідко (25‑49%); іноді (50‑74%); часто (75‑89%); дуже часто (90‑99%); постійно (100%). Тяжкість ПЕ: 0 – не було; 1 – дуже легкі; 2 – легкі; 3 – помірні; 4 – виразні; 5 – сильні; 6 – надзвичайно сильні. Функціональна обтяженість: 0 – зовсім не заважали; 1 – майже не заважали; 2 – трохи заважали; 3 – помітно заважали; 4 – суттєво заважали; 5 – дуже сильно заважали; 6 – повністю порушували повсякденну активність. |
||||
Клінічна картина ПЕ мала типовий для габапентиноїдів профіль та включала виразну денну сонливість, седацію, запаморочення і відчуття нестійкості, що обмежувало фізичну активність пацієнтів. Часто відзначалися когнітивне уповільнення, труднощі з концентрацією уваги та зниження швидкості психічних процесів, що негативно впливало на професійну діяльність і побутову продуктивність. Також поширеними були астенія, загальна слабкість, порушення координації рухів, периферичні набряки та тенденція до збільшення маси тіла. Зазначені ПЕ під час приймання прегабаліну або габапентину зумовлювали зниження соціальної залученості, обмеження фізичної активності та погіршення якості життя пацієнтів, що відображалося у помірному рівні функціональної обтяжливості за FIBSER.
На 4-му тижні лікування дулоксетином після повної відміни габапентиноїдів було зафіксоване статистично значуще зниження частоти ПЕ до 24,2±20% (p<0,001), що відповідало ступеням «дуже рідко / рідко» за FIBSER. Водночас спостерігалося достовірне зменшення середнього показника тяжкості ПЕ до 1,63±0,98 бала (p<0,001), що характеризувало їх як «легкі» або «дуже легкі», а також зниження функціональної обтяжливості до 1,56±0,96 бала (p<0,001).
Отримана динаміка свідчила про суттєве поліпшення профілю переносимості терапії дулоксетином. Клінічно це проявлялося зникненням або значним ослабленням седативних ефектів, редукцією когнітивних скарг (як-от уповільнення мислення, труднощі з концентрацією уваги), зменшенням відчуття загальної слабкості та нестійкості. Відновлювалася повсякденна активність, підвищувалися працездатність та соціальне функціонування пацієнтів.
На 8-му тижні лікування спостерігалося подальше зниження частоти ПЕ до 13,2±7,65% (p<0,001), що відповідало категорії «дуже рідко». Тяжкість ПЕ становила 0,93±0,63 бала (p<0,001), а функціональна обтяжливість – 0,67±0,40 бала (p<0,001), що практично відповідало відсутності клінічно значущого впливу на повсякденне функціонування. ПЕ, якщо й зберігалися, були мінімальними, короткочасними та не потребували корекції терапії.
Таким чином, отримані результати свідчать про суттєве поліпшення переносимості лікування після переходу із габапентиноїдів на дулоксетин. Редукція седативних, когнітивних, неврологічних та соматовегетативних ПЕ, пов’язаних із попередньою терапією габапентиноїдами, була пов’язана з відновленням функціональної активності пацієнтів, підвищенням рівня їхнього соціального функціонування та поліпшенням суб’єктивної якості життя.
Висновки
1. У межах дослідження було використано препарат Симода (дулоксетин) компанії «Фармліга», оскільки саме він першим з’явився на фармацевтичному ринку України та має найбільший накопичений досвід клінічного застосування серед антидепресантів цього класу. Вибір лікарського засобу також обгрунтовується такими перевагами:
- Симода виробляється із застосуванням унікальної технології «специфічна оптична ротація», що дозволяє синтезувати еталонний дулоксетин, який проходить багаторівневе очищення від сторонніх домішок та структурно невідповідних молекул; це забезпечує кращу взаємодію із рецепторами, вищу біодоступність та клінічну ефективність порівняно з іншими дулоксетинами;
- Симода є безпечним європейським дулоксетином, що не викликає канцерогенної дії за рахунок відсутності у складі капсули токсичних синтетичних харчових барвників класу Е, які є у дешевих аналогах дулоксетинів.
2. Попереднє лікування габапентиноїдами, незважаючи на застосування терапевтичних доз, характеризувалося недостатньою суб’єктивною ефективністю та клінічно значущими ПЕ за опитувальником FIBSER, що значно обмежувало функціональні результати.
3. Препарат Симода (дулоксетин) демонстрував потужний та стійкий анальгетичний ефект. Було встановлене достовірне та клінічно значуще зменшення інтенсивності больового синдрому: середній показник за ВАШ знизився із 7,41±1,30 бала на початку лікування до 2,39±1,15 бала на 8-му тижні (Δ=-5,02; p<0,001). Загальна ефективність лікування хронічного болю становила 68%, що свідчило про виразний потенціал дулоксетину в пацієнтів із недостатньою відповіддю на попередню терапію габапентиноїдами та підтвердило доцільність його застосування у комплексному веденні осіб із хронічним больовим синдромом.
4. Препарат Симода (дулоксетин) забезпечував клінічно та статистично значущу редукцію тривожної симптоматики у пацієнтів із хронічним больовим синдромом. Середній показник за опитувальником GAD‑7 достовірно знизився впродовж восьми тижнів лікування із переходом від помірного рівня тривоги (12,8±2,4 бала) до мінімального або субклінічного (5,0±1,8 бала, Δ=-6,5; p<0,001). Загальна ефективність лікування становила 54% зниження тривоги від вихідного рівня, що відповідало виразній клінічній терапевтичної відповіді.
5. При використанні Симоди (дулоксетину) мала місце статистично достовірна та клінічно значуща редукція депресивної симптоматики у пацієнтів із хронічним больовим синдромом. Впродовж восьми тижнів лікування середній показник за опитувальником PHQ‑9 знизився від рівня помірно вираженої депресії (14,93±5,54 бала) до мінімальних або субклінічних значень (4,76±2,29 бала, Δ=-10,17; p<0,001) із загальною ефективністю 68%, що відповідало значущій клінічній відповіді та наближенню до стану функціональної ремісії.
6. Застосування Симоди (дулоксетин) забезпечувало достовірне зниження впливу болю за всіма сферами опитувальника BPI‑I та відновлення соціального і психоемоційного функціонування. Показники впливу болю наблизилися до мінімального рівня, що відображало відновлення повсякденної активності (2,48±1,35 бала, Δ=-4,80; p<0,001), фізичної витривалості (2,16±1,52 бала, Δ=-4,74; p<0,001), професійної продуктивності (1,84±1,4 бала, Δ=-5,06; p<0,001) та міжособистісної взаємодії (1,61±1,25 бала, Δ=-5,22; p<0,001). Суттєве зменшення больового навантаження супроводжувалося нормалізацією сну (1,67±1,57 бала, Δ=-5,22; p<0,001), зниженням емоційної напруженості та редукцією тривожно-депресивної симптоматики (1,91±1,43 бала, Δ=-5,30; p<0,001).
7. Отримані результати засвідчили виразне поліпшення показників безпеки та переносимості терапії після заміни габапентиноїдів на Симоду (дулоксетин). Уже на 4-му тижні відзначалося достовірне зниження частоти та тяжкості ПЕ, а до 8-го тижня їх рівень наближався до мінімального або клінічно незначущого. Приймання Симоди (дулоксетину) не асоціювалося із виразною седацією, когнітивним уповільненням або астенією та сприяло відновленню фізичної активності, працездатності й соціального функціонування пацієнтів.
8. Висновки дослідження дають підстави розглядати Симоду (дулоксетин) як патогенетично обґрунтовану та клінічно ефективну терапевтичну стратегію у пацієнтів із хронічним больовим розладом за умов недостатньої відповіді на стандартні методи лікування болю, включно із застосуванням габапентиноїдів. Продемонстровані ефективність та сприятливий профіль переносимості препарату Симода (дулоксетин) підтверджують доцільність його використання в межах персоналізованої фармакотерапії при коморбідних больових та тривожно-депресивних розладах.
Отже, Симода (дулоксетин) може розглядатися як препарат із технологічними перевагами, що сприяють реалізації виразного клінічного ефекту, забезпеченню сприятливого профілю безпеки та переносимості при лікуванні хронічного болю і коморбідних тривожно-депресивних симптомів.
Література
- Dahlhamer J., Lucas J., Zelaya C., Nahin R., Mackey S., DeBar L., Kerns R., Von Korff M., Porter L., Helmick C. Prevalence of Chronic Pain and High-Impact Chronic Pain Among Adults – United States, 2016// MMWR Morb Mortal Wkly Rep. – 2018. – 67 (36). – Р. 1001‑1006; doi:10.15585/mmwr.mm6736a2.
- Xie J., Wang P., Zhang F. et al. Prevalence of chronic pain among US adults and association with mental health and opioid use // JAMA Netw Open.– 2023. – 6 (2). – e2313563; doi:10.1001/jamanetworkopen.2023.13563.
- Yong R.J., Mullins P.M., Bhattacharyya N. Prevalence of chronic pain among adults in the United States // Pain. – 2022. – 163 (2). – e328-e332; doi:10.1097/j.pain.0000000000002291.
- Murray C. J.L. Findings from the Global Burden of Disease Study 2021 // Lancet. – 2024. – 403(10440). – Р. 2259‑2262; doi:10.1016/S0140‑6736(24)00885‑0.
- Aaron R.V., Ravyts S.G., Carnahan N.D., Bhattiprolu K., Harte N., McCaulley C.C., Vitalicia L., Rogers A.B., Wegener S.T., Dudeney J. Prevalence of Depression and Anxiety Among Adults With Chronic Pain: ASystematic Review and Meta-Analysis // JAMA Netw Open. – 2025. – 8 (3).– e250268; doi:10.1001/jamanetworkopen.2025.0268.
- De La Rosa J.S., Brady B.R., Ibrahim M.M., Herder K.E., Wallace J.S., Padilla A.R., Vanderah T.W. Co-occurrence of chronic pain and anxiety/depression symptoms in U.S. adults: prevalence, functional impacts, and opportunities // Pain. – 2023. – 165 (3). – Р. 666‑673; doi:10.1097/j.pain.0000000000003056.
- Марута Н. О., Семікіна О. С., Шевченко-Бітенський К.В., Панько Т. В., Федченко В. Ю., Явдак І. О. Емоційне вигорання серед медичних працівників в галузі ментального здоров’я в умовах війни – клініко-соціальні аспекти та шляхи подолання // Український вісник психоневрології. – 2025. – 33 (1). – С. 69‑75; doi:10.36927/2079‑0325-V33-is1‑2025‑11.
- Brookfield R. Coexisting Conditions: A Discussion of Chronic Pain and Depression // Pain Manag Nurs. – 2025. – 26 (2). – e236; doi:10.1016/j.pmn.2025.01.085.
- Volcheck M.M., Graham S.M., Fleming K.C., Mohabbat A.B., Luedtke C.A. Central sensitization, chronic pain, and other symptoms: better understanding, better management // Cleve Clin J Med. – 2023. – 90 (4).– Р. 245‑254; doi:10.3949/ccjm.90a.22019.
- Moore R.A., Wiffen P.J., Derry S., Toelle T., Rice A.S.C. Gabapentin for chronic neuropathic pain and fibromyalgia in adults // Cochrane Database Syst Rev. – 2014. – (4). – CD007938; doi:10.1002/14651858.CD007938.pub3.
- Chen Q., Heinricher M.M. Descending Control Mechanisms and Chronic Pain // Curr Rheumatol Rep. – 2019. –21 (5). – Р. 13; doi:10.1007/s11926‑019‑0813‑1.
- Rugnath R., Orzechowicz C., Newell C., Carullo V., Rugnath A. ALiterature Review: The Mechanisms and Treatment of Neuropathic Pain – ABrief Discussion // Biomedicines. – 2024. – 12 (1). – Р. 204; doi:10.3390/biomedicines12010204.
- Birkinshaw H., Friedrich C.M., Cole P., Eccleston C., Serfaty M., Stewart G., White S., Moore R.A., Phillippo D.M., Pincus T. Antidepressants for pain management in adults with chronic pain: a network meta-analysis // Cochrane Database Syst Rev. – 2023. – 5. – CD014682; doi:10.1002/14651858.CD014682.pub2.
- Lam R.W., Kennedy S.H., Adams C., Bahji A., Beaulieu S. et al. Canadian Network for Mood and Anxiety Treatments (CANMAT) 2023 Update on Clinical Guidelines for Management of Major Depressive Disorder in Adults // Can J Psychiatry. – 2024. – 69 (9). – Р. 641‑687; doi:10.1177/07067437241245384.
- Bafail D., Mohammed H.E., Bady Z., Akl A.Z., Shehata M.S.A. Duloxetine for individuals with chronic back pain: A systematic review and meta-analysis of randomized controlled trials // Exp Ther Med. – 2024. – 28 (6). – Р. 448. doi:10.3892/etm.2024.12738.
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 1 (76) 2025 р.