1 жовтня, 2014
Програма безкоштовного PD-L1 тестування для пацієнтів з недрібноклітинним метастатичним раком легень стартувала в Україні
З 22 травня 2017 року пацієнти з діагнозом «недрібноклітинний метастатичний рак легень» (НДРЛ), яким за рекомендацією лікуючого онколога може бути призначено лікування імуноонкологічним лікарським засобом, можуть пройти безкоштовний тест на біомаркер PD-L1. Програма PD-L1 тестування впроваджується компанією MSD безкоштовно у спеціалізованих онкологічних центрах в Україні.
Щоб направити пацієнта з НДРЛ на безкоштовне PD-L1 тестування, лікарю слід зв’язатись із представником лабораторії CSD "Сі Ес Ді Хелс Кеа"¹ у своєму регіоні. Програма триватиме до кінця 2017 року або ж завершиться раніше у разі досягнення 1000 протестованих пацієнтів.
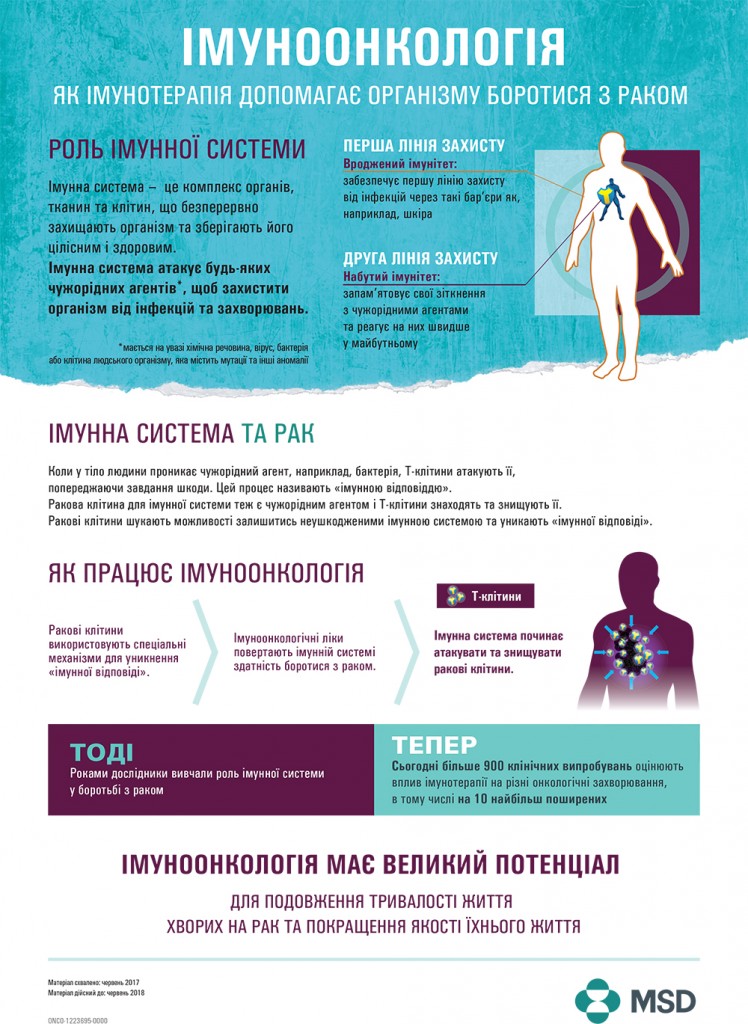
Імуноонкологічні препарати активують імунну систему організму для боротьби з раком на пізніх стадіях захворювання. Вони спрямовані на повернення клітинам імунної системи здатності розпізнавати ракові клітини та знищувати їх. Ця здатність може блокуватись раковими клітинами за допомогою білка PD-L1 та PD-L2.
Дослідження біомаркеру PD-L1 дозволяє передбачити ефективність дії імуноонкологічних ліків у пацієнтів з недрібноклітинним раком легень (НДРЛ) та допомогти лікарю-онкологу визначитись із шляхами лікування пацієнта.
Маргарита Огнівенко, керівник департаменту інноваційних лікарських засобів компанії MSD, пояснює, що за допомогою цієї програми тестування компанія прагне покращити результати медичного обслуговування пацієнтів зі складним захворюванням: «Компанія MSD працює задля того, щоб покращувати здоров’я пацієнтів. Ми усвідомлюємо, що проходження PD-L1 тестування може бути додатковою витратою для хворого з урахуванням вартості лікування загалом. Водночас цей тест є невід’ємним діагностичним інструментом. Саме визначення статусу PD-L1 дозволяє попередньо оцінити можливий позитивний ефект від призначеного імуноонкологічного лікування пацієнту з недрібноклітинним раком легень. Це в свою чергу дає лікарю та пацієнту більш повну картину для визначення подальшого лікування. Саме тому ми вирішили розгорнути всеукраїнську програму безкоштовного PD-L1 тестування. Сподіваємось, що це дасть шанс пацієнтам на продовження їхнього життя».
Онкологічні захворювання є другою найпоширенішою причиною смертності в Україні. Щорічно реєструється 170 тисяч нових випадків онкозахворювань.² 31% пацієнтів проживає менше 1-го року після встановлення діагнозу, 17% померлих – особи працездатного віку, що свідчить про беззаперечний вплив цієї патології на трудовий та репродуктивний потенціал нації². Перше місце по захворюваності та смертності серед чоловіків посідає рак легень – близько 10 000 нових випадків на рік. Понад 60% пацієнтів із раком легень не доживають і року після діагностування.²
Про MSD
MSD – один зі світових лідерів у галузі охорони здоров’я. Компанія має 125-річний досвід роботи у фармацевтичній сфері як розробник та виробник лікарських засобів і вакцин, що допомагають покращувати та зберігати здоров’я людей у більш ніж 140 країнах світу.
Імуноонкологія – пріорітетний напрямок роботи компанії. У 2014 році в США зареєстрували перший імуноонкологічний препарат «Кітруда
®», який містить пембролізумаб, здатний активувати імунну систему для боротьби з раком. MSD активно займається вивченням потенціалу застосування пембролізумабу для лікування різних видів раку. З цією метою компанія проводить одну з наймасштабніших дослідницьких програм. Більше 40 країн світу беруть участь у 500 клінічних дослідженнях для оцінки ефективності та перспектив застосування препарату Кітруда
® у лікуванні більше 30 видів пухлин.
В Україні з 2016 року препарат Кітруда
® зареєстрований та показаний для лікування нерезектабельної або метастатичної меланоми у дорослих та лікування локально прогресуючого або метастатичного недрібноклітинного раку легень у дорослих пацієнтів, у яких пухлина експресує PD-L1, та які раніше отримали як мінімум один курс хіміотерапії та/або планову терапію при позитивних мутаціях EGFR або ALK.³
КІТРУДА® (пембролізумаб), концентрат для розчину для інфузій (100 мг у флаконі)
Перед застосуванням препарату обов’язково ознайомтесь з повною інструкцією до застосування препарату КІТРУДА®. Даний матеріал призначений для спеціалістів охорони здоров’я і для розповсюдження на спеціалізованих медичних заходах та для публікації в спеціалізованих медичних виданнях. Матеріал виготовлений: червень 2017. Матеріал придатний до: червень 2017.
ТОВ «МСД Україна», адреса: 03038, м. Київ, БЦ «Горизонт Парк», вул. М.Амосова 12, 3 поверх.
Тел.: +38(044) 393-74-80; факс.: +38(044) 393-74-81
Якщо у Вас з’явилися питання стосовно препаратів компанії МСД, пишіть нам на адресу: medinfo@merck.com, або звертайтесь на http://medical-msd.com
Авторські права ©[2017] ТОВ «МСД Україна». Всі права захищені.
ONCO-1222435-0000
Посилання:
- http://csdclinic.com.ua/
- http://unci.org.ua/spetsialistam/nacionalnij-kancer-reyestr/
- Інструкція до застосування препарату Кітруда®. Реєстраційне посвідчення № UA/15484/01/01, наказ МОЗ №987 від 21.09.2016 року.



