28 січня, 2021
Стан антибіотикорезистентності в Україні: результати дослідження АУРА. Частина 1.
Перейти до частини 2 >>
У статті представлено результати визначення чутливості до 23 антибактеріальних препаратів на підставі мікробіологічних досліджень патологічного вмісту ран при інфекціях шкіри та м’яких тканин, інтраабдомінальних інфекціях, інфекціях кісток та суглобів.
Ключові слова: антибіотикорезистентність, метицилін-резистентні S. aureus, метицилін-чутливі S. aureus, антибактеріальні препарати, β-лактамази розширеного спектра дії.
 Відкриття і впровадження у клінічну практику антибіотиків стало найбільшим досягненням медицини ХХ століття. За різними оцінками, воно дозволило збільшити тривалість життя людей приблизно на 10 років [1]. Однак поява й поширення резистентності до антибіотиків у багатьох видів бактерій завдала непоправної шкоди здоров’ю мільйонів людей і суттєво ускладнила клінічну практику. Тільки у країнах Європейського Союзу та Європейського економічного регіону 33 тис. осіб щорічно помирають від інфекцій, викликаних антибіотикорезистентними бактеріями [2].
Відкриття і впровадження у клінічну практику антибіотиків стало найбільшим досягненням медицини ХХ століття. За різними оцінками, воно дозволило збільшити тривалість життя людей приблизно на 10 років [1]. Однак поява й поширення резистентності до антибіотиків у багатьох видів бактерій завдала непоправної шкоди здоров’ю мільйонів людей і суттєво ускладнила клінічну практику. Тільки у країнах Європейського Союзу та Європейського економічного регіону 33 тис. осіб щорічно помирають від інфекцій, викликаних антибіотикорезистентними бактеріями [2].
На даний час Всесвітня організація охорони здоров’я розглядає антибіотикорезистентність як одну з найбільших проблем, що загрожують здоров’ю людей [3]. Відповідний план дій для боротьби з антибіотикорезистентністю прийнятий у Європейському Союзі [4], а для контролю і спостереження за стійкістю бактерій до антибіотиків вже понад 20 років функціонує відповідна мережа – EARS-Net (Європейська мережа зі спостереження за антибіотикорезистентністю) [5].
Надійні дані про стан антибіотикорезистентності в Україні доступні, мабуть, тільки щодо пневмококів і гемофільних паличок, причому результати спостережень в останні роки публікувалися спочатку за кордоном [6, 7]. На жаль, національної програми з нагляду та боротьби з антибіотикорезистентністю в нашій країні немає.
З грудня 2018 р. по травень 2019 р. на базі медичної лабораторії Інституту мікробіологічних досліджень (м. Київ) за підтримки корпорації «Артеріум» проводився моніторинг антибіотикорезистентності в Україні (дослідження АУРА), результати якого представлені нижче.
Матеріал і методи
Матеріалом для мікробіологічних досліджень слугував патологічний вміст ран при інфекціях шкіри та м’яких тканин, інтраабдомінальних інфекціях, інфекціях кісток і суглобів. Матеріал сіяли на ряд поживних середовищ як загального призначення, так і селективні й диференційно-діагностичні виробництва bioMerieux (Франція) і Liofilchem (Італія). Ідентифікацію отриманих культур виконували на автоматичному мікробіологічному аналізаторі Vitek MS (bioMerieux, Франція) з технологією часопролітної матрикс-асоційованої іонізації/десорбції. Чутливість до антибіотиків визначали на автоматичному мікробіологічному аналізаторі Vitek 2 Compact (bioMerieux, Франція) і за допомогою карток із певним набором антибіотиків для різних груп мікроорганізмів: ентеробактерій, стафілококів, неферментуючих мікроорганізмів, ентерококів і стрептококів.
Загалом тестувалася чутливість до 41 антибактеріального препарату, аналіз отриманих результатів проводився щодо 23 найактуальніших антибактеріальних препаратів. Крім того, через відсутність антибіотиків у картках, для визначення чутливості до цефоперазону/сульбактаму, тейкопланіну, цефтароліну, фосфоміцину використовували МIC Test Strip (градієнтний метод визначення чутливості) (Liofilchem, Італія) і ComASPTM Colistin (Liofilchem, Італія) – комерційний тест для визначення чутливості методом мікророзведень у бульйоні). Для визначення чутливості до антибіотиків використовували методологію EUCAST (Європейського комітету з визначення чутливості до антимікробних засобів). Інтерпретація отриманих результатів проводилася відповідно до критеріїв EUCAST версії 8.1 від 2018 р. і 9.0 від 2019 р. [8]. Інтерпретація чутливості до цефоперазону/сульбактаму проводилася згідно з критеріями NCCLS (документ M100-S13, 2003).
Усього за 6-місячний період для мікробіологічного дослідження було отримано 554 зразки, із них позитивними (тобто такими, із яких були висіяні мікроорганізми) виявилися 439 (79,2%). Кількість виділених із одного зразка видів бактерій коливалася від 1 до 6. Загальна кількість ізолятів становила 800.
Найбільша кількість культур «походила» із Дніпропетровської та Львівської областей (рис. 1).
Результати
З 800 виділених мікроорганізмів більшість виявилися грампозитивними (n=453; 56,6%), за якими слідували грамнегативні (n=344; 43%) бактерії і гриби роду Candida (n=3; 0,4%).
Грампозитивні бактерії
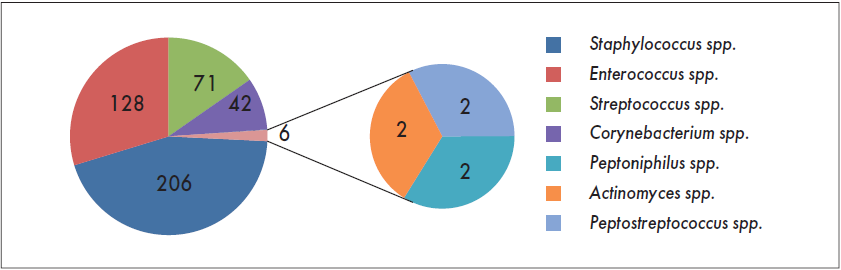
Розподіл виділених ізолятів за родами представлено на рис. 2. Серед стафілококів найчастіше зустрічалися представники виду Staphylococcus aureus (n=169), за якими, у порядку спадання, слідували: Staphylococcus haemolyticus (n=17), Staphylococcus epidermidis (n=9), Staphylococcus lugdunensis (n=6), Staphylococcus simulans (n=3) і по 1 ізоляту Staphylococcus pasteuri та Staphylococcus sciuri.
Стафілококи висівали у хворих із різними захворюваннями, серед яких частіше за інші зустрічалися діабетична стопа (28 пацієнтів), флегмона (20), абсцес підшкірно-жирової клітковини (16) і трофічна виразка (11). Понад третину всіх Staphylococcus spp. виявилися метицилін-резистентними (n=72; 35%), у тому числі майже всі S. haemolyticus (16 із 17) і S. еpidermidis (8 із 9).
Серед S. aureus частка метицилін-резистентних (MRSA) виявилася рівною 27,2% (46 ізолятів). Дані щодо чутливості S. aureus представлені окремо для чутливих до метициліну (MSSA) і MRSA (рис. 3-5).
Рис. 2. Грампозитивні мікроорганізми, виділені у хворих у дослідженні АУРА
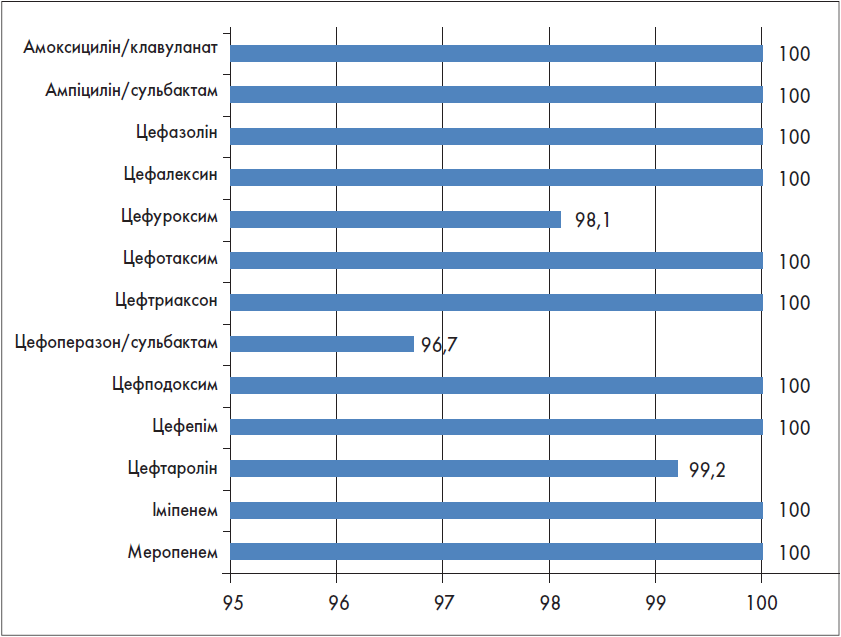
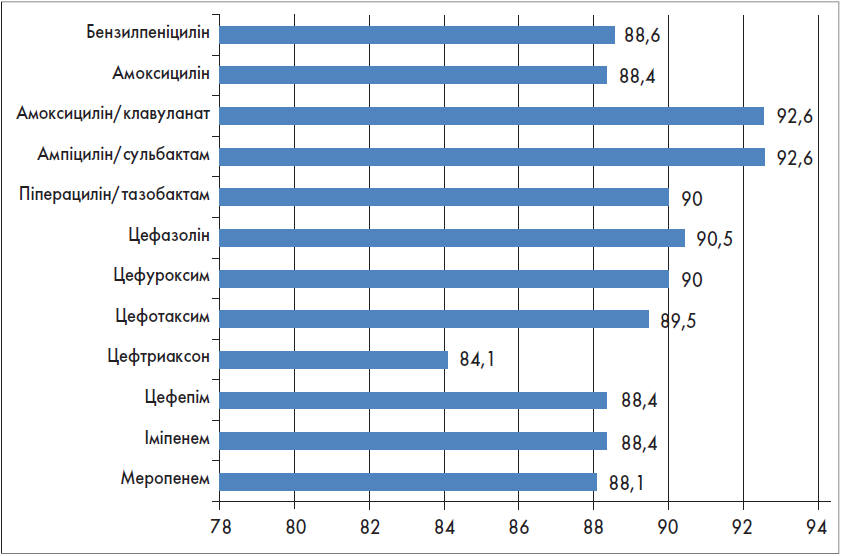
Рис. 3. Чутливість MSSA до β-лактамних антибіотиків, % (n=123)
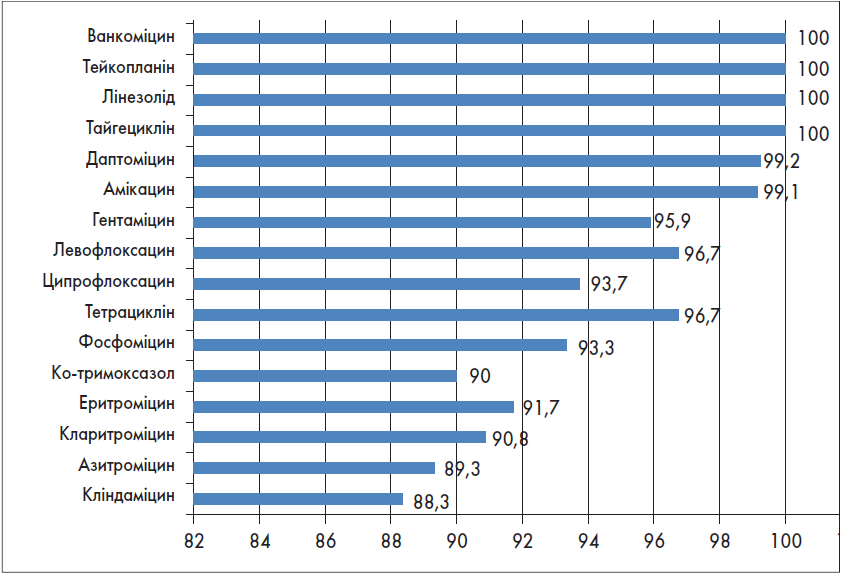
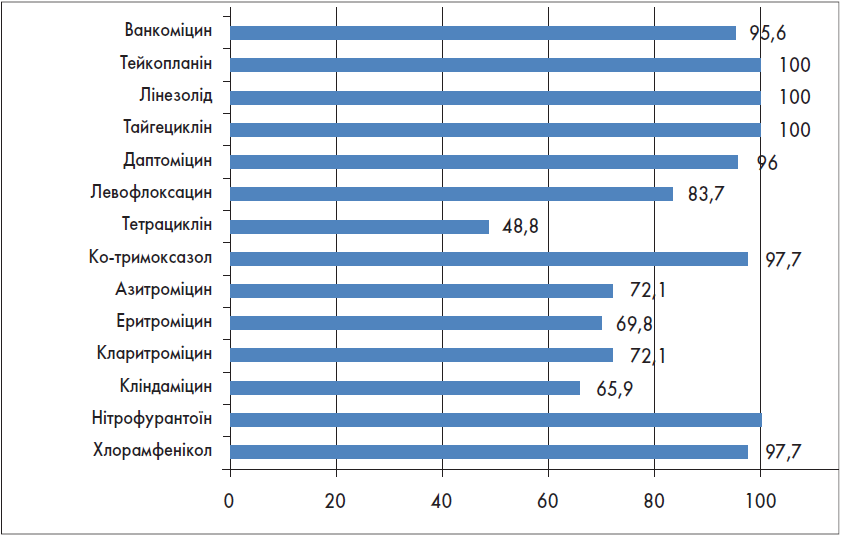
Рис. 4. Чутливість MSSA до не-β-лактамних антибіотиків,% (n=123)
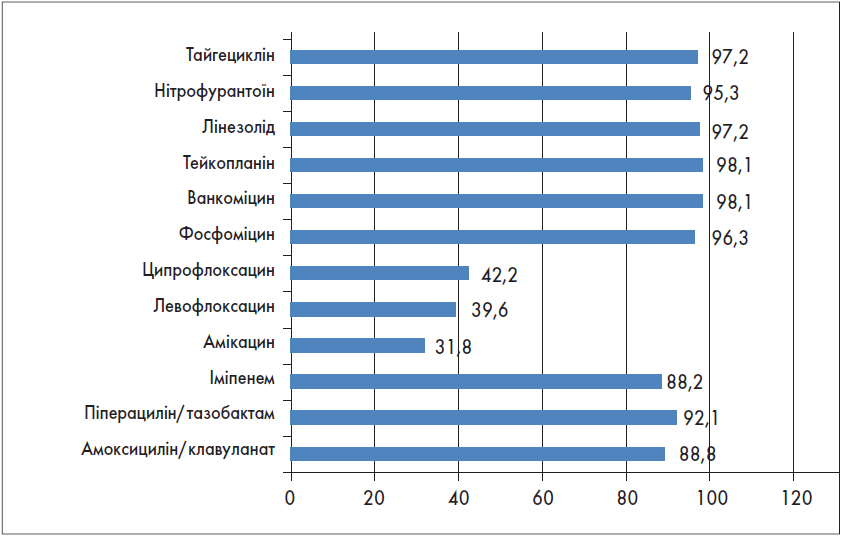
Рис. 5. Чутливість MRSA до антибіотиків,% (n = 46)
У MSSA встановлено 100%-ву чутливість майже до всіх β-лактамних антибіотиків, глікопептидів (ванкоміцин, тейкопланін), оксазолідинонів (лінезолід) і гліцилциклінів (тайгециклін). Дуже висока чутливість (>95%) зберігається до ліпопептидів (даптоміцин), аміноглікозидів (амікацин > гентаміцин), тетрацикліну, фторхінолонів (левофлоксацин > ципрофлоксацин). Чутливість MSSA до макролідів (еритроміцин > кларитроміцин > азитроміцин), лінкозамідів (кліндаміцин), ко-тримоксазолу коливається в межах 90% або трохи перевищує її (фосфоміцин).
На відміну від MSSA, метицилін-резистентні S. aureus стійкі до всіх β-лактамних антибіотиків (за винятком цефалоспоринів 5-го покоління, наприклад цефтароліну). У дослідженні АУРА встановлено дуже високу чутливість MRSA (>95%) до лінезоліду, тайгецикліну, одного із двох протестованих глікопептидів – тейкопланіну та фосфоміцину. Чутливість до іншого глікопептиду – ванкоміцину, а також до ко-тримоксазолу, даптоміцину й цефтароліну виявилася нижчою, хоча й залишалася високою (86-91%).
Серед ентерококів найчастіше виділялися Enterococcus faecalis (n=107), за якими, у порядку спадання, слідували Enterococcus faecium (n=15), Enterococcus avium (n=4), Enterococcus raffinosus (n=2).
Дуже висока чутливість у E. faecalis встановлена по відношенню до обох глікопептидів, лінезоліду, тайгецикліну, фосфоміцину й нітрофурантоїну (рис. 6). Чутливість до інгібіторозахищених пеніцилінів (піперацилін/тазобактам > амоксицилін/клавуланат) та іміпенему була дещо нижчою, у межах 88-92%.
У двох ванкоміцин-резистентних ізолятів E. faecalis було встановлено фенотип стійкості, який в обох випадках виявився VanB. Обидва ізоляти, виділені у хворих із діабетичною стопою і гострим холециститом, які проживали на Вінниччині, були чутливими до фосфоміцину і фторхінолонів (левофлоксацину й ципрофлоксацину), один із двох – до тейкопланіну або нітрофурантоїну, обидва – резистентними до лінезоліду, тайгецикліну, пеніцилінів та амікацину.
У E. faecium 100%-ву чутливість встановлено до ванкоміцину, лінезоліду й тайгецикліну (рис. 7). По одному ізоляту були стійкими до тейкопланіну та фосфоміцину.
Із 71 ізолята Streptococcus spp. 31 ідентифікований як Streptococcus agalactiae, 12 – Streptococcus pyogenes, 8 – Streptococcus anginosus, 6 – Streptococcus mitis, 5 – Streptococcus salivarius, 3 – Streptococcus constellatus, 2 – Streptococcus sanguinis, по одному ізоляту – Streptococcus pneumoniae, Streptococcus gallolyticus, Streptococcus intermedius та Streptococcus parasanguinis.
Чутливість Streptococcus spp. щодо протестованих β-лактамів була високою і загалом порівнянною (88-93%) (рис. 8). Дещо меншу чутливість стрептококів виявлено щодо цефтриаксону (84%).
Серед не-β-лактамних антибіотиків 100%-ву чутливість Streptococcus spp. встановлено до лінезоліду, тайгецикліну, одного із двох глікопептидів – тейкопланіну, а також нітрофурантоїну. Дуже високу чутливість (>95%) виявлено щодо ко-тримоксазолу, хлорамфеніколу, даптоміцину й ванкоміцину (рис. 9).
Більшість із 42 ізолятів Corynebacterium spp. припадало на частку Corynebacterium striatum – 37, інші були представлені Corynebacterium simulans – 2 і по 1 ізоляту – Corynebacterium propinquum, Corynebacterium xerosis та Corynebacterium tuberculostearicum.
Дані про антибіотикочутливість дифтероїдів не наводяться, оскільки клінічного значення при інфекціях шкіри та м’яких тканин (за винятком еритразми), інтраабдомінальних інфекціях та інфекціях кісток і суглобів ці бактерії не мають і, ймовірно, потрапляли у тестовані зразки в результаті контамінації. Слід підкреслити, що в дослідженні АУРА не ставилося за мету вивчити титр (кількість колонієутворюючих одиниць бактерій в 1 мл або в 1 г матеріалу) або оцінити етіологічну значущість виділених мікроорганізмів.
У зв’язку з малою кількістю ізолятів інших грампозитивних бактерій (по два штами Peptoniphilus spp., Actinomyces spp. і Peptostreptococcus spp., усього 6 ізолятів) дані про їх чутливість до антибіотиків не наводяться.
Рис. 6. Чутливість E. faecalis до антибіотиків, % (n=107)
Рис. 7. Чутливість E. faecium до антибіотиків,% (n=15)
Рис. 8. Чутливість Streptococcus spp. до β-лактамів, % (n=71)
Рис. 9. Чутливість Streptococcus spp. до не-β-лактамних антибіотиків, % (n=71)
Грамнегативні бактерії
Більшість виділених ізолятів грамнегативних мікроорганізмів належали до сімейства Enterobacteriaceae (n=174) і неферментуючих бактерій (n=150). Решта були представлені одиничними ізолятами в кількості не більше двох (Pantoea agglomerans, Achromobacter xylosoxidans) або максимум трьох (Alcaligenes faecalis).
Представники сімейства Enterobacteriaceae. Escherichia coli. Усього виділено 47 ізолятів. Високу чутливість (92-94%) встановлено до нітрофуранів (нітрофурантоїн), поліміксину (колістин), епоксидів* (фосфоміцин), карбапенемів (меропенем, ертапенем), трохи нижчу (87%) – до інгібіторозахищених цефалоспоринів 3-го покоління (цефоперазон/сульбактам), рис. 10).
Чотирнадцять ізолятів E. coli (29,8%) продукували β-лактамази розширеного спектра дії (БЛРС). Вони виявилися абсолютно нечутливими до цефалоспоринів 3-, 4- і 5-го поколінь і захищених амінопеніцилінів. Нульову або близьку до неї чутливість встановлено до фторхінолонів. Висока чутливість у цих ізолятів зберігалася до карбапенемів і нітрофурантоїну (93%), трохи нижча (86%) – до цефоперазону/сульбактаму, фосфоміцину й колістину (рис. 11). Єдиний карбапенем-резистентний ізолят E. coli, який виробляв БЛРС, був чутливим до всіх аміноглікозидів і нітрофурантоїну.
В одного хворого із вторинним перитонітом на Львівщині було виділено E. coli, що виробляла метало-β-лактамази. Цей ізолят був резистентним до всіх β-лактамних антибіотиків (включаючи карбапенеми), фторхінолонів, аміноглікозидів, ко-тримоксазолу й нітрофурантоїну і зберігав чутливість тільки до колістину й фосфоміцину.
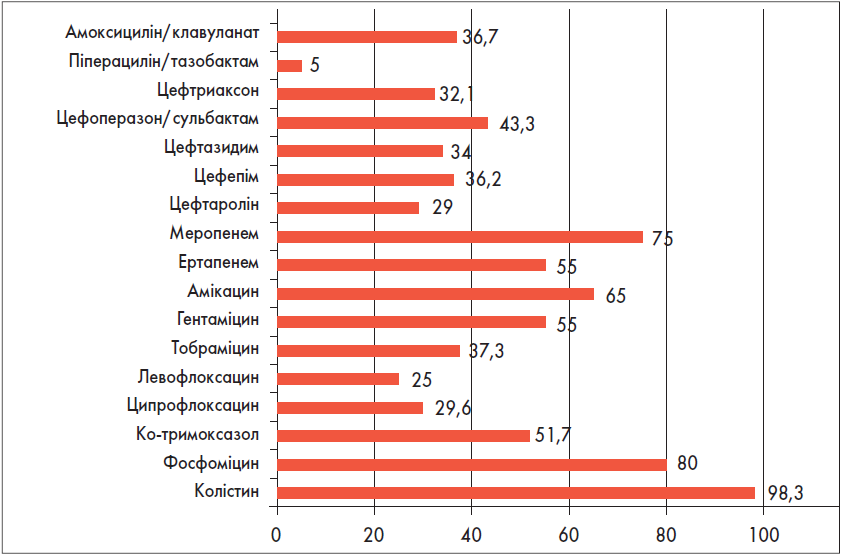
Klebsiella spp. виділялася частіше за інші ентеробактерії: усього отримано 60 штамів (K. pneumoniae – 51, K. oxytoca – 8, K. aerogenes – 1). На жаль, клебсієли зберігають дуже високу чутливість тільки до колістину (98%). Рівень чутливості до фосфоміцину й меропенему не перевищував 75-80%, а до препаратів інших класів – був іще нижчим (рис. 12).
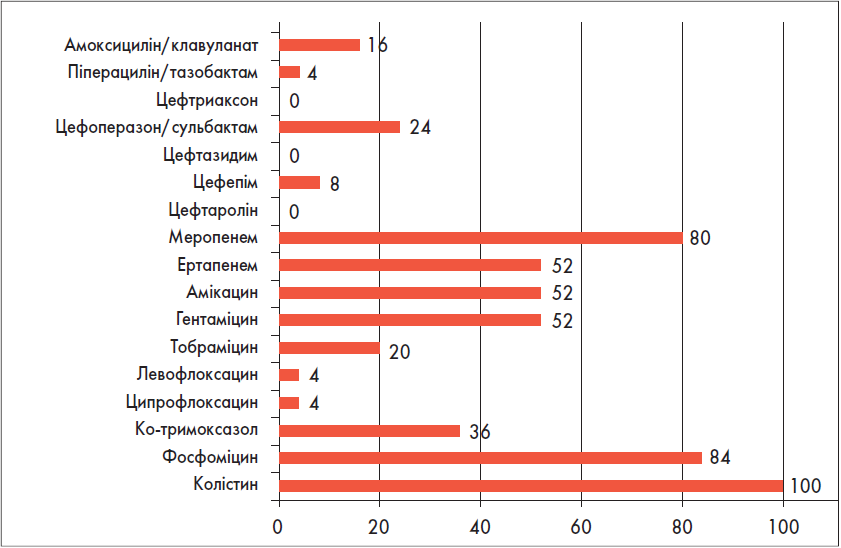
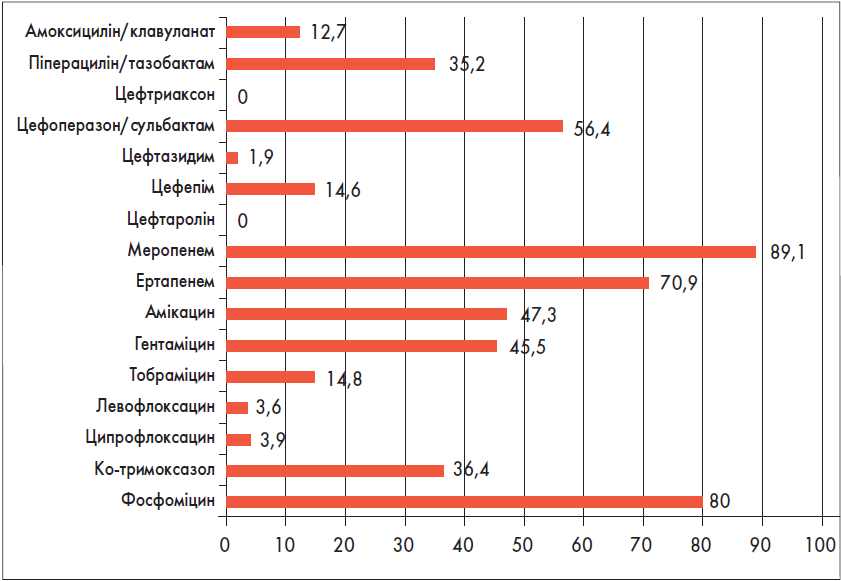
Вироблення БЛРС виявлено у 25 ізолятів (24 – K. pneumoniae, 1 – K. aerogenes). Усі вони виявилися чутливими до колістину (рис. 13). Чутливість до фосфоміцину й меропенему коливалася в межах 80-84%.
В одного пацієнта із синдромом діабетичної стопи, який проживає на Вінниччині, виділено штам K. pneumoniae, що виробляє метало-β-лактамази. Він виявився чутливим тільки до колістину. До всіх інших тестованих антибіотиків – β-лактамів (включно з карбапенемами), фосфоміцину, фторхінолонів, аміноглікозидів, ко-тримоксазолу – даний штам був резистентним.
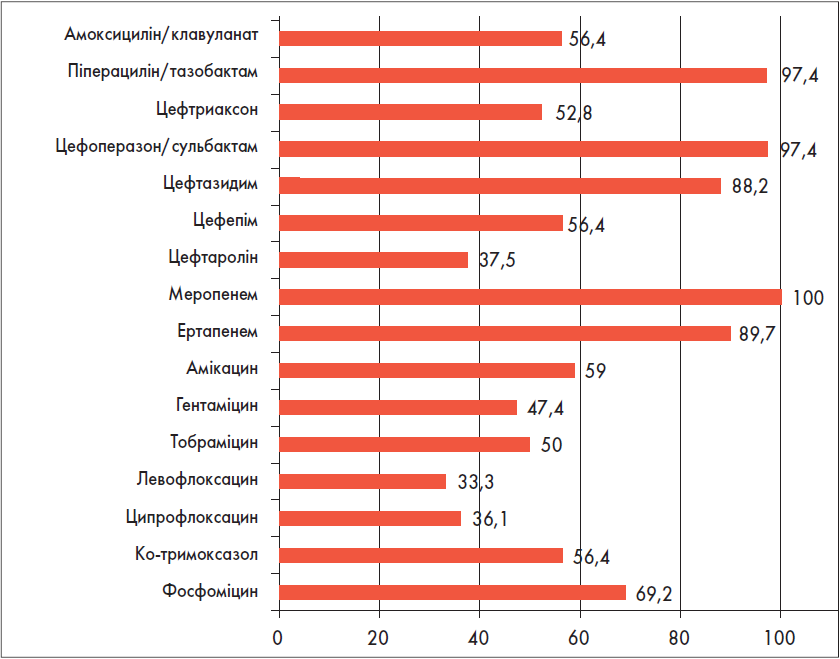
Виділені ізоляти Proteus spp. (n=39) розподілилися наступним чином: 36 – Proteus mirabilis, 2 – Proteus vulgaris, 1 – Proteus penneri. Усі вони виявилися чутливими до меропенему (рис. 14). Дуже високу чутливість зареєстровано щодо цефоперазону/сульбактаму та піперациліну/тазобактаму (97%), високу – до ертапенему і цефтазидиму (близько 90%).
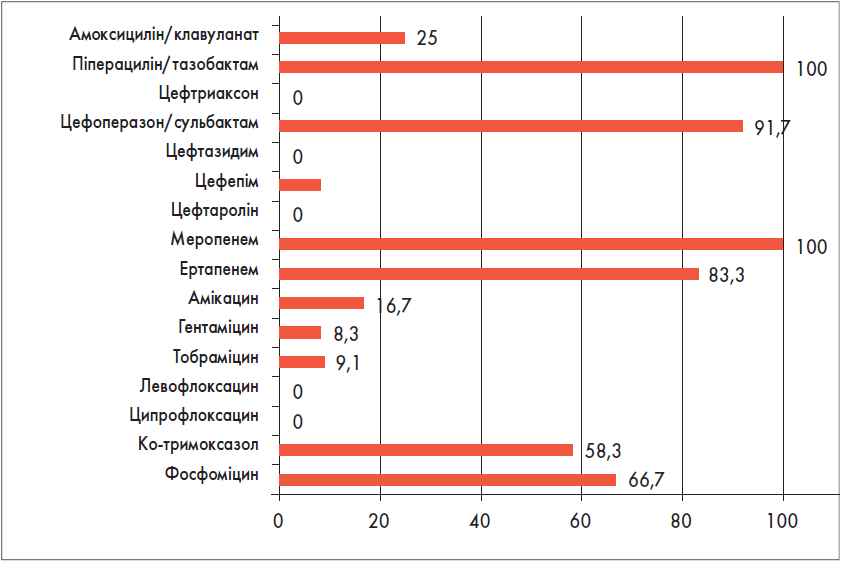
Вироблення БЛРС встановлено у 12 штамів (11 – P. mirabilis, 1 – P. vulgaris). Усі вони були чутливими до меропенему й піперациліну/тазобактаму (рис. 15). Чутливість до цефоперазону/сульбактаму була нижчою, але залишалася високою (близько 92%).
Інші ентеробактерії. Усього виділено 28 ізолятів: Enterobacter cloacae (n=11), Citrobacter freundii (n=7), Morganella morganii (n=6), Serratia marcescens (n=3) і Enterobacter asburiae (n=1). Найбільш чутливими вони були до меропенему (близько 90%) і колістину (85%) (рис.16). Продукцію БЛРС виявлено у 4 ізолятів (3 – E. cloacae, 1 – M. morganii). З огляду на малу кількість таких штамів дані про антибіотикочутливість не наводяться. Можна лише відзначити, що всі продуценти БЛРС були чутливими до меропенему.
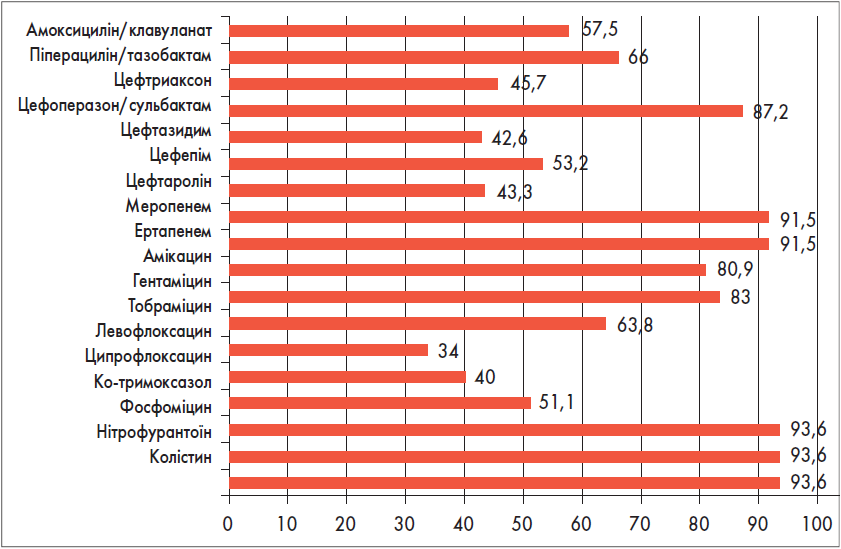
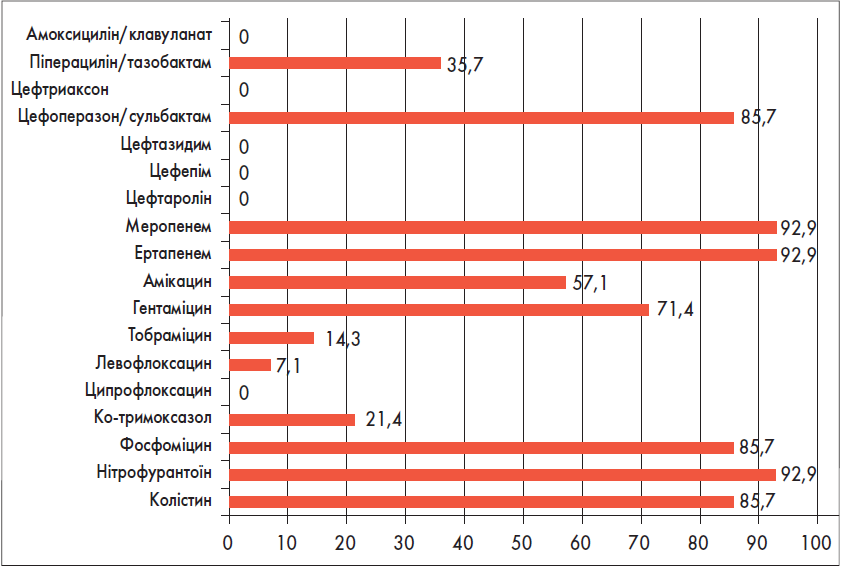
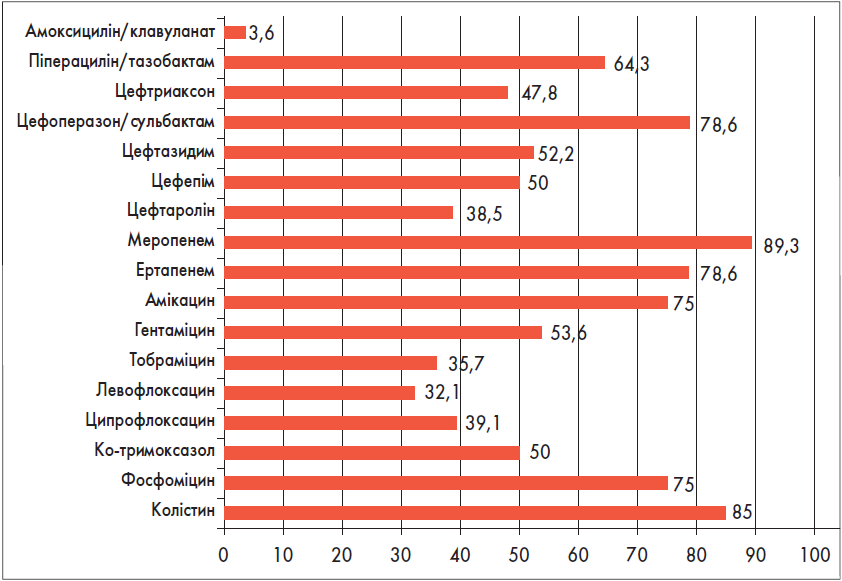
Для загального уявлення про антибіотикочутливість ентеробактерій-продуцентів БЛРС отримані дані зведено на рис. 17. Найактивнішим антибіотиком виявився меропенем (89%), за яким із відривом слідували фосфоміцин (80%) та ертапенем (71%).
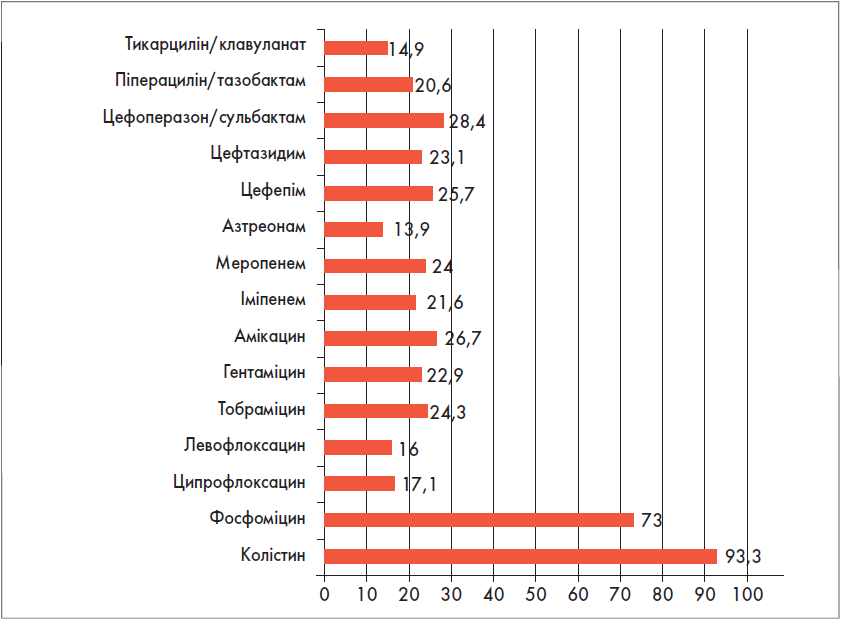
Неферментуючі бактерії. Усього було виділено 157 ізолятів: по 75 – Pseudomonas spp. і Acinetobacter spp., 7 – Stenotrophomonas maltophilia. Pseudomonas spp. були представлені P. aeruginosa (n=72), P. putida (n=2) і P. stutzeri (n=1). Псевдомонади зберігали високу чутливість тільки до колістину (93%), за яким із великим відривом слідував фосфоміцин (73%). На жаль, чутливість Pseudomonas spp. до жодного іншого антибіотика, включаючи карбапенеми, не досягала 30% (рис. 18).
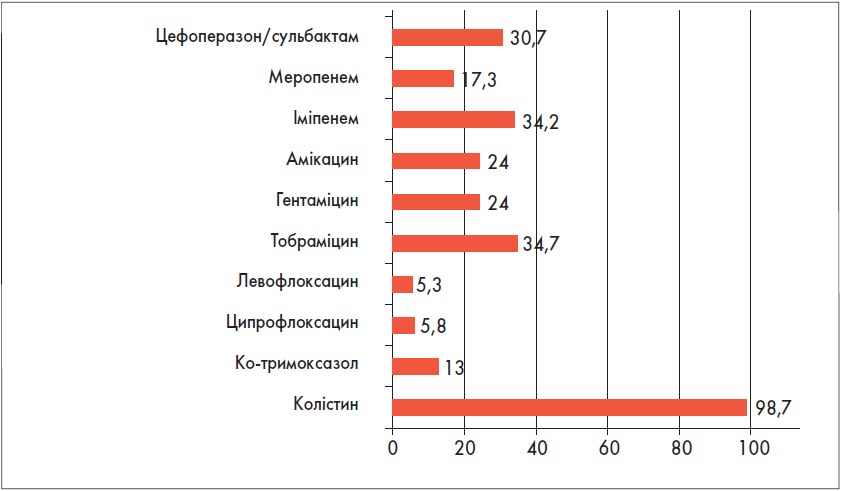
Із 75 ізолятів Acinetobacter spp. 72 припадало на Acinetobacter baumannii. Крім того, було виділено два штами Acinetobacter johnsonii й один – Acinetobacter haemolyticus. Як і у випадку з Pseudomonas spp., високу чутливість ацінетобактер зберігали тільки до колістину (99%). Говорити про значну чутливість Acinetobacter spp. до антибіотиків інших класів, на жаль, не доводиться (рис. 19).
Stenotrophomonas maltophilia. Чутливість цього мікроорганізму тестували до 4 антибіотиків. Вона виявилася рівною 85,7% по відношенню до ко-тримоксазолу й левофлоксацину і 71,4% – до цефтазидиму та тикарциліну/клавуланату.
Рис. 10. Чутливість E. coli до антибіотиків,% (n=47)
Рис. 11. Чутливість до антибіотиків (%) штамів E. coli, які виробляли БЛРС
Рис. 12. Чутливість Klebsiella spp. до антибіотиків,% (n=60)
Рис. 13. Чутливість до антибіотиків (%) штамів Klebsiella spp., які виробляють БЛРС (n=25)
Рис. 14. Чутливість Proteus spp. до антибіотиків, % (n=39)
Рис. 15. Чутливість до антибіотиків (%) штамів Proteus spp., які виробляють БЛРС (n=12)
Рис. 16. Чутливість до антибіотиків штамів Enterobacter spp., C. freundii, M. morganii та S. marcescens, % (n=28)
Рис. 17. Чутливість до антибіотиків усіх штамів представників сімейства Enterobacteriaceae, які виробляли БЛРС (E. coli + Klebsiella spp. + Proteus spp. + E. cloacae + M. morganii), % (n=55)
Рис. 18. Чутливість Pseudomonas spp. до антибіотиків, % (n=75)
Рис. 19. Чутливість Acinetobacter spp. до антибіотиків, % (n=75)
Продовження в наступному номері. Перейти до частини 2 >>
Тематичний номер «Хірургія, Ортопедія, Травматологія, Інтенсивна терапія» № 4 (42), 2020 р.