1 квітня, 2026
Оцінювання аугментації бупропіоном у пацієнтів із великим депресивним розладом за недостатньої відповіді на СІЗЗС/СІЗЗСН: вплив на ангедонію та астенію
Великий депресивний розлад (ВДР) посідає провідне місце серед причин втрати працездатності, зниження якості життя та соціального функціонування у популяції, що зумовлює його суттєву медико-соціальну значущість. Незважаючи на наявність сучасних антидепресивних засобів, досягнення повної клінічної ремісії в межах стандартної фармакотерапії залишається складним клінічним завданням [1]. У реальній клінічній практиці в значної кількості пацієнтів спостерігається часткова або недостатня відповідь на лікування селективними інгібіторами зворотного захоплення серотоніну (СІЗЗС) або селективними інгібіторами зворотного захоплення серотоніну й норадреналіну (СІЗЗСН), що зумовлює збереження залишкової (резидуальної) афективної симптоматики та підтримання функціональних обмежень [2, 3].
У структурі резидуальних симптомів особливе клінічне значення мають ангедонія та астенічний симптомокомплекс (втомлюваність, знижена денна активність, виснаження когнітивних функцій). Вони пов’язані з гіршим прогнозом, нижчою прихильністю до лікування та повільнішим відновленням соціального й професійного функціонування пацієнтів [4].
Додатковим чинником, що обмежує користь від лікування, є побічні ефекти (ПЕ) СІЗЗС/СІЗЗСН, зокрема сексуальна дисфункція, а також потенційне посилення симптомів емоційного притуплення, апатії, астенії та ангедонії, що може маскувати або збільшувати залишкові прояви депресії. У цьому контексті терапевтичні стратегії, спрямовані на зниження ангедонії та астенії при збереженні сприятливої переносимості, є актуальними як із позицій досягнення ремісії, так і відновлення якості життя пацієнтів [5].
Однією з найбільш практично значущих стратегій оптимізації лікування у пацієнтів із недостатньою відповіддю на СІЗЗС/СІЗЗСН є підсилення (аугментація) бупропіоном – антидепресантом із норадренергічно-дофамінергічним механізмом дії. Теоретичні підстави для такого підходу полягають у тому, що ангедонія й астенія значною мірою пов’язані з дисфункцією системи винагороди, мотивації та енергетичної регуляції, де дофамінергічні й норадренергічні механізми відіграють ключову роль [6].
Ефективність посилення бупропіоном після недостатньої відповіді на СІЗЗС вивчалася у масштабних клінічних дослідженнях [7]. Зокрема, М. Н. Trivedi et al. (2006) встановили клінічну доцільність додавання бупропіону пацієнтам, які не досягли адекватної відповіді на СІЗЗС [8]. Також С. DeBattista et al. (2003) підтвердили користь додавання бупропіону в межах відкритого проспективного дослідження аугментації препаратом в осіб із частковою відповіддю на серотонінергічні антидепресанти або її відсутністю [9].
Водночас у наявній літературі недостатньо висвітленим залишається питання комплексного впливу аугментації бупропіоном саме на ангедонію та астенічні прояви у пацієнтів із ВДР та недостатньою відповіддю на СІЗЗС/СІЗЗСН під час стандартизованого клінічного спостереження з оцінюванням ефективності й переносимості. У цьому контексті було проведене дослідження з метою оцінити вплив додавання бупропіону до поточної антидепресивної терапії СІЗЗС або СІЗЗСН в осіб із ВДР за недостатньої відповіді на лікування, із фокусом на ангедонії та астенії.
Матеріали й методи дослідження
Шеститижневе проспективне відкрите обсерваційне наукове дослідження було виконане на кафедрі психіатрії, психотерапії, наркології та медичної психології Донецького національного медичного університету (м. Кропивницький). Всі пацієнти до включення у дослідження надали письмову інформовану згоду відповідно до вимог етичних стандартів та положень, викладених в Інформованій згоді пацієнта.
У межах дослідження пацієнтам проводили аугментацію базової антидепресивної терапії шляхом додавання препарату Бупрінол (бупропіону гідрохлорид) у дозі 150 мг/добу в формі таблеток із модифікованим вивільненням. Бупрінол призначали як додатковий засіб до стабільної терапії СІЗЗС або СІЗЗСН без зміни типу та дозування основного антидепресанту впродовж усього періоду спостереження.
Клінічне та психометричне оцінювання проводили на чотирьох часових етапах: на вихідному візиті (день 0) перед початком аугментації, на візиті 2 (2-й тиждень лікування), на візиті 3 (4-й тиждень лікування) та на візиті 4 (6-й тиждень лікування), який відповідав завершенню періоду спостереження. Аналіз клінічної ефективності лікування здійснювали із застосуванням стандартизованих психометричних інструментів. Виразність депресивної симптоматики визначали за допомогою анкети психічного здоров’я PHQ‑9 [10]. Рівень ангедонії оцінювали із використанням шкали Снейта–Гамільтона (SHAPS), тоді як астенічні прояви та втомлюваність – за допомогою суб’єктивної шкали оцінювання астенії (MFI‑20), що дозволяє аналізувати як загальний рівень астенії, так і окремі її домени [11, 12].
Безпеку та переносимість терапії визначали шляхом систематичної реєстрації ПЕ на тлі приймання антидепресантів на кожному візиті за анкетою для оцінювання частоти, інтенсивності та тягаря побічних ефектів (FIBSER) [13]. Обов’язковим компонентом клінічного спостереження було оцінювання суїцидального ризику.
Додатково, з метою визначення впливу ВДР на суб’єктивне благополуччя та повсякденне функціонування пацієнтів, рівень якості життя оцінювали на вихідному візиті (день 0) та на візиті завершення дослідження (6-й тиждень) із застосуванням короткої форми опитувальника щодо задоволеності якістю життя (Q-LES-Q-SF). Даний інструмент дозволяє кількісно оцінити рівень задоволеності пацієнтів ключовими сферами життєдіяльності, зокрема фізичним здоров’ям, емоційним станом, професійною або повсякденною діяльністю, домашньою активністю, соціальними й сімейними стосунками, сексуальним життям, загальним відчуттям благополуччя, задоволеністю від медикаментозної терапії, здатністю до концентрації уваги, рівнем енергії та життєвого тонусу, а також інтегральним показником якості життя.
Первинні кінцеві точки оцінки:
- зміна сумарного бала шкали ангедонії за шкалою SHAPS від дня 0 до тижня 6;
- зміна доменів / сумарного показника за шкалою MFI‑20 від дня 0 до тижня 6.
Вторинні кінцеві точки:
- зміна депресивної симтпоматики та загальна ефективність за анкетою PHQ‑9 від дня 0 до тижня 6;
- зміна показників суб’єктивого благополуччя та якості життя під час лікування від дня 0 до тижня 6 за опитувальником Q-LES-Q-SF;
- динаміка переносимості та безпеки лікування за анкетою FIBSER.
Критерії включення:
- Вік від 18 до 80 років.
- Діагноз ВДР згідно з Діагностичним та статистичним посібником із психічних розладів 5-го перегляду (DSM‑V) або первинний чи рекурентний депресивний розлад за Міжнародною класифікацією хвороб 10-го перегляду (МКХ‑10).
- Недостатня або часткова відповідь на поточну антидепресивну терапію СІЗЗС чи СІЗЗСН, яку проводили у стабільній дозі протягом щонайменше 4‑6 тижнів. Недостатня реакція на лікування визначалася як зниження виразності депресивної симптоматики в межах 25‑50% від вихідного рівня, що відповідало частковій клінічній відповіді. При цьому в пацієнтів зберігалися клінічно значущі резидуальні симптоми депресії, зокрема афективні та когнітивні порушення, що зумовлювали зниження функціональної спроможності.
- Наявність в анамнезі щонайменше одного попереднього курсу антидепресивної терапії; поточний антидепресант не був першим призначенням у лікуванні першого депресивного епізоду.
- Наявність клінічно значущих проявів ангедонії та/або астенії на момент включення за шкалами SHAPS і MFI‑20.
- Здатність надати письмову інформовану згоду та виконувати процедури дослідження.
Критерії виключення:
- Тяжка депресія із суїцидальними ідеями або високий суїцидальний ризик під час дослідження.
- Біполярний афективний розлад, психотичні й органічні психічні розлади.
- Психічний розлад унаслідок вживання психоактивних речовин.
- Тяжкі неконтрольовані соматичні стани, що можуть викликати втомлюваність або астенію незалежно від депресії.
- Клінічно значуща та неконтрольована артеріальна гіпертензія.
- Судомні стани в анамнезі або інші суттєві фактори ризику судом під час дослідження.
- Зміна базового антидепресанту СІЗЗС/СІЗЗСН або його дози впродовж періоду спостереження.
Математично-статистичний метод дослідження проводили за допомогою програмного забезпечення Microsoft Excel 2019. Кількісні математичні зміни наведені як середне значення (М) та стандартне відхилення (SD). Порівняння кількісних показників між двома незалежними групами виконували із застосуванням непараметричного критерію Манна–Уїтні. Рівень статистичної значущості вважали досягнутим при p<0,05.
Результати дослідження та обговорення
У таблиці 1 наведені основні соціально-демографічні характеристики пацієнтів, включених у дослідження, та основні клініко-анамнестичні дані.
|
Таблиця 1. Соціально-демографічні та клініко-анамнестичні характеристики пацієнтів (n=42) |
|
|
Показник |
Значення |
|
Вік, роки (M±SD) Мin/max, рік |
38,4±12,6 20‑77 |
|
Стать, n (%) Чоловіки Жінки |
14 (33,3%) 28 (66,7%) |
|
Сімейний стан, n (%) Одружені Неодружені Розлучені |
23 (54,8%) 14 (33,3%) 5 (11,9%) |
|
Освіта, n (%) Вища Середня спеціальна |
26 (61,9%) 16 (38,1%) |
|
Зайнятість, n (%) Працюють Не працюють Пенсіонери за віком |
21 (50%) 19 (45,2%) 2 (4,8%) |
|
Місце проживання, n (%) Міська місцевість Сільська місцевість |
38 (90,5%) 4 (9,5%) |
|
Тривалість поточного депресивного епізоду, місяці (M±SD) Мin/max, місяць |
6,1±3,2 2‑18 |
|
Кількість депресивних епізодів в анамнезі (M±SD) Діапазон |
2,38±1,62 1‑7 |
|
Вік початку ВДР, роки (M±SD) Мin/max, рік |
33,9±9,5 17‑58 |
|
Тривалість ВДР, місяці (M±SD) |
25,4±28,6 |
|
Нозологічна форма ВДР за МКХ‑10, n (%) Первинний депресивний епізод (F32) Легкий (F32.0) Помірний (F32.1) Тяжкий без психотичних симптомів (F32.2) Рекурентний депресивний розлад (F33) Легкий поточний епізод (F33.0) Помірний поточний епізод (F33.1) Тяжкий поточний епізод (F33.2) |
16 (38,1%) 3 (7,1%) 9 (21,4%) 4 (9,5%) 26 (61,9%) 1 (2,4%) 16 (38,1%) 9 (21,4%) |
|
Психіатрична коморбідність, n (%) Будь-яка коморбідність Тривожні розлади Зловживання психоактивними речовинами Посттравматичний стресовий розлад Відсутня |
26 (61%) 20 (48,8%) 3 (7,3%) 2 (4,9%) 16 (39%) |
|
Фармакотерапія ВДР, n (%) Есциталопрам, 10‑20 мг/добу Сертралін, 50‑150 мг/добу Пароксетин, 20‑40 мг/добу Венлафаксин, 75‑150 мг/добу Дулоксетин, 60 мг/добу |
20 (48,8%) 11 (26,8%) 6 (14,6%) 3 (7,3%) 2 (4,9%) |
|
Відповідь на антидепресанти (6‑8 тижнів), n (%) Часткова відповідь (25‑45% зниження симптомів) Відсутність відповіді (<25% зниження симптомів) |
35 (83,3%) 6 (14,3%) |
Середній вік обстежуваних становив 38,4±12,6 року, що свідчило про значну вікову варіабельність із переважанням осіб молодого та середнього дорослого віку. За статтю вибірка була представлена 14 (33,3%) чоловіками та 28 (66,7%) жінками, що відповідало загальновідомій тенденції до більшої поширеності депресивних розладів серед жінок.
Середня тривалість поточного депресивного епізоду становила 6,1±3,2 місяця, із мінімальним значенням два місяці та максимальним – 18 місяців, що вказувало на наявність як відносно коротких, так і затяжних депресивних епізодів. Кількість депресивних епізодів в анамнезі коливалася від 1 до 7, при середньому значенні 2,38±1,62, що свідчило про переважання рекурентного перебігу ВДР у більшості пацієнтів.
Відповідно до діагностичних критеріїв МКХ‑10, у структурі вибірки переважали помірні та тяжкі депресивні стани із домінуванням рекурентного перебігу.
Аналіз коморбідної психіатричної патології продемонстрував, що у 61% пацієнтів були наявні супутні психічні захворювання – тривожні розлади (48,8%), залежність від психоактивних речовин (7,3%) та посттравматичний стресовий розлад (4,9%).
Усі пацієнти з метою лікування ВДР отримували антидепресанти груп СІЗЗС та СІЗЗСН у терапевтичних дозах – есциталопрам (48,8%), сертралін (26,8%), пароксетин (14,6%), венлафаксин (7,3%) та дулоксетин (4,9%). Оцінювання ефективності терапії показало, що у переважної більшості пацієнтів (83,3%) спостерігалася часткова відповідь на лікування, яка характеризувалася зниженням виразності депресивної симптоматики на 25‑45% упродовж 6‑8 тижнів терапії. Водночас у 14,3% учасників відзначалася відсутність клінічно значущої відповіді на антидепресанти, що проявлялося зменшенням симптомів депресії менш ніж на 25% за аналогічний період лікування. Це свідчило про наявність клінічно значущої групи пацієнтів із недостатньою ефективністю стандартної антидепресивної терапії.
Зміна середнього бала депресивної симптоматики за PHQ‑9
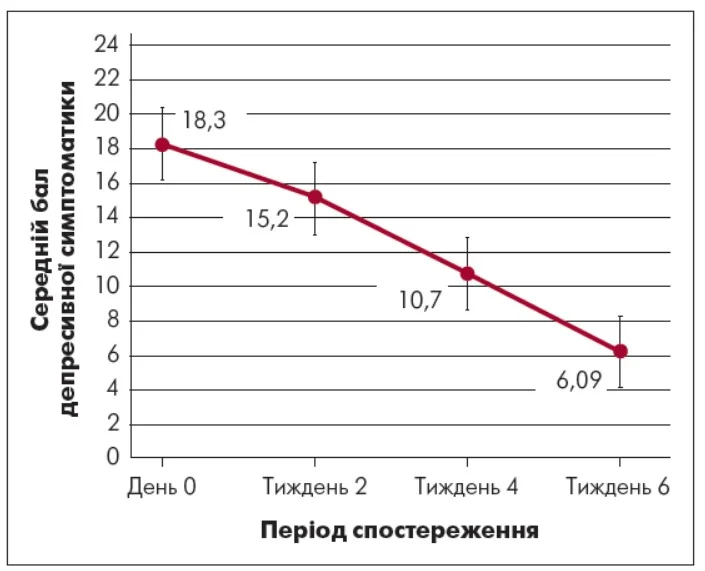
Ефективність додавання бупропіону до СІЗЗС/СІЗЗСН у разі недостатньої відповіді на антидепресанти при лікуванні ВДР оцінювали за зміною середнього бала депресивної симптоматики за анкетою PHQ‑9 впродовж шести тижнів спостереження (рис. 1).
Примітки: 0‑4 балів – мінімальні симптоми / відсутність; 5‑9 балів – легка депресія; 10‑14 – помірна депресія; 15‑19 балів – помірно тяжка депресія; 20‑27 балів – тяжка депресія.
Рис. 1. Динаміка редукції депресивної симптоматики при додаванні бупропіону до СІЗЗС/СІЗЗСН за PHQ‑9
На початку дослідження (день 0) середній сумарний бал за PHQ‑9 становив 18,3±4,66, що відповідало помірно тяжкому рівню депресивної симптоматики. Клінічно це проявлялося постійним відчуттям смутку, емоційної порожнечі, внутрішньої безнадійності та суттєвим зниженням або повною втратою здатності отримувати задоволення від раніше приємних занять. Ангедонічні прояви були стійкими та становили один із центральних і найбільш обтяжливих симптомів депресивного епізоду.
Втомлюваність і зниження енергії на початку дослідження були виразними та носили стійкий характер. Виснажуваність виникала навіть за мінімальних фізичних або розумових навантажень і не зникала після відпочинку, що призводило до суттєвого обмеження функціональної спроможності. Когнітивні порушення включали труднощі з концентрацією уваги, уповільнення мислення та зниження здатності приймати рішення, що додатково посилювало дезадаптацію. Проблеми зі сном мали переважно інсомнічний характер і проявлялися труднощами засинання, нічними та ранніми пробудженнями. При цьому сон не приносив відчуття відновлення, що підтримувало денну втомлюваність і поглиблювало астенічні прояви.
Вже на 2-му тижні лікування Бупрінолом (бупропіоном) у дозі 150 мг/добу було зафіксоване статистично достовірне зниження середнього показника за PHQ‑9 до 15,2±3,56 (Δ=-3,15; p<0,05), що свідчило про ранню позитивну динаміку. На цьому етапі першочергово зменшувалися суб’єктивне відчуття енергетичного дефіциту, втрати інтересу й задоволення і зниження апатії, з’явилися елементи внутрішнього спонукання та часткове відновлення ініціативності.
На 4-му тижні лікування середній бал за PHQ‑9 знизився до 10,7±2,67 (Δ=-7,6; p<0,001), що відповідало переходу до помірного/легкого рівня депресії. У цьому періоді відзначалося виразніше зниження пригніченого настрою, почуття безнадійності та емоційної спустошеності. Паралельно зменшувалися симптоми втомлюваності та нестачі енергії.
До 6-го тижня спостереження середній показник за PHQ‑9 знизився до 6,09±2,67 (Δ=-12,21; p<0,001), що відповідало легкому рівню депресії або близькому до ремісії стану. Клінічно це відзначалося виразним зменшенням афективної симптоматики, зокрема пригніченого настрою та почуття безнадійності. Паралельно спостерігалася значуща редукція астенічних проявів депресії. Пацієнти відзначали зростання рівня енергії, повсякденної активності та зменшення відчуття перевантаження навіть під час звичайної активності, що мало позитивний вплив на функціональну спроможність і якість життя.
Важливою складовою клінічного поліпшення після додавання Бупрінолу (бупропіону) в дозі 150 мг/добу стала редукція когнітивних симптомів депресії, включно із труднощами з концентрацією уваги, уповільненням мислення та складністю прийняття рішень. Зменшення когнітивного виснаження супроводжувалося підвищенням розумової продуктивності та зниженням психомоторної загальмованості.
Окремо слід відзначити помірне, але клінічно значуще поліпшення сну, яке відбувалося без посилення денної седації чи загальмованості. Це є важливою терапевтичною перевагою бупропіону, оскільки дозволяє досягти інсомнічних проявів без погіршення денного функціонування.
Загальна ефективність лікування за період спостереження становила 12,21 бала, що відповідало приблизно 66,7% зниженню виразності депресії від вихідного рівня до кінця лікування.
Динаміка редукції ангедонії за SHAPS
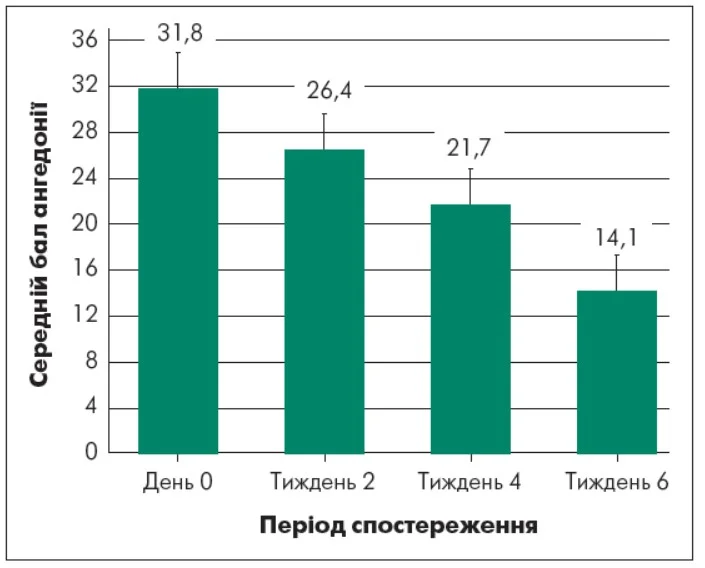
Аналіз динаміки показників за шкалою SHAPS продемонстрував послідовну та клінічно значущу тенденцію до зменшення виразності ангедонії у пацієнтів із ВДР при додаванні Бупрінолу (бупропіону) в дозі 150 мг/добу до базової терапії СІЗЗС/СІЗЗСН (рис. 2).
Примітки: 0‑8 балів – мінімальні симптоми / відсутність; 9‑17 балів – легка ангедонія; 18‑24 – помірна ангедонія; ≥25 балів – виразна ангедонія.
Рис. 2. Динамика редукції ангедонії при додаванні бупропіону до СІЗЗС/СІЗЗСН за SHAPS
На початку лікування (день 0) середній сумарний бал за SHAPS становив 31,8 бала, що відповідало виразній ангедонії. Клінічно це проявлялося глибоким зниженням здатності отримувати задоволення від повсякденної діяльності, соціальної взаємодії, сенсорних стимулів та емоційно значущих подій. Ангедонія на цьому етапі мала стійкий характер та була одним із провідних чинників функціональної недостатності пацієнтів.
Вже на 2-му тижні лікування було зафіксоване статистично достовірне зниження середнього показника за SHAPS до 26,4 бала (Δ=-8,00; p<0,05), що відповідало помірному рівню ангедонії. Така рання позитивна динаміка свідчила про швидкий вплив бупропіону на емоційно-вольову сферу та систему винагороди, що узгоджується з його дофамінергічним і норадренергічним механізмами дії. На клінічному рівні це супроводжувалося зменшенням апатії, появою епізодів зацікавленості та частковим відновленням внутрішнього спонукання до діяльності.
На 4-му тижні терапії середній бал шкали SHAPS знизився до 21,7 бала (Δ=-10,1; p<0,05), що відображало подальшу редукцію ангедонії. На цьому етапі більшість пацієнтів (70%) повідомляли про поступове відновлення інтересу до раніше приємних занять, поліпшення емоційної реактивності, зростання ініціативності та підвищення суб’єктивної залученості у повсякденну діяльність. Ангедонія втрачала тотальний характер і починала проявлятися більш вибірково.
До 6-го тижня лікування середній показник SHAPS зменшився до 14,1 бала (Δ=-17,7; p<0,001), що відповідало легкому рівню ангедонії або її субклінічним проявам. Загальна редукція ангедонії при ВДР за період спостереження становила близько 55,7%, що стало клінічно значущим результатом та свідчило про високу ефективність терапії. На цьому етапі пацієнти відзначали відновлення здатності отримувати задоволення від повсякденних й соціальних активностей та стабільніший емоційний відгук на приємні стимули.
Динаміка редукції астенії за MFI‑20
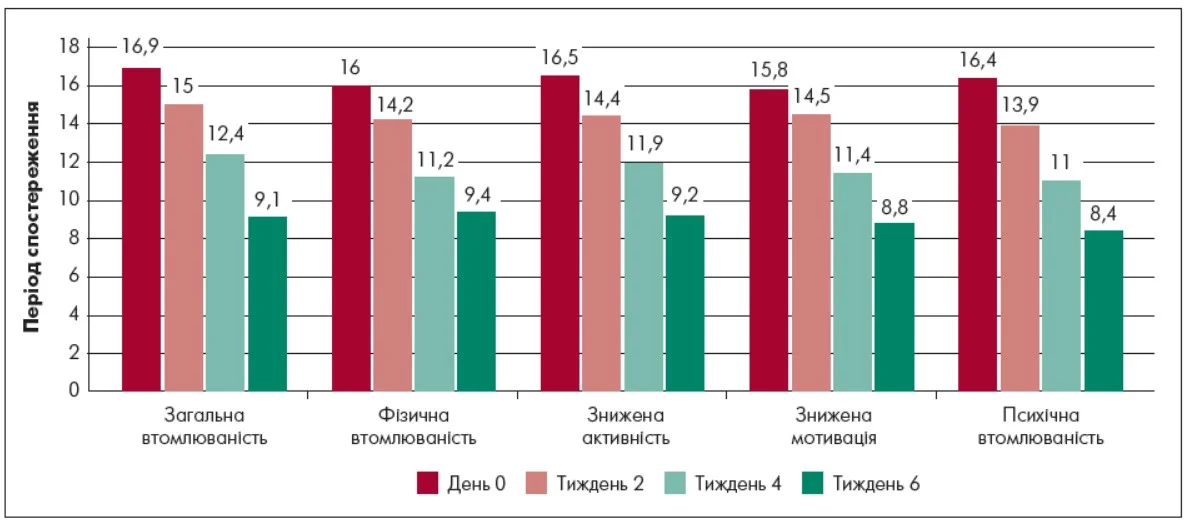
Аналіз змін показників із п’яти доменів астенії (загальна та фізична втома, знижені активність і мотивація, психічна втома) за шкалою MFI‑20 був проведений з метою оцінки динаміки астенії на тлі додавання бупропіону в дозі 150 мг до СІЗЗС/СІЗЗСН (рис. 3).
Примітки: 4‑7 балів – мінімальні симптоми / відсутність; 8‑11 балів – легка астенія; 12‑15 – помірна астенія; 16‑20 балів – виразна астенія.
Рис. 3. Динамика редукції астенії при додаванні бупропіону до СІЗЗС/СІЗЗСН за MFI‑20
Оцінювання показників за MFI‑20 показало, що додавання Бупрінолу (бупропіону)в дозі 150 мг/добу до базової терапії СІЗЗС/СІЗЗСН супроводжувалося послідовним та клінічно значущим зниженням виразності астенічної симптоматики при ВДР в усіх п’яти доменах. Уже на 2-му тижні лікування відзначалося початкове зменшення проявів втомлюваності.
Найвиразнішу редукцію було зафіксовано за доменом психічної втомлюваності, показники якої знизилися із 16,41 до 8,41 бала (Δ=-8,00; p<0,001). Це вказувало на суттєве зменшення когнітивного виснаження, труднощів із концентрацією уваги, суб’єктивного відчуття «перевантаження від мислення» та ментальної перевтомлюваності. Подібна динаміка спостерігалася і щодо загальної втомлюваності, де відзначалося зменшення із 16,92 до 9,12 бала (Δ=-7,80; p<0,001), а також зниженої активності (з 16,51 до 9,19 бала; Δ=-7,32; p<0,001), що відображало зростання загального енергетичного тонусу та повсякденної функціональної спроможності. Водночас було виявлене статистично достовірне зменшення фізичної втомлюваності з 16,00 до 9,39 бала (Δ=-6,61; p<0,05). Пацієнти повідомляли про підвищення толерантності до повсякденних навантажень, зменшення потреби в частому відпочинку й те, що фізична активність переставала сприйматися як надмірно обтяжлива.
На окрему увагу заслуговує динаміка домену зниженої мотивації, показники якого знизилися із 15,8 до 8,98 бала (Δ=-6,98; p<0,05). На тлі лікування поступово відновлювалася мотиваційно-вольова складова поведінки: пацієнтам ставало легше розпочинати діяльність, вони рідше відкладали виконання завдань і частіше залучалися до активності.
За період 6-тижневого спостереження загальна редукція астенічної симптоматики при ВДР становила близько 49% від вихідного рівня, що відображає суттєве зниження виразності астенії та втомлюваності й може свідчити про високу загальну ефективність лікування.
Поліпшення якості життя за Q-LES-Q-SF
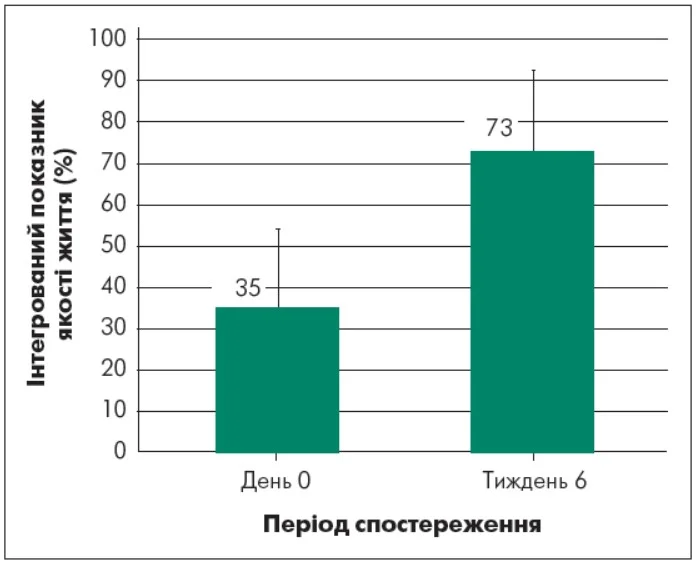
Аналіз показників якості життя за опитувальником Q-LES-Q-SF був проведений для оцінювання впливу ВДР на суб’єктивне благополуччя та повсякденне функціонування пацієнтів (рис. 4).
Примітки: <30% – вкрай низька оцінка; 30‑49% – значно знижена оцінка; 50‑69% – помірно знижена оцінка; 70‑79% – задовільна оцінка; ≥80% – добра/висока оцінка.
Рис. 4. Динамика поліпшення якості життя за опитувальником Q-LES-Q-SF при лікуванні бупропіоном
На вихідному етапі дослідження середній інтегральний показник якості життя становив близько 35%, що відповідало суттєво зниженому рівню та відображало глибокі порушення у різних сферах життєдіяльності, характерні для ВДР.
До 6-го тижня спостереження середній показник якості життя зріс до 73% (Δ=38%; p<0,001), що відповідало задовільному/сприятливому рівню.
Наприкінці лікування пацієнти відзначали зниження соматичного дискомфорту і втомлюваності, а також підвищення загального рівня енергії. Зростання фізичної витривалості сприяло активнішій участі у повсякденній діяльності та зменшенню обмежень, пов’язаних із депресивним станом. Окрім того, спостерігалося істотне поліпшення настрою, зменшення афективної спустошеності та підвищення суб’єктивного відчуття психологічного благополуччя.
Зростання показників задоволеності у професійній сфері свідчило про відновлення працездатності, підвищення продуктивності та зменшення труднощів у виконанні професійних або щоденних обов’язків. Водночас відзначалося збільшення залученості у побутові справи, зменшення інертності та пасивності, що є важливим маркером функціонального відновлення у повсякденному житті пацієнтів.
Поліпшення показників задоволеності сексуальним життям свідчило про редукцію сексуальної дисфункції, пов’язаної як із ВДР, так і з ПЕ на тлі терапії СІЗЗС. Враховуючи активуючий дофамінергічний та норадренергічний механізми дії Бупрінолу (бупропіону), отримані результати підтвердили його потенціал у корекції сексуальної дисфункції, пов’язаної з депресією та СІЗЗС-індукованими порушеннями, без погіршення ефективності антидепресивної терапії.
Безпека та переносимість терапії за FIBSER
Аналіз за шкалою FIBSER був проведений з метою комплексного оцінювання безпеки та переносимості терапії у пацієнтів із ВДР упродовж періоду спостереження. За результатами, спостерігалося статистично достовірне та клінічно значуще зниження частоти, тяжкості й функціональної обтяжливості ПЕ впродовж шести тижнів лікування (табл. 2).
|
Таблиця 2. Динаміка побічних ефектів за шкалою FIBSER |
||||
|
Час спостереження |
Частота ПЕ, % (M±SD) |
Тяжкість ПЕ (M±SD) |
Функціональна обтяжливість (M±SD) |
p |
|
День 0 |
57,63±24,47 |
3,44±1,05 |
3,26±1,13 |
|
|
Тиждень 2 |
37,80±23,54 |
2,40±1,04 |
2,24±1,01 |
p<0,05 |
|
Тиждень 4 |
17,80±14,65 |
1,40±0,87 |
1,32±0,80 |
p<0,001 |
|
Тиждень 6 |
8,80±9,71 |
0,80±0,65 |
0,64±0,25 |
p<0,001 |
|
Примітки: Частота ПЕ: 0% – не було; 10‑24% – дуже рідко; 25‑49% – рідко; 50‑74% – іноді; 75‑89% – часто; 90‑99% – дуже часто; 100% – постійно. Тяжкість ПЕ: 0 – не було; 1 – дуже легкі; 2 – легкі; 3 – помірні; 4 – виразні; 5 – сильні; 6 – надзвичайно сильні. Функціональна обтяженість: 0 – зовсім не заважали, 1 – майже не заважали; 2 – трохи заважали; 3 – помітно заважали; 4 – суттєво заважали; 5 – дуже сильно заважали; 6 – повністю порушували повсякденну активність. |
||||
На вихідному етапі лікування ПЕ реєструвалися із середньою частотою (57,63±24,47), мали помірну тяжкість (3,44±1,05 бала) та помітно впливали на повсякденну активність (3,26±1,13 бала). Найпоширенішим ПЕ при лікуванні СІЗЗС була сексуальна дисфункція, яка спостерігалася у 36% пацієнтів та проявлялася зниженням лібідо, утрудненням досягнення оргазму і зменшенням сексуальної задоволеності.
Розлади шлунково-кишкового тракту реєструвалися у 27% учасників і включали нудоту, блювання, закрепи та діарею різного ступеня виразності. Зазначені симптоми мали переважно легкий або помірний характер. Підвищена тривожність, внутрішнє напруження й акатизія відзначалися у 12% пацієнтів і проявлялися психомоторним неспокоєм, відчуттям внутрішнього збудження та труднощами із розслабленням. Ці ПЕ частіше спостерігалися в осіб із тривожним компонентом депресивного розладу. Порушення сну, зокрема безсоння або фрагментований сон, були зафіксовані у 10% обстежуваних, що могло бути зумовлено як активуючим ефектом окремих СІЗЗС, так і взаємодією з основною депресивною симптоматикою. Підвищена пітливість відзначалася у 9% пацієнтів та зазвичай мала нейровегетативний характер, тоді як головний біль – у 6% осіб, що переважно був транзиторним і не потребував відміни терапії.
Вже на 2-му тижні спостереження відзначалося статистично достовірне зниження показників за всіма доменами шкали FIBSER (p<0,05), що свідчило про ранню адаптацію пацієнтів до терапії та зниження частоти (37,8±23,54, Δ=-19,8%; p<0,05) і тяжкості ПЕ (2,40± 1,04, Δ=-1,04; p<0,05), а також функціональної обтяжливості (2,24±1,01, Δ=-1,02; p<0,05).
На 4-му тижні лікування редукція побічних ефектів досягала високого рівня статистичної значущості, а середні показники відповідали легкому чи мінімальному рівню виразності.
До 6-го тижня спостереження показники ПЕ знизилися до субклінічних значень для частоти (8,80±9,71, Δ=-48,8%; p<0,001) і до 0,80±0,65 балів (Δ=-2,64; p<0,001) для тяжкості порівняно із вихідним рівнем. Вплив ПЕ на повсякденне функціонування був мінімальним або повністю відсутній (0,64±0,25 балів, Δ=-2,62; p<0,001), що свідчило про сприятливу переносимість на пізніх етапах лікування.
Особливо важливим клінічним спостереженням стало те, що аугментація Бупрінолом (бупропіоном) у дозі 150 мг не лише не призводила до кумуляції ПЕ, але й сприяла їх клінічно значущій редукції або повному купіруванню. Зокрема, було відзначене достовірне зменшення або повне зникнення таких ПЕ, як сексуальна дисфункція (зниження лібідо, сексуальної задоволеності, аноргазмія), астенічні прояви та підвищена втомлюваність, седація і денна сонливість, когнітивне уповільнення та труднощі з концентрацією уваги, гастроінтестинальні розлади (нудота, диспепсія, діарея), внутрішнє напруження та тривожність на тлі приймання СІЗЗС чи СІЗЗСН.
Зазначені зміни мають важливе клінічне значення, оскільки саме ці ПЕ найчастіше обмежують досягнення повної ремісії та знижують прихильність пацієнтів до лікування. У даному дослідженні зменшення ПЕ відбувалося паралельно зі зростанням клінічної ефективності терапії, що формувало оптимальне співвідношення користь/ризик та сприяло збереженню високого рівня комплаєнсу впродовж усього періоду спостереження.
Висновки
1. У дослідженні використовувався препарат Бупрінол компанії «Фармліга» – єдиний зареєстрований в Україні бупропіону гідрохлорид, таблетки 150 мг із модифікованим вивільненням. Бупрінол є унікальним стимулювальним дофамінергічним антидепресантом, що має вагомі переваги перед СІЗЗС/СІЗЗСН:
- Бупрінол підвищує рівень дофаміну, що стимулює емоційну і фізичну активність, тому є антидепресантом вибору для комбінації з СІЗЗС у пацієнтів з емоційним притупленням, зниженою мотивацією, втомлюваністю та сонливістю;
- Бупрінол має переваги серед стимулювальних антидепресантів за рахунок виразного дофамінергічного ефекту в стандартній дозі 150 мг (1 таблетка). Для порівняння, щоб досягти навіть мінімальної дофамінергічної дії при застосуванні венлафаксину, необхідна доза 375 мг, що значно підвищує ризик розвитку ПЕ;
- Бупрінол не взаємодіє із серотоніновими рецепторами, тому не має серотонінергічних ПЕ (нудоти, кровотеч тощо), поліпшує сексуальну функцію, сприяє зниженню надмірної ваги.
2. Проведене 6-тижневе проспективне відкрите обсерваційне дослідження продемонструвало, що додавання Бупрінолу в дозі 150 мг/добу до стабільного лікування СІЗЗС/СІЗЗСН у пацієнтів із ВДР та недостатньою терапевтичною відповіддю пов’язано зі статистично та клінічно значущим поліпшенням психічного стану.
3. За даними анкети PHQ‑9, встановлено виразну редукцію депресивної симптоматики впродовж періоду спостереження із використанням Бупрінолу: середній бал знизився з 18,3±4,66 на вихідному рівні до 6,09±2,67 на 6-му тижні (Δ=-12,21; p<0,001), що відповідало загальному зменшенню виразності депресії на 66,7% та свідчило про наближення до ремісії у значної частки пацієнтів.
4. Аугментація Бупрінолом забезпечувала істотну редукцію ангедонії вже з 2-го тижня лікування як одного із провідних та найбільш резистентних симптомокомплексів ВДР: сумарний бал SHAPS зменшився з 31,8 до 14,1 на 6-му тижні (Δ=-17,7; p<0,001), що відповідало загальному зниженню ангедонічних проявів на 55,7% і супроводжувалося відновленням емоційно-вольової активності та здатності отримувати задоволення.
5. Додавання Бупрінолу до СІЗЗС/СІЗЗСН забезпечувало послідовне та статистично значуще зниження астенічної симптоматики за шкалою MFI‑20 у всіх п’яти доменах, починаючи з 2-го тижня, та із максимальною динамікою на 6-му тижні. Найвиразніше поліпшення стосувалося зменшення психічної (Δ=-8,00; p<0,001), загальної (Δ=-7,80; p<0,001), фізичної втомлюваності (Δ=-6,61; p<0,05) і зниженої активності (Δ=-7,32; p<0,001), а також підвищення мотивації (Δ= –6,98; p<0,05). Інтегральна редукція астенічної симптоматики становила близько 49% від вихідного рівня.
6. За результатами опитувальника Q-LES-Q-SF, додаткова терапія Бупрінолом сприяла суттєвому поліпшенню суб’єктивного благополуччя та повсякденного функціонування. Зокрема, інтегральний показник якості життя зріс із 35% на вихідному рівні до 73% на 6-му тижні (Δ=+38%; p<0,001), що відображало функціонально значуще відновлення у провідних сферах життєдіяльності (як-от фізичне самопочуття, емоційний стан, працездатність / щоденна активність, соціальні й сімейні стосунки, когнітивна ефективність, енергія та життєвий тонус).
7. Профіль безпеки й переносимості аугментивної терапії Бупрінолом був сприятливим. За шкалою FIBSER відзначалося статистично достовірне зниження частоти (з 57,63±24,47 до 8,80±9,71; Δ=-48,8%; p<0,001), тяжкості (з 3,44±1,05 до 0,80±0,65; Δ=-2,64; p<0,001) та функціональної обтяжливості ПЕ (з 3,26±1,13 до 0,64±0,25; Δ =-2,62; p<0,001) протягом шести тижнів, без ознак зростання або кумуляції ПЕ.
8. Клінічно важливим є те, що аугментація Бупрінолом пов’язана не лише із відсутністю посилення ПЕ, але й з їхньою редукцією, зокрема щодо сексуальної дисфункції, астенічних проявів, седації, когнітивного уповільнення, гастроінтестинальних скарг та внутрішнього напруження, що потенційно сприяє підвищенню прихильності пацієнтів до лікування.
9. Отримані результати свідчать, що додавання Бупрінолу в дозі 150 мг/добу до СІЗЗС/СІЗЗСН є доцільною клінічною стратегією при ВДР із частковою відповіддю на терапію, забезпечуючи комплексне зниження депресивної симптоматики, ангедонії та астенії з паралельним поліпшенням якості життя і сприятливим співвідношенням користь/ризик.
10. Завдяки оптимальному профілю ефективності та безпеки, Бупрінол доцільно застосовувати у загальній клінічній практиці для корекції супутніх афективних розладів і депресивних станів на тлі хронічних соматичних захворювань, що супроводжуються зниженням мотивації, активності та емоційного фону.
Література
- Hohls J. K., Kцnig H. H., Quirke E., Hajek A. Anxiety, depression and quality of life – a systematic review of evidence from longitudinal observational studies // International Journal of Environmental Research and Public Health. – 2021. – Vol. 18, Art. 12022; DOI: 10.3390/ijerph182212022.
- Trivedi M. H., Rush A. J., Wisniewski S. R. et al. Evaluation of outcomes with citalopram for depression using measurement-based care in STAR*D: implications for clinical practice // American Journal of Psychiatry. – 2006.– Vol. 163, № 1. – P. 28‑40; DOI: 10.1176/appi.ajp.163.1.28.
- Rush A. J., Trivedi M. H., Wisniewski S. R. et al. Acute and longer-term outcomes in depressed outpatients requiring one or several treatment steps: a STAR*D report // American Journal of Psychiatry. – 2006. – Vol. 163, № 11. – P. 1905‑1917; DOI: 10.1176/ajp.2006.163.11.1905.
- Cao B., Bauer I. E., Sharma A. N. et al. Effects of anhedonia on health-related quality of life and functional outcomes in major depressive disorder: a systematic review and meta-analysis // Journal of Affective Disorders.– 2024. – Vol. 358. – P. 162‑171; DOI: 10.1016/j.jad.2024.04.097.
- Sansone R. A., Sansone L. A. SSRI-induced indifference // Psychiatry (Edgmont). – 2010. – Vol. 7, № 10. – P. 14‑18; PMC2989833.
- Gorwood P., Demyttenaere K., Vaiva G. et al. Anhedonia predicts poor psychosocial functioning: results from a large cohort of patients treated for major depressive disorder by general practitioners // Journal of Affective Disorders. – 2017. – Vol. 218. – P. 28‑35; DOI: 10.1016/j.jad.2017.04.029.
- Stahl S. M., Pradko J. F., Haight B. R., Modell J. G., Rockett C. B., Learned-Coughlin S. A review of the neuropharmacology of bupropion, a dual norepinephrine and dopamine reuptake inhibitor // Primary Care Companion to the Journal of Clinical Psychiatry. – 2004. – Vol. 6, № 4. – P. 159‑166; DOI: 10.4088/pcc.v06n0403.
- Trivedi M. H., Fava M., Wisniewski S. R. et al. Medication augmentation after the failure of SSRIs for depression // New England Journal of Medicine. – 2006. Vol. – 354, № 12. – P. 1243‑1252; DOI: 10.1056/NEJMoa052964.
- DeBattista C., Solvason H. B., Poirier J., Kendrick E., Schatzberg A. F. A prospective trial of bupropion SR augmentation of partial and non-responders to serotonergic antidepressants // Journal of Clinical Psychopharmacology. – 2003. – Vol. 23, № 1. – P. 27‑30; DOI: 10.1097/00004714‑200302000‑00005.
- Kroenke K., Spitzer R. L., Williams J. B. W. The PHQ‑9: validity of a brief depression severity measure // Journal of General Internal Medicine. – 2001.– Vol. 16, № 9. – P. 606‑613; DOI: 10.1046/j.1525‑1497.2001.016009606.x.
- Snaith R. P., Hamilton M., Morley S., Humayan A., Hargreaves D., Trigwell P. A scale for the assessment of hedonic tone: the Snaith-Hamilton Pleasure Scale // British Journal of Psychiatry. – 1995. – Vol. 167, №1.– P. 99‑103; DOI: 10.1192/bjp.167.1.99.
- Smets E. M. A., Garssen B., Bonke B., De Haes J. C. J. M. The Multidimensional Fatigue Inventory (MFI): psychometric qualities of an instrument to assess fatigue // Journal of Psychosomatic Research. – 1995. – Vol.39, № 3. – P. 315‑325; DOI: 10.1016/0022‑3999(94)00125-O.
- Wisniewski S. R., Rush A. J., Balasubramani G. K., Trivedi M. H., Nierenberg A. A., STARD Investigators. Self-rated global measure of the frequency, intensity, and burden of side effects // Journal of Psychiatric Practice. – 2006. – Vol. 12, № 2. – P. 71‑79; DOI: 10.1097/00131746‑200603000‑00002.
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 1 (76) 2025 р.



 \
\