20 квітня, 2026
Потенціал фенібуту для корекції тривожності та стрес-асоційованих станів
Тривожні та стрес-асоційовані розлади залишаються одними з найпоширеніших психоемоційних порушень у клінічній практиці. Їх розвиток значною мірою пов’язаний із дисрегуляцією нейромедіаторних систем центральної нервової системи (ЦНС), зокрема системи, що базується на дії γ-аміномасляної кислоти (ГАМК) – основного гальмівного нейромедіатора головного мозку. У зв’язку з цим особливу увагу привертають препарати, здатні відновлювати баланс між збуджувальними та гальмівними процесами в мозку. Одним із таких засобів є фенібут, що поєднує анксіолітичні, антистресові та ноотропні властивості. Розглянемо сучасні дані щодо механізмів дії фенібуту, його клінічного застосування при тривожності та стрес-індукованих станах, а також профілю безпеки.
Механізми дії фенібуту
Фенібут (β-феніл-γ-аміномасляна кислота) є синтетичним похідним ГАМК, до молекули якої приєднано фенільну групу. Саме наявність фенільного радикала забезпечує здатність сполуки ефективніше, ніж ГАМК, проникати через гематоенцефалічний бар’єр. Завдяки цьому фенібут чинить центральні нейромедіаторні ефекти в головному мозку. Препарат було розроблено у 1960-х рр. як анксіолітичний і ноотропний засіб для зменшення тривожності та проявів стресу без виразного седативного ефекту (Vavers et al., 2016).
Основним фармакологічним механізмом дії фенібуту вважається агоністична дія на ГАМКB-рецептори. Активація цих метаботропних рецепторів сприяє зниженню нейрональної збудливості та пригніченню вивільнення збуджувальних нейромедіаторів. Це зумовлює протитривожні та антистресові властивості препарату. Водночас фенібут значно слабше взаємодіє з ГАМКA-рецепторами, що відрізняє його від класичних седативних засобів і пояснює відносно помірний седативний ефект.
Окрім впливу на ГАМК-ергічну систему, фенібут взаємодіє з α2-δ-субодиницею потенціалзалежних кальцієвих каналів, подібно до габапентиноїдів. Це зменшує надходження кальцію у пресинаптичні нейрони та пригнічує вивільнення збуджувальних медіаторів, зокрема глутамату. Такий механізм може додатково сприяти зниженню тривожності, стабілізації емоційного стану та зменшенню стрес-індукованої нейрональної гіперактивності. В експериментальних дослідженнях також показано, що фенібут може помірно підвищувати рівень дофаміну в деяких структурах головного мозку, зокрема у стріатумі, що частково пояснює його позитивний вплив на мотивацію, когнітивні функції та адаптацію до стресу (Kupats et al., 2020).
Фармакокінетичні особливості фенібуту зумовлені тим, що він добре всмоктується після перорального приймання, широко розподіляється у тканинах організму, включно із ЦНС, майже не метаболізується та виводиться переважно нирками у незміненому вигляді. Сукупність зазначених механізмів – вплив на ГАМКB-рецептори, кальцієві канали та нейромедіаторні системи – пояснює його анксіолітичні, антистресові й потенційні ноотропні властивості (Kupats et al., 2020).
Зв’язок ГАМК-ергічної системи зі стресом і тривожністю
ГАМК відіграє ключову роль у регуляції емоційної реактивності, стресу й тривожності. Порушення ГАМК-ергічної нейротрансмісії розглядається як один із важливих патофізіологічних механізмів розвитку тривожних розладів. Зниження активності ГАМК-ергічних нейронів або зміни функції їхніх рецепторів призводять до підвищення нейрональної збудливості у структурах мозку, залучених до формування реакцій страху та стресу, а також можуть спричиняти порушення сну.
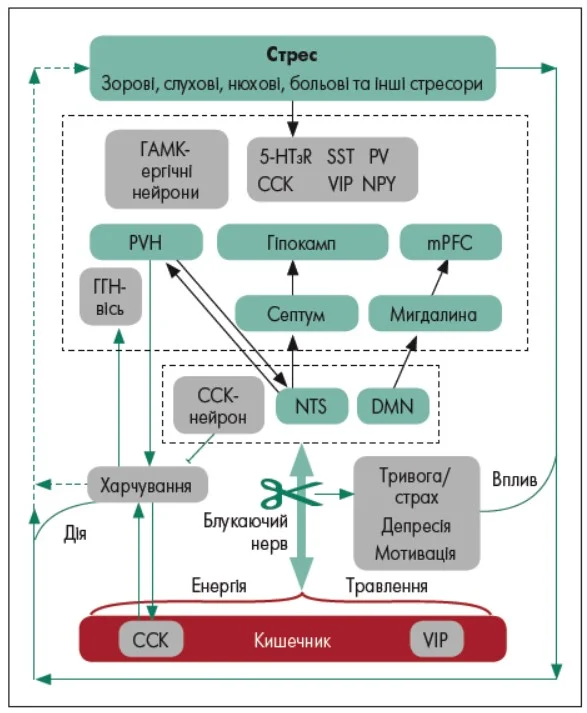
Дані сучасних досліджень підтверджують складну взаємодію ГАМК-ергічної нейротрансмісії, структур мозку, що регулюють емоційні реакції, та кишково-мозкової осі, в якій важливу роль відіграє блукаючий нерв. Як показано на рисунку, зв’язок між гіпокампом, мигдалиною, префронтальною корою та гіпоталамусом формує нейрональні мережі, залучені до регуляції реакцій страху, тривожності та стресу (Hou et al., 2020).
Примітки: 5-HT3R – рецептор серотоніну 5-HT3, CCK – холецистокінін, SST – соматостатин, VIP – вазоактивний інтестинальний пептид, PV – парвальбумін, NPY – нейропептид Y, PVH – паравентрикулярне ядро гіпоталамуса, mPFC – медіальна префронтальна кора, ГГН-вісь – гіпоталамо-гіпофізарно-надниркова вісь, NTS – ядро одиночного тракту, DMN – дорсальне моторне ядро.
Рисунок. Роль ГАМК-ергічної системи в регуляції стресу через кишково-мозкову вісь із залученням блукаючого нерва
Адаптовано за X. Hou et al. (2020)
Тривога і порушення сну мають тісний двобічний зв’язок. Недостатній або фрагментований сон може підсилювати емоційну реактивність і сприяти формуванню тривожності, тоді як хронічний стрес і тривожні стани здатні порушувати архітектуру сну. Одним із механізмів цієї взаємодії є активація гіпоталамо-гіпофізарно-надниркової осі, що супроводжується підвищенням рівня кортизолу та підсиленням реактивності мигдалеподібного тіла до сигналів загрози (Jiang et al., 2025).
Таким чином, дисрегуляція ГАМК-ергічної системи може призводити до формування хронічного стресу, тривожності та пов’язаних із ними розладів сну. Натомість фармакологічні агенти, які посилюють ГАМК-ергічну нейротрансмісію, здатні знижувати активність нейрональних мереж, відповідальних за реакцію страху та гіперзбудливість, що пояснює їхній анксіолітичний ефект. Саме тому застосування препаратів, що впливають на ГАМК-ергічні механізми, вже тривалий час розглядаються як одна з основних стратегій лікування тривожних розладів (Gomes et al., 2019).
Користь фенібуту як анксіолітичного та антистресового засобу
Актуальні дані свідчать, що фенібут і далі розглядається передусім як анксіолітичний засіб для корекції тривожності, внутрішнього напруження, страху та асоційованих із ними порушень сну. Зокрема, в обсерваційному дослідженні підтверджено ефект фенібуту після тритижневого курсу терапії щодо зниження рівня дезадаптації, причому найвиразніше поліпшення стосувалося порушень сну, неспокою, страху та тривоги. Кількість осіб із клінічно значущою виразністю симптомів суттєво зменшилася, а частина пацієнтів після лікування вже не досягала діагностичного порогу розладу адаптації. Водночас через нерандомізований дизайн без контрольної групи результати потребують обережної інтерпретації (Terauds et al., 2025).
Із патофізіологічного погляду анксіолітичний і антистресовий потенціал фенібуту є біологічно обґрунтованим. Стрес-асоційовані стани, включно із тривожним і посттравматичним стресовим розладами, пов’язані з дисрегуляцією ГАМК-ергічної нейромедіації, а відновлення гальмівного контролю у ЦНС розглядають як одну із ключових мішеней фармакотерапії (Kyrychenko et al., 2024).
Отже, завдяки зазначеним властивостям фенібуту його приймання є особливо актуальним у сучасному клінічному контексті. В умовах тривалого хронічного стресу, зокрема пов’язаного з війною, різко зростає частота розвитку тривожних розладів, порушень сну, дратівливості та внутрішнього неспокою, що формує запит пацієнтів на препарати із поєднаним анксіолітичним і антистресовим профілем дії без виразного седативного ефекту.
Ноотропні й нейропротекторні властивості фенібуту
Окрім анксіолітичного ефекту, фенібут має ноотропні властивості, завдяки чому позитивно впливає на когнітивні функції, зокрема увагу, пам’ять і здатність до навчання. Вище зазначалося, що препарат розроблявся як анксіолітичний засіб із потенційними ноотропними властивостями, що пов’язують передусім із його впливом на ГАМК-ергічну нейротрансмісію. Передбачається, що активація ГАМКB-рецепторів і взаємодія з α2-δ-субодиницею потенціалзалежних кальцієвих каналів сприяють зниженню нейрональної гіперзбудливості та стабілізації нейромедіаторного балансу. Завдяки цьому фенібут може поліпшувати функціонування нейронних мереж, що беруть участь у когнітивній обробці інформації та адаптації до стресових впливів (Vavers et al., 2016).
На окрему увагу заслуговує нейропротекторний потенціал фенібуту. Препарат здатний запобігати пошкодженню нейронів завдяки пригніченню глутамат-опосередкованої ексайтотоксичності та зниженню окисного стресу в тканинах головного мозку. Ці властивості потенційно можуть бути корисними при нейродегенеративних патологіях (хворобі Паркінсона, хворобі Альцгеймера), а також для мінімізації наслідків церебральної ішемії та черепно-мозкової травми (Kyrychenko et al., 2024).
Профіль безпеки фенібуту
За наявними доказами, при застосуванні фенібуту в терапевтичних дозах він загалом добре переноситься. У систематичному огляді даних клінічних досліджень і клінічних випадків показано, що побічні ефекти були рідкісними, а найчастішим небажаним явищем була сонливість (Kupats et al., 2020).
Як і при застосуванні інших психоактивних засобів, під час використання фенібуту доцільно враховувати потенційний ризик розвитку залежності, інтоксикації та синдрому відміни. Водночас більшість сучасних повідомлень про такі ускладнення стосуються випадків приймання препарату в значно вищих за терапевтичні дозах, нерідко протягом тривалого часу та у поєднанні з алкоголем або іншими психоактивними речовинами (Stewart et al., 2024).
Окрему увагу в літературі приділяють ситуаціям, пов’язаним із неконтрольованим застосуванням фенібуту, зокрема у вигляді продуктів, придбаних через інтернет як харчові добавки. У таких випадках склад, дозування та якість продукту можуть бути недостатньо стандартизованими, що ускладнює оцінювання його безпеки. Саме в цьому контексті найчастіше описують серйозні небажані явища, інтоксикації або прояви синдрому відміни (Behmer Hansen et al., 2023).
Таким чином, профіль безпеки фенібуту значною мірою залежить від режиму застосування: при короткочасному прийманні у терапевтичних дозах препарат зазвичай добре переноситься, тоді як тривале або високодозове використання може підвищувати ймовірність небажаних ефектів. Водночас обмежена кількість контрольованих клінічних досліджень не дозволяє остаточно охарактеризувати безпеку фенібуту при тривалому застосуванні, що зумовлює необхідність подальшого вивчення цього питання (Kyrychenko et al., 2024).
Фенібут у вітчизняній клінічній практиці: переваги та схема застосування
Серед лікарських засобів, що містять фенібут, на фармацевтичному ринку України широко застосовується Біфрен® (Acino, part of Arcera). Препарат випускається у формі капсул, що містять 250 мг фенібуту. Наявність стандартизованої лікарської форми та контроль якості виробництва мають важливе значення для забезпечення передбачуваного терапевтичного ефекту й належного профілю безпеки.
Середня добова доза препарату зазвичай становить 0,75‑1,5 г, що відповідає 3‑6 капсулам по 250 мг. Тривалість курсу лікування найчастіше становить 4‑6 тижнів, після чого за потреби можливе повторення терапії декілька разів на рік залежно від клінічної ситуації та рекомендацій лікаря.
Отже, з огляду на анксіолітичні, ноотропні та нейропротекторні властивості фенібуту, Біфрен® може розглядатися як варіант фармакологічної підтримки для корекції тривожності, психоемоційного напруження, порушень сну та інших стрес-індукованих станів. При цьому, як за приймання інших психоактивних засобів, доцільним є дотримання рекомендованих дозувань і тривалості курсу лікування, що сприяє оптимальному співвідношенню ефективності й безпеки терапії. Загалом фенібут залишається перспективним фармакологічним засобом із цікавим механізмом дії, потенціал якого заслуговує на поглиблене вивчення в межах добре спланованих клінічних випробувань.
Підготувала Олена Коробка
UA-BIFR-PUB-032026-120
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 1 (76) 2026 р.