3 вересня, 2022
Фармакологічне лікування біполярної манії: систематичний огляд і мережевий метааналіз подвійних сліпих рандомізованих контрольованих досліджень
За даними Всесвітньої організації охорони здоров’я (ВООЗ) на тлі пандемії COVID‑19 у всьому світі поширеність тривожних розладів та депресії зросла на 25%. Також зазначається, що у кожної п’ятої (22%) особи, яка пережила війну або інші збройні конфлікти, розвивається депресія, тривожний розлад, посттравматичний стресовий розлад (ПТСР), біполярний афективний розлад (БАР) або шизофренія (WHO, 2022). При цьому особи зі вже наявними психічними розладами є вкрай вразливими в умовах надзвичайних ситуацій і потребують доступу до психіатричної допомоги та адекватної фармакологічної терапії. Пропонуємо до вашої уваги огляд статті Taro Kishi et al. «Pharmacological treatment for bipolar mania: a systematic review and network meta-analysis of double-blind randomized controlled trials» видання Molecular Psychiatry (2022; 27: 1136–1144).
Біполярний афективний розлад: систематичний огляд і мережевий метааналіз даних подвійних сліпих рандомізованих контрольованих досліджень
БАР – це тяжкий хронічний розлад настрою, що характеризується епізодами манії та депресії, які чергуються або переплітаються; його поширеність в усьому світі становить близько 1% (McIntyre et al., 2020). Пацієнт із гострим епізодом манії часто потребує невідкладної медичної допомоги, що може призводити до психіатричної госпіталізації, метою якої є захист від гіперактивності та імпульсивності (Baldessarini et al., 2019).
Фармакотерапія є одним з основних методів лікування пацієнтів із гострим БАР. Сучасні настанови рекомендують різні антипсихотики, літій та вальпроати як засоби монотерапії першої лінії для дорослих осіб (Yatham et al., 2019). Ці рекомендації ґрунтуються на доказових даних із посиланням на два важливі мережеві метааналізи (Cipriani et al., 2011; Yildiz et al., 2015).
Однак після опублікування цих метааналізів було проведено клінічні дослідження щодо ефективності деяких нових препаратів для осіб із гострою манією. Власне, ці метааналізи не оцінювали такі важливі результати, як клінічну ремісію, ефективність щодо психотичних симптомів і ризик розвитку окремих побічних ефектів. Саме тому здійснено систематичний огляд і мережевий метааналіз для отримання результатів щодо ефективності, прийнятності, переносимості та безпеки 23 препаратів для лікування дорослих із гострими ознаками БАР (Kishi et al., 2021).
Основними результатами щодо ефективності та прийнятності були відповідь на лікування та його припинення з усіх причин відповідно. Вторинними результатами були зменшення ознак манії та припинення лікування через неефективність.
Інші результати охоплювали клінічну ремісію, зменшення ознак психозу, припинення лікування через небажані явища, згоду на відміну, депресію та окремі побічні дії. Дослідники орієнтувалися на оцінку результатів через три або чотири тижні лікування. Було включено дані всіх досліджень із гнучким дозуванням, оскільки вони дають змогу здійснювати титрування до оптимальної дози для кожного пацієнта. Також розглядали результати досліджень із фіксованою дозою, власне, рекомендованою для лікування БАР відповідно до останніх настанов.
Загалом метааналіз охоплював дані 72 подвійних сліпих рандомізованих клінічних досліджень (РКД) (n = 16 442, чоловіки – 50,93%, середній вік – 39,55 року, середня тривалість дослідження 3,96 ± 2,39 тижня). Вивчали такі групи лікування (кількість груп / кількість осіб): арипіпразол (9/1205), азенапін (3/620), брекспіпразол (2/321), карбамазепін (6/305), карипразин (3/612), хлорпромазин (1/10), ендоксифен (2/55), еслікарбазепін (2/148), галоперидол (10/1023), ламотриджин (3/173), лікарбазепін (1/324), літій (20/965), оланзапін (14/1565), окскарбазепін (1/30), паліперидон (2/542), кветіапін (5/630), рисперидон (7/676), тамоксифен (2/43), топірамат (4/659), вальноктамід (1/71), вальпроат (14/981), верапаміл (1/17), зипразидон (3/458) і плацебо (48/5009).
Реакція на лікування
Для арипіпразолу, азенапіну, карбамазепіну, карипразину, галоперидолу, літію, оланзапіну, паліперидону, кветіапіну, рисперидону, тамоксифену, вальпроату та зипразидону було продемонстровано кращу відповідь на лікування, ніж для плацебо.
Арипіпразол, карипразин і кветіапін перевершували еслікарбазепін, лікарбазепін і топірамат. Своєю чергою, азенапін, ламотриджин, паліперидон та зипразидон мали вищу ефективність за топірамат; карбамазепін був ефективнішим, ніж азенапін, ендоксифен, еслікарбазепін, ламотриджин, лікарбазепін і топірамат. Відповідь на лікування галоперидолом, оланзапіном і рисперидоном була кращою, ніж при терапії азенапіном, еслікарбазепіном, лікарбазепіном і топіраматом, тоді як літій і вальпроат були дієвішими за еслікарбазепін і топірамат (тамоксифен перевершував усі активні препарати, крім карбамазепіну та верапамілу). Порівняно з плацебо терапія такими препаратами, як оланзапін, кветіапін, арипіпразол, азенапін, карбамазепін, карипразин, галоперидол, літій, паліперидон, рисперидон, тамоксифен, вальпроат і зипразидон ефективніше сприяла поліпшенню показників за шкалою оцінювання манії.
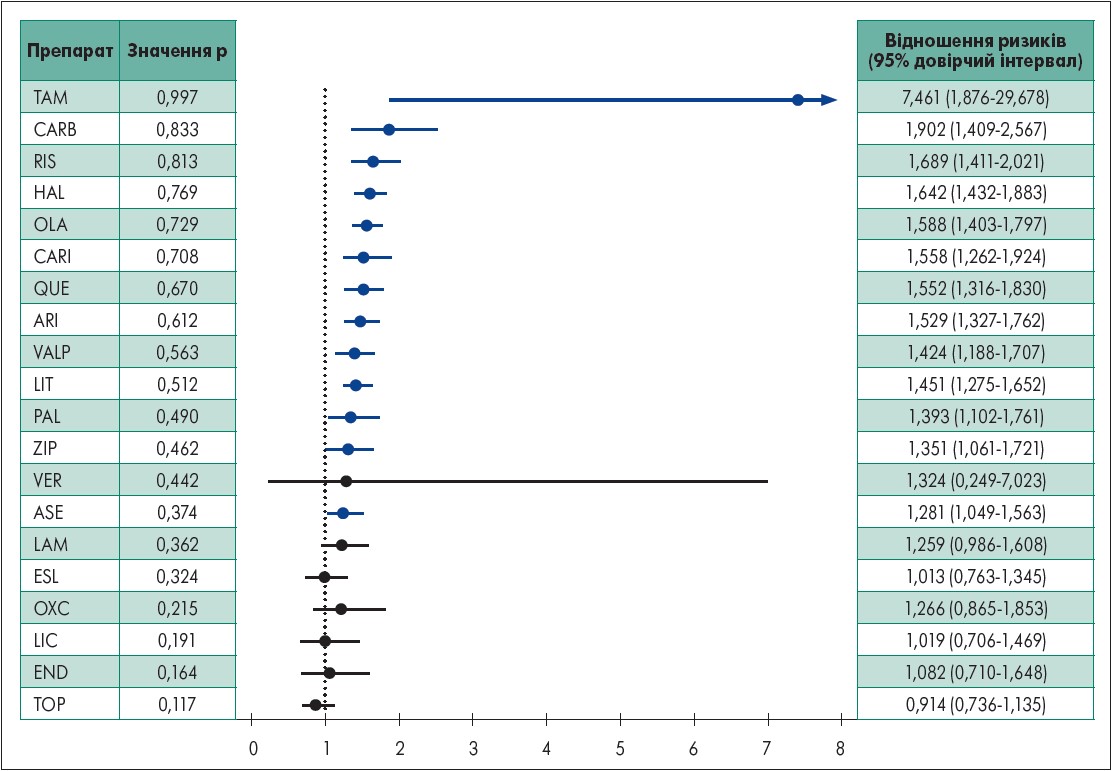
Арипіпразол, азенапін, карипразин, галоперидол, літій, оланзапін, паліперидон, кветіапін, рисперидон і тамоксифен перевершували плацебо щодо клінічної ремісії. Своєю чергою, порівняно з плацебо терапія такими препаратами, як арипіпразол, карипразин, галоперидол, оланзапін, кветіапін, рисперидон, тамоксифен і зипразидон краще сприяла поліпшенню психотичних симптомів. Встановлено, що при лікуванні арипіпразолом, оланзапіном, кветіапіном і рисперидоном частота припинення приймання з усіх причин була меншою, тоді як у разі терапії топіраматом кількість випадків припинення застосування з усіх причин була найбільшою. Щодо детального оцінювання припинення лікування з усіх причин, то показники для арипіпразолу, карбамазепіну, галоперидолу, вальпроату та зипразидону були кращими, ніж для топірамату й вальноктаміду. Оланзапін за цим показником перевершував арипіпразол, азенапін, брекспіпразол, карипразин, галоперидол, ламотриджин, лікарбазепін, літій, топірамат, вальноктамід, вальпроат, верапаміл та зипразидон. Паліперидон і рисперидон були дієвішими за топірамат, вальноктамід і верапаміл, тоді як кветіапін перевершував літій, топірамат, вальноктамід і верапаміл (рисунок).
Рисунок. Відповідь на терапію порівняно з плацебо (синій – препарат значуще перевершував плацебо; чорний – препарат не перевершував плацебо). ARI – арипіпразол, ASE – азенапін, CARB – карбамазепін, CARI – карипразин, END – ендоксифен, ESL – еслікарбазепін, HAL – галоперидол, LAM – ламотриджин, LIC – лікарбазепін, LIT – літій, OLA – оланзапін, OXC – окскарбазепін, PAL – паліперидон, QUE – кветіапін, RIS – рисперидон, TAM – тамоксифен, TOP – топірамат, VALP – вальпроат, VER – верапаміл, ZIP – зипразидон.
Адаптовано згідно з T. Kishi et al., 2021.
Кількість випадків припинення приймання через неефективність препарату була меншою в разі терапії арипіпразолом, азенапіном, оланзапіном, кветіапіном, карбамазепіном, карипразином, галоперидолом, літієм, паліперидоном, рисперидоном, вальпроатом і зипразидоном.
Оцінювання проявів манії
Порівняно з плацебо для арипіпразолу, азенапіну, карбамазепіну, карипразину, галоперидолу, літію, оланзапіну, паліперидону, кветіапіну, рисперидону, тамоксифену, вальпроату й зипразидону було продемонстровано суттєвіше зменшення проявів манії, визначене за шкалою оцінювання манії: величина стандартизованої різниці середніх значень коливалася від -1,806 (95% довірчий інтервал [ДІ] від -2,454 до -1,159) для тамоксифену до -0,216 (95% ДІ від -0,371 до -0,061) для вальпроату.
Припинення терапії через неефективність
У разі приймання арипіпразолу, азенапіну, карбамазепіну, карипразину, галоперидолу, літію, оланзапіну, паліперидону, кветіапіну, рисперидону, вальпроату та зипразидону спостерігалася менша кількість випадків припинення лікування через неефективність порівняно з групою застосування плацебо: значення відношення ризиків коливалося в діапазоні від 0,349 (95% ДІ 0,216–0,564) для паліперидону до 0,716 (95% ДІ 0,534–0,961) для літію.
Клінічна ремісія і психотичні симптоми
Терапія арипіпразолом, азенапіном, карипразином, галоперидолом, літієм, оланзапіном, паліперидоном, кветіапіном, рисперидоном і тамоксифеном сприяла кращій клінічній ремісії, ніж приймання плацебо: відношення ризиків коливалося в діапазоні від 8,441 (95% ДІ 1,116–63,841) для тамоксифену до 1,259 (95% ДІ 1,007–1,576) для літію. Щодо психотичних симптомів, то лікування арипіпразолом, карипразином, галоперидолом, оланзапіном, кветіапіном, рисперидоном, тамоксифеном і зипразидоном сприяло значнішій їх редукції, ніж приймання плацебо: величина стандартизованої різниці середніх значень коливалася від -1,640 (95% ДІ від -2,335 до -0,945) для тамоксифену до -0,266 (95% ДІ від -0,490 до -0,041) для арипіпразолу.
Переносимість і результати щодо безпеки
Порівняно з плацебо застосування азенапіну, галоперидолу та літію супроводжувалося більшою кількістю побічних ефектів, відношення ризиків становило 1,896 (95% ДІ 1,117–3,218), 1,867 (95% ДІ 1,255–2,776) і 1,791 (95% ДІ 1,093–2,936) відповідно. Водночас оланзапін рідше спричиняв припинення терапії через згоду на її скасування: відношення ризиків 0,643 (95% ДІ 0,466–0,889). Терапія жодним із препаратів не асоціювалася із частішим, ніж у разі приймання плацебо, розвитком депресії. Окрім того, порівняно з плацебо лікування оланзапіном та кветіапіном було пов’язане з нижчою частотою використання анксіолітичних засобів: відношення ризиків становило 0,881 (95% ДІ 0,800–0,971) і 0,767 (95% ДІ 0,665–0,885) відповідно. Своєю чергою, арипіпразол, карипразин, галоперидол, паліперидон, рисперидон та зипразидон асоціювалися з вищою частотою застосування антихолінергічних засобів: діапазон значень відношення ризиків становив від 2,374 (95% ДІ 1,384–4,072) для паліперидону до 6,299 (95% ДІ 4,159–9,541) для галоперидолу. На тлі терапії арипіпразолом, брекспіпразолом, карипразином, галоперидолом, паліперидоном, рисперидоном і зипразидоном частіше спостерігалася акатизія: значення відношення ризиків коливалися в діапазоні від 2,586 (95% ДІ 1,188–5,631) для паліперидону до 5,579 (95% ДІ 3,959–7,862) для галоперидолу. Також було встановлено, що арипіпразол, азенапін, карипразин, галоперидол, літій, оланзапін, рисперидон та зипразидон співвідносилися з вищою частотою екстрапірамідних симптомів: відношення ризиків становили від 1,817 (95% ДІ 1,012–3,261] для оланзапіну до 5,337 (95% ДІ 3,997–7,126) для галоперидолу. Збільшення частоти сонливості було зафіксовано на тлі приймання арипіпразолу, азенапіну, карбамазепіну, карипразину, галоперидолу, літію, оланзапіну, паліперидону, кветіапіну, рисперидону, вальпроату та зипразидону: значення відношення ризиків коливалися від 1,609 (95% ДІ 1,055–2,453) для літію до 5,158 (95% ДІ 1,515–17,561) для карипразину.
Азенапін, карбамазепін, галоперидол, оланзапін, кветіапін, вальпроат і зипразидон асоціювалися з вищою частотою запаморочення: діапазон значень відношення ризиків становив від 2,037 (95% ДІ 1,334–3,110) для вальпроату до 3,552 (95% ДІ 2,369–5,323) для карбамазепіну. Терапія карбамазепіном, оланзапіном і кветіапіном частіше асоціювалася з сухістю в роті: значення відношення ризиків становили 4,079 (95% ДІ 1,109–15,010]), 3,758 (95% ДІ 2,147–6,577) і 3,630 (95% ДІ 2,243–5,876) відповідно. Зокрема, арипіпразол, карипразин, оланзапін і кветіапін частіше спричиняли закрепи: величина відношення ризиків коливалася від 1,735 (95% ДІ 1,152–2,613) для арипіпразолу до 2,866 (95% ДІ 1,537–5,345) для кветіапіну.
Як зазначають дослідники, збільшення маси тіла спостерігали в разі приймання азенапіну, оланзапіну, паліперидону, кветіапіну, вальпроату та зипразидону: діапазон значень відношення ризиків становив від 2,928 (95% ДІ 1,259–6,807) для зипразидону до 8,180 (95% ДІ 4,419–15,142) для оланзапіну.
Водночас порівняно з плацебо застосування кветіапіну асоціювалося з нижчою частотою нудоти (відношення ризиків 0,313 (95% ДІ 0,130–0,758), тоді як арипіпразол, карбамазепін, карипразин, літій, рисперидон та вальпроат були пов’язані із частішим розвитком цього побічного ефекту (значення відношення ризиків коливалися від 1,558 [95% ДІ 1,164–2,085] для арипіпразолу до 4,664 [95% ДІ 1,320–16,479] для рисперидону). Не зафіксовано суттєвих відмінностей щодо частоти головного болю та діареї за приймання згаданих вище препаратів і плацебо.
Оцінка гетерогенності, непослідовності та результатів мережевого метааналізу за допомогою моделі CINeMA
Використана для оцінювання модель CINeMA (Confidence in Network Meta-Analysis) охоплює шість сфер доказів достовірності: ризик систематичних помилок усередині дослідження, ризик систематичних помилок між дослідженнями, побічність, невідповідність, неоднорідність і непослідовність.
Загальна неоднорідність була низькою або від низької до помірної для більшості результатів; від помірної до високої для припинення лікування через побічні явища та діарею; високою для частоти розвитку депресії. Була наявною значуща локальна неоднорідність для більшості результатів конкретних порівнянь і значуща загальна невідповідність для припинення лікування з усіх причин, психотичних симптомів, припинення терапії через побічні явища та розвиток депресії.
Тест SIDE (відокремлення прямих доказів від непрямих) на локальну невідповідність засвідчив деякі «гарячі точки»: порівняння галоперидолу та літію, галоперидолу та плацебо, літію та рисперидону, рисперидону та вальноктаміду, вальноктаміду та плацебо щодо психотичних симптомів; зіставлення вальпроату та плацебо щодо припинення лікування через побічні ефекти; порівняння оланзапіну та плацебо щодо розвитку депресії. Частка порівнянь із доказами неоднорідності була невеликою для всіх результатів (0,00%–20,83%).
Узагальнення результатів
Систематичний огляд і мережевий метааналіз було проведено для порівняння ефективності, прийнятності, переносимості та безпеки фармакологічних втручань для дорослих пацієнтів із гострою біполярною манією. Було включено лише дані подвійних сліпих рандомізованих контрольованих досліджень, додано результати щодо брекспіпразолу, ендоксифену й еслікарбазепіну, досліджено результати щодо багатьох побічних ефектів.
Засобами, які перевершували плацебо за первинними та вторинними результатами, були арипіпразол, оланзапін, кветіапін і рисперидон. Ці препарати також були дієвішими за плацебо щодо клінічної ремісії та зменшення психотичних симптомів. Саме вказані лікарські засоби характеризуються кращим балансом ефективності та прийнятності при лікуванні гострого БАР, ніж інші досліджувані препарати.
Оскільки лікування гострого епізоду БАР зазвичай продовжується підтримувальною терапією, клініцисти та пацієнти мають брати до уваги ефективність та безпеку застосування препаратів під час цієї фази терапії. Нещодавні дані мережевого метааналізу на етапі підтримки продемонстрували, що антипсихотики другого покоління запобігають повторенню / рецидиву будь-якого епізоду різкої зміни настрою (Kishi et al., 2020). Але оскільки згадані засоби чинять деякі побічні ефекти, клініцисти мають контролювати стан здоров’я пацієнтів із БАР.
Нещодавній метарегресійний аналіз, що включав дані рандомізованих контрольованих досліджень ефективності антипсихотичних препаратів і стабілізаторів настрою порівняно з плацебо, продемонстрував, що на величину ефекту мали вплив показники відповіді як на препарат, так і на плацебо (Bartoli et al., 2018). Тож Т. Kishi et al. зазначають, що в подальших дослідженнях необхідно буде з’ясувати, чи існує взаємодія між реакцією на ліки та плацебо щодо розміру ефекту. Важливо також визначити модифікатори реакції на препарати та дослідити, як вони взаємодіють з модифікаторами реакції на плацебо у формуванні розміру ефекту. Автори наголошують, що не охоплювали низку важливих клінічних питань, які могли б мати вплив на прийняття рішень щодо лікування в рутинній клінічній практиці (наприклад, поєднання з нефармакологічними методами терапії та економічну ефективність).
Хоча результати мережевого метааналізу підтвердили, що літій і вальпроат були ефективними для лікування пацієнтів із симптомами БАР, їхній рейтинг ефективності був нижчим порівняно з більшістю антипсихотичних препаратів.
Терапія більшістю нейролептиків зменшувала психотичні симптоми, проте цього не спостерігалося в разі застосування карбамазепіну, літію та вальпроатів.
Як зауважують дослідники, ці антипсихотичні засоби слід зарезервувати для осіб із психотичними особливостями. Зокрема, у висновку систематичного огляду та мережевого метааналізу зазначено, що карбамазепін, літій, тамоксифен і вальпроат демонструють ефективність при гострому епізоді БАР. Однак переносимість є кращою, ніж для плацебо, лише за терапії арипіпразолом, кветіапіном, оланзапіном та рисперидоном (Kishi et al., 2021).
Довідка «ЗУ»
Застосування форм із пролонгованим вивільненням
Як відомо, широкий перелік доступних варіантів медикаментозної терапії формує потребу в індивідуалізованому підході до вибору належного препарату та його лікарської форми.
Ретардні (із пролонгованим вивільненням) форми лікарських засобів є, беззаперечно, бажаними при терапії пацієнтів з афективними розладами, особливо в разі комбінації згаданих порушень зі зниженим комплаєнсом, активним ритмом життя або похилим віком, а також за наявності поліорганної патології. Стабільна та оптимальна концентрація таргетної діючої речовини є запорукою адекватної корекції поведінки і стану пацієнта, відсутності добових коливань та безпеки терапії відповідно (Мангубі, 2020).
Кветіапін пролонгованої дії (Кетилепт® Ретард), відповідно до впливу на конкретні рецептори, має дозозалежний ефект. Зокрема, в разі використання малих доз (50–100 мг) препарат чинить протитривожний вплив завдяки блокаді гістамінових (Н1-), адренергічних (α1- та α2-), серотонінових (5HT2A- та 5HT1A-) рецепторів. Це дає змогу успішно призначати кветіапін пролонгованої дії за наявності тривожних симптомів (Kapur et al., 2000). Його сприятливий вплив на пацієнтів із нічними кошмарами може бути результатом дії на структуру сну та його швидку фазу (Robert et al., 2005). Кветіапін має вищу спорідненість до 5-HT2, ніж до D2-рецепторів, водночас він слабко зв’язується з рецепторами D2-, що забезпечує їх тимчасову занятість і легке заміщення дофаміном. Завдяки цьому механізму препарат може зменшувати тривогу, поліпшувати настрій та когнітивні функції, а також зменшувати ризик виникнення екстрапірамідних побічних ефектів і гіперпролактинемії (Meltzer et al., 2001). Також згадані ефекти, як зазначають дослідники, можуть сприяти клінічній редукції симптомів ПТСР (Ahearn et al., 2003).
У середніх дозуваннях (100–300 мг) кветіапін пролонгованої дії додатково блокує зворотне захоплення норадреналіну, зумовлюючи здатність ефективно зменшувати депресивну симптоматику. Завдяки таким властивостям кветіапін ухвалений FDA як засіб ад’ювантної (додаткової) терапії для лікування депресії, особливо в разі резистентних випадків та для аугментації дії антидепресантів.
Слід також пам’ятати про відмінність початкових дозувань препаратів Кетилепт® і Кетилепт® Ретард: призначення пролонгованої форми в дозуванні 300 мг/добу впродовж наступних 20 годин забезпечує надходження до організму невеликої дози кветіапіну; оптимальним та безпечним є підвищення дозування препарату Кетилепт® Ретард до 600 мг і навіть до 800 мг щонайбільше за 2–3 дні (Мангубі, 2020).
Застосування кветіапіну пролонгованої дії сприяє призначенню індивідуалізованої дози та чіткому відстеженню позитивного терапевтичного ефекту без ризику ятрогенії та без потреби у поліпрагмазії. Проте в будь-якому разі остаточне рішення про індивідуалізований підбір дози покладається на лікаря-практика.
Підготувала Олександра Демецька