9 серпня, 2024
Європейські рекомендації з атопічного дерматиту (EuroGuiDerm)
Частина І: Системна терапія
 Метою цього керівництва є надання рекомендацій щодо ведення та лікування хворих на атопічний дерматит (АД) будь-якого ступеня тяжкості та всіх вікових груп. Відповідно до технічного документу, цілі керівництва такі: створити засновані на останніх доказах рекомендації та алгоритми місцевої терапії, фототерапії, а також як новітньої, так і вже впровадженої системної терапії АД; надати рекомендації щодо ведення пацієнтів з АД під час вагітності, а також хворих на АД з алергійними та іншими супутніми захворюваннями.
Метою цього керівництва є надання рекомендацій щодо ведення та лікування хворих на атопічний дерматит (АД) будь-якого ступеня тяжкості та всіх вікових груп. Відповідно до технічного документу, цілі керівництва такі: створити засновані на останніх доказах рекомендації та алгоритми місцевої терапії, фототерапії, а також як новітньої, так і вже впровадженої системної терапії АД; надати рекомендації щодо ведення пацієнтів з АД під час вагітності, а також хворих на АД з алергійними та іншими супутніми захворюваннями.
Цільова популяція та питання здоров’я, охоплені керівництвом
Цільовою популяцією керівництва є пацієнти з АД усіх вікових груп. Основні питання щодо здоров’я (незалежно від статі та етнічної приналежності) при AД:
- Яке лікування є оптимальним з урахуванням потреб пацієнтів, ефективності, безпеки, переносимості різних варіантів терапії та наявності супутніх захворювань?
- Як найкраще здійснювати моніторування та контроль обраного варіанту лікування?
Де це було можливим і здійсненним, рекомендації ґрунтуються на доказах, з урахуванням результатів систематичного узагальнення доказів на основі суворих методів і практичного досвіду, отриманого групою експертів.
Цільові користувачі керівництва
Це керівництво було підготовлено для лікарів, зокрема дерматологів, педіатрів, алергологів, лікарів загальної практики та інших спеціалістів, які надають медичну допомогу хворим на АД. Пацієнти й опікуни також можуть отримати достовірну інформацію та поради щодо заснованих на доказах варіантів терапії.
Призначення експертів, управління конфліктом інтересів
До групи розробників рекомендацій увійшли 26 експертів із 12 країн, номіновані національними товариствами-партнерами EuroGuiDerm або двома співкоординаторами керівництва (A. Wollenberg і C. Flohr). Рада директорів EuroGuiDerm була ознайомлена з усіма претендентами, всі претенденти були затверджені Радою. Крім того, у розробці рекомендацій брали участь три представники пацієнтів.
Розробка рекомендацій і процес досягнення консенсусу
Розділи керівництва та рекомендації були розроблені членами групи, які сформували декілька робочих підгруп. Кожна глава та всі рекомендації були переглянуті та обговорені зі внесенням доречних змін усією групою експертів. Усі тексти та рекомендації були затверджені голосуванням під час консенсусних конференцій із необхідним мінімальним погодженням >50%. Було проведено як внутрішнє, так і зовнішнє рецензування. Розроблено плани поширення та впровадження.
Формулювання рекомендацій було стандартизовано (як запропоновано робочою групою Group Reading Assessment and Diagnostic Evaluation, GRADE).
Формулювання рекомендацій
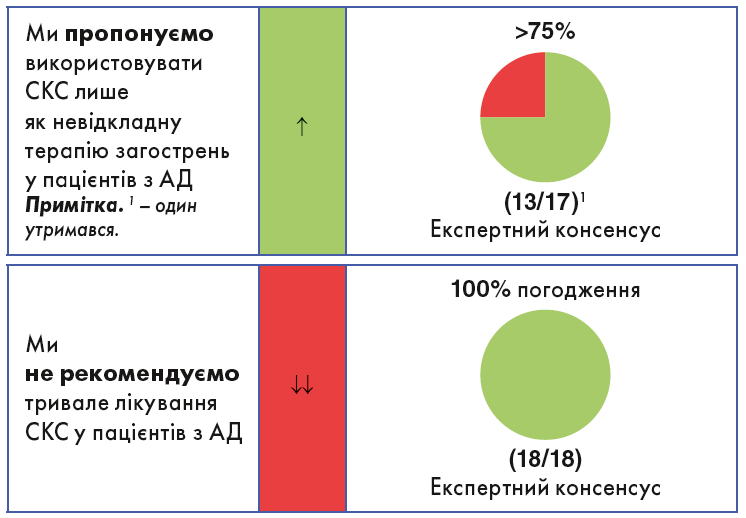
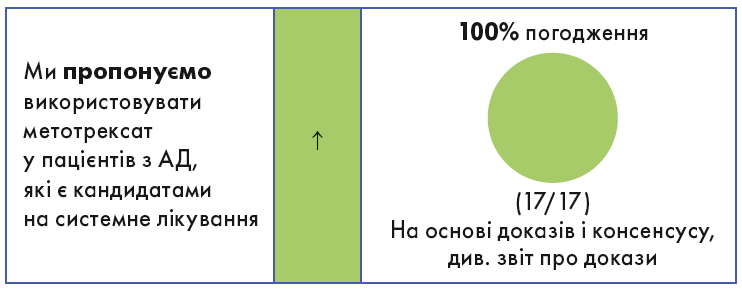
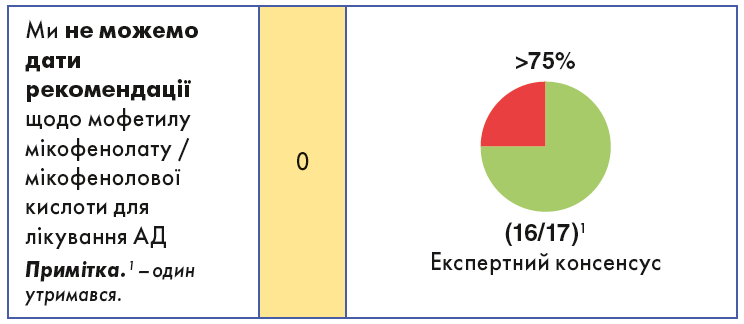
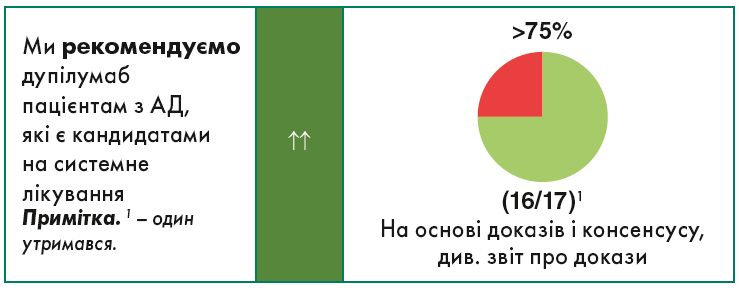
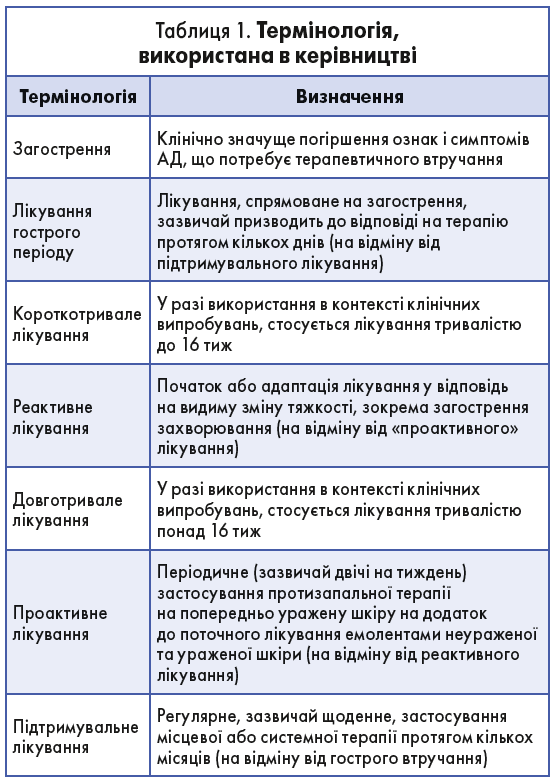
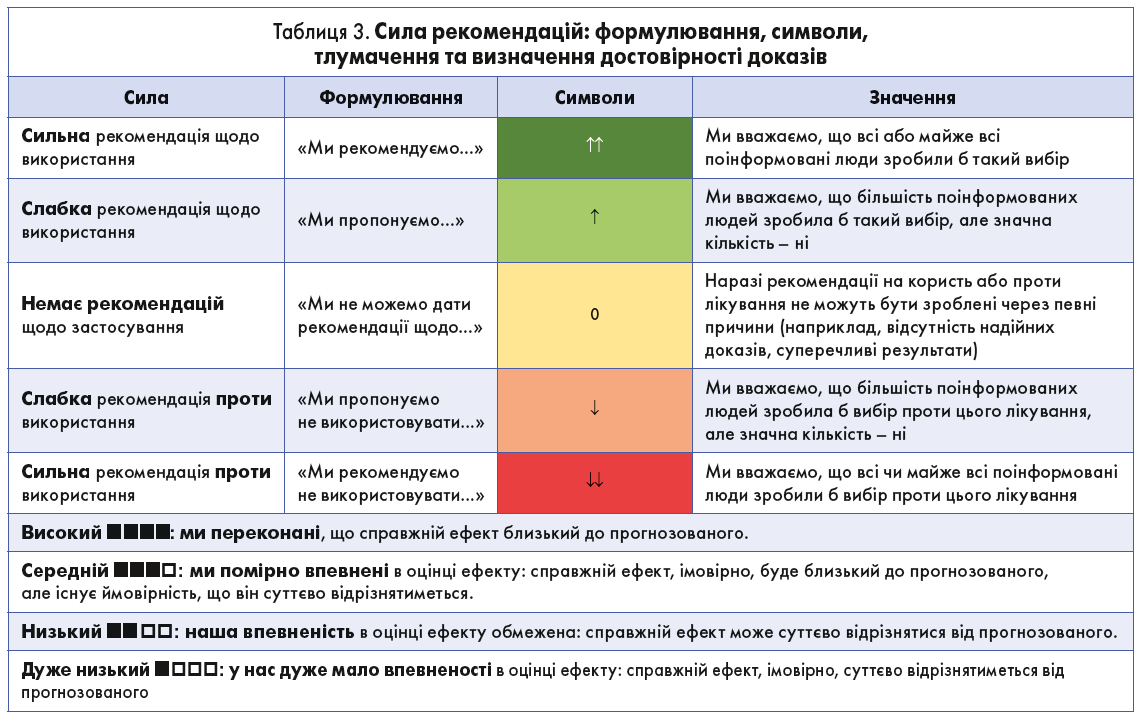
У цьому керівництві рекомендації подано таким чином: поряд із формулюванням (табл. 1, 2) стрілка(и) і кольори вказують напрям і силу кожної з них (табл. 3). Рівень згоди (консенсусна сила) відображено як фактичний відсоток, а також у формі категорійної кругової діаграми. Для всіх системних препаратів ми додали дозування (згідно з даними Європейського агентства з лікарських засобів). Крім того, де це можливо, було додано достовірність доказів (див. табл. 3; жирним шрифтом – значуща різниця; посилання подано відповідно до Drucker та співавт.).
Огляд рекомендацій
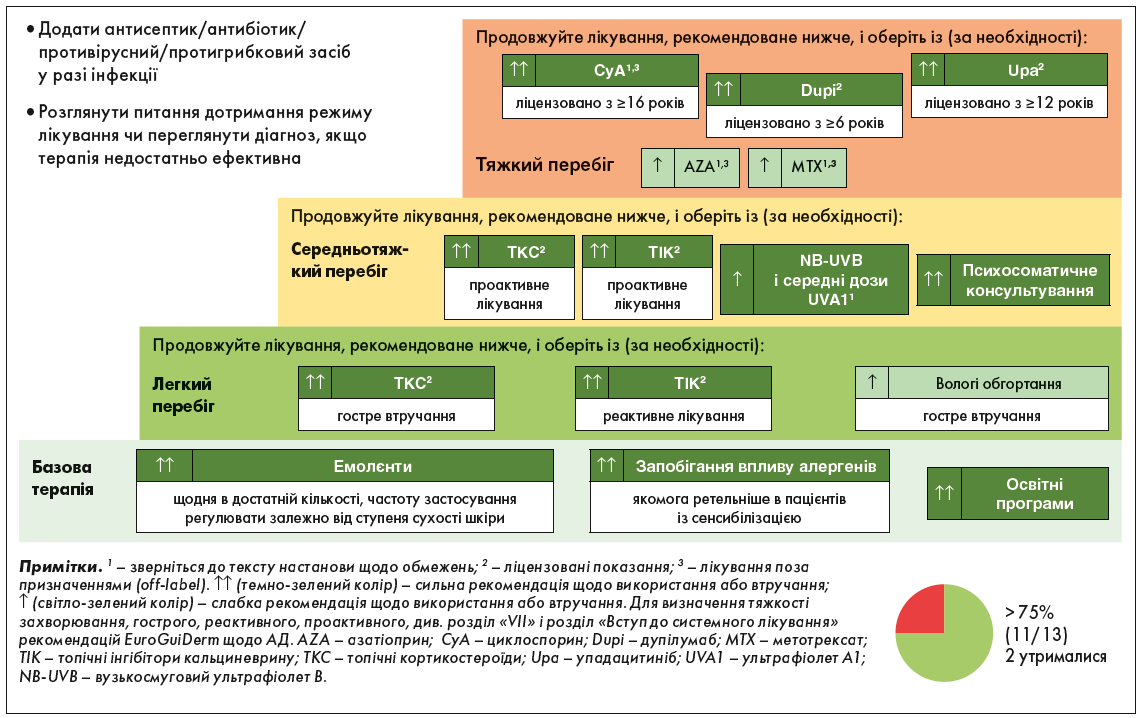
Покрокову терапію АД у дорослих і дітей та підлітків подано нижче на рисунках 1 і 2.
Рис. 1. Покрокова терапія АД у дорослих (Wollenberg et al., 2022)
Рис. 2. Покрокова терапія АД у дітей і підлітків
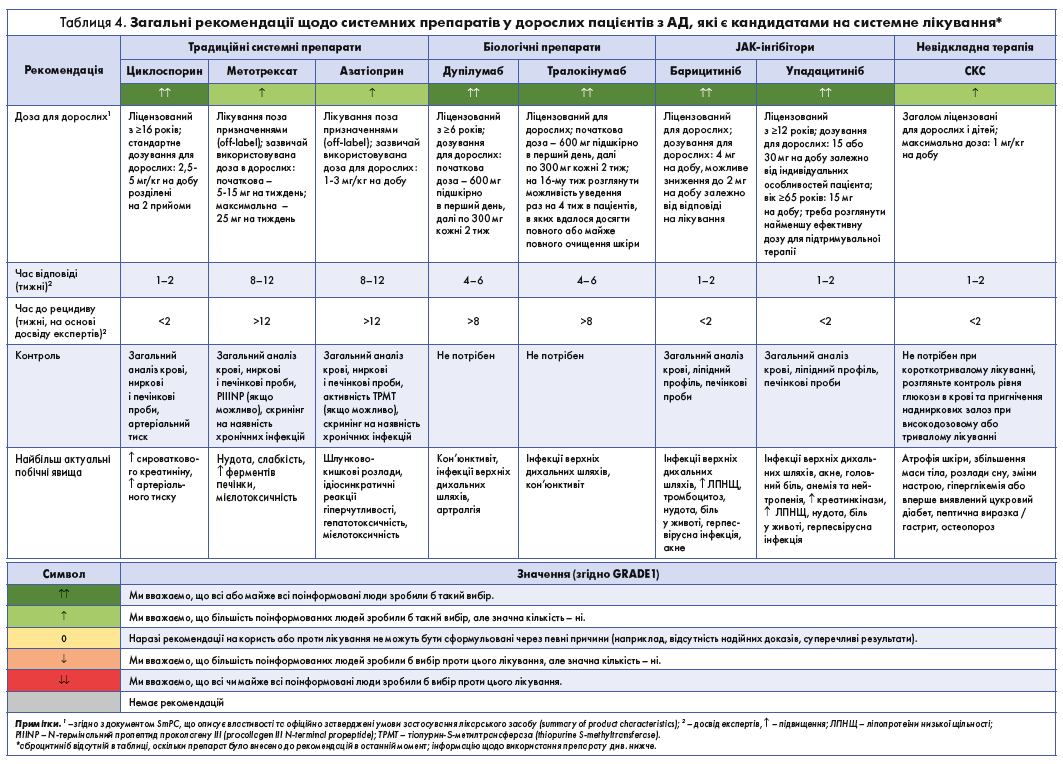
У таблиці 4 наведено загальні рекомендації щодо системних препаратів для дорослих пацієнтів з АД, які є кандидатами на системне лікування.
Вступ до системного лікування
Сфера системної терапії АД протягом останніх кількох років процвітає, оскільки багато нових речовин надходять на ринок, ліцензуються або перебувають на останньому етапі клінічної розробки. Програми ліцензування різноманітних нових біологічних препаратів і малих молекул забезпечують набагато кращий рівень доказів, ніж існує для ліків, які давно застосовують у практиці.
Традиційно системна терапія АД вважається необхідною, якщо ознаки та симптоми не можна належним чином контролювати за допомогою відповідних місцевих методів лікування та УФ-фототерапії. Системна терапія також може бути корисною для зменшення потреби в місцевих (топічних) кортикостероїдах (ТКС) у пацієнтів, які для контролю AД потребують застосування великої кількості потужних ТКС на значних ділянках тіла протягом тривалого часу.
Кандидатами на системне лікування можуть бути або пацієнти з високим сукупним балом, таким як SCORAD (SCORing Atopic Dermatitis) >50 (визначення за шкалою), або пацієнти, які клінічно не реагують на належним чином проведену місцеву терапію (функціональне визначення), або пацієнти, які не можуть брати участь у повсякденній діяльності, незважаючи на дотримання адекватного режиму лікування (соціальне визначення).
Місцеві настанови можуть потребувати використання інших оцінок, таких як лікарська шкала (наприклад, Eczema Area and Severity Index, EASI) у поєднанні з оцінкою симптомів пацієнтами (наприклад, Dermatology Life Quality Index, DLQI). Існує багато інших оцінок, узагальнених та оцінених ініціативою HOME (Harmonising Outcome Measures for Eczema), які також можуть слугувати основою для класифікації тяжкості захворювання.
 Необхідно підкреслити, що рішення про початок системного лікування є індивідуальним вибором пацієнта і що оцінка лише симптомів, наприклад EASI, не є адекватним інструментом для вирішення питання про призначення чи відміну системної терапії окремому пацієнту.
Необхідно підкреслити, що рішення про початок системного лікування є індивідуальним вибором пацієнта і що оцінка лише симптомів, наприклад EASI, не є адекватним інструментом для вирішення питання про призначення чи відміну системної терапії окремому пацієнту.
Перед початком системного лікування важливо виключити відповідні диференційні діагнози, такі як Т-клітинна лімфома шкіри та, в окремих випадках, первинні імунодефіцити. Треба переконатися, що з’ясовано потенційні тригерні фактори, а саме алергійний контактний дерматит, поведінкові та освітні причини поганої відповіді на лікування.
Донедавна імунодепресанти досить широкого спектра дії, такі як системні кортикостероїди (СКС), циклоспорин, азатіоприн, мофетилу мікофенолат, мікофенолат натрію в кишковорозчинній оболонці і метотрексат, були єдиним доступним варіантом системної терапії AД, що важко лікується. Більшість із них не були ліцензовані для цього показання (див. табл. 4).
Ці препарати можна умовно розділити на дві групи: СКС і циклоспорин мають швидкий початок дії та можуть використовуватися для лікування загострень АД або для покриття часу до початку дії системних імунодепресантів повільної дії, таких як метотрексат, азатіоприн та мофетилу мікофенолат / мікофенолат натрію в кишковорозчинній оболонці. Кінетика нових інгібіторів янус-кінази барицитинібу, аброцитинібу і упадацитинібу відносить ці препарати до групи швидкодіючих, тоді як для досягнення ефекту Th2-блокаторів дупілумабу, тралокінумабу і лебрикізумабу, а також засобу, що блокує рецептори IL31 – немолізумабу, потрібно кілька тижнів.
Під час пандемії COVID‑19 системній терапії потрібно приділяти особливу увагу, як зазначено в рекомендаціях Європейської робочої групи з атопічного дерматиту (European task force for atopic dermatitis). Особлива обережність потрібна, якщо пацієнти отримують комбіновану системну терапію.
Наведені рекомендації щодо системних препаратів базуються на висновках експертів, актуальному систематичному огляді Drucker та співавт., іншій опублікованій літературі та медичних міркуваннях і можуть відрізнятися від правового статусу ліцензування та шляхів доступу, які не є однаковими в європейських країнах.
Традиційні системні препарати
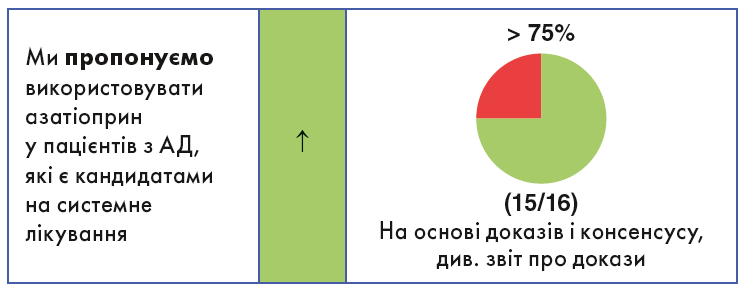
Азатіоприн
Механізм дії та ефективність
Азатіоприн належить до проліків, які in vivo швидко перетворюються на антиметаболіт 6-меркаптопурин (6‑МП) після розщеплення бічного ланцюга імідазолу.
Вважають, що він виявляє свій основний імуносупресивний ефект через метаболіти 6-МП, тіогуанінові нуклеотиди, які згодом вбудовуються в ДНК, пригнічуючи її синтез.
Ефективність азатіоприну порівнянна з такою метотрексату, але нижча, ніж у дупілумабу і циклоспорину, щодо усунення клінічних ознак АД.
Комбінація з іншими методами лікування
Одночасно з азатіоприном можна застосовувати місцеву терапію КС і/або інгібіторами кальциневрину.
Через потенційно підвищений ризик розвитку раку шкіри азатіоприн не можна поєднувати з ультрафіолетовими променями (A, B та PUVA).
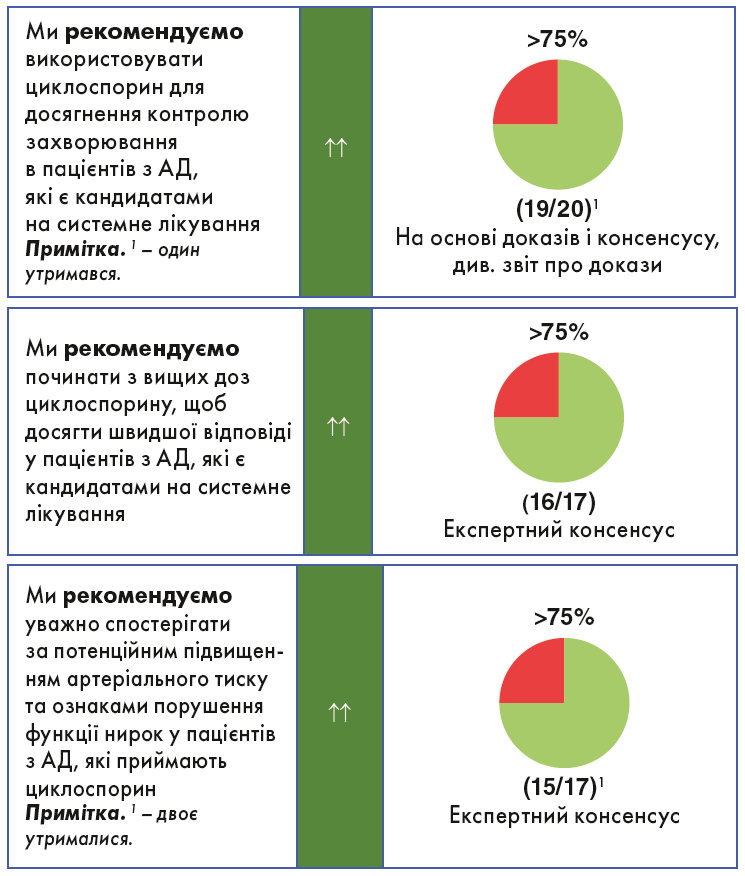
Циклоспорин
Механізм дії та ефективність
Циклоспорин пригнічує активацію та проліферацію Т-клітин шляхом блокування утворення цитокінів, залежного від ядерного фактора активованих Т-клітин (nuclear factor of activated T-cell, NFAT).
Циклоспорин був схвалений для лікування АД у дорослих у багатьох європейських країнах і вважається препаратом першої лінії для пацієнтів із тяжким захворюванням, якщо інші нові методи лікування недоступні або не показані. Циклоспорин дуже ефективний при АД як у дітей, так і в дорослих, із кращою переносимістю у дітей.
У метааналізі, що оцінює лікування терміном до 16 тиж, виявлено схожу ефективність циклоспорину й дупілумабу. Реальні дані демонструють, що після 16 міс лікування триваліше застосування без потреби у відміні препарату спостерігали щодо дупілумабу порівняно з циклоспорином. У прямих дослідженнях циклоспорин перевершував метотрексат, преднізолон, внутрішньовенний імуноглобулін, ультрафіолетові промені А та B і був схожим за ефективністю на мікофенолат натрію в кишковорозчинній оболонці.
При короткотривалому лікуванні АД вищі дози циклоспорину (5 мг/кг на добу) призводять до швидшої відповіді та є ефективнішими, ніж нижчі дози (2,5-3 мг/кг на добу). Довготривале застосування циклоспорину впродовж до 1 року може бути рекомендовано на основі кількох досліджень; однак їх докази обмежені через відкритий дизайн і високі показники вибуття.
Комбінація з іншими методами лікування
Одночасно з циклоспорином можна застосовувати ТКС і/або ТІК.
Через потенційно підвищений ризик розвитку раку шкіри циклоспорин не треба поєднувати з ультрафіолетовими променями (A, B та PUVA).
СКС
Механізм дії та ефективність
КС – це клас стероїдних гормонів, які зв’язуються з глюкокортикоїдними рецепторами. Активований глюкокортикоїдний рецепторний комплекс посилює експресію протизапальних білків і пригнічує експресію прозапальних білків, що призводить до широких протизапальних ефектів.
Існує лише декілька досліджень у дорослих і дітей з АД, незважаючи на регулярне застосування СКС у клінічній практиці. У дослідженнях, проведених в дітей і дорослих, СКС не забезпечували досягення тривалої ремісії, і швидкі рецидиви були поширеним явищем. СКС значно менш ефективні, ніж циклоспорин.
Дозування: загострення, короткотривале, довготривале
- Загострення: початкова доза зазвичай становить 0,5 мг/кг маси тіла на добу. Якомога швидше треба припинити лікування або зменшити дозу.
- Короткотривале та довготривале: не рекомендується.
Ми рекомендуємо поєднувати СКС, як і в разі будь-якого системного лікування, з емолентами та, за необхідності, місцевою протизапальною терапією в пацієнтів з АД.
Безпека
СКС мають широкий терапевтичний індекс. Токсичність залежить від середньої дози, кумулятивної дози і тривалості використання. У високих дозах і за тривалого застосування (зазвичай >0,5 мг/кг/добу) важливими побічними ефектами є атрофія шкіри, збільшення маси тіла, розлади сну, зміни настрою, гіперглікемія або вперше виявлений цукровий діабет, пептична виразка /гастрит, остеопороз та підвищена сприйнятливість до інфекцій. Зокрема, у разі довготривалого застосування в пацієнтів може відбуватися пригнічення функції надниркових залоз, і разом із високим ризиком розвитку повторних загострень у разі зниження дози відміна терапії може бути складною. Тому необхідно уникати довготривалого застосування СКС у дорослих і дітей. Навіть доволі високу дозу можна просто відмінити, не зменшуючи її, якщо приймати препарат не більш ніж 3 тижні.
Комбінація з іншими методами лікування
Жоден з інших методів лікування АД при застосуванні СКС не протипоказаний.
Метотрексат
Механізм дії та ефективність
Метотрексат є антагоністом фолієвої кислоти, який перешкоджає поділу клітин, синтезу та репарації ДНК/РНК і синтезу білка, повністю пригнічуючи активність імунної системи. Хоча його точна дія при АД повністю не вивчена, припускають можливість пригнічення шляху янус-кінази / переносників сигналів та активаторів транскрипції (Janus kinase/signal transducers and activators of transcription, JAK/STAT).
Метотрексат використовували для лікування середньотяжкого й тяжкого АД протягом багатьох років, але його ефективність і схеми застосування вивчали лише в обмеженій кількості нерандомізованих контрольованих досліджень. Отже, рекомендації здебільшого ґрунтувалися на серії випадків і консенсусі експертів, одному контрольованому дослідженні, в якому метотрексат порівнювали з азатіоприном у дорослих, і відкритому рандомізованому багатоцентровому дослідженні в дітей.
Загалом ці дослідження підтверджують, що метотрексат можна вважати помірно ефективним, відносно безпечним препаратом із хорошою переносимістю для лікування тяжкого АД як у дітей, так і в дорослих; ці результати також відповідають даним нещодавніх ретроспективних досліджень. Ефективність метотрексату щодо усунення клінічних ознак АД на 16-му тиж лікування порівнянна з такою азатіоприну і є нижчою, ніж у дупілумабу і циклоспорину. Однак немає довгострокових прямих досліджень для подальшого порівняння.
Початок дії розвивається впродовж кількох тижнів, а максимальна ефективність спостерігається через місяці, але швидкість настання терапевтичного ефекту залежить від режиму дозування. Одне дослідження у дорослих демонструє, що пацієнти, які не отримують користі від терапії середніми дозами метотрексату (10-15 мг/тиж) протягом 3 міс, імовірно, не отримають користі від збільшення дози. Однак повільне поступове підвищення дози метотрексату може призвести до недооцінки терапевтичного потенціалу препарату при АД. Для дітей рекомендована доза становить 0,4 мг/кг/тиж, що значно вище, ніж дозування для дорослих. 25 мг/тиж є широко використовуваною максимальною дозою для лікування дорослих і дітей з АД.
Комбінація з іншими методами лікування
Комбінація з ТКС, ТІК або вузькосмуговою УФ-фототерапією є загальноприйнятою комбінацією лікування і вважається безпечною. Одночасне застосування циклоспорину є відносним протипоказанням. Є досвід використання з інгібітором JAK барицитинібом при ревматоїдному артриті.
Мофетилу мікофенолат
Механізм дії та ефективність
Мофетилу мікофенолат є проліками мікофенолової кислоти (mycophenolic acid, МФК), інгібітора інозин‑50-монофосфатдегідрогенази. МФК виснажує гуанозинові нуклеотиди переважно в Т- і В-лімфоцитах і пригнічує їхню проліферацію. МФК також пригнічує глікозилювання та експресію молекул адгезії і залучення лімфоцитів і моноцитів до місць запалення.
У недавньому систематичному огляді і метааналізі, що охопили 18 досліджень за участю 140 дорослих і дітей, оцінювали ефективність використання мофетилу мікофенолату не за призначенням у пацієнтів з АД із рефрактерністю до інших системних препаратів першого ряду або їх непереносимістю. Було встановлено значне, на 18 балів (р=0,0002), зниження оцінки SCORAD внаслідок лікування, при цьому 77,6% пацієнтів повідомили про часткову або повну ремісію. Рецидиви розвивалися у 8,2% випадків. Середній час до розвитку ефекту становив 6,8±7 тижнів.
Комбінація з іншими методами лікування
Одночасно з мофетилу мікофенолатом можна застосовувати місцеву терапію КС і/або інгібіторами кальциневрину.
Біологічні препарати
Дупілумаб
Механізм дії та ефективність
Дупілумаб є першим повним людським моноклональним антитілом IgG4 (МАТ) для лікування АД. Він уже більш ніж 2 роки доступний для лікування дорослих у багатьох країнах. Нещодавно в деяких країнах препарат також був схвалений для підлітків і дітей старших 6 років. Дупілумаб зв’язується з α-субодиницею рецептора IL‑4, який є частиною рецепторного комплексу як IL‑4, так і IL‑13. Безпека та ефективність дупілумабу переважно були встановлені в плацебо-контрольованих дослідженнях помірнотяжкого і тяжкого АД. Дупілумаб продемонстрував значні клінічні ефекти за трьома різними інструментами оцінки тяжкості: індекс площі та тяжкості екземи (Eczema Area and Severity Index, EASI), глобальна оцінка дослідника (Investigator’s Global Assessment, IGA) і SCORing АД (SCORAD). Крім того, лікування дупілумабом значно зменшує свербіж.
Препарат продемонстрував ефективність як за наявності, так і в разі відсутності підвищеного рівня IgE у пацієнтів з АД. Дупілумаб також зареєстрований для лікування астми середнього і тяжкого ступеня, еозинофільного езофагіту та хронічного риносинуситу з назальними поліпами, таким чином охоплюючи кілька захворювань з 2-м типом запалення.
Комбінація з іншими методами лікування
У додатковому дослідженні III фази вивчали лікування дупілумабом у комбінації з ТКС у порівнянні з плацебо плюс ТКС протягом 52 тижнів. Первинними кінцевими точками серед інших були кількість пацієнтів, які досягли 0/1 балу загальної оцінки дослідника (IGA) і 75% поліпшення за шкалою EASI, що оцінювали на 16-й тиж лікування: більшість пацієнтів, які отримували дупілумаб і ТКС, досягли комбінованих первинних кінцевих точок IGA‑0/1 та EASI‑75. Результати через 52 тиж були подібними. У цьому дослідженні приблизно на 15% більше осіб досягли 75% зниження показника EASI на 16-му тиж порівняно з попередніми дослідженнями III фази, де дупілумаб застосовували у вигляді монотерапії.
Добре зарекомендувала себе комбінована терапія дупілумабом з ТКС, ТІК та УФ-фототерапією.
Особливі зауваження
Пацієнти з АД і супутніми захворюваннями з 2-м типом запалення, такими як астма, алергійний ринокон’юнктивіт із назальними поліпами або еозинофільний езофагіт, також можуть мати користь від лікування дупілумабом.
Інші біологічні препарати: лебрикізумаб і немолізумаб
Зазначені препарати наразі не ліцензовані для будь-яких показань ні в Україні, ні у світі.
Омалізумаб
Механізм дії та ефективність
Більшість пацієнтів з АД мають підвищений рівень IgE в сироватці крові, але патогенетична роль IgE при АД залишається невідомою. Анти-IgE-антитіла – омалізумаб – з великим успіхом використовують для лікування хронічної спонтанної кропив’янки. Нещодавній систематичний огляд і метааналіз оцінили доклінічні і випробувальні дані щодо лікування АД омалізумабом, які є суперечливими.
Омалізумаб ліцензовано для лікування астми та хронічної спонтанної кропив’янки, але не для лікування АД.
Омалізумаб зв’язує вільний IgE, що призводить до утворення імунних комплексів IgE та омалізумабу. IgE, зв’язаний з омалізумабом, не може зв’язуватися з альфа-ланцюгом високоафінного рецептора IgE, тим самим пригнічуючи його зв’язування з опасистими клітинами, базофілами та епідермальними дендритними клітинами, і подальші імунологічні ефекти.
Є багато повідомлень про клінічні випадки та серії випадків, але лише кілька контрольованих досліджень вивчали застосування омалізумабу для лікування АД.
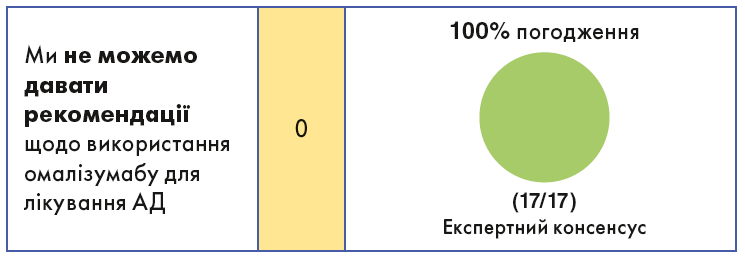
Підсумкові дані демонструють помітну, але помірну ефективність омалізумабу щодо полегшення ознак і симптомів АД. Не визначено прогностичних маркерів, пов’язаних із кращою клінічною відповіддю, а більшість опублікованих доказів є низької якості. Безпека омалізумабу є дуже хорошою, але непередбачувана та статистично низька ефективність не дає змогу давати загальні рекомендації щодо омалізумабу для лікування АД.
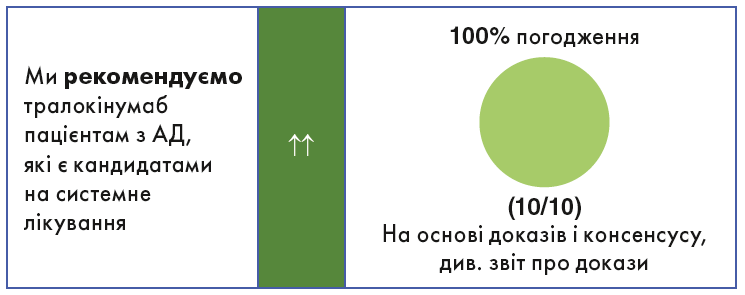
Тралокінумаб
Препарати тралокінумабу в Україні не зареєстровані.
JAK-інгібітори
Родина янус-кіназ (JAK), що охоплює JAK1, JAK2, JAK3 і тирозинкіназу‑2 (tyrosine kinase 2, TYK2), є класом цитоплазматичних тирозинкіназ. JAK приєднуються до внутрішньоклітинної частини ланцюгів рецепторів цитокінів для утворення функціональних сигнальних комплексів і регуляції запального процесу шляхом активації внутрішньоцитоплазматичних факторів транскрипції (STAT). У разі активації білки STAT виробляють димери, які транслокуються в ядро і активують або пригнічують експресію цільового гена медіаторів запалення, що свідчить про те, що інгібування активності JAK може бути ефективнішим, ніж прицільне блокування окремого цитокіну. Повідомляють, що окрім порушення передачі сигналів шкірних запальних цитокінів інгібування JAK послаблює хронічний свербіж і покращує функцію шкірного бар’єра шляхом регулювання експресії шкірного бар’єрного білка філагрину.
Аброцитиніб
Аброцитиніб сьогодні ліцензований для лікування АД в осіб віком від 12 років у Великій Британії. 14 жовтня 2021 р. Комітет із лікарських засобів (European Medicines Agency, EMA) прийняв позитивний висновок лише для дорослих. Оскільки це схвалення було отримано після наших консенсусних конференцій, жодна консенсусна рекомендація не увійшла до цієї редакції керівництва.
Механізм дії та ефективність
Аброцитиніб – пероральний селективний інгібітор JAK1, що продемонстрував ефективність у пацієнтів із помірнотяжким і тяжким АД при застосуванні як у монотерапії (дослідження MONO‑1 і -2), так і в комбінації з місцевою терапією для досягнення відповіді на лікування порівняно з плацебо (дослідження COMPARE). Ефективність визначали за допомогою інструментів IGA та EASI‑75.
Наприклад, у дослідженнях MONO частка пацієнтів із відповіддю EASI‑75 на 12-му тиж була значно вищою в разі прийому аброцитинібу в дозі 100 мг (~40-45%) і аброцитинібу в дозі 200 мг (~61-63%) порівняно з плацебо (~10-12%). У дослідженні COMPARE частка пацієнтів із відповіддю EASI‑75 при прийомі аброцитинібу в дозі 100 мг (~59%) і аброцитинібу в дозі 200 мг (~70%) була значно більшою порівняно з плацебо (27%). Подібна ефективність була продемонстрована в дослідженні JADE TEEN серед підлітків у дозуванні 100 і 200 мг у поєднанні з місцевою терапією.
Важливо зазначити, що в дослідженні COMPARE (в якому проводили порівняння з дупілумабом) після 16 тиж лікування спостерігали вищі показники відповіді на терапію аброцитинібом у дозі 200 мг порівняно з дупілумабом (значення р не розраховували). Ефективність аброцитинібу в дозі 100 мг і дупілумабу була подібною. Результати показують, що аброцитиніб у дозі 200 мг може забезпечити вищу ймовірність відповіді на лікування порівняно з дупілумабом у пацієнтів із тяжким АД.
Комбінація з іншими методами лікування
На сьогодні не було опубліковано жодних досліджень, які б оцінювали використання аброцитинібу з іншими системними методами лікування.
Інші JAK-інгібітори – барицитиніб та упадацитиніб
Зазначені представники JAK-інгібіторів, що не зареєстровані в Україні.
Інше системне лікування. Алітретиноїн
Механізм дії та ефективність
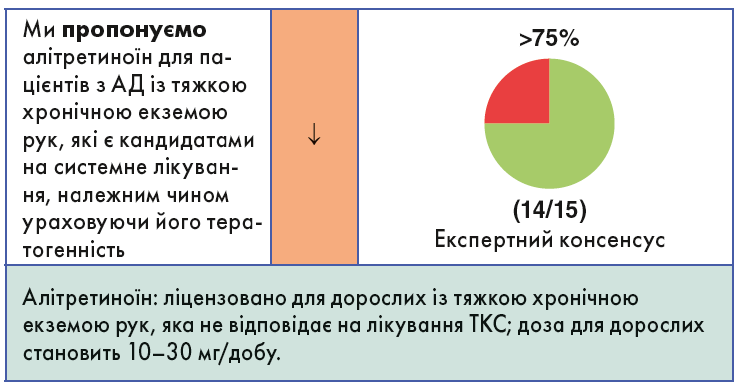
Алітретиноїн – це ретиноїд, який зв’язує 2 типи рецепторів – ретиноєвої кислоти (retinoid acid receptor, RAR) і ретиноїду X (retinoid X receptor, RXR), таким чином забезпечуючи протизапальну й антипроліферативну дію. Він ліцензований у деяких європейських країнах для лікування хронічної екземи рук незалежно від її патогенезу.
Існує одне велике багатоцентрове рандомізоване плацебо-контрольоване клінічне випробування за участю 1032 пацієнтів із хронічною екземою рук, приблизно одна третина з яких, імовірно, були пацієнтами з атопічною екземою рук. Поліпшення перебігу екземи спостерігали в 75% пацієнтів. Групу пацієнтів, які страждають на атопічну екзему рук, окремо не аналізували, а позадолонні симптоми в цьому дослідженні не оцінювали.
У неконтрольованому відкритому дослідженні 6 пацієнтів з АД і вираженим ураженням рук отримували алітретиноїн протягом 12 тижнів. За даними модифікованої загальної оцінки симптомів ураження рук (modified Total Lesion Symptom Score, mTLSS) і балів SCORAD, як долонне, так і позадолонне ураження в процесі дослідження покращилися.
Комбінація з іншими методами лікування
Одночасно з алітретиноїном можна застосовувати ТКС, ТІК та емоленти.
За матеріалами Wollenberg A., Kinberger M., Arents B., et al. European guideline (EuroGuiDerm) on atopic eczema: part I – systemic therapy. J Eur Acad Dermatol Venereol. 2022 Sep;36(9):1409–1431. doi: 10.1111/jdv.18345.
Друкується в скороченому обсязі, повна версія: https://onlinelibrary.wiley.com/doi/10.1111/jdv.18345
Підготувала к. мед. н. Світлана Опімах
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (67) 2024 р.




.png)