9 жовтня, 2023
Клініко-лабораторна ефективність комплексного лікування гострого тонзилофарингіту в дітей і дорослих
 Гострі запальні захворювання ротової частини глотки є дуже поширеними серед населення та становлять близько 30% у структурі патології верхніх дихальних шляхів. Хворі цього профілю становлять значну частку амбулаторної практики як отоларингологічного, так і педіатричного й терапевтичного профілю [4].
Гострі запальні захворювання ротової частини глотки є дуже поширеними серед населення та становлять близько 30% у структурі патології верхніх дихальних шляхів. Хворі цього профілю становлять значну частку амбулаторної практики як отоларингологічного, так і педіатричного й терапевтичного профілю [4].
Біль у горлі є одним із перших і провідних симптомів гострих респіраторних захворювань, серед яких найпоширенішим є гострий тонзилофарингіт (ГТФ) [3, 5]. Слід зазначити, що тонзилофарингіт передбачає одночасне ураження тканини глотки та піднебінних мигдаликів (ПМ). Серед діагнозів, які найчастіше встановлюють оториноларингологи, це захворювання відзначається приблизно у 20% випадків (за даними Medical Data Management).
Результати численних наукових досліджень, що ґрунтуються на принципах доказової медицини, свідчать про необхідність уникати застосування антибіотиків у разі ГТФ нестрептококової етіології [6-8]. Симптоматичне лікування таких пацієнтів рекомендовано як терапію першої лінії, антибіотики мають залишатися в резерві для хворих насамперед із високим ризиком розвитку ускладнень.
У зв’язку із цим значний клінічний інтерес для лікарів-практиків становить можливість комплексного застосування препаратів Целіста Спрей і Целіста Дуо, які мають потужну протизапальну, антисептичну й імуномодулювальну дію, навіть у групах ризику [1, 2]. Поєднання двох різних антисептиків дає змогу використати силу двох механізмів дії, що посилює ефективність протимікробної терапії топічними антисептиками. Крім того, Целіста у формі спрею допомагає значно збільшити площу контакту антисептика, дістатися важкодоступних місць (у лакунах і криптах мигдаликів), чого непросто досягнути тільки при розсмоктуванні таблеток або льодяників.
Метою цього клінічного дослідження було оцінювання клініко-лабораторної ефективності комплексної терапії препаратами Целіста Спрей і Целіста Дуо виробництва компанії «Дарниця» при лікуванні дітей і дорослих із ГТФ.
Матеріали та методи
Клініко-лабораторні дослідження хворих було проведено на клінічній базі кафедри дитячої оториноларингології, аудіології та фоніатрії Національного університету охорони здоров’я України ім. П.Л. Шупика.
Протягом першої половини 2023 року було обстежено 40 хворих із ГТФ, які були розподілені за віком на дві групи спостереження. До першої групи (Г-1) входили діти від 4 до 12 років; основна терапія: Целіста Спрей – 1-разове натискання 3-4 рази на добу для дітей віком 4-6 років і 2-разове натискання 3-4 рази на добу для дітей віком 7-12 років; Целіста Дуо – по 1 таблетці що 3 год, після зменшення симптомів запалення – по 1 таблетці що 4 год протягом 5-7 днів. Хлопчиків було 11, дівчаток – 9, середній вік – 6,5±0,4 року. Середня тривалість перебігу ГТФ – 5,2±0,3.
Другу групу (Г-2) становили пацієнти віком від 15 років; основна терапія: Целіста Спрей – 3-4-разове натискання 3-4 рази на добу; Целіста Дуо – по 1 таблетці що 2 год, після зменшення симптомів запалення – по 1 таблетці що 4 год протягом 5-7 днів. Хлопчиків було 12, дівчаток – 8, середній вік – 16,8±0,7 року. Середня тривалість перебігу ГТФ – 5,4±0,4.
Ефективність проведеної терапії оцінювалася за зменшенням виразності клінічних проявів захворювання, а також за динамікою даних бактеріологічного та цитологічного досліджень із ПМ.
Переносимість препаратів оцінювалася на підставі суб’єктивних відчуттів, про які повідомляли пацієнти, а також об’єктивних даних, отриманих у процесі лікування. Враховувалися динаміка лабораторних показників, а також частота виникнення й характер побічних реакцій у хворих після застосування препаратів.
Дослідження передбачало два етапи: скринінг (період набору пацієнтів) і період лікування (5-7 днів). Для обстеження хворих було використано такі клінічні та лабораторні методи:
- збір суб’єктивних скарг пацієнтів (біль/сухість/пирхота в горлі);
- об’єктивне обстеження – орофарингоскопія (ступінь гіперемії, набряк, зернистість слизової оболонки, наявність і характер патологічного вмісту в мигдаликах).
Виразність показників у балах оцінювали відповідно до такої шкали: 0 – відсутність ознаки, 1 – помірний ступінь, 2 – середній ступінь, 3 – сильний ступінь.
Мікробіологічні та цитологічні дослідження з ПМ виконували згідно з чинними нормативними документами за загальноприйнятими методиками. Кількісну оцінку мікробіоценозу встановлювали за показниками пенетрантності, популяційного рівня бактерій при підрахунку колонієутворювальних одиниць в 1 г матеріалу (lg КУО/г). Мікроорганізми ідентифікували за біохімічними властивостями до рівня роду або виду з міжнародного визначення бактерій Берджи.
Статистичну обробку матеріалу здійснювали з використанням методу кутового перетворення за Фішером.
Результати дослідження
Під час об’єктивного обстеження хворих на ГТФ такі симптоми, як гіперемія, набряк ПМ, зернистість слизової оболонки задньої стінки глотки, в перший день лікування спостерігалися в переважної більшості пацієнтів. Дані клінічної картини ГТФ у дітей групи спостереження до та після лікування представлено в таблицях 1 і 2.
|
Таблиця 1. Дані фарингоскопії дітей із Г-1, хворих на ГТФ, до та після лікування |
||
|
Клінічні ознаки ГТФ |
Група спостереження 1 (n=20) |
|
|
До лікування |
Після лікування |
|
|
Гіперемія ПМ і слизової оболонки задньої стінки глотки |
2,72±0,06 |
0,54±0,05* |
|
Набряк ПМ і слизової оболонки задньої стінки глотки |
2,44±0,03 |
0,61±0,04* |
|
Зернистість слизової оболонки задньої стінки глотки |
2,12±0,07 |
0,82±0,03* |
|
Примітка: * p<0,05 – різниця до та після лікування достовірна. |
||
|
Таблиця 2. Дані фарингоскопії дітей із Г-2, хворих на ГТФ, до та після лікування |
||
|
Клінічні ознаки ГТФ |
Група спостереження 2 (n=20) |
|
|
До лікування |
Після лікування |
|
|
Гіперемія ПМ і слизової оболонки задньої стінки глотки |
2,82±0,08 |
0,62±0,04* |
|
Набряк ПМ і слизової оболонки задньої стінки глотки |
2,38±0,06 |
0,53±0,07* |
|
Зернистість слизової оболонки задньої стінки глотки |
2,33±0,07 |
0,91±0,04* |
|
Примітка: * p<0,05 – різниця до та після лікування достовірна. |
||
Результати аналізу виразності суб’єктивних скарг пацієнтів із ГТФ, яку було оцінено в балах до та після проведеного лікування, представлено в таблицях 3 та 4.
|
Таблиця 3. Суб’єктивні скарги дітей із Г-1, хворих на ГТФ, до та після лікування |
||
|
Скарги хворих на ГТФ |
Група спостереження 1 (n=20) |
|
|
До лікування |
Після лікування |
|
|
Біль у горлі |
2,84±0,06 |
0,32±0,05* |
|
Відчуття сухості в горлі |
2,32±0,08 |
0,41±0,03* |
|
Пирхота в горлі |
2,12±0,04 |
0,33±0,04* |
|
Примітка: * p<0,05 – різниця до та після лікування достовірна. |
||
|
Таблиця 4. Суб’єктивні скарги дітей із Г-2, хворих на ГТФ, до та після лікування |
||
|
Скарги хворих на ГТФ |
Група спостереження 2 (n=20) |
|
|
До лікування |
Після лікування |
|
|
Біль у горлі |
2,91±0,03 |
0,42±0,04* |
|
Відчуття сухості в горлі |
2,32±0,06 |
0,34±0,05* |
|
Пирхота в горлі |
2,47±0,05 |
0,24±0,06* |
|
Примітка: * p<0,05 – різниця до та після лікування достовірна. |
||
За результатами клінічного спостереження пацієнтів, гіперемія ПМ і слизової оболонки задньої стінки глотки швидко зменшувалася та практично була відсутня на 2-3-й день лікування. Загалом під час оцінювання клінічної ефективності локальної терапії 17 пацієнтів із 20 Г-1 і 19 пацієнтів із 20 Г-2 відзначили добру переносимість терапії та значне поліпшення вже на 2-гу добу лікування.
Проведені мікробіологічні дослідження з ПМ установили, що в дітей, хворих на ГТФ, найчастіше виділяли мікробні асоціації, представлені Streptococcaceae (S. pyogenes), непатогенні штами (S. viridans, коки роду Neisseria) та мікроорганізми родини Micrococcaceae (Staphylococcus aureus), а також були висіяні гриби роду Candida.
|
Таблиця 5. Мікрофлора ПМ у дітей із Г-1, хворих на ГТФ, до та після лікування |
||
|
Мікрофлора |
Група спостереження 1 (n=20) |
|
|
До лікування |
Після лікування |
|
|
Streptococcus spр. |
11 |
4* |
|
S. pyogenes |
8 |
3* |
|
S. aureus |
9 |
3* |
|
Н/п нейсерії |
11 |
8 |
|
S. viridans |
10 |
12 |
|
Примітка: * p<0,05 – різниця до та після лікування достовірна. |
||
|
Таблиця 6. Мікрофлора ПМ у дітей із Г-2, хворих на ГТФ, до та після лікування |
||
|
Мікрофлора |
Група спостереження 2 (n=20) |
|
|
До лікування |
Після лікування |
|
|
Streptococcus spр. |
12 |
5* |
|
S. viridans |
8 |
12* |
|
Н/п нейсерії |
7 |
9 |
|
S. aureus |
10 |
5* |
|
S. pyogenes |
7 |
4* |
|
Klebsiella pneumoniae |
6 |
4 |
|
Candida spp. |
7 |
3 |
|
Примітка: * p<0,05 – різниця до та після лікування достовірна. |
||
Після проведеного комплексного лікування препаратами Целіста Спрей і Целіста Дуо в дітей, хворих на ГТФ, етіологічно значущі види мікроорганізмів висівали в зменшеній кількості до <2,5×10 КУО/тампон, що може оцінюватися виключно як носійство. Згідно з отриманими даними щодо зміни мікробного пейзажу ПМ після застосування місцево препаратів Целіста Спрей і Целіста Дуо було встановлено, що їх використання сприяє достовірному відновленню мікробіоценозу ПМ через зменшення кількості патогенної й умовно-патогенної флори, а також збільшення кількості індигенної нормофлори.
При цитологічному дослідженні клітинних елементів із ПМ було встановлено, що застосування препаратів Целіста Спрей і Целіста Дуо сприяло достовірному зниженню числа нейтрофільних лейкоцитів і збільшенню кількості епітеліальних клітин (табл. 7, 8).
|
Таблиця 7. Дані цитологічного аналізу з ПМ у дітей із Г-1, хворих на ГТФ, до та після лікування |
|||
|
Діти, хворі на ГТФ |
Відносний уміст клітин, % |
||
|
Нейтрофіли |
Епітеліальні клітини |
Лімфоцити |
|
|
До лікування |
37,0 |
54,0 |
9,0 |
|
Після лікування |
11,0* |
82,0* |
7,0 |
|
Примітка: * p<0,05 – різниця до та після лікування достовірна. |
|||
|
Таблиця 8. Дані цитологічного аналізу з ПМ у дітей із Г-2, хворих на ГТФ, до та після лікування |
|||
|
Діти, хворі на ГТФ |
Відносний уміст клітин, % |
||
|
Нейтрофіли |
Епітеліальні клітини |
Лімфоцити |
|
|
До лікування |
41,0 |
51,0 |
8,0 |
|
Після лікування |
15,0* |
80,0* |
5,0 |
|
Примітка: * p<0,05 – різниця до та після лікування достовірна. |
|||
Переносимість лікування ГТФ препаратами Целіста Спрей і Целіста Дуо в усіх пацієнтів груп спостереження при місцевому застосуванні була добра, в жодному клінічному випадку побічних дій і алергічних реакцій зафіксовано не було.
Усі пацієнти, які були залучені до клінічного дослідження, відзначали зручність у застосуванні та хороші смакові властивості препаратів Целіста Спрей і Целіста Дуо, відсутність побічних ефектів від прийому, відмінний дизайн упаковки.
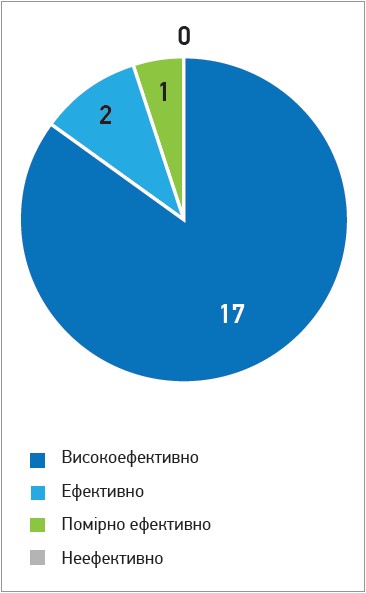
Рис. 1. Оцінка ефективності комплексного застосування препаратів Целіста Спрей і Целіста Дуо, на думку хворих із Г-1
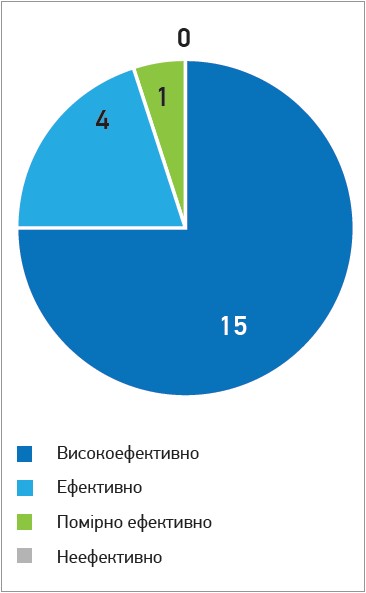
Рис. 2. Оцінка ефективності комплексного застосування препаратів Целіста Спрей і Целіста Дуо, на думку хворих із Г-2
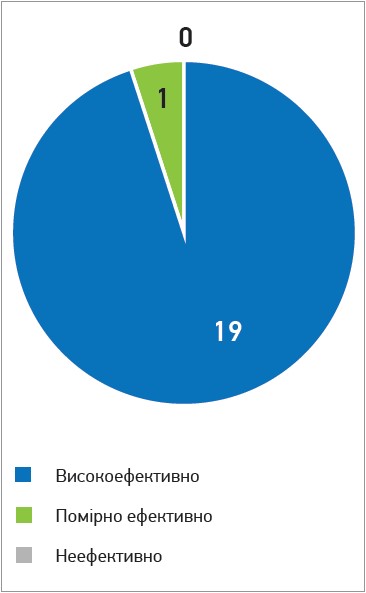
Рис. 3. Оцінка ефективності комплексного застосування препаратів Целіста Спрей і Целіста Дуо, на думку лікарів
Висновки
Проведений аналіз клініко-лабораторних даних щодо впливу комплексу препаратів Целіста Спрей + Целіста Дуо при лікуванні ГТФ у дітей віком від 4 років і понад 15 років показав високий клінічний ефект і хорошу переносимість терапії. Важливим механізмом дії цих препаратів є виразний протизапальний, бактерицидний ефекти й відсутність токсичного впливу на слизову оболонку ротової частини глотки та ПМ. Зниження числа нейтрофілів і збільшення епітеліальних клітин за результатами цитологічного дослідження з ПМ у хворих на ГТФ розглядають як індикатор зменшення запалення та посилення регенерації епітелію ПМ і слизової оболонки ротової частини глотки.
Отримані нами результати клінічного спостереження свідчать про виразний позитивний вплив комплексу препаратів Целіста Спрей + Целіста Дуо на клінічний перебіг ГТФ у дітей і стан місцевих механізмів захисту слизових оболонок. Запропонований комплекс препаратів довів свою високу клінічну ефективність і безпечність у лікуванні ГТФ у дітей, що вказує на можливість його застосування для амбулаторних і стаціонарних пацієнтів.
Усе вищевикладене дає змогу рекомендувати препарати Целіста Спрей і Целіста Дуо для лікування не тільки ГТФ, а й інших запальних процесів ротової частини глотки, особливо в тих випадках, коли захворювання супроводжується не лише больовим синдромом, але й виразними запальними змінами слизових оболонок і лімфоїдної тканини глотки.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 16 (552), 2023 р