25 вересня, 2023
Лікарські рослини в терапії риносинуситу: наукові аргументи та клінічні факти
 Риносинусит (РС) – поширене захворювання в більшій частині світу, що спричиняє суттєвий тягар на суспільство стосовно споживання послуг у сфері охорони здоров’я та втрати працездатності. Гострий РС (ГРС) має щорічну поширеність 6-15% і зазвичай є наслідком ГРВІ. ГРС зазвичай самовиліковується, проте описувалися серйозні наслідки, що зумовлюють загрозливі для життя стани та навіть смертельні випадки. Це одна з найчастіших причин призначення антибіотиків; правильне ведення пацієнтів є надзвичайно актуальним у контексті глобальної кризи внаслідок антибіотикорезистентності.
Риносинусит (РС) – поширене захворювання в більшій частині світу, що спричиняє суттєвий тягар на суспільство стосовно споживання послуг у сфері охорони здоров’я та втрати працездатності. Гострий РС (ГРС) має щорічну поширеність 6-15% і зазвичай є наслідком ГРВІ. ГРС зазвичай самовиліковується, проте описувалися серйозні наслідки, що зумовлюють загрозливі для життя стани та навіть смертельні випадки. Це одна з найчастіших причин призначення антибіотиків; правильне ведення пацієнтів є надзвичайно актуальним у контексті глобальної кризи внаслідок антибіотикорезистентності.
Клінічне визначення РС у дорослих:
- запалення носа та навколоносових пазух, що характеризується ≥2 симптомами, одним з яких має бути закладеність носа / обструкція / застійні явища або виділення з носа (виділення спереду / ззаду носоглотки):
± біль / тиск у ділянці обличчя;
± зниження або втрата нюху, а також
- ендоскопічні ознаки:
- назальних поліпів,
та/або
- слизово-гнійні виділення здебільшого із середньої частини носового ходу, та/або
- набряк / обструкція слизом переважно в середній частині носового ходу,
та/або
- зміни на КТ:
- зміни в слизовій оболонці в межах остіомеатального комплексу та/або пазух.
Клінічне визначення РС у дітей:
- наявність ≥2 симптомів, одним з яких має бути закладеність носа / обструкція / застійні явища або виділення з носа (виділення спереду / ззаду носоглотки):
± біль / тиск у ділянці обличчя;
± кашель,
а також
- ендоскопічні ознаки:
– назальних поліпів,
та/або
– слизово-гнійні виділення здебільшого із середньої частини носового ходу,
та/або
– набряк / обструкція слизом переважно в середній частині носового ходу,
та/або
- зміни на КТ:
– зміни в слизовій оболонці в межах остіомеатального комплексу та/або пазух.
ГРС у дорослих визначається як раптове виникнення ≥2 симптомів, одним з яких має бути закладеність носа / обструкція / застійні явища або виділення з носа (виділення спереду / ззаду носоглотки):
- ± біль / тиск у ділянці обличчя;
- ± зниження або втрата нюху протягом <12 тиж; із безсимптомними інтервалами, якщо патологія рецидивує, із підтвердженням телефоном або під час співбесіди.
ГРС у дітей визначається як раптове виникнення ≥2 симптомів:
- закладеність носа / обструкція / застійні явища;
- виділення з носа без кольору;
- кашель (удень та вночі) протягом <12 тиж; із безсимптомними інтервалами, якщо патологія рецидивує, із підтвердженням телефоном або під час особистого спілкування. Слід включити запитання про наявність алергічних симптомів (чхання, водянисті виділення з носа, свербіж у носі, вологість і свербіж очей).
Рецидивувальний ГРС (РГРС)
ГРС може виникати одноразово чи >1 раз протягом визначеного періоду часу. Це зазвичай виражається в епізодах/рік, проте з повним зникненням симптомів між епізодами.
РГРС вважається наявність >4 епізодів/рік із безсимптомними інтервалами. Кожен епізод має відповідати критеріям ГРС після перенесеної вірусної інфекції (або бактеріального РС, БРС). Координаційна група EPOS (2020) рекомендує діагностувати РГРС за наявності щонайменше одного підтвердженого діагнозу ГРС після перенесеної вірусної інфекції з проведенням ендоскопії та/або КТ перед розглядом діагнозу РГРС.
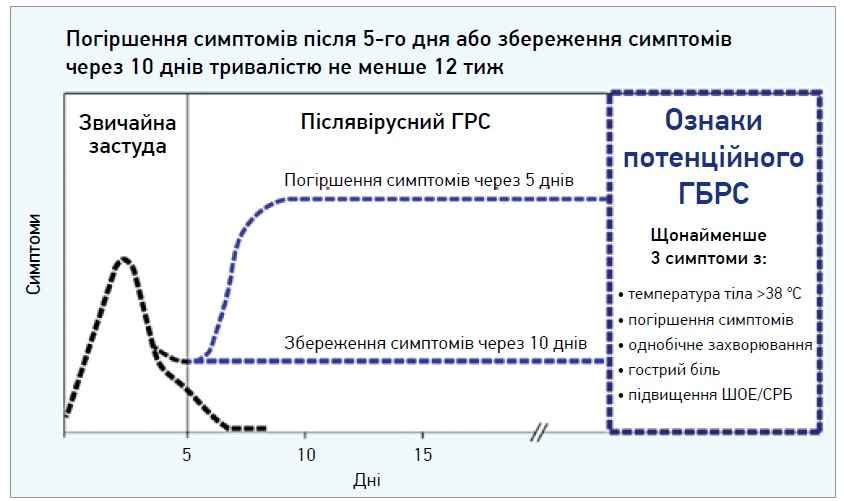
Багато пацієнтів звертаються до свого сімейного лікаря або фармацевта із проблемами, пов’язаними з інфекціями верхніх дихальних шляхів. Більшість з них є самообмежувальними та можуть бути класифіковані як звичайна застуда (ІВДШ). Звичайна застуда визначається як гострий вірусний РС із тривалістю симптомів <10 днів (але <12 тиж) (рис. 1).
Рис. 1. Визначення ГРС за EPOS
Якщо симптоми посилюються через 5 днів або коли спостерігаються протягом >10 днів (за тривалості <12 тиж), за класифікацією EPOS це – гострий післявірусний РС. Лише незначна частка ГРС спричинена бактеріями.
EPOS визначає гострий бактеріальний РС (ГБРС) за щонайменше 3 симптомами / ознаками з 5:
- безбарвні слизові виділення;
- гострий локальний біль (переважно однобічний);
- гарячка (температура тіла >38 °C);
- підвищення СРБ / ШОЕ;
- погіршення симптомів.
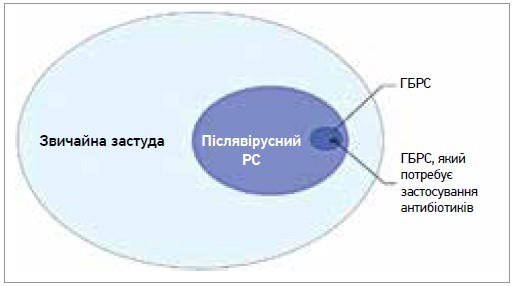
Загалом ГРС – поширена проблема, точну частоту виникнення якої складно визначити. Захворюваність на гострий вірусний РС (звичайна застуда) дуже висока (як це було описано раніше й узагальнено в даних літературних джерел). Підраховано, що дорослі переносять від 2 до 5 епізодів вірусного ГРС (або застуди) на рік, а школярі можуть переносити від 7 до 10 епізодів застуди на рік. У нещодавно оприлюдненій нідерландській роботі з використанням опитувальника GA2LEN виявлено поширеність 18% (17-21%) для симптомів, які свідчать про післявірусний / ГБРС / ГРС у 3 різних містах у Нідерландах; ≈0,5-2% вірусних ІВДШ ускладнюються бактеріальною інфекцією (рис. 2).
Рис. 2. Захворюваність на різні форми ГРС: звичайна застуда, післявірусний РС і ГБРС
Діагностика та диференційна діагностика ГРС у дорослих і дітей
ГРС після перенесеної вірусної інфекції – це поширена патологія в суспільстві, що зазвичай розвивається після ІВДШ. Більшість гострих вірусних ІВДШ минають самостійно, отже, ГРС після перенесеної вірусної інфекції не слід діагностувати до 10-денної тривалості симптомів, якщо немає чіткого їхнього погіршення через 5 днів.
Суб’єктивна оцінка має ураховувати тяжкість та тривалість симптомів. Рекомендовано метод оцінки тяжкості симптомів із застосуванням візуальної аналогової шкали, де пацієнт робить відмітки на 10 см лінії, надаючи оцінку в діапазоні від 1 до 10. При ГРС може виникати бактеріальна інфекція, проте в більшості випадків антибіотики мають незначний вплив на перебіг захворювання. В багатьох дослідженнях клініцисти намагалися підібрати комбінації симптомів та ознак, що прогнозують тяжче захворювання (особливо бактеріальної етіології), а також імовірність відповіді на антибіотикотерапію. Координаційна група EPOS (2020) вирішила залишити пропозиції, внесені до більш ранніх версій EPOS: щонайменше 3 з 5 симптомів виділень без кольору, сильного місцевого болю, лихоманки, підвищення ШОЕ / СРБ і посилення нездужання.
Лікування ГРС у дорослих і дітей
Слід зазначити, що в EPOS (2020) було проведено систематичний огляд, де окремо оцінювали лікування різних категорій ГРС (вірусний, після перенесеної вірусної інфекції або ГБРС). Зокрема, для гострого вірусного РС було знайдено багато відмінних систематичних оглядів і повідомлень про них. Різні види рекомендованого лікування, рівні доказовості та рекомендації GRADE, наведені в EPOS (2020), виділені для кожного діагнозу ГРС.
У Європейському посібнику із РС і поліпозу носа (EPOS, 2020) зазначено >10 методів лікування, а також полегшення симптомів РС вірусного й бактеріального походження (серед яких і фітотерапія). Терапевтичні можливості лікарських рослин у хворих із симптомами ГРС використовувалися в народній медицині впродовж багатьох років. Останнім часом накопичуються результати наукових досліджень, які обґрунтовують доцільність використання за цієї патології певних лікарських рослин та їхніх комбінацій.
Лікувальний ефект фітопрепаратів опосередковано наявністю в рослинах біологічно активних речовин (БАР): алкалоїдів (складні органічні азотовмісні сполуки з високою різноспрямованою фізіологічною активністю); глікозидів (органічні сполуки, до складу яких входять вуглеводи, невуглеводний компонент, – стероїдний спирт або фенол), поліфенолів (клас хімічних сполук, що містять >1 фенольну групу, а також характеризуються потужними антиоксидантними і протизапальними властивостями); ефірних олій (чинять антисептичну, протизапальну, заспокійливу дію); вітамінів і мікроелементів (регулюють обмін речовин, підвищують імунітет). Різновиди рослинних поліфенолів – флавоноїди, яким притаманні виразні протизапальні та антиоксидантні властивості. Деякі флавоноїди мають також противірусну активність. Терпеноїди (terebinthine – скипидар) – численна група природних сполук із регулярною будовою вуглецевого скелета. Представники терпенів мають високу фізіологічну активність, наприклад фітогормональну (стероїди, цитокіни, ксантотоксини тощо). Сапоніни (sapo – мило) – складні безазотисті сполуки групи глікозидів із поверхнево-активними властивостями.
Безумовними перевагами сучасних комбінованих рослинних препаратів є:
- полівалентність і різнобічна спрямованість дії БАР, що містяться в 1 рослині;
- багатокомпонентність складових, що дозволяє посилювати лікувальний ефект за рахунок синергізму БАР різних рослин;
- виражена терапевтична активність за меншого спектра побічних ефектів, ніж у синтетичних препаратів;
- можливість застосування протягом тривалого періоду часу;
- можливість комбінування з багатьма хіміосинтетичними препаратами;
- економічна (цінова) доступність комплексних фітопрепаратів.
Дуже важливими є такі запитання: наскільки вивчено рослинні компоненти комплексних фітопрепаратів, чи є наукові докази їхньої ефективності? Результати наукових досліджень належного рівня доказовості – надійне підґрунтя для подальшого використання певних рослин у клінічній практиці, внесення їх до клінічних настанов.
Яскравим прикладом цього положення є андрографіс волотистий (Andrographis paniculata) – лікарська рослина, позначена в EPOS (2020) окремим рядком. Андрографіс традиційно використовувався в Індії та Китаї для лікування застуди і грипу як протизапальний, а також антибактеріальний агент. Вивчення рослини сучасними методами фармакології дозволило визначити основні БАР екстракту андрографісу, а також їхні фармакологічні властивості. Основний активний компонент Andrographis paniculata (андрографолід) чинить різноманітні фармакологічні дії, включаючи аналгетичну, жарознижувальну, антиретровірусну, антипроліферативну, протималярійну, антитромботичну, антигіперглікемічну, антиуролітіальну, протилейшманіозну, гепатопротекторну, імуномодулювальну, захисну від токсичності, спричиненої алкоголем, кардіопротекторну, а також протипухлинну активність [9]. За даними S. Hossain і співавт. (2021) [10], андрографолід може пригнічувати фактори вірулентності інвазивних мікробів, регулювати імунітет господаря. Як установлено в дослідженні A.K. Jadhav, S.M. Karuppayil (2021) [11], основні мішені андрографоліду – злиття, адсорбція вірусу в клітині-хазяїні, зв’язування з вірусним рецептором і корецептором, вплив на ферменти, залучені до реплікації ДНК/РНК / генома вірусів, трансляція, посттрансляція, зворотна транскрипція. Підтвердження потужної противірусної дії (особливо проти вірусів грипу та респіраторних вірусів) – робота M. Jiang і співавт. (2021) [12]. Автори зазначають, що механізми противірусного ефекту екстракту листя андрографісу переважно включають регуляцію проникнення вірусу, реплікацію генів і синтез функціонально зрілих білків. Установлено, що андрографолід, неоандрографолід, дегідроандрографолід, які містяться в екстракті листя андрографісу, чинять значну противірусну дію проти вірусу грипу А, вірусу SARS-CoV-2, а також вірусу герпесу, гепатиту В, гепатиту С, ВІЛ, папіломи.
|
Таблиця 1. Дані та рекомендації щодо лікування для дорослих і дітей із гострим вірусним РС (застуда) |
||
|
Рівень доказовості |
Рекомендація GRADE |
|
|
Антибіотики |
1a (-) |
Відсутні дані про переваги застосування антибіотиків при застуді чи персистувальному гострому гнійному риніті в дітей або дорослих. Існують дані про те, що антибіотики спричиняють серйозні побічні явища в дорослих за умови прийому в разі застуди та в усіх вікових групах при гострому гнійному риніті. Не рекомендується рутинне застосування антибіотиків за цих умов |
|
Назальний кортикостероїд |
1a (-) |
Сучасні дані не підтримують застосування назальних кортикостероїдів для симптоматичного лікування застуди |
|
Антигістамінні |
1a |
Антигістамінні препарати мають обмежений короткотривалий (дні 1 та 2 лікування) позитивний ефект на тяжкість усіх симптомів у дорослих, а не середньо- чи довготривалий. Немає клінічно значущого впливу на закладеність носа, ринорею або чхання |
|
Деконгестант (пероральний/назальний) |
Ia |
Згідно із сучасними даними, високі дози деконгестантів можуть мати незначний позитивний вплив на суб’єктивний ступінь закладеності носа в дорослих із застудою. Малоймовірно, що деконгестанти підвищують ризик побічних явищ у дорослих у короткий термін |
|
Парацетамол |
Ia |
Парацетамол може допомагати полегшувати назальну обструкцію та ринорею, проте, ймовірно, не покращує інших симптомів застуди (біль у горлі, чхання, кашель) |
|
НПЗП |
Ia |
НПЗП суттєво не знижують оцінки за шкалою загальних симптомів або тривалість застуди. Проте для наслідків, пов’язаних з аналгезувальними впливами НПЗП (головний біль, біль у вухах, м’язах і суглобах), НПЗП мають значні переваги, а загальне нездужання демонструє граничне покращення, хоча відсутнє поліпшення щодо подразнення горла. Озноб демонструє змішані результати. Оцінки для респіраторних симптомів, кашлю та виділень з носа не покращуються, проте оцінка для чхання суттєво поліпшується. Відсутні дані про зростання частоти побічних явищ у групах лікування НПЗП |
|
Комбінації антигістамінний препарат – деконгестант – аналгетик |
Ia |
Комбінації антигістамінний препарат – деконгестант – аналгетик мають певний загальний позитивний ефект у дорослих і дітей старшого віку із застудою. Слід зважувати ці переваги проти ризику виникнення побічних явищ. Відсутні дані про ефективність у дітей молодшого віку |
|
Іпратропію бромід |
Ia |
Згідно з наявними даними, іпратропію бромід, імовірно, є ефективним у поліпшенні ринореї. Іпратропію бромід не чинить впливу на закладеність носа, а його застосування асоційовано з більшою кількістю побічних явищ порівняно із плацебо або групою без лікування, хоча вони добре переносилися та минали самостійно |
|
Зрошення порожнини носа сольовим розчином |
Ib |
Зрошення порожнини носа сольовим розчином, імовірно, має переваги в полегшенні симптомів гострих ІВДШ (здебільшого в дітей) |
|
Пара / нагріте зволожене повітря |
1a (-) |
Сучасні дані не демонструють жодних переваг або шкоди від використання нагрітого зволоженого повітря, що застосовується для лікування застуди |
|
Пробіотики |
Ia |
Пробіотики можуть мати більшу користь порівняно із плацебо для попередження гострих ІВДШ. Однак якість даних була (дуже) низькою |
|
Вітамін С |
Ia |
З огляду на стабільний вплив вітаміну C на тривалість і тяжкість застуди в дослідженнях із регулярним прийомом, а також низьку вартість і безпечність його застосування може бути доцільним у пацієнтів із застудою для індивідуального визначення того, чи надає їм користь терапія вітаміном С |
|
Вакцини |
1b (-) |
Відсутні остаточні результати на підтримку застосування вакцин для попередження застуди в здорових людей (на противагу вакцинам проти грипу) |
|
Фізичні вправи |
Ia |
Регулярні вправи з помірною інтенсивністю можуть впливати на попередження застуди |
|
Ехінацея |
1a (-) |
Препарати ехінацеї не продемонстрували позитивного впливу на лікування застуди, хоча, ймовірно, існувала незначна користь від деяких препаратів ехінацеї: результати досліджень індивідуальної профілактики постійно демонструють позитивні (якщо статистично незначущі) тенденції, хоча клінічна значущість потенційних впливів є суперечливою |
|
Цинк |
Ia |
Цинк, що приймається у вигляді таблеток для розсмоктування ацетату чи глюконату цинку, в дозі ≥75 мг/добу (протягом 24 год від появи симптомів) значуще знижує тривалість застуди. Його рекомендовано застосовувати в цій дозі під час застуди. Що стосується профілактичного прийому цинку, то наразі не можна розробити чітких рекомендацій через недостатню кількість даних |
|
Рослинні препарати |
Ib |
Деякі рослинні препарати, як-от BNO 1016, Cineole та екстракт Andrographis paniculata SHA-10, чинять значущий вплив на симптоми застуди без значних побічних явищ. Не вистачає проведення формального систематичного огляду |
|
Фузафунгін |
Ia |
Фузафунгін ефективний для лікування застуди, особливо за раннього прийому. Проте після застосування фузафунгіну виникали серйозні алергічні реакції з бронхоспазмом, хоча й рідко. З цієї причини препарату більше немає на ринку |
Не менш значущою є антитоксична дія екстракту листя андрографісу волотистого, особливо коли йдеться про пацієнтів із грипом, які під час агресивного періоду терапії застосовують значні дози лікарських засобів, що можуть індукувати гепатотоксичний та/або нефротоксичний ефекти [13].
На ґрунті визначеного спектра фармакологічних властивостей у подальшому клінічна ефективність і переносимість екстракту Andrographis paniculata при лікуванні гострих ІВДШ, у т. ч. синуситу, була досліджена в 2 подвійних сліпих плацебо-контрольованих клінічних дослідженнях, що належать до високого рівня доказовості [17, 18]. Доведена ефективність у поєднанні з хорошою переносимістю стали підставою для внесення Andrographis paniculata в 2020 році до EPOS як засобу для лікування гострого вірусного РС у дітей та дорослих. Згодом вивчення Andrographis paniculata було продовжено; накопичені дані щодо його використання поєднано та проаналізовано в 3 метааналізах [14, 19, 20]. На особливу увагу заслуговує той факт, що в масштабному метааналізі X.Y. Hu та співавт. (2017) [14], де проаналізовано результати 33 рандомізованих контрольованих досліджень участю 7175 пацієнтів, проведено клінічну оцінку ефективності й безпеки застосування екстракту листя андрографісу, який у деяких випробуваннях призначали замість рутинної антибіотикотерапії при гострих інфекціях дихальних шляхів, синуситах, ринітах. Установлено, що досліджуваний екстракт достовірно скоротив тривалість кашлю, болю в горлі, покращив носове дихання, зменшив час на лікарняному порівняно зі стандартними схемами лікування. Про жодні серйозні побічні ефекти не повідомлялося, а незначні побічні ефекти виявилися переважно шлунково-кишковими.
На сьогодні в Україні зареєстровано лише 1 комплекс рослинних екстрактів з андрографісом – Синудафен (АТ «Фармак», Україна), представлений на вітчизняному фармацевтичному ринку у вигляді капсул і сиропу. В складі цього комплексу також наявні екстракти інших рослин.
Екстракт квіток бузини. Сучасний метааналіз J. Hawkins і співавт. [1], який включав 180 учасників, дозволив установити, що застосування екстракту Sambucus nigra значно зменшує симптоми верхніх дихальних шляхів і є ефективною альтернативою неправильному та надмірному використанню антибіотиків для лікування симптомів верхніх дихальних шляхів, спричинених вірусними інфекціями. Екстракт квіток бузини продемонстрував потенційно безпечнішу альтернативу лікам, що відпускаються за рецептом, для випадків звичайної застуди та грипу.
Бузина чорна збагачена біологічно активними сполуками (насамперед поліфенолами, терпеноїдами); демонструє полімодальну фармакологічну дію, в т. ч. антиоксидантну, протизапальну, протипухлинну, протигрипозну, протимікробну, протидіабетичну, кардіо- та нейропротекторну. До складу поліфенолів бузини входять добре відомі флавоноїди рутин та ізокверцетин [21]. Цим сполукам притаманна виразна антиоксидантна, пов’язана з нею протизапальна, а також капілярозміцнювальна дія. Потенційні молекулярні механізми БАР пов’язані з регулюванням деяких ключових сигнальних шляхів і молекулярних мішеней, що й обумовлює їхню ефективність у профілактиці та терапії захворювань верхніх дихальних шляхів, у т. ч. хронічних [2]. Дослідження останніх років продемонстрували антимікробну активність екстрактів бузини щодо низки штамів грампозитивних і грамнегативних бактерій: Staphylococcus, Pseudomonas, Enterococcus, Escherichia, Streptococcus, Klebsiella, Bacillus. Встановлено, що антимікробна активність обумовлена комбінацією БАР, а не окремими активними компонентами [22]. Зовсім нещодавно в БАР цієї рослини виявлено властивості пребіотика – здатність модулювати мікробіоту кишечнику. Суттєвий пребіотичний потенціал доведено, зокрема, для таких представників нормальної мікрофлори, як L. plantarum, L. casei, L. rhamnosus, L. fermentum [23].
Екстракт квіток коров’яку. Містить різні біологічно активні сполуки, в т. ч. флавоноїди, іридоїди, фенілетаноїди, фенілпропаноїдні глікозиди, сапоніни, а також вітамін С і мінерали, які, за даними S. Mahdavi та співавт. (2020) [3], чинять потужну антиоксидантну й антимікробну дію на грампозитивні, грамнегативні бактеріальні штами, що робить екстракт ефективним у терапії інфекційних захворювань верхніх дихальних шляхів. В огляді A. Gupta (2022) [4] доведено потужну противірусну, антиоксидантну, протизапальну, антибактеріальну та протигрибкову дію екстракту коров’яку.
Екстракт трави вербени. Є джерелом переважно терпеноїдів, глікозидів, флавоноїдів, ефірної олії; за даними аналітичного огляду P. Kubica та співавт. (2020) [5], має доведену багатьма дослідженнями антиоксидантну, антимікробну, протизапальну, знеболювальну дію. Слід зауважити, що в найновішому дослідженні X. Dai та співавт. (2023) [6] вивчено механізм реалізації протизапальної дії екстракту вербени за інфікування вірусом грипу. Встановлено, що природні клітини-кілери (NK) відіграють ключову роль у знищенні клітин, інфікованих патогенами. Вербена лікарська (V. officinalis) регулює реакцію запалення та функцій NK-клітин. Пероральне введення екстракту зменшувало ушкодження легень, сприяло дозріванню та активації NK-клітин у легенях, знижувало рівні запальних цитокінів (IL-6, TNF-α, IL-1β) у сироватці. Серед 5 біологічно активних компонентів екстракту V. officinalis вербеналін значно підвищив ефективність знищення NK in vitro, як було визначено аналізами знищення в реальному часі на основі планшет-рідера чи зображення живих клітин із високим умістом у 3D із використанням первинних NK-клітин людини. Результати подальших випробувань показали, що лікування вербеналіном прискорило процес знищення вірусу грипу шляхом скорочення часу контакту NK-клітин з їхніми клітинами-мішенями без впливу на проліферацію NK-клітин, експресію цитотоксичних білків або дегрануляцію літичних гранул. Такі результати свідчать про те, що екстракт V. officinalis чинить достатню протизапальну дію проти вірусної інфекції, регулює активацію, дозрівання та функції знищення NK-клітин. Отже, автори резюмують, що екстракт вербени – ефективний терапевтичний засіб для боротьби з вірусною інфекцією дихальних шляхів.
Екстракт квіток липи. За рахунок синергічної взаємодії між хімічними складовими екстракту (флавоноїди: акацетин-7-глюкозид (тиліанін), кемпферол, тилірозид, кверцетин, гербогастрин, рутинозид кверцетину, афцелін, кемпферитрин; тритерпеноїд тараксерол, вітамін С, фенолкарбонові кислоти, проантоціанідини, ефірна олія, фарнезол, 2-феніл-етанол, монотерпеноїди) екстракт квіток липи чинить потужну протизапальну та антиоксидантну дію [7].
Останнім часом значна увага приділяється профілактиці та лікуванню респіраторних вірусів, у т. ч. вірусів грипу. E. Kwon і співавт. (2022) оцінили противірусний ефект липи щодо вірусу грипу А. Встановлено, що БАР липи збільшували продукцію та секрецію інтерферону 1 типу (IFN-1) і прозапальних цитокінів, що стимулює противірусну відповідь імунної системи. Крім того, БАР липи посилили експресію генів, що стимулюють синтез IFN-1 та трансмембранного білка, який перешкоджає реплікації вірусу і його проникненню до клітини. В сукупності отримані результати свідчать про те, що БАР липи пригнічують інфекцію вірусу грипу А регулюванням вродженої імунної відповіді в макрофагах та можуть бути рекомендовані за такої інфекції, як імунологічний ад’ювант [8].
Екстракт листя м’яти перцевої. Mentha piperita добре відома традиційним використанням для лікування різноманітних захворювань. Наукові дослідження свідчать про антиоксидантну, антимікробну, противірусну, протизапальну, радіозахисну, антидіабетичну активність екстракту листя м’яти перцевої, що реалізується через високий вміст флавоноїдів, фенольних сполук, лігнанів, стильбенів, а також ефірної олії [15].
Відомо, що БАР із листя Mentha piperita ефективні за різних респіраторних захворювань (риніт, синусит); новітні дані доводять ефективність екстракту листя м’яти перцевої також у разі алергічного риніту. N. Park і співавт. (2022) [16] встановлено, що БАР м’яти перцевої значно зменшували товщину епітелію, дегрануляцію мастоцитів, секрецію келихоподібних клітин, інфільтрацію запальних клітин у тканині носа, а також регулювали сигнальний шлях MAPK-NF-κB, який був пов’язаний зі щільними з’єднаннями в епітеліальних клітинах носа. Це дослідження підтвердило ефективність БАР м’яти перцевої у лікуванні алергічного риніту.
Екстракт плодів ацероли. Malpighia punicifolia – рослина з найвищим вмістом вітаміну С. Крім того, ацерола містить провітамін А, вітаміни групи В, залізо, кальцій, фосфор. У її складі є багато фенольних каротиноїдів, антоціанів, флавоноїдів, зокрема кверцетин і ресвератрол [24]. Завдяки такій комбінації БАР ацерола чинить високу антиоксидантну дію, крім того, має загальну тонізувальну активність [25]. Нещодавно продемонстровано пребіотичні властивості ацероли [26].
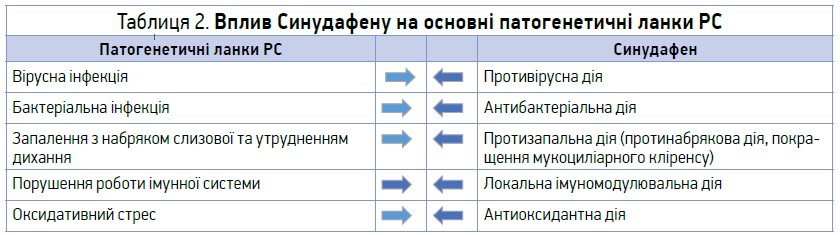
Отже, рослинні компоненти, які входять до складу засобу Синудафен, ефективно впливають на основні патогенетичні ланки РС (табл. 2).
Фармакологічні властивості Синудафену дозволяють розглядати його як засіб для підтримання нормального функціонального стану придаткових пазух носа, належного функціонування синусів і слизових оболонок верхніх дихальних шляхів, оптимізації функціонування імунної системи під час поширення застудних захворювань. Ці положення підтверджує нижчезазначений клінічний випадок.
Хворий В., 35 років, звернувся до сімейного лікаря щодо сильного головного болю, слизових виділень жовтуватого кольору з порожнини носа, які, зі слів пацієнта, тривали >3 днів. З анамнезу відомо, що чоловік захворів гостро: з підвищенням температури тіла до 38 °C упродовж 2 днів, з утрудненим носовим диханням, виділеннями з носа, головним болем, покашлюванням. Алергологічний анамнез не обтяжений. Самостійно не лікувався. Попередньо встановлено діагноз гострого назофарингіту. Призначено парацетамол, Риназолін у ніс, Зіпелор-спрей на задню стінку глотки, тепле пиття.
На 3-тю добу лікування хворий звернувся повторно щодо погіршення свого стану – температура тіла зберігалася до 37,3 °C, з’явився дискомфорт у проєкції правого фронтального та верхньощелепного синусів. Було проведено рентгенографію приносових пазух в прямій проєкції: виявлено пристінкове затемнення правої верхньощелепної пазухи та нижніх відділів фронтального синусу справа. Сімейний лікар змінив діагноз на «гострий вірусний РС, фронтит». Було відкрито лікарняний лист, призначено відповідне консервативне лікування амбулаторно: Синудафен упродовж 10 діб, Риназолін продовжити до 5 днів, пацієнта було терміново скеровано на консультацію до оториноларинголога.
Під час об’єктивного обстеження за допомогою ендоскопії оцінено оториноларингологічний статус. Виявлено девіацію (викривлення) носової перегородки вправо в передніх і середніх відділах. Слизова оболонка носа набрякла, була гіперемованою, спостерігалися густі слизові виділення в загальному та середньому носовому ході (більше справа). Нижні носові раковини дещо збільшені в об’ємі, передні відділи середніх носових раковин не змінені, середній носовий хід – із густим слизом. Просвіт носових ходів у середніх і задніх відділах звужений, був практично непрохідним для прямого (торцевого) ендоскопу 4 мм справа. Під час пальпації та перкусії ділянок проєкції приносових пазух болючості не спостерігалося. Установлено діагноз гострого вірусного РС, викривлення носової перегородки справа.
Пацієнту рекомендовано продовження застосування Синудафену до 10-14 днів, Форінекс (2 інстиляції у ніс 2 р/добу) після санації носових ходів Спаркліном (у кожну ніздрю 2-3 р/добу).
Попередня оцінка ефективності лікування, проведена через 5 днів, показала позитивну динаміку. В хворого поліпшилося носове дихання, зменшилися виділення з носа, відсутній головний біль. При ендоскопічному огляді слизова оболонка носа була помірно гіперемованою та набрякла переважно на боці викривлення носової перегородки, в загальному та середньому носових ходах – без патологічних виділень, натікання слизу задньою стінкою глотки не спостерігалося. Щодо інших ЛОР-органів – без особливостей. Саме тому призначену терапію було продовжено до 14 днів.
Отже, за результатами спостереження зроблено такі ключові висновки щодо наведеного клінічного випадку: по-перше, спостерігалися недостатність чіткої верифікації первинного діагнозу на основі скарг і симптомів. Інструментально підтверджений уточнений діагноз, який був установлений на підставі оцінки клінічних даних і рентгенологічного обстеження, по-іншому трактував стан пацієнта. Враховано зміни слизової оболонки носової порожнини, наявність схожих змін у пазухах і відсутність позитивної динаміки від стартової терапії сімейного лікаря, що надає підстави для зміни діагнозу та розширення схеми лікування. Призначення рентгенографії приносових пазух вплинуло на клінічне рішення, оскільки надало змогу змінити діагноз, визначити пріоритетність комплексного консервативного лікування. По-друге, спостерігалися тактичні помилки: невідповідність урахування симптомів у хворого на ГРС (а не гострого назофарингіту) не забезпечувала бажаного клінічного ефекту, що спричинило відсутність позитивної динаміки. Недоліки можна відзначити також і в недостатніх методах обстеження хворого – ендоскопічний огляд на сьогодні надає чітку верифікацію запальних змін у порожнині носа, виявляє обтяжливі стани за порушення архітектоніки носа, зокрема викривлення носової перегородки справа. Саме ці дані доцільно враховувати лікарям-практикам для діагностики та оцінки результатів ефективного комплексного лікування хворих із ГРС, що може бути успішно проведено з використанням препарату Форінекс із додаванням назального спрею Спарклін та рослинного комплексу Синудафен.
Список літератури знаходиться в редакції.