12 грудня, 2023
Нові можливості фармакотерапії алергійного риносинуситу з поліпозом
 Поліпозний риносинусит (ПРС) – це хронічне захворювання слизової оболонки носа і приносових пазух запального характеру, для якого характерна поліпозна проліферація (розростання) тканин. Частота поліпозу носа становить приблизно 0,5-4,3%, тобто це захворювання є одним із найпоширеніших серед хронічних хвороб верхніх дихальних шляхів. Поширеність поліпозу носа зростає у хворих на бронхіальну астму (БА) (7-15%), муковісцидоз (39-56%), а також на тлі непереносимості ацетилсаліцилової кислоти (АСК) (36-96%). Потрібно зазначити, що хронічний РС (ХРС) із поліпозом носа і хронічний РС без поліпозу – це дві різні форми захворювання [1, 2, 6, 8, 9].
Поліпозний риносинусит (ПРС) – це хронічне захворювання слизової оболонки носа і приносових пазух запального характеру, для якого характерна поліпозна проліферація (розростання) тканин. Частота поліпозу носа становить приблизно 0,5-4,3%, тобто це захворювання є одним із найпоширеніших серед хронічних хвороб верхніх дихальних шляхів. Поширеність поліпозу носа зростає у хворих на бронхіальну астму (БА) (7-15%), муковісцидоз (39-56%), а також на тлі непереносимості ацетилсаліцилової кислоти (АСК) (36-96%). Потрібно зазначити, що хронічний РС (ХРС) із поліпозом носа і хронічний РС без поліпозу – це дві різні форми захворювання [1, 2, 6, 8, 9].
Відповідно до сучасного уявлення в основі ХРС і БА лежить хронічний запальний процес, який супроводжується дифузною інфільтрацією еозинофільними гранулоцитами всіх шарів слизової оболонки, а слиз, який її вкриває, містить велику кількість еозинофілів [3-7]. Так, під час мікроскопічного дослідження назальних поліпів спостерігають зміни, властиві слизовій оболонці бронхів у хворих на БА. В обох випадках у зразках тканин виявляють ушкодження епітелію, гіперплазію келихоподібних клітин, стовщення базальної мембрани, збільшення об’єму позаклітинного матриксу, фіброз та еозинофільне запалення. Причому вираженість еозинофільного запалення в тканині назальних поліпів в осіб із поліпозом носа, поєднаного з БА, більша, ніж у пацієнтів, які мають назальні поліпи, але не страждають на БА [1, 9].
Виникнення поліпів може зумовлюватися різними патологічними механізмами. Проте етіологія і патогенез цього запального процесу до кінця не з’ясований. Поліпоз носа є гетерогенним захворюванням, але доволі складно визначити, які чинники є ключовими в його розвитку.
Набряковий, або еозинофільний, поліп носа є найпоширенішим (85-90%) типом поліпів. Він утворений набряклою сполучною тканиною, містить залози й кісти, вкриті найчастіше незміненою слизовою оболонкою. Морфологічно тканина характеризується набряком, гіперплазією келихоподібних клітин епітелію, стовщенням базальної мембрани та інфільтрована переважно еозинофілами, лімфоцитами, плазмоцитами й опасистими клітинами. Активовані еозинофіли, що інфільтрують тканину поліпа, продукують велику кількість білків із різними токсичними властивостями. Крім цих медіаторів еозинофіли також здатні продукувати безліч цитокінів, хемокінів і факторів росту. Наприклад, вони виробляють інтерлейкін‑5 (IL‑5), гранулоцитарно-макрофагальний колонієстимулювальний фактор (GM-CSF), хемокін RANTES і білок ростового регуляторного онкогена (GRO)-α. Таким чином, еозинофіли сприяють інфільтрації тканини [1, 8, 9].
Останніми десятиліттями проводили дослідження, які показали значну роль фактора агрегації тромбоцитів (ФАТ) у патогенезі поліпозу носа. ФАТ є прозапальним ліпідним медіатором. Його виділяють багато клітин – еозинофіли, макрофаги, ендотеліальні та опасисті клітини (мастоцити) і тромбоцити, причетні до таких алергійних захворювань (АЗ), як БА, алергійний риніт (АР) і анафілаксія [10, 11, 13, 19-21]. Є докази, що ФАТ може активувати опасисті клітини легень людини (hLMC).
Роль ФАТ в астмі добре вивчена, і в кількох дослідженнях було продемонстровано, що ФАТ пов’язаний із бронхоконстрикцією та гіперреактивністю бронхів [15, 16]. Крім того, ФАТ вважають найпотужнішим індуктором проникності судин серед медіаторів, які беруть участь у запаленні слизової оболонки носа, із ключовою роллю в разі ринореї та закладеності носа [12]. Нарешті, рівні ФАТ та, що цікавіше, активність ФАТ ацетилгідролази (АГ) були пов’язані з тяжкістю анафілаксії [13]. Рецептор ФАТ також було виявлено в опасистих клітинах легень людини. Дегрануляція мастоцитів, індукована ФАТ, частково залежить від позаклітинного кальцію, що продемонстровано на опасистих клітинах периферичної крові людини [14].
Незважаючи на достовірну роль ФАТ у патофізіології алергії та запальних реакцій, його роль у патогенезі носових поліпів залишається неясною, і на сьогодні немає досліджень із селективними антагоністами ФАТ при риніті або анафілаксії в людини. Відсутність доказів клінічної ефективності антагоністів ФАТ, імовірно, пояснює їх відсутність у нинішньому арсеналі засобів для лікування АЗ дихальних шляхів і обмежене їх використання в дослідженнях.
У дослідженнях японських учених (Furukawa M., Yamashita T., Kumazawa T., Satouchi K., Saito K., 1992; Furukawa M. et al., 2002) концентрація ФАТ була значно більшою в поліпах носа, ніж кількість пептидних лейкотрієнів (peptLT) в усіх препаратах. Активність ФАТ корелювала з тканинною еозинофілією, а в поліпах пацієнтів із чутливою до АСК астмою виявляли відносно велику кількість ФАТ з еозинофільною інфільтрацією. Уміст ФАТ у поліпах носа був значно вищим у групі тяжкого, ніж у групі легкого ураження (p<0,01).
Нині тривають пошуки нових мішеней для терапевтичного впливу при ПРС. Причиною цього є відсутність методів, які б дали можливість повністю вилікувати пацієнта. Хірургічне лікування має симптоматичний характер, відновлюючи прохідність порожнини носа, співусть пазух, їх пневматизацію. Але воно не перериває патогенетичний ланцюг хвороби і тому суттєво не впливає на тривалість ремісії.
Сучасна фармакотерапія поліпозної форми алергійного РС, на відміну від хірургічного лікування, має бути патогенетичною і спрямованою на блокування ефектів біологічно активних речовин і клітин, які безпосередньо беруть участь у розвитку патологічного процесу [1].
Загальноприйнятим є якнайшвидше призначення протирецидивної терапії ПРС після ліквідації реактивних післяопераційних змін у порожнині носа. Основою такої терапії сьогодні є інтраназальні кортикостероїди (ІнКС).
Стає зрозумілим, яке велике значення має рання реабілітація в кожного окремого пацієнта. Вона полягає у застосуванні засобів, що забезпечують швидку регресію реактивних післяопераційних явищ із боку слизової оболонки носа і приносових пазух із першого дня післяопераційного періоду. У комплексі традиційних засобів, що їх використовують на етапі раннього післяопераційного ведення хворих із поліпозом при алергійному РС, ми почали застосовувати препарат Рупафін у таблетках, який містить діючу речовину рупатадин у формі рупатадину фумарату по 10 мг.
Рупатадин (C26H26CIN3-C4H4O4) є похідним N-алкілпіридину, що класифікується як сучасний антигістамінний препарат (АГП) ІІ покоління. Структурно важливі дві хімічні групи: піперидиніл група, відповідальна за антигістамінну активність, і лутидинільна група, відповідальна за активність проти ФАТ. Рупатадин специфічно взаємодіє з H1-гістаміновими рецепторами і рецепторами ФАТ поза межами центральної нервової системи. Тому він одночасно є АГП і антагоністом ФАТ. Це забезпечує прямий і непрямий вплив на численні запальні хімічні речовини або медіатори [27].
Рупатадин міцно зв’язується (має високу спорідненість) з H1-гістаміновими рецепторами порівняно з АГП І та іншими представниками ІІ покоління, як було показано в дослідженнях, у рамках яких вивчали цю характеристику препарату. Наприклад, у клітинах яєчників китайського хом’яка (CHO) рупатадин зв’язувався з Н1-рецепторами сильніше, ніж інші АГП ІІ покоління (левоцетиризин, фексофенадин). Рупатадин був приблизно в 7 разів сильніший за левоцетиризин і приблизно в 29 разів сильніший за фексофенадин [28].
На відміну від різних АГП І покоління (наприклад, гідроксизин) і засобів ІІ покоління (наприклад, левоцетиризин, лоратадин) рупатадин є конкурентним інгібітором рецепторів ФАТ. Активність проти ФАТ також була продемонстрована у функціональному тесті in vitro на тромбоцитах кролика і людини (фізіологічний антагонізм) [22]. Активність антагоніста ФАТ зазвичай перевіряють, використовуючи здатність цього медіатора агрегувати тромбоцити кількох видів, у тому числі кроликів, завдяки наявності рецепторів ФАТ у мембрані тромбоцитів. Рупатадин був у 160 разів сильнішим за лоратадин і в більш як 500 разів ефективнішим, ніж терфенадин або кетотифен, щодо інгібування ФАТ-індукованої агрегації тромбоцитів кролика [29]. In vivo рупатадин був так само ефективним, як цетиризин і лоратадин, щодо протидії підвищенню проникності судин, спровокованому гістаміном, але перевершує ці засоби щодо протидії спричиненому ФАТ підвищенню проникності судин. Рупатадин був так само ефективним, як і чистий антагоніст ФАТ, а також пригнічував агрегацію тромбоцитів у дослідженні ex vivo [36]. Ці дані додатково підтверджують спостереження, що рупатадин має подвійну здатність блокувати H1-рецептори і рецептори ФАТ у людини.
Нейтрофіли також відіграють важливу роль в алергійних реакціях. У дослідженнях in vitro оцінювали вплив рупатадину на індукований ФАТ хемотаксис нейтрофілів людини. При порівнянні рупатадину з іншими АГП рупатадин був значно активнішим (74,1%), ніж лоратадин (34,5%), фексофенадин (7,9%) або цетиризин, який не виявив жодної інгібувальної активності [34]. Рупатадин має широкий спектр протизапальної та протиалергійної дії щодо клітин і хімічних речовин і, як було показано, пригнічує дегрануляцію опасистих клітин [38]. У фармакологічних дослідженнях рупатадин пригнічував індуковане антигеном вивільнення гістаміну з опасистих клітин шкіри собаки ефективніше за лоратадин (IC50=5,3 мкМ і 19 мкМ відповідно) [30].
Рупатадин сильніше, ніж дезлоратадин, пригнічує вивільнення цитокінів з активованих лімфоцитів людини, серед них GM-CSF; IL-5; IL‑6; IL‑8; фактор некрозу пухлини-α (TNF-α) [41]. In vitro рупатадин був найпотужнішим із чотирьох АГП щодо пригнічення продукції IL‑6 та IL‑8 у стимульованих гістаміном ендотеліальних клітинах пупкової вени людини. За показником зменшення продукції IL‑6 рупатадин був приблизно вдвічі потужнішим, ніж дезлоратадин, приблизно в 48 разів сильнішим за левоцетиризин і у 460 разів сильнішим за фексофенадин (відповідні середні значення IC50 становили 0,046; 0,1; 2,2 і 21 нМ). Подібним чином, при інгібуванні вироблення IL‑8, рупатадин був утричі сильнішим, ніж дезлоратадин, і в 60 разів сильнішим за левоцетиризин (відповідні середні значення IC50 становили 0,04; 0,12 і 2,4 нМ) [43, 44].
Було проведено декілька досліджень для оцінки антихолінергічних ефектів рупатадину. Ці ефекти виникають при застосуванні багатьох АГП І покоління. Рупатадин не виявляв периферичної антихолінергічної активності при одноразових дозах 10-80 мг [33, 43, 44].
Таким чином, рупатадин є АГП ІІ покоління, який має потужну антигістамінну та анти-ФАТ-активність. І саме ФАТ може бути терапевтичною мішенню і в разі АР, і в разі ПРС.
На відміну від інших АГП тільки рупатадин блокує дегрануляцію опасистих клітин унаслідок пригнічення індукованої ФАТ активації опасистих клітин, з багатообіцяючими результатами щодо поліпшення носових симптомів.
Оскільки безпека та ефективність Рупафіну (рупатадину) були продемонстровані в ході численних попередніх досліджень і клінічних випробувань [45-78], ми провели клінічні спостереження за 23 пацієнтами (11 чоловіків, 12 жінок) віком від 31 до 60 років із поліпозною формою алергійного РС. В усіх випадках спостерігали явища полісинуситу із залученням верхньощелепної, решітчатої, лобної, у деяких випадках основної пазух. Контрольну групу становила така сама кількість хворих. Для вивчення морфологічних змін носової порожнини як перед початком лікування, так і в його процесі проводили отоларингологічне обстеження за допомогою ендоскопічного оптичного методу. Використовували неспецифічні і специфічні методи лабораторної діагностики, у тому числі визначення кількості еозинофілів у периферичній крові, концентрації загального ІgЕ і цитологічні дослідження з носа, алергопроби (шкірне тестування, специфічні ІgЕ). Вираженість симптомів назальної обструкції оцінювали за 4-бальною шкалою TNSS: 0 – відсутність симптомів, 1 – легкі прояви (симптоми є, але не дошкуляють), 2 – помірні (симптоми є і дошкуляють), 3 – тяжкі прояви симптомів.
Хірургічне лікування в рамках функціональної ендоскопічної хірургії синусів (FESS) застосовували лише для усунення поліпів, які не відреагували на ІнКС. Проводили відкриття просвіту верхньощелепної, клиноподібної або лобної пазух.
Проте навіть сучасні малоінвазивні ендоскопічні хірургічні втручання супроводжуються реактивними явищами в післяопераційному періоді. Утруднення носового дихання в перший день післяопераційного періоду було практично в усіх пацієнтів обох груп. Після анемізації слизової оболонки носової порожнини в усіх хворих зазначалося поліпшення назальної прохідності.
Пацієнти основної групи з першого дня післяопераційного періоду, крім загальноприйнятих заходів догляду, отримували препарат Рупафін у дозі 10 мг 1 таблетку 1 р./добу. Інші протиалергійні засоби в ході дослідження не використовували.
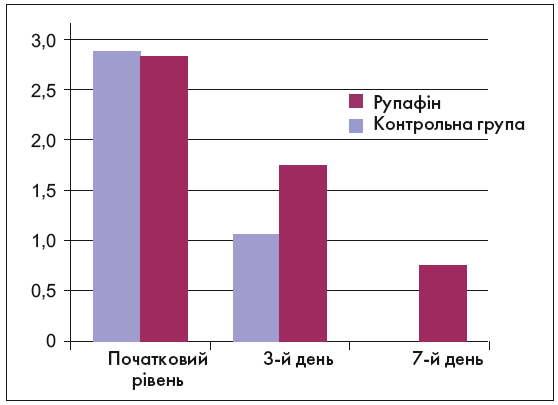
Виражену регресію закладеності носа у хворих, яким призначали Рупафін, спостерігали вже на 3-тю добу післяопераційної реабілітації (рис.). За показником зниження назальної обструкції ці хворі значуще випереджали пацієнтів контрольної групи. На 3-й день спостереження показник закладеності носа в основній групі становив 1,06±0,15, у контрольній – 1,75±0,21. На 7-му добу післяопераційного періоду носове дихання значно поліпшилось у 100% пацієнтів, що отримували Рупафін, і у 77,8% учасників контрольної групи. Загалом, Рупафін був ефективний в усіх обстежуваних. При цьому загальні оцінки ефективності лікування, зроблені лікарем і пацієнтами, повністю збігалися. Було зроблено висновок про хорошу переносимість препарату, лише у 2 учасників спостерігали помірну сонливість, але це не потребувало відміни препарату.
Рис. Середні значення закладеності носа в ранньому післяопераційному періоді в учасників групи Рупафіну і контрольної групи
Таким чином, наші спостереження показали значну ефективність препарату Рупафін, що проявлялось у швидшій регресії реактивних післяопераційних явищ із боку слизової оболонки носа і, як наслідок, відновленні функції носового дихання в пацієнтів із ПРС на тлі алергійного процесу. На нашу думку, це пов’язано з доведеною в ході численних експериментальних і клінічних досліджень in vitro та in vivo подвійною дією (антигістамінною і анти-ФАТ) молекули рупатадину, який блокує вивільнення прозапальних цитокінів (IL‑4, IL‑8, IL‑6, IL‑5, TNF-α, GM-CSF) і хемотаксис клітин крові до вогнища запалення, забезпечуючи потужну протизапальну дію. Тому ми вважаємо, що препарат Рупафін можна рекомендувати для пришвидшення регресії післяопераційних реактивних змін із боку слизової оболонки носа і приносових пазух із першого дня післяопераційного періоду при поліпозній формі АРС. Однак необхідні подальші дослідження, які допоможуть визначити оптимальні параметри фармакотерапії цим засобом у хворих на АР із поліпозом і розробити ефективні схеми протирецидивної терапії ПРС.
Література
- Безшапочний С.Б., Пухлик С.М., Лобурець В.В. Сучасні аспекти поліпозних риносинуситів. Клінічна імунологія, алергологія, інфектологія. – 2008. – 1 (12).
- Заболотний Д.І., Юрочко Ф.Б. Поліпоз носа. Теорія та практика. – 2006. – 143 с.
- Нейко Є.М., Чернюк Н.В., Ковальчук Л.Є. Бронхіальна астма: клініко-генетичні аспекти патогенезу, діагностики лікування, профілактики. – К.: Здоров’я. – 2003. – С. 166.
- Нейко Є.М., Думка Р.М., Яцишин Р.І. і ін. Бронхіальна астма: визначення, етіопатогенез, сучасна класифікація (Методичні рекомендації) // Івано-Франківськ. – 1998. – С. 11.
- Попович В.І., Ковальчук Л.Є., Ерстенюк Г.М., Рижик В.М., Кошель І.В. «Аспіринова тріада» як метаболічне захворювання. Журнал вушних, носових і горлових хвороб. – № 2. – 2009. – С. 76-85.
- Нamilos DL: Chronic sinusitis // J Allergy Clin Immunol. – 2000. – 106: Р. 213-227.
....
78. Dubertret L., Zalupca L., Cristodoulo T., Benea V. et al. Once-daily rupatadine improves the symptoms of chronic idiopathic urticaria: a randomized, double-blind, placebo-controlled study. Eur J Dermatol. 2007;17:223-28
Повний список літератури – у редакції.
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 3-4 (64-65) 2023 р.